
Come usare EKLIRA GENUAIR
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra traduzioneContenuto del foglietto illustrativo
Eklira Genuair 322 microgrammi polvere per inalazione
Aclidinio (bromuro di aclidinio)
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Cos’è Eklira Genuair e a cosa serve
- 2. Cosa deve sapere prima di usare Eklira Genuair
- 3. Come usare Eklira Genuair
- 4. Possibili effetti indesiderati
- 5. Come conservare Eklira Genuair
- 6. Contenuto della confezione e altre informazioni Istruzioni per l’Uso
1. Cos’è Eklira Genuair e a cosa serve
Che cos’è Eklira Genuair
Il principio attivo di Eklira Genuair è bromuro di aclidinio, che appartiene a un gruppo di medicinali
chiamati broncodilatatori. I broncodilatatori rilassano la muscolatura delle vie aeree e aiutano a
mantenere aperti i bronchioli. Eklira Genuair è un inalatore a polvere secca che usa il respiro per
somministrare il medicinale direttamente nei polmoni, rendendo più agevole la respirazione dei
pazienti con broncopneumopatia cronica ostruttiva (BPCO).
A che cosa serve Eklira Genuair
Eklira Genuair è indicato per aiutare ad aprire le vie respiratorie e alleviare i sintomi della BPCO, una
grave malattia polmonare a lungo termine caratterizzata da respirazione difficoltosa. L’uso regolare di
Eklira Genuair può aiutarla quando ha il respiro affannoso a causa della malattia e la aiuterà a limitare
gli effetti della malattia nella quotidianità e a ridurre il numero di riacutizzazioni (il peggioramento dei
sintomi della BPCO per diversi giorni).
2. Cosa deve sapere prima di usare Eklira Genuair
Non usi Eklira Genuair
- se è allergico al bromuro di aclidinio o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6).
Avvertenze e precauzioni
Si rivolga al medico, al farmacista o all’infermiere prima di usare Eklira Genuair:
- se ha problemi di cuore;
- se vede aloni attorno alle luci o alle immagini colorate (glaucoma);
- se ha la prostata ingrossata, problemi ad urinare o un blocco della vescica.
Eklira Genuair è indicato come terapia di mantenimento e non deve essere usato per trattare attacchi
improvvisi di affanno o respiro sibilante. Se i sintomi della BPCO (affanno, respiro sibilante, tosse)
non migliorano o peggiorano, deve consultare il medico il prima possibile.
La bocca secca, osservata con medicinali come Eklira Genuair, dopo l’uso del medicinale per lungo
tempo può essere associata a carie dentali. Pertanto, si ricordi di fare attenzione all’igiene orale.
Interrompa l’assunzione di Eklira Genuair e si rivolga immediatamente al medico:
- se avverte oppressione toracica, tosse, respiro sibilante o affanno immediatamente dopo aver usato il medicinale. Potrebbero essere segni di una condizione denominata broncospasmo.
Bambini e adolescenti
Eklira Genuair non deve essere usato in bambini e adolescenti di età inferiore a 18 anni.
Altri medicinali e Eklira Genuair
Informi il medico o il farmacista se sta assumendo, ha recentemente assunto o potrebbe assumere
qualsiasi altro medicinale.
Informi il medico se ha usato o sta usando medicinali simili per i problemi respiratori, come
medicinali contenenti tiotropio o ipratropio. Se ha dei dubbi, consulti il medico o il farmacista. L’uso
di Eklira Genuair con questi medicinali è sconsigliato.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con
latte materno chieda consiglio al medico o al farmacista prima di prendere questo medicinale. Non
deve usare Eklira Genuair se è in gravidanza o se sta allattando, salvo in caso il medico le abbia detto
di farlo.
Guida di veicoli e utilizzo di macchinari
Eklira Genuair altera lievemente la capacità di guidare veicoli o di usare macchinari. Questo
medicinale può provocare mal di testa, capogiri o visione offuscata. Se lamenta uno qualsiasi di questi
effetti, non guidi o usi macchinari fino a quando il mal di testa è passato, la sensazione di capogiro è
scomparsa e la vista è tornata normale.
Eklira Genuair contiene lattosio
Se il medico le ha diagnosticato una intolleranza ad alcuni zuccheri, lo contatti prima di prendere
questo medicinale.
3. Come usare Eklira Genuair
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico o del farmacista. Se ha
dubbi consulti il medico o il farmacista.
- La dose raccomandata è un’inalazione due volte al giorno, mattino e sera.
- Gli effetti di Eklira Genuair durano 12 ore; pertanto deve tentare di usare l’inalatore Eklira Genuair alla stessa ora ogni mattino e ogni sera. In questo modo si garantisce che nell’organismo sia presente sempre una quantità sufficiente di farmaco, aiutandola a respirare più facilmente durante tutto il giorno e la notte. La aiuterà anche a ricordare di usarlo.
La dose raccomandata può essere usata in pazienti anziani e in pazienti con problemi ai reni o al
fegato. Non sono necessari aggiustamenti della dose.
La BPCO è una malattia cronica, pertanto si raccomanda di usare Eklira Genuair ogni giorno, due
volte al giorno, e non solo quando si avvertono problemi respiratori o altri sintomi della BPCO.
Via di somministrazione
Questo medicinale è per uso inalatorio.
Per istruzioni su come usare l’inalatore Genuair, consulti le Istruzioni per l’Uso. Se ha dei dubbi su
come usare Eklira Genuair, si rivolga al medico o al farmacista.
Può usare Eklira Genuair in qualsiasi momento prima o dopo l’assunzione di cibo o bevande.
Se usa più Eklira Genuair di quanto deve
Se ritiene di aver usato più Eklira Genuair di quanto deve, si rivolga al medico o al farmacista.
Se dimentica di usare Eklira Genuair
Se dimentica una dose di Eklira Genuair, inali la dose non appena se ne ricorda. Tuttavia, se è quasi
ora della dose successiva, tralasci la dose dimenticata.
Non prenda una dose doppia per compensare la dimenticanza della dose.
Se interrompe il trattamento con Eklira Genuair
Questo medicinale è destinato all’uso a lungo termine. Se desidera interrompere il trattamento, ne
discuta prima con il medico, perché i sintomi potrebbero peggiorare.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico, al farmacista o
all’infermiere.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Molto raramente possono insorgere reazioni allergiche (possono interessare fino a una persona su
1000). Interrompa l’uso del medicinale e si rivolga immediatamente al medico se manifesta gonfiore
del viso, della gola, delle labbra o della lingua (con o senza difficoltà di respirazione o deglutizione),
capogiri o svenimento, accelerazione del battito cardiaco o se sviluppa bolle gravemente pruriginose
sulla pelle (orticaria), perché potrebbero essere i sintomi di una reazione allergica.
Durante l’uso di Eklira Genuair possono verificarsi i seguenti effetti indesiderati :
Comuni:possono interessare fino a 1 persona su 10
- Mal di testa (cefalea)
- Infiammazione dei seni paranasali (sinusite)
- Raffreddore comune (nasofaringite)
- Tosse
- Diarrea
- Nausea
Non comuni:possono interessare fino a 1 persona su 100
- Capogiro
- Bocca secca
- Infiammazione della bocca (stomatite)
- Raucedine (disfonia)
- Battito cardiaco accelerato (tachicardia)
- Battito cardiaco anormale o irregolare (aritmie cardiache)
- Percezione del battito cardiaco (palpitazioni)
- Difficoltà a urinare (ritenzione urinaria)
- Visione offuscata
- Eruzione cutanea
- Prurito della pelle
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ Allegato V . Segnalando gli effetti
indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Eklira Genuair
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sull’etichetta e sulla scatola
dell’inalatore dopo “Scad.” o “EXP”. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Tenga l’inalatore all’interno del sacchetto fino all’inizio del periodo di somministrazione.
Utilizzare entro 90 giorni dall’apertura del sacchetto.
Non usi Eklira Genuair se nota che la confezione è danneggiata o evidenzia segni visibili di
manomissione.
Dopo aver assunto l’ultima dose, l’inalatore deve essere gettato. Non getti alcun medicinale nell’acqua
di scarico e nei rifiuti domestici. Chieda al farmacista come eliminare i medicinali che non utilizza più.
Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Eklira Genuair
- Il principio attivo è bromuro di aclidinio. Ogni dose erogata contiene 375 microgrammi di bromuro di aclidinio, equivalenti a 322 microgrammi di aclidinio.
- L’altro componente è il lattosio monoidrato (vedere paragrafo 2 “Eklira Genuair contiene lattosio”).
Descrizione dell’aspetto di Eklira Genuair e contenuto della confezione
Eklira Genuair è una polvere bianca o quasi bianca.
L’inalatore Genuair è di colore bianco, con un indicatore di dosi integrato e un tasto di erogazione
verde. Il boccaglio è coperto da un cappuccio protettivo rimovibile di colore verde. Viene fornito in un
sacchetto di plastica.
Formato di vendita:
Scatola contenente 1 inalatore da 30 dosi.
Scatola contenente 1 inalatore da 60 dosi.
Scatola contenente 3 inalatori, ciascuno da 60 dosi.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Covis Pharma Europe B.V.
Gustav Mahlerplein 2
1082MA Amsterdam
Paesi Bassi
Produttore:
Industrias Farmacéuticas Almirall, S.A.
Ctra. de Martorell 41-61
08740 Sant Andreu de la Barca, Barcellona
Spagna
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Covis Pharma Europe B.V.
Tel: 80013067
Lietuva
Covis Pharma Europe B.V.
Tel: 880000890
България
Covis Pharma Europe B.V.
Tel: 008002100654
Luxembourg/Luxemburg
Covis Pharma Europe B.V.
Tel: 80024119
Česká republika
Covis Pharma Europe B.V.
Tel: 800144474
Magyarország
Covis Pharma Europe B.V.
Tel.: 0680021540
Malta
Covis Pharma Europe B.V.
Tel: 80065149
Deutschland
Zentiva Pharma GmbH
Tel: +49 (0) 800 53 53 010
Danmark
Zentiva Denmark ApS
Tlf: +45 787 68 400
Nederland
Covis Pharma Europe B.V.
Tel: 08000270008
Eesti
Covis Pharma Europe B.V
Tel: 8000100776
Norge
Zentiva Denmark ApS
Tlf: +47 219 66 203
Ελλάδα
Specialty Therapeutics IKE
Τηλ: +30 213 02 33 913
Österreich
Covis Pharma Europe B.V.
Tel: 0800006573
España
Zentiva Spain S.L.U.
Tel: +34 931 815 250
Polska
Covis Pharma Europe B.V.
Tel.: 0800919353
France
Zentiva France
Tél: +33 (0) 800 089 219
Portugal
Zentiva Portugal, Lda
Tel: +351210601360
Hrvatska
Covis Pharma Europe B.V.
Tel: 08004300
România
Covis Pharma Europe B.V.
Tel: 0800410175
Ireland
- A. Menarini Pharmaceuticals Ireland Ltd Tel: +353 1 284 6744 SlovenijaCovis Pharma Europe B.V. Tel: 080083003
Ísland
Zentiva Denmark ApS
Sími: +354 539 0650
Slovenská republika
Covis Pharma Europe B.V.
Tel: 0800008203
Italia
Covis Pharma Europe B.V.
Tel: 800168094
Suomi/Finland
Zentiva Denmark ApS
Puh/Tel: +358 942 598 648
Κύπρος
Specialty Therapeutics IKE
Τηλ: +30 213 02 33 913
Sverige
Zentiva Denmark ApS
Tel: +46 840 838 822
Latvija
Covis Pharma Europe B.V.
Tel: 80005962
United Kingdom (Northern Ireland)
Zentiva, k.s.
Tel: +44 (0) 800 090 2408
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
dei medicinali: http://www.ema.europa.eu.
Istruzioni per l’Uso
Questa sezione contiene informazioni su come usare Genuair inalatore. È importante leggere queste
informazioni poichè Genuair potrebbe funzionare diversamente rispetto agli inalatori che ha usato
precedentemente. In caso di dubbi su come usare il Suo inalatore, si rivolga al medico, al farmacista o
all’infermiere per assistenza.
Le istruzioni per L’Uso sono divise in due nelle seguenti sezioni:
- Fasi preliminari
- Passaggio 1: Preparare la dose
- Passaggio 2: Inalare il medicinale
- Informazioni aggiuntive
Fasi preliminari
Legga queste istruzioni per l’Uso prima di iniziare ad usare questo medicinale.
Familiarizzare con i componenti di Genuair inalatore.
Indicatore
di dose
Finestra di controllo
Verde = inalatore pronto
all’uso
Tasto verde

Cappuccio
Protettivo
Finestra di controllo
Rosso = conferma la corretta
inalazione
Boccaglio
Figura A
Prima dell’uso:
a) Prima del primo utilizzo, aprire il sacchetto sigillato ed estrarre l’inalatore Genuair dal
sacchetto.
b) Non premere il tasto verde fino a quando non è pronto ad assumere una dose.
c) Togliere il cappuccio premendo leggermente le frecce presenti su entrambi i lati (Figura
B).
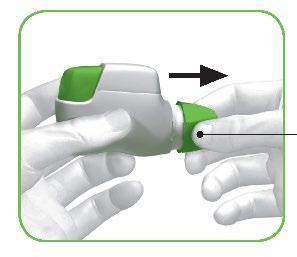
Premere qui e
tirare
Figura B
PASSAGGIO 1: Preparare la dose
- 1.1 Guardare nell’apertura del boccaglio e assicurarsi che niente lo stia bloccando (Figura C).
- 1.2 Guardare la finestra di controllo (deve essere rossa, Figura C).

ROSSO
Controlli l’apertura
del boccaglio
Figura C
- 1.3 Tenere l’inalatore orizzontale con il boccaglio verso di sé e il tasto verde dritto verso l’alto (Figura D).
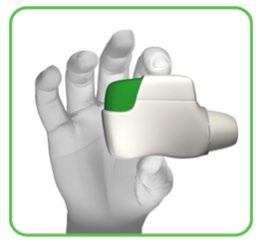
Figura D
- 1.4 Premere fino in fondo il tasto verde per caricare la dose (Figura E).
Quando si preme il tasto verde fino in fondo la finestra di controllo cambia diventando da rossa a
verde.
Assicurarsi che il tasto verde sia dritto verso l’alto. Non inclinare.
- 1.5. Rilasciare il tasto verde (Figura F).
Assicurarsi di aver rilasciato il tasto in modo che l’inalatore funzioni correttamente.
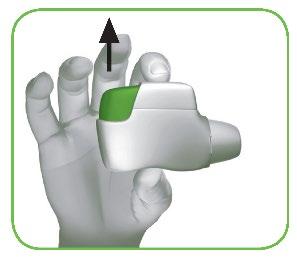
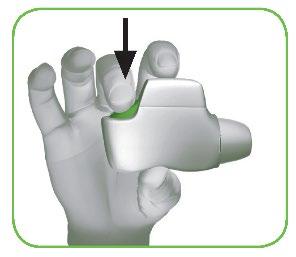
Figura EFigura F
Fermarsi e Controllare:
- 1.6 Assicurarsi che la finestra di controllo sia diventata ora verde (Figura G).
Il suo medicinale è pronto per essere inalato.
Passare al ‘PASSAGGIO 2: Inalare il medicinale’.

VERDE
Figura G
Cosa fare se la finestra di controllo è ancora rossa dopo aver premuto il tasto (Figura H).

Figura H
La dose non è preparata. Torni indietro al ‘PASSAGGIO 1 Preparare la dose’ e ripeta i
passaggi da 1.1. a 1.6.
PASSAGGIO 2: Inalare il medicinale
Legga per intero i passaggi da 2.1 a 2.7 prima dell’uso. Non inclinare.
- 2.1 Tenere l’inalatore lontano dalla bocca ed espiri completamente. Non espirare mai nell’inalatore (Figura I).
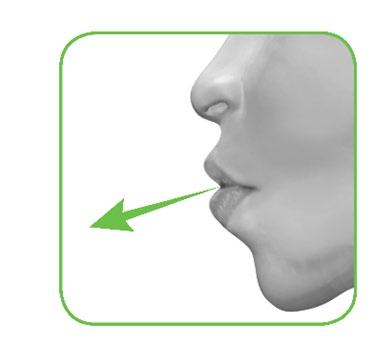
Figura I
- 2.2 Tenere la testa dritta, metta il boccaglio tra le labbra, e chiuda le labbra saldamente intorno ad esso (Figura J).
Non tenga il tasto verde premuto mentre inala.

Figura J
- 2.3 Faccia un respiro forte e profondocon la bocca. Tenga il respiro il più a lungo possibile.
Si sentirà un ‘clic’ che Le segnala che sta inalando correttamente. Tenga il respiro il più a lungo
possibile dopo aver sentito il ‘clic’. Alcuni pazienti possono non sentire il ‘clic’. Usi la finestra di
controllo per assicurarsi che ha inalato correttamente.
- 2.4 Allontani l’inalatore dalla bocca.
- 2.5 Tenga il respiro il più a lungo possibile.
- 2.6 Espiri lentamente lontano dall’inalatore.
Alcuni pazienti potrebbero avvertire una sensazione di granulosità in bocca, o un lieve sapore
dolciastro o amarognolo. Non assuma una dose supplementare anche se non avverte alcun sapore o
non percepisce nulla dopo l’inalazione.
Fermarsi e Controllare:
- 2.7 Assicurarsi che la finestra di controllo sia ora diventata rossa (Figura K). Questo significa che ha inalato il medicinale correttamente.

Figure K
Cosa fare se la finestra di controllo è ancora verde dopo l’inalazione (Figura L).

Figura L
Questo significa che non ha inalato il medicinale correttamente. Torni indietro al ‘PASSAGGIO 2
Inalare il medicinale’ e ripeta i passaggi da 2.1 a 2.7.
Se la finestra di controllo non è ancora diventata rossa potrebbe aver dimenticato di rilasciare il tasto
verde prima di inalare, o potrebbe non aver inalato abbastanza. Se ciò si verifica, provi di nuovo. Si
assicuri di aver rilasciato il tasto verde, e di aver espirato completamente. Poi, faccia un respiro forte e
profondo con la bocca attraverso il boccaglio.
Contatti il Suo medico se la finestra di controllo è verde dopo tentativi ripetuti.
Prema il cappuccio protettivo indietro verso il boccaglio dopo ogni uso (Figura M), per prevenire la
contaminazione dell’inalatore con polveri o altri materiali. Deve smaltire il Suo inalatore se ha perso il
cappuccio.

Figura M
Informazioni aggiuntive
Cosa deve fare se accidentalmente ha preparato una dose?
Conservi il Suo inalatore con il cappuccio protettivo posizionato su di esso fino a quando non deve
inalare ilmedicinale, poi rimuova il cappuccio ed inizi dal passaggio 1.6.
Come funziona l’indicatore di dose?
- L’indicatore di dose mostra il numero totale di dosi rimaste nell’inalatore (Figura N).
- Al primo uso, ogni inalatore contiene almeno 60 dosi, o almeno 30 dosi, a seconda della confezione.
- Ogni volta che tu carichi una dose premendo il tasto verde, l’indicatore di dose si sposta di piccoli intervalli fino al numero successivo (50, 40, 30, 20, 10, o 0).
Quando deve richiedere un nuovo inalatore?
Deve richiedere un nuovo inalatore:
- Se il suo inalatore appare danneggiato o se ha perso il cappuccio, o
- Quando una banda rossaappare nell’indicatore di dose, questo significa che è quasi vuoto (Figura N), o
- Se il Suo inalatore è vuoto (Figura O).
L’indicatore di dose si sposta lentamente
da 60 a 0: 60, 50, 40, 30, 20, 10, 0.

Banda rossa
Indicatore di
Dose
Figura N
Come si sa che l’inalatore è vuoto?
Quando il tasto verde non ritorna completamente verso l’alto e rimane bloccato in posizione
intermedia, si è raggiunta l’ultima dose (Figura O). Sebbene il tasto verde è bloccato, l’ultima dose
può essere comunque inalata. Dopo questa dose l’inalatore non può essere utilizzato di nuovo e
bisogna iniziare a usare un nuovo inalatore.

Bloccato
Figura O
Come pulire l’inalatore?
Non usare MAI l’acqua per pulire l’inalatore, poichè questo può danneggiare il medicinale.
Se desidera pulire il Suo inalatore, strofini la parte esterna del boccaglio con un tessuto asciutto o un
tovagliolo.
ALLEGATO IV
CONCLUSIONI SCIENTIFICHE E MOTIVAZIONI PER LA VARIAZIONE DEI
TERMINI DELL’AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO
Conclusioni scientifiche
Tenendo conto della valutazione del Comitato per la valutazione dei rischi in farmacovigilanza
( Pharmacovigilance and Risk Assessment Committee, PRAC) per il rapporto finale dello studio non
interventistico PASS imposto per i medicinali menzionati sopra, le conclusioni scientifiche del
Comitato dei medicinali per uso umano ( Committee for Human Medicinal Products, CHMP) sono
le seguenti:
I risultati dello studio mostrano che aclidinio aumenta il rischio di aritmie cardiache e fibrillazione
atriale rispetto ai LABA e altri LAMA. Inoltre, i risultati mostrano anche che aclidinio/formoterolo
FDC aumenta il rischio di eventuali aritmie cardiache e fibrillazione atriale rispetto ai LABA o altre
combinazioni LAMA/LABA. Pertanto, alla luce dei dati disponibili sul rapporto finale dello studio
PASS, il PRAC ha ritenuto che debbano essere apportate modifiche alle informazioni sul prodotto.
Il CHMP concorda con le conclusioni scientifiche del PRAC.
Motivazioni per la variazione dei termini dell’autorizzazione all'immissione in commercio
Sulla base delle conclusioni scientifiche dei risultati dello studio per i medicinali menzionati sopra,
il CHMP ritiene che il rapporto beneficio/rischio di tali medicinali ia invariato fatte salve le
modifiche proposte alle informazioni sul medicinale.
Il CHMP raccomanda la variazione dei termini dell’autorizzazione all’immissione in commercio
dei medicinali menzionati sopra.
-

- Paese di registrazione
- Forma farmaceuticaPolvere per inalazione, 322 MICROGRAMMI
- Codice ATCR03BB05
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a EKLIRA GENUAIRForma farmaceutica: Polvere per inalazione, 322 MICROGRAMMIPrincipio attivo: aclidinium bromideProduttore: COVIS PHARMA EUROPE BVPrescrizione richiestaForma farmaceutica: Soluzione da nebulizzare, 0,5 MG/2 MLPrincipio attivo: ipratropium bromideProduttore: PROMEDICA S.R.L.Prescrizione richiestaForma farmaceutica: Polvere per inalazione, capsula rigida, 44 MCGPrincipio attivo: glycopyrronium bromideProduttore: NOVARTIS EUROPHARM LIMITEDPrescrizione non richiesta
Medici online per EKLIRA GENUAIR
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di EKLIRA GENUAIR — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per EKLIRA GENUAIR online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.










