
Come usare HYQVIA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
HyQvia 100 mg/mL soluzione per infusione per uso sottocutaneo
immunoglobulina umana normale
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è HyQvia e a cosa serve
- 2. Cosa deve sapere prima di usare HyQvia
- 3. Come usare HyQvia
- 4. Possibili effetti indesiderati
- 5. Come conservare HyQvia
- 6. Contenuto della confezione e altre informazioni
1. Cos’è HyQvia e a cosa serve
Cos’è HyQvia
HyQvia contiene 2 soluzioni per infusione (flebo) sotto la pelle (infusione sottocutanea o infusione
SC). È fornito in una confezione contenente:
- un flaconcino di immunoglobulina umana normale 10% (il principio attivo)
- un flaconcino di ialuronidasi umana ricombinante (una sostanza che aiuta a far arrivare l’immunoglobulina umana normale 10% nel sangue).
L’immunoglobulina umana normale 10% appartiene a una classe di medicinali chiamati
“immunoglobuline umane normali”. Le immunoglobuline sono dette anche anticorpi e sono presenti
nel sangue delle persone sane. Gli anticorpi fanno parte del sistema immunitario (le difese naturali
dell’organismo) e aiutano l’organismo a combattere le infezioni.
Come agisce HyQvia
La ialuronidasi umana ricombinante è una proteina che facilita l’infusione sottocutanea delle
immunoglobuline e il raggiungimento della circolazione sanguigna.
Il flaconcino di immunoglobuline è stato preparato dal sangue di persone sane. Le immunoglobuline
sono prodotte dal sistema immunitario del corpo umano. Aiutano il corpo a combattere le infezioni
causate da batteri e virus o mantengono l’equilibrio nel sistema immunitario (fenomeno noto come
immunomodulazione). Il medicinale agisce allo stesso modo delle immunoglobuline naturalmente
presenti nel sangue.
A cosa serve HyQvia
Terapia sostitutiva in adulti e bambini (di età compresa tra 0 e 18 anni)
HyQvia si usa nei pazienti che hanno un sistema immunitario debole, che non possiedono anticorpi
sufficienti nel loro sangue e quindi sono più frequentemente esposti a infezioni, inclusi i seguenti
gruppi:
- pazienti che presentano un’incapacità o una capacità ridotta congenita di produrre anticorpi (immunodeficienze primarie)
- pazienti con infezioni severe o ricorrenti a causa di un sistema immunitario indebolito da altre condizioni o trattamenti (immunodeficienze secondarie).
Dosi regolari e sufficienti di HyQvia possono aumentare livelli anormalmente bassi di
immunoglobuline nel sangue fino a livelli normali (terapia sostitutiva).
Terapia immunomodulante in adulti, bambini e adolescenti (di età compresa tra 0 e 18 anni)
HyQvia è utilizzato nei pazienti adulti, bambini e adolescenti (di età compresa tra 0 e 18 anni) affetti
da poliradiculoneuropatia demielinizzante infiammatoria cronica (CIDP), una forma di malattia
autoimmune. La CIDP è caratterizzata da un’infiammazione cronica dei nervi periferici che causa
debolezza muscolare e/o intorpidimento principalmente alle gambe e alle braccia. Si ritiene che il
sistema di difesa del corpo attacchi i nervi periferici e causi danni ai nervi e infiammazioni. Si pensa
che le immunoglobuline presenti in HyQvia aiutino a proteggere i nervi dai danni causati dal sistema
immunitario.
2. Cosa deve sapere prima di usare HyQvia
Non si inietti osi esegua l’infusione di HyQvia:
- se è allergico alle immunoglobuline, alla ialuronidasi, alla ialuronidasi ricombinante o a uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6, “Contenuto della confezione e altre informazioni”).
- se ha anticorpi anti-immunoglobulina A (IgA) nel sangue, ad esempio, se soffre di carenza di IgA. Poiché HyQvia contiene tracce di IgA, lei potrebbe sviluppare una reazione allergica.
- in un vaso sanguigno (via endovenosa) o in un muscolo (via intramuscolare).
Avvertenze e precauzioni
Si rivolga al medico o all’infermiere prima di utilizzare HyQvia.
► Informi il medico o l’operatore sanitario prima del trattamento se una delle circostanze
elencate di seguito la riguarda:
- Lei o il bambino potrebbe essere allergico alle immunoglobuline senza saperlo. Le reazioni allergiche quali la diminuzione improvvisa della pressione sanguigna o lo shock anafilattico (una brusca caduta della pressione arteriosa con altri sintomi, quali gonfiore della gola, difficoltà nella respirazione ed esantema della cute) sono rare ma possono manifestarsi occasionalmente anche se in passato non ha avuto problemi con trattamenti simili. È a maggior rischio di reazioni allergiche se soffre di carenza di IgA e presenta anticorpi anti-IgA. I segni o i sintomi di queste reazioni allergiche rare comprendono:
- sensazione di confusione mentale, capogiro o mancamento; o eruzione cutanea e prurito, gonfiore della bocca o della gola, respirazione difficoltosa, respiro sibilante;
o frequenza cardiaca anormale, dolore toracico, colore blu delle labbra o delle dita delle
mani e dei piedi;
o visione annebbiata.
► Se nota uno dei seguenti segni durante l’infusione, lo comunichi immediatamente
al medico o all’infermiere che deciderà se rallentare la velocità dell’infusione
o interrompere completamente l’infusione.
Il medico o l’infermiere le infonderà la ialuronidasi umana ricombinante (HY) seguita
dall’immunoglobulina (IG) lentamente e la terrà sotto controllo attentamente durante la 1 infusione
per poter rilevare e trattare immediatamente qualsiasi eventuale reazione allergica.
Il medico presterà particolare attenzione se lei è in sovrappeso, è anziano, ha il diabete, è stato
costretto a letto per lungo tempo, ha la pressione alta, ha un volume sanguigno basso (ipovolemia), ha
problemi ai vasi sanguigni (malattie vascolari), ha una maggiore tendenza alla coagulazione del
sangue (trombofilia o episodi trombotici) o ha una malattia o una condizione che causa l’aumento
della densità del sangue (sangue iper viscoso). In queste circostanze, le immunoglobuline possono
aumentare il rischio di attacco cardiaco (infarto cardiaco), ictus, coaguli di sangue nel polmone
(embolia polmonare) o ostruzione di un vaso sanguigno nella gamba, anche se solo molto raramente.
► Se nota uno qualsiasi di questi segni e sintomi, inclusi fiato corto, dolore, gonfiore di un
arto e dolore toracico durante l’infusione, informi immediatamente il medico o
l’infermiere. Loro decideranno se rallentare la velocità di infusione o interromperla
completamente.
Il medico o l’infermiere la monitoreranno attentamente durante le infusioni in modo che eventuali
eventi tromboembolici possano essere rilevati e trattati immediatamente.
- Riceverà questo medicinale ad alte dosi per 1 o 2 giorni e se ha un gruppo sanguigno A, B o AB e una condizione infiammatoria sottostante. In queste circostanze, è stato comunemente riportato che le immunoglobuline aumentano il rischio di rottura dei globuli rossi (emolisi).
- È stata segnalata l’infiammazione delle membrane che circondano il cervello e il midollo spinale (sindrome da meningite asettica) in associazione al trattamento con immunoglobuline. ► Se nota uno qualsiasi di questi segni e sintomi, inclusi forte mal di testa, rigidità del collo, sonnolenza, febbre, fotofobia, nausea e vomito dopo l’infusione, informi immediatamente il medico o l’infermiere. Il medico deciderà se sono necessari ulteriori esami e se continuare il trattamento con HyQvia.
Velocità di infusione
È molto importante che il medicinale venga infuso alla velocità corretta. Il medico o l’infermiere
le comunicheranno la velocità di infusione appropriata da usare quando si somministrerà HyQvia
a casa (vedere paragrafo 3, “ Come usare HyQvia”).
Monitoraggio durante l’infusione
Determinati effetti indesiderati possono verificarsi più frequentemente se:
- sta usando HyQvia per la prima volta.
- è passato a HyQvia dopo aver ricevuto un’altra immunoglobulina.
- è trascorso un lungo intervallo di tempo (ad es. più di 2 o 3 intervalli di infusione) dall’ultima somministrazione di HyQvia. ► In questi casi, sarà tenuto sotto controllo attentamente durante la prima infusione e per la prima ora dopo l’interruzione dell’infusione.
In tutti gli altri casi, nelle prime infusioni, dovrà essere tenuto in osservazione durante l’infusione e per
almeno 20 minuti dopo la somministrazione di HyQvia.
Trattamento domiciliare
Prima di iniziare un trattamento domiciliare, è opportuno avere una persona che si prende cura di lei.
Lei e la persona che la assiste sarete istruiti a riconoscere i primi segni di effetti indesiderati, in
particolare le reazioni allergiche. La persona che si prende cura di lei deve aiutarla a controllare
i potenziali effetti indesiderati. Durante l’infusione, è necessario osservare attentamente i primi segni
di effetti indesiderati (per ulteriori informazioni, vedere paragrafo 4, “ Possibili effetti indesiderati”).
► Se si manifestano effetti indesiderati, il paziente o la persona che si prende cura di lui
deve interrompere immediatamente l’infusione e contattare il medico.
► In presenza di un effetto indesiderato grave, il paziente o la persona che si prende cura
di lui deve richiedere immediatamente un trattamento di emergenza.
Diffusione di infezioni localizzate
Non eseguire l’infusione di HyQvia in o intorno a un’area infettata o gonfia e arrossata della pelle,
perché HyQvia potrebbe causare la diffusione dell’infezione.
Nel corso degli studi clinici non si sono osservate alterazioni a lungo termine (croniche) della
pelle. Occorre riferire al medico qualsiasi infiammazione a lungo termine, noduli o infiammazione
che si verificano in sede di infusione e che durano più di qualche giorno.
Effetti sulle analisi del sangue
HyQvia contiene molti anticorpi diversi, alcuni dei quali possono influire sugli esami del sangue
(analisi sierologiche).
► Prima di essere sottoposto a qualsiasi esame del sangue, informi il medico del trattamento
con HyQvia.
Informazioni sul materiale originario di HyQvia
L’immunoglobulina umana normale 10% di HyQvia e l’albumina sierica umana (un componente
della ialuronidasi umana ricombinante) sono prodotte da plasma umano (la parte liquida del sangue).
Quando i medicinali sono prodotti con sangue o plasma umano, vengono adottate determinate misure
per impedire la trasmissione di infezioni ai pazienti, tra cui:
- attenta selezione dei donatori di sangue e plasma, per garantire l’esclusione di coloro che sono a rischio di trasmissione di infezioni,
- analisi di ciascuna donazione e dell’insieme delle donazioni di sangue e plasma per rilevare segni di virus/infezioni.
I produttori di tali medicinali includono anche fasi di lavorazione del sangue e del plasma che
possono inattivare o rimuovere i virus. Malgrado tali misure, quando vengono utilizzati medicinali
derivati da sangue o plasma umano, la possibilità di trasmissione di infezioni non può essere
totalmente esclusa. Ciò si applica anche a virus sconosciuti o emergenti o ad altri tipi di infezione.
Le misure adottate per la produzione di HyQvia sono considerate efficaci per virus capsulati, come
il virus dell’immunodeficienza umana (HIV), il virus dell’epatite B e il virus dell’epatite C, nonché
per i virus non capsulati dell’epatite A e il parvovirus B19.
Le immunoglobuline non sono state associate a infezioni da epatite A o da parvovirus B19,
probabilmente perché gli anticorpi contro queste infezioni, contenuti in HyQvia, esercitano un effetto
protettivo.
► Si raccomanda vivamente, ogni volta che si usa HyQvia, di registrare nel diario del
trattamento i seguenti dati:
- il nome del prodotto
- la data di somministrazione
- il numero di lotto del medicinale,
- il volume iniettato, la velocità di infusione, il numero e la posizione delle sedi di infusione.
Bambini e adolescenti
Terapia sostitutiva
Per i bambini e gli adolescenti (di età compresa tra 0 e 18 anni) si applicano le stesse indicazioni, dose
e frequenza di infusione impiegate negli adulti.
Terapia immunomodulante nei pazienti con CIDP
La sicurezza e l’efficacia di HyQvia nei bambini e negli adolescenti (di età compresa tra 0 e 18 anni)
con CIDP non sono state stabilite.
Altri medicinali e HyQvia
Informi il medico, il farmacista o l’infermiere se sta assumendo, ha recentemente assunto o potrebbe
assumere qualsiasi altro medicinale.
Vaccinazioni
HyQvia può ridurre l’effetto di alcuni vaccini antivirali quali quelli anti-morbillo, anti-rosolia,
anti-parotite e anti-varicella (vaccini contenenti virus vivi). Pertanto, dopo la somministrazione
di HyQvia, è necessario far passare un intervallo di 3 mesi prima di procedere alla vaccinazione
con certi vaccini. Per il morbillo, potrebbe essere necessario attendere anche 1 anno.
► Informi del trattamento con HyQvia il medico o l’infermiere che somministra il vaccino.
Gravidanza, allattamento e fertilità
I dati sugli effetti dell’uso a lungo termine della ialuronidasi umana ricombinante su gravidanza,
allattamento e fertilità sono limitati. HyQvia deve essere utilizzato da donne in gravidanza e che
allattano solo dopo averne discusso con il proprio medico.
Guida di veicoli e utilizzo di macchinari
I pazienti potrebbero manifestare effetti indesiderati, come capogiro o nausea, durante il trattamento
con HyQvia che possono influire sulla capacità di guidare veicoli, di andare in bicicletta o di usare
macchinari. Nel caso in cui si verifichino tali reazioni, occorre che lei o il suo bambino attendiate che
scompaiano prima di riprendere queste attività. Se lei o il suo bambino manifesta un qualsiasi effetto
indesiderato, si rivolga al medico.
HyQvia contiene sodio
Questo medicinale contiene da 5,0 a 60,5 mg di sodio (componente principale del sale da cucina) in
ciascun flaconcino di HyQvia contenente ialuronidasi umana ricombinante. Questo equivale allo
0,25-3% dell’assunzione massima giornaliera raccomandata con la dieta di un adulto. Il componente
IG 10% è essenzialmente senza sodio.
3. Come usare HyQvia
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico. Se ha dubbi consulti il
medico.
HyQvia deve essere infuso sotto la pelle (somministrazione sottocutanea o SC).
Il trattamento con HyQvia sarà iniziato dal medico o dall’infermiere, ma potrebbe esserle consentito
di usare il medicinale a casa dopo che le saranno state somministrate le prime infusioni sotto
supervisione medica e quando lei (e/o la persona che si prende cura di lei) avrà ricevuto un
addestramento adeguato. Lei e il medico deciderete se può usare HyQvia a casa. Non inizi
il trattamento con HyQvia a casa senza aver ricevuto istruzioni complete sul suo utilizzo.
Dosaggio
Terapia sostitutiva
Il medico calcolerà la dose corretta per lei in base al suo peso corporeo, a eventuali trattamenti
precedenti che possono esserle stati somministrati e alla sua risposta al trattamento. La dose iniziale
raccomandata fornisce 400-800 mg di principio attivo per kg di peso corporeo al mese. All’inizio le
sarà somministrato un quarto di questa dose a intervalli di 1 settimana. Con le infusioni successive,
la dose verrà aumentata e somministrata a intervalli di 3-4 settimane. A volte il medico può
raccomandare che dosi maggiori siano suddivise e somministrate in 2 sedi. Il medico può modificare
la dose anche in base alla sua risposta al trattamento.
Terapia immunomodulante
Il medico calcolerà la dose corretta per lei in base ai trattamenti precedenti ricevuti e alla sua risposta
al trattamento. La terapia inizia generalmente 1-2 settimane dopo l’ultima infusione di
immunoglobuline, somministrata per via sottocutanea alla dose equivalente settimanale calcolata. Il
medico può modificare la dose e la frequenza in base alla risposta al trattamento.
Nel caso in cui venga superata la dose massima giornaliera (> 120 g) o se non tollera il volume di
infusione di immunoglobuline, la dose può essere suddivisa e somministrata in più giorni, con un
intervallo di 48--72 ore tra le somministrazioni ai fini di un corretto assorbimento; anche la
somministrazione della ialuronidasi dovrebbe essere suddivisa in modo appropriato.
Inizio del trattamento
Il trattamento sarà iniziato da un medico o un infermiere esperto nel trattamento di pazienti con
sistema immunitario debole (immunodeficienza) e CIDP allo scopo di addestrare questi pazienti al
trattamento domiciliare. Sarà tenuto in osservazione attentamente durante l’intera infusione e per
almeno 1 ora dopo l’interruzione dell’infusione per verificare come sopporta il medicinale. All’inizio,
il medico o l’infermiere userà una velocità di infusione lenta e la aumenterà gradualmente durante la
prima infusione e nelle infusioni successive. Non appena il medico o l’infermiere avrà stabilito la dose
e la velocità di infusione corrette per lei, potrebbe esserle permesso di somministrarsi il trattamento a
domicilio in autonomia.
Trattamento domiciliare
Non utilizzi HyQvia a casa finché non riceve le istruzioni e la formazione dall’operatore sanitario.
Le verranno insegnati:
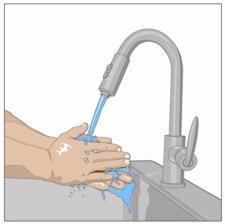
- L’uso di tecniche di infusione senza germi (asettiche),
- L’uso di una pompa di infusione o di una siringa temporizzata (se necessaria),
- Il mantenimento di un diario del trattamento
- Le misure da adottare in caso di effetti indesiderati gravi.
Deve seguire attentamente le istruzioni del medico in merito alla dose, alla velocità di infusione
e allo schema di infusione di HyQvia in modo che il trattamento le risulti efficace.
Si raccomandano le seguenti velocità di infusione per l’IG 10% per sede di infusione:
Le velocità di infusione di cui sopra si riferiscono a una singola sede di infusione. Nel caso in cui il
paziente necessiti di 2 o 3 sedi di infusione, le velocità di infusione possono essere regolate di
conseguenza (ovvero, raddoppiate o triplicate in base alla velocità di infusione massima della pompa).
Se ha una perdita in sede di infusione
Chieda al medico, al farmacista o all’infermiere se sarebbe più appropriato un ago di un’altra
dimensione.
Qualsiasi cambiamento di dimensione dell’ago deve essere supervisionato dal medico curante.
Se usa più HyQvia di quanto deve
Se pensa di aver usato più HyQvia di quanto deve, contatti il medico appena possibile.
Se dimentica di usare HyQvia
Non usi una dose doppia di HyQvia per compensare la dimenticanza della dose. Se pensa di aver
dimenticato una dose, contatti il medico appena possibile.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico, al farmacista
o all’infermiere.
| Soggetti < 40 kg | Soggetti ≥ 40 kg | |||
| Intervallo/minuti | Prime 2 infusioni (mL/ora/sede di infusione) | 2-3 infusioni successive (mL/ora/sede di infusione) | Prime 2 infusioni (mL/ora/sede di infusione) | o 2-3 infusioni c successive (mL/ora/sede di infusione) |
| 10 minuti | 5 | 10 | 10 | a 10 |
| 10 minuti | 10 | 20 | 30 | 30 |
| 10 minuti | 20 | 40 | 60 | m 120 |
| 10 minuti | 40 | 80 | 120 | 240 |
| Resto dell’infusione | 80 | 160 | r 240 | 300 |
Nel paragrafo successivo sono fornite istruzioni dettagliate per l’uso.
| a r m a c o |
d
| |
a
|  |
i
|  |
a
|  |
| a r m a c o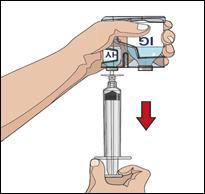 |
n
| 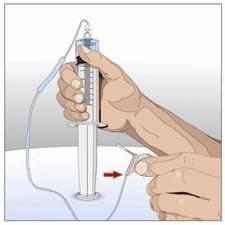 |
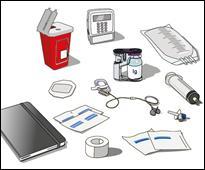
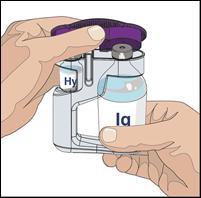
8. Preparare il flaconcino di immunoglobulina umana
normale 10%:
- Preparare il trasferimento del componente immunoglobulina 10% di HyQvia sfregando il tappo di ogni flaconcino con un tampone separato inumidito con alcool, se istruiti in tal senso, e lasciare asciugare all’aria (almeno 30 secondi).
- L’immunoglobulina umana normale 10% di HyQvia può essere infusa: trasferendo il contenuto dei flaconcini nella siringa più grande ( a) o in una sacca per infusione ( b), in base alle istruzioni dell’operatore sanitario, a seconda della pompa in uso; o direttamente dal flaconcino IG. Inserire la punta del tubo della pompa con sfiato o una punta e ago con sfiato nel flaconcino o nei flaconcini di immunoglobulina umana normale 10%. Riempire il tubo della pompa di somministrazione e metterlo da parte fino a quando sarà terminata la somministrazione della ialuronidasi umana ricombinante.
- Se occorre più di un flaconcino per una dose intera, utilizzare i flaconcini successivi dopo la somministrazione del primo.
- (a)(b)
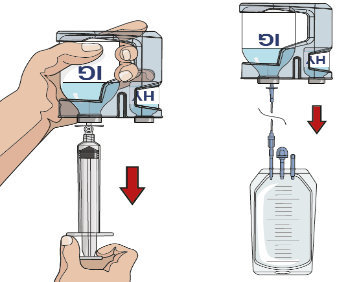
9. Preparare la pompa:
Seguire le istruzioni del produttore per preparare la pompa.
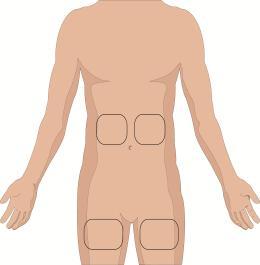
10. Preparare la sede di infusione:
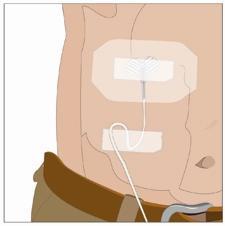
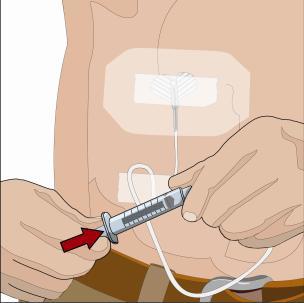
- Scegliere una o più sedi di infusione nella parte centrale o superiore dell’addome o nelle cosce. Vedere l’immagine per le posizioni delle sedi di infusione. Scegliere sedi di infusione su lati opposti del corpo se si sono ricevute istruzioni di somministrare in due sedi per dosi superiori a 600 mL. Se si utilizzano tre sedi, queste devono essere distanti tra loro 10 cm.
- Evitare aree ossute, vasi sanguigni visibili, cicatrici e aree infiammate o infette.
- Alternare le sedi di infusione scegliendo lati opposti del corpo tra un’infusione e l’altra.
- Se istruiti in tal senso dall’operatore sanitario, pulire la sede o le sedi di infusione con un tampone inumidito con alcool. Lasciare asciugare (almeno 30 secondi).
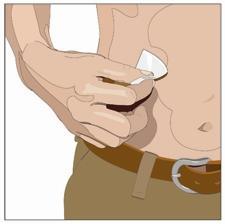
| Angolo di 90 gradi con la pelle o c a m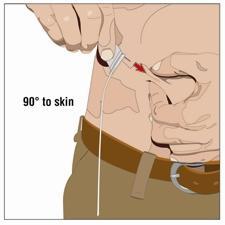 |
| a r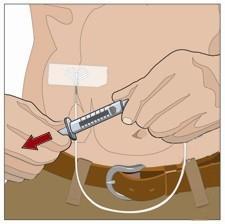 |
l e
|  |
n
|  |
z
|
| o |
| a r m a c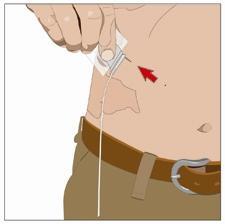 |
|
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino. Alcuni effetti indesiderati, quali mal di testa, brividi o dolori nel corpo, possono essere
ridotti rallentando la velocità di infusione.
Effetti indesiderati gravi
Le infusioni di medicinali come HyQvia talvolta possono causare reazioni allergiche rare, ma gravi.
Si potrebbe manifestare un abbassamento improvviso della pressione del sangue e, in casi isolati,
shock anafilattico. I medici sono al corrente di questi possibili effetti indesiderati e la controlleranno
durante e dopo le infusioni iniziali.
Segni e sintomi tipici comprendono: sensazione di confusione mentale, capogiro o svenimento,
eruzione cutanea e prurito, gonfiore della bocca o della gola, respirazione difficoltosa, respiro
sibilante, frequenza cardiaca anormale, dolore toracico, colore blu delle labbra o delle dita delle mani
e dei piedi, visione annebbiata.
Se nota uno di questi segni durante l’infusione, lo comunichi immediatamente al medico
o all’infermiere.
Quando usa HyQvia a casa, deve eseguire l’infusione in presenza di una persona che si prende cura di
lei che la aiuterà a osservare la comparsa di reazioni allergiche, interrompere l’infusione e chiedere
aiuto, se necessario.
HyQvia a casa.
Effetti indesiderati molto comuni (possono interessare più di 1 infusione su 10):
Reazioni locali, presso la sede di infusione (comprende tutte le reazioni a livello delle sedi di infusione
elencate di seguito). Queste reazioni in genere scompaiono dopo qualche giorno.
Effetti indesiderati comuni (possono interessare fino a 1 infusione su 10):
- mal di testa
- nausea
- reazioni nella sede di infusione inclusi dolore, fastidio, dolorabilità, arrossamento, gonfiore e prurito
- sensazione di caldo, febbre
- debolezza (astenia), stanchezza, mancanza di energia (letargia) e malessere generale (disagio)
Effetti indesiderati non comuni (possono interessare fino a 1 infusione su 100):
- capogiro
- emicrania
- sensazioni come intorpidimento, formicolio, pizzicamento (parestesia)
- battito cardiaco accelerato (tachicardia)
- pressione arteriosa alta (ipertensione)
- dolore addominale/dolorabilità addominale
- gonfiore dello stomaco (distensione addominale)
- diarrea
- vomito
- arrossamento della pelle (eritema)
- eruzione cutanea
- prurito
- eruzione cutanea pruriginosa (orticaria)
- dolore muscolare (mialgia)
- dolori articolari (artralgia)
- mal di schiena
- dolore alle estremità (compreso fastidio agli arti)
- dolore toracico muscoloscheletrico
- rigidità articolare
- reazioni in sede di infusione (quali colorazione anormale, lividi, arrossamento (ematoma), sanguinamento (emorragia), perforazione di vasi sanguigni, massa (nodulo), indurimento, gonfiore (edema), brividi, sensazione di bruciore, eruzione cutanea)
- gonfiore ai genitali
Effetti indesiderati rari (possono interessare fino a 1 infusione su 1 000):
- agitazione (tremore)
- ictus
- pressione arteriosa bassa (ipotensione)
- difficoltà respiratorie (dispnea)
- dolore all’inguine
- urine marroni (emosiderinuria)
- sudorazione eccessiva (iperidrosi)
- infiammazione nella sede di infusione
- calore nella sede di infusione
- sensazioni quali intorpidimento, formicolio, pizzicamento nella sede di infusione (parestesia nella sede di infusione)
- esito positivo del test di coombs
Frequenza non nota (la frequenza non può essere definita sulla base dei dati disponibili):
- infiammazione delle membrane che circondano il cervello e il midollo spinale (meningite asettica)
- reazioni allergiche (ipersensibilità)
- perdita in sede di infusione
- malattia simil-influenzale
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’allegato V. Segnalando gli effetti
indesiderati, può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare HyQvia
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sull’etichetta e sulla scatola
dopo Scad. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2 °C – 8 °C). Non congelare.
Il prodotto può essere tenuto fuori dal frigorifero per un massimo di 3 mesi e conservato ad una
temperatura superiore a +8 °C e inferiore a +25 °C. Non refrigerare una volta conservato a temperatura
ambiente. Smaltire dopo 3 mesi a temperatura ambiente o al raggiungimento della data di scadenza, a
seconda di quale evento si verifica prima.
Annotare sulla confezione esterna la data in cui il prodotto viene estratto dal frigorifero.
Non agitare.
Tenere i flaconcini nell’imballaggio esterno per proteggerli dalla luce.
Non usi questo medicinale se nota che le soluzioni sono torbide o presentano particelle o depositi.
Dopo l’apertura, scartare eventuali soluzioni non utilizzate rimaste nei flaconcini.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene HyQvia
HyQvia è un’unità a doppio flaconcino contenente:
- una soluzione di ialuronidasi umana ricombinante (fase 1 di HyQvia/eseguire l’infusione di questo flaconcino per primo) e
- una soluzione di immunoglobulina umana normale 10% (fase 2 di HyQvia/eseguire l’infusione di questo flaconcino per secondo).
Di seguito è descritto il contenuto di ciascun flaconcino:
- 1. Ialuronidasi umana ricombinante
Questo flaconcino contiene ialuronidasi umana ricombinante.
Gli altri componenti sono sodio cloruro, sodio fosfato, albumina umana, acido
etilenediaminetetracetico (EDTA) disodico, cloruro di calcio e acqua per preparazioni iniettabili
(vedere anche paragrafo 2, “HyQvia contiene sodio”).
- 2. Immunoglobulina umana normale 10%
Un mL di soluzione di questo flaconcino contiene 100 mg di immunoglobulina umana normale, di cui
almeno il 98% è immunoglobulina G (IgG).
Il principio attivo di HyQvia è l’immunoglobulina umana normale. Questo medicinale contiene tracce
di immunoglobulina A (IgA) (non più di 140 microgrammi/mL, in media 37 microgrammi).
Gli altri componenti di questo flaconcino sono glicina e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di HyQvia e contenuto della confezione
HyQvia 100 mg/mL soluzione per infusione per uso sottocutaneo (infusa sotto la pelle)
HyQvia è fornito in una confezione contenente:
- un flaconcino di vetro di ialuronidasi umana ricombinante e
- un flaconcino di vetro di immunoglobulina umana normale 10%.
La ialuronidasi umana ricombinante è una soluzione limpida e incolore.
L’immunoglobulina umana normale 10% è una soluzione limpida e incolore o giallo chiaro.
Sono disponibili le seguenti confezioni:
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Titolare dell’autorizzazione all’immissione in commercio:
Baxalta Innovations GmbH
Industriestrasse 67
A-1221 Vienna
Austria
Produttore:
Baxalta Belgium Manufacturing SA
Boulevard René Branquart 80
B-7860 Lessines
Belgio
| Ialuronidasi umana ricombinante | n Immunoglobulina umana normale 10% | |
| Volume (mL) | Proteine (g) | Volume (mL) |
| a 1,25 | 2,5 | 25 |
| 2,5 | 5 | 50 |
| i 5 | 10 | 100 |
| l 10 | 20 | 200 |
| a 15 | 30 | 300 |
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Takeda Belgium NV
Tél/Tel: +32 2 464 06 11
[email protected]
Lietuva
Takeda, UAB
Tel: +370 521 09 070
[email protected]
България
Такеда България ЕООД
Тел.: +359 2 958 27 36
[email protected]
Luxembourg/Luxemburg
Takeda Belgium NV
Tél/Tel: +32 2 464 06 11
[email protected]
Česká republika
Takeda Pharmaceuticals Czech Republic s.r.o.
Tel: +420 234 722 722
[email protected]
Magyarország
Takeda Pharma Kft.
Tel: +36 1 270 7030
[email protected]
Danmark
Takeda Pharma A/S
Tlf.: +45 46 77 10 10
[email protected]
Malta
Drugsales Ltd
Tel: +356 21419070
[email protected]
Deutschland
Takeda GmbH
Tel: +49 (0)800 825 3325
[email protected]
Nederland
Takeda Nederland B.V.
Tel: +31 20 203 5492
[email protected]
Eesti
Takeda Pharma OÜ
Tel: +372 6177 669
[email protected]
Norge
Takeda AS
Tlf: +47 800 800 30
[email protected]
Ελλάδα
Τakeda ΕΛΛΑΣ Α.Ε.
Tηλ: +30 210 6387800
[email protected]
Österreich
Takeda Pharma Ges.m.b.H.
Tel: +43 (0) 800-20 80 50
[email protected]
España
Takeda Farmacéutica España, S.A.
Tel: +34 917 90 42 22
[email protected]
Polska
Takeda Pharma Sp. z o.o.
Tel: +48223062447
[email protected]
France
Takeda France SAS
Tél. + 33 1 40 67 33 00
[email protected]
Portugal
Takeda Farmacêuticos Portugal, Lda.
Tel: + 351 21 120 1457
[email protected]
Hrvatska
Takeda Pharmaceuticals Croatia d.o.o.
Tel: +385 1 377 88 96
[email protected]
România
Takeda Pharmaceuticals SRL
Tel: +40 21 335 03 91
[email protected]
Ireland
Takeda Products Ireland Ltd
Tel: 1800 937 970
[email protected]
Slovenija
Takeda Pharmaceuticals farmacevtska družba d.o.o.
Tel: + 386 (0) 59 082 480
[email protected]
Ísland
Vistor ehf.
Sími: +354 535 7000
[email protected]
Slovenská republika
Takeda Pharmaceuticals Slovakia s.r.o.
Tel: +421 (2) 20 602 600
[email protected]
Italia
Takeda Italia S.p.A.
Tel: +39 06 502601
[email protected]
Suomi/Finland
Takeda Oy
Puh/Tel: 0800 774 051
[email protected]
Κύπρος
Proton Medical (Cyprus) Ltd
Τηλ: +357 22866000
[email protected]
Sverige
Takeda Pharma AB
Tel: 020 795 079
[email protected]
Latvija
Takeda Latvia SIA
Tel: +371 67840082
[email protected]
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, http://www.ema.europa.eu/
- Paese di registrazione
- Forma farmaceuticaSoluzione per infusione, 100 MG/ML
- Codice ATCJ06BA01
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a HYQVIAForma farmaceutica: Soluzione iniettabile, 165 MG/MLPrincipio attivo: immunoglobulins, normal human, for extravascular adm.Produttore: OCTAPHARMA ITALY S.P.A.Prescrizione richiestaForma farmaceutica: Soluzione iniettabile, 200 MG/MLPrincipio attivo: immunoglobulins, normal human, for extravascular adm.Produttore: BAXALTA INNOVATIONS GMBHPrescrizione richiestaForma farmaceutica: Soluzione iniettabile, 200 MG/MLPrincipio attivo: immunoglobulins, normal human, for extravascular adm.Produttore: CSL BEHRING GMBHPrescrizione richiesta
Medici online per HYQVIA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di HYQVIA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per HYQVIA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.














