
Come usare SPIKEVAX (EX COVID-19 VACCINE MODERNA)
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Spikevax 0,2 mg/mL dispersione per preparazione iniettabile, 0,1 mg/mL dispersione per preparazione iniettabile, 50 microgrammi dispersione iniettabile in siringa preriempita
Vaccino a mRNA anti-COVID-19
elasomeran
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di ricevere questo vaccino perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Spikevax e a cosa serve
- 2. Cosa deve sapere prima di ricevere Spikevax
- 3. Come viene somministrato Spikevax
- 4. Possibili effetti indesiderati
- 5. Come conservare Spikevax
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Spikevax e a cosa serve
Spikevax è un vaccino usato per prevenire il COVID-19, malattia causata dal coronavirus SARS-CoV-
- 2. Viene somministrato ad adulti e bambini di età pari o superiore a 6 mesi. Il principio attivo di Spikevax è l’mRNA che codifica per la proteina spike del SARS-CoV-2. L’mRNA è inserito in nanoparticelle lipidiche SM-102.
Poiché Spikevax non contiene il virus, non può provocare il COVID-19.
Come funziona il vaccino
Spikevax stimola le naturali difese dell’organismo (il sistema immunitario). Il vaccino induce
l’organismo a produrre una protezione (anticorpi) contro il virus che causa il COVID-19. Spikevax
utilizza una sostanza chiamata acido ribonucleico messaggero (mRNA) per trasportare una serie di
istruzioni che le cellule del corpo possono utilizzare per creare la proteina spike presente anche sul
virus. Le cellule producono quindi anticorpi contro la proteina spike per contribuire a combattere il
virus. Questo aiuta a proteggersi dal COVID-19.
2. Cosa deve sapere prima di ricevere Spikevax
Il vaccino non deve essere somministratose è allergicoal principio attivo o ad uno qualsiasi degli
altri componenti di questo vaccino (elencati al paragrafo 6).
Avvertenze e precauzioni
Si rivolga al medico, al farmacista o all’infermiere prima di ricevere Spikevax se:
- ha già avuto in passato una reazione allergicagrave, potenzialmente letale, dopo qualsiasi altra iniezione di un vaccino o dopo la somministrazione di Spikevax..
- ha un sistema immunitario molto debole o compromesso.
- ha avuto in precedenza uno svenimento a seguito di un’iniezione con un ago.
- soffre di un disturbo della coagulazione.
- ha febbre alta o un’infezione grave; tuttavia può ricevere la vaccinazione se ha una leggera febbre o una leggera infezione delle vie respiratore come ad esempio un raffreddore.
- ha una malattia grave.
- soffre di ansia associata alle iniezioni.
Dopo la vaccinazione con Spikevax esiste un maggiore rischio di miocardite (infiammazione del
cuore) e pericardite (infiammazione del rivestimento esterno del cuore) (vedere paragrafo 4).
Queste condizioni possono svilupparsi pochi giorni dopo la vaccinazione e si sono verificate
principalmente entro 14 giorni. Sono state osservate più spesso in maschi giovani, e più spesso dopo la
seconda dose rispetto alla prima dose.
La maggior parte dei casi di miocardite e pericardite si risolve. Alcuni casi hanno richiesto una terapia
intensiva e si sono osservati casi fatali.
Dopo la vaccinazione presti particolare attenzione ai segni di miocardite e pericardite, quali respiro
corto, palpitazioni e dolore toracico, e si rivolga immediatamente al medico in caso di comparsa di tali
sintomi.
Se rientra in una qualsiasi delle condizioni sopra descritte (o se ha dei dubbi) si rivolga al medico, al
farmacista o all’infermiere prima di ricevere Spikevax.
Riacutizzazioni della sindrome da perdita capillare (CLS)
Sono stati segnalati alcuni casi di riacutizzazioni della sindrome da perdita capillare a seguito della
vaccinazione con Spikevax. Tale affezione provoca perdita di liquido da piccoli vasi sanguigni
(capillari) con conseguente rapido gonfiore delle braccia e delle gambe, aumento improvviso del peso
e sensazione di svenimento, bassa pressione sanguigna. Se in precedenza ha manifestato episodi di
CLS, si rivolga al medico prima della somministrazione di Spikevax.
Durata della protezione
Come con qualsiasi vaccino, il ciclo primario di vaccinazione di 2 dosi di Spikevax potrebbe non
proteggere completamente tutti coloro che lo ricevono, né è nota la durata del periodo di copertura.
Bambini
Spikevax non è raccomandato nei bambini di età inferiore a 6 mesi.
Altri medicinali e Spikevax
Informi il medico o il farmacista se sta assumendo, ha recentemente assunto o potrebbe assumere
qualsiasi altro medicinale. Spikevax può influenzare la modalità di azione di altri medicinali e altri
medicinali possono influenzare la modalità di azione di Spikevax.
Soggetti immunocompromessi
Se è una persona immunocompromessa, potrebbe ricevere una terza dose di Spikevax. L’efficacia di
Spikevax anche dopo una terza dose potrebbe essere inferiore nelle persone immunocompromesse.
In tal caso, dovrà continuare a prendere le precauzioni fisiche per contribuire a prevenire COVID-
- 19. Se opportuno, inoltre, i suoi contatti stretti dovranno essere vaccinati. Parli con il medico delle raccomandazioni più adatte a lei.
Gravidanza e allattamento
Se è in corso una gravidanza o se sospetta una gravidanza, informi il medico, l’infermiere o il
farmacista prima di ricevere questo vaccino. Spikevax può essere usato durante la gravidanza. Un
ampio numero di dati relativi a donne in gravidanza vaccinate con Spikevax durante il secondo e terzo
trimestre di gestazione non ha mostrato effetti negativi sulla gravidanza o sul neonato. Sebbene i dati
relativi agli effetti sulla gravidanza o sul neonato dopo la somministrazione del vaccino durante il
primo trimestre di gestazione siano limitati, non è stata osservata alcuna variazione del rischio di
aborti spontanei.
Spikevax può essere somministrato durante l’allattamento.
Guida di veicoli e utilizzo di macchinari
Eviti di guidare o di utilizzare macchinari se non si sente bene dopo la vaccinazione. Aspetti che
eventuali effetti del vaccino siano scomparsi prima di guidare o utilizzare macchinari.
Spikevax contiene sodio
Questo medicinale contiene meno di 1 mmol di sodio (23 mg) per dose, cioè essenzialmente “senza
sodio”.
3. Come viene somministrato Spikevax
Tabella 1. Posologia di Spikevax per il ciclo primario, terza dose nei soggetti gravemente
immunocompromessi e dosi di richiamo
| Dosaggio | Tipo di vaccinazione | Età | l Dose | Raccomandazioni |
| Spikevax 0,2 mg/mL dispersione per preparazione iniettabile e g A | Ciclo primario i l a t | Soggetti con età pari o superiore a 12 anni a | e 2 (due) dosi d (0,5 mL ciascuna, contenenti 100 microgrammi di mRNA). | Si raccomanda di somministrare la seconda dose 28 giorni dopo la prima. |
| n Bambini di età a compresa tra 6 e 11 anni | 2 (due) dosi (0,25 mL ciascuna, contenenti 50 microgrammi di mRNA, ossia metà della dose del ciclo primario per i soggetti di età pari o superiore a 12 anni) | |||
| I Terza dose in soggetti a gravemente immunocompromessi i z n | Soggetti con età pari o superiore a 12 anni | 1 (una) dose da 0,5 mL, contenente 100 microgrammi di mRNA | Una terza dose può essere somministrata almeno 28 giorni dopo la seconda dose. | |
| Bambini di età compresa tra 6 e 11 anni | 1 (una) dose da 0,25 mL, contenente 50 microgrammi di mRNA | |||
| Dose di richiamo | Soggetti con età pari o superiore a 12 anni | 1 (una) dose da 0,25 mL, contenente 50 microgrammi di mRNA | Spikevax può essere usato come richiamo in soggetti con età pari o superiore a 12 anni che hanno ricevuto un ciclo primario con Spikevax |
| Dosaggio | Tipo di vaccinazione | Età | Dose | Raccomandazioni |
| o oppure un ciclo primario c comprendente un altro vaccino a a mRNA o un vaccino a vettore m adenovirale almeno 3 mesi dopo il completamento del ciclo primario. | ||||
| Spikevax 0,1 mg/mL dispersione per preparazione iniettabile e Spikevax 50 microgrammi dispersione iniettabile in siringa preriempita* | Ciclo primario† | Bambini di età compresa tra 6 e 11 anni | r a 2 (due) dosi (0,5 mL ciascuna, F contenenti 50 microgrammi di mRNA ciascuna). | Si raccomanda di somministrare la seconda dose 28 giorni dopo la prima |
| Bambini di età compresa tra 6 mesi e 5 anni a n a | l 2 (due) dosi e (0,25 mL ciascuna, d contenenti 25 microgrammi di mRNA ciascuna, ossia metà della dose del ciclo primario per i bambini di età compresa tra 6 e 11 anni)* | |||
| i l Terza dose in a soggetti gravemente immunocompromessi‡ t I a i z | Bambini di età compresa tra 6 e 11 anni | 1 (una) dose da 0,5 mL, contenente 50 microgrammi di mRNA | Una terza dose può essere somministrata almeno 28 giorni dopo la seconda dose. | |
| Bambini di età compresa tra 6 mesi e 5 anni | 1 (una) dose da 0,25 mL, contenente 25 microgrammi di mRNA | |||
| g e | n Dose di richiamo | Soggetti con età pari o superiore a 12 anni | 1 (una) dose da 0,5 mL, contenente 50 microgrammi di mRNA | Spikevax può essere usato come richiamo in soggetti con età pari o superiore a 6 anni che hanno ricevuto un ciclo primario con Spikevax |
| Dosaggio | Tipo di vaccinazione | Età | Dose | Raccomandazioni |
| Bambini di età compresa tra 6 e 11 anni | 1 (una) dose da 0,25 mL contenente 25 microgrammi di mRNA* | o oppure un ciclo primario c comprendente un altro vaccino a a mRNA o un vaccino a vettore m adenovirale almeno 3 mesi dopo il completamento del ciclo primario. |
* Non utilizzare la siringa preriempita per erogare un volume parziale di 0,25 mL.
† Per il ciclo primario in soggetti di età pari o superiore a 12 anni, deve essere usato il flaconcino con
dosaggio 0,2 mg/mL.
‡Per la terza dose in soggetti gravemente immunocompromessi di età pari o superiore a 12 anni, deve
essere usato il flaconcino con dosaggio 0,2 mg/mL.
Se salta l’appuntamento per la 2dose del ciclo primario di vaccinazione con Spikevax
- Se salta l’appuntamento, fissi un nuovo appuntamento con il medico, il farmacista o l’infermiere non appena possibile.
- Se salta l’iniezione programmata, la protezione contro COVID-19 potrebbe essere incompleta.
Il medico, il farmacista o l’infermiere inietterà il vaccino in un muscolo (iniezione intramuscolare)
nella parte superiore del braccio.
Dopoogni iniezione del vaccino il medico, il farmacista o l’infermiere la terrà sotto osservazione per
almeno 15 minutiper monitorare eventuali segni di reazione allergica.
Se ha qualsiasi dubbio sull’uso di questo vaccino, si rivolga al medico, al farmacista o all’infermiere.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo vaccino può causare effetti indesiderati sebbene non tutte le persone li
manifestino.
Si rivolga urgentementea un medico se manifesta uno qualsiasi dei seguenti segni e sintomi di una
reazione allergica:
- sensazione di svenimento o stordimento;
- alterazioni del battito cardiaco;
- respiro affannoso;
- respiro sibilante;
- gonfiore della lingua, del viso o della gola;
- orticaria o eruzione cutanea;
- nausea o vomito;
- dolore allo stomaco.
Si rivolga al medico o all’infermiere se dovesse manifestarsi qualsiasi altro effetto indesiderato. Questi
possono includere:
Molto comuni(possono riguardare più di 1 persona su 10)
- gonfiore/dolorabilità sotto le ascelle
- appetito ridotto (osservato nei bambini di età compresa tra 6 mesi e 5 anni)
- irritabilità/pianto (osservati nei bambini di età compresa tra 6 mesi e 5 anni)
- mal di testa
- sonnolenza (osservata nei bambini di età compresa tra 6 mesi e 5 anni)
- nausea
- vomito
- dolore ai muscoli, alle articolazioni e rigidità
- dolore o gonfiore in corrispondenza del sito di iniezione
- arrossamento in corrispondenza del sito di iniezione (in alcuni casi può verificarsi all’incirca da 9 a 11 giorni dopo l’iniezione)
- sensazione di estrema stanchezza
- brividi
- febbre
Comuni(possono riguardare fino a 1 persona su 10)
- diarrea
- eruzione cutanea
- eruzione cutanea o orticaria in corrispondenza del sito di iniezione (in alcuni casi possono verificarsi all’incirca da 9 a 11 giorni dopo l’iniezione)
Non comuni(possono riguardare fino a 1 persona su 100)
- prurito in corrispondenza del sito di iniezione
- capogiro
- dolore allo stomaco
- pomfi sulla pelle accompagnati da prurito (orticaria) (che possono comparire subito dopo l’iniezione e fino a un massimo di due settimane circa dopo l’iniezione)
Rari(possono riguardare fino a 1 persona su 1 000)
- paralisi temporanea di un lato del viso (paralisi di Bell)
- gonfiore del viso (può manifestarsi gonfiore del viso nei soggetti che si sono precedentemente sottoposti a iniezioni cosmetiche facciali)
- diminuzione del senso del tatto o della sensibilità
- sensazione insolita sulla pelle, come sensazione di formicolio o pizzicore (parestesia)
Molto rari(possono riguardare fino a 1 persona su 10 000)
- infiammazione del cuore (miocardite) o infiammazione del rivestimento esterno del cuore (pericardite) che possono causare respiro corto, palpitazioni o dolore toracico
Frequenza non nota
- reazioni allergiche gravi con difficoltà respiratorie (anafilassi)
- reazione del sistema immunitario di aumentata sensibilità o intolleranza (ipersensibilità)
- reazione cutanea che causa macchie o chiazze rosse sulla pelle, che possono avere l’aspetto di un bersaglio o “occhio di bue” con un nucleo rosso scuro circondato da anelli rosso chiaro (eritema multiforme)
- gonfiore esteso dell’arto vaccinato
- flusso mestruale abbondante (la maggior parte dei casi appariva di natura non grave e transitoria)
- irritazione cutanea indotta da stimoli esterni quali strofinio, prurito o pressione sulla pelle (orticaria meccanica)
- irritazione cutanea pruriginosa, in rilievo, di durata superiore alle sei settimane (orticaria cronica)
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti
indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo vaccino.
5. Come conservare Spikevax
Conservi questo vaccino fuori dalla vista e dalla portata dei bambini.
Non usi questo vaccino dopo la data di scadenza che è riportata sull’etichetta dopo Scad. La data di
scadenza si riferisce all’ultimo giorno di quel mese.
Le informazioni sulla conservazione, la scadenza, l’impiego e la manipolazione sono descritte nella
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Spikevax
Tabella 2. Composizione per tipo di contenitore
| Dosaggio | Contenitore | Dose(i) | Composizione |
| Spikevax 0,2 mg/mL dispersione per preparazione iniettabile | Flaconcino multidose l a t I a | a Massimo 10 dosi n da 0,5 mL ciascuna a i | Una dose (0,5 mL) contiene 100 microgrammi di elasomeran, un vaccino a mRNA anti- COVID-19 (modificato a livello dei nucleosidi) (inserito in nanoparticelle lipidiche SM- 102). |
| Massimo 20 dosi da 0,25 mL ciascuna | Una dose (0,25 mL) contiene 50 microgrammi di elasomeran, un vaccino a mRNA anti- COVID-19 (modificato a livello dei nucleosidi) (inserito in nanoparticelle lipidiche SM- 102). | ||
| i z Spikevax 0,1 mg/mL dispersione per n preparazione iniettabile e g A | Flaconcino multidose | 5 dosi da 0,5 mL ciascuna Massimo 10 dosi da 0,25 mL ciascuna | Una dose (0,5 mL) contiene 50 microgrammi di elasomeran, un vaccino a mRNA anti- COVID-19 (modificato a livello dei nucleosidi) (inserito in nanoparticelle lipidiche SM- 102). Una dose (0,25 mL) contiene 25 microgrammi di elasomeran, un vaccino a mRNA anti- COVID-19 (modificato a livello dei nucleosidi) (inserito in nanoparticelle lipidiche SM- 102). |
| Dosaggio | Contenitore | Dose(i) | Composizione |
| c o | |||
| Spikevax 50 microgrammi dispersione iniettabile in siringa preriempita | Siringa preriempita | 1 dose da 0,5 mL Esclusivamente monouso. Non utilizzare la siringa preriempita per erogare un volume parziale di 0,25 mL. | a m Una dose (0,5 mL) contiene 50 microgrammi di elasomeran, un vaccino a mRNA anti- COVID-19 (modificato a livello r dei nucleosidi) (inserito in a nanoparticelle lipidiche SM- 102). F |
Elasomeran è un RNA messaggero (mRNA) a singola elica con cappingin 5’, prodotto mediante
trascrizione in vitrosenza l’ausilio di cellule dai corrispondenti DNA stampo, che codifica per la
proteina virale spike (S) del SARS-CoV-2 (originale).
Gli altri componenti sono SM-102 (eptadecano-9-il 8-{(2-idrossietil)[6-osso-6-
(undecilossi)esil]ammino}ottanoato), colesterolo, 1,2-distearoil-sn-glicero-3-fosfocolina (DSPC), 1,2-
dimiristoil-rac-glicero-3-metossipolietilenglicole-2000 (PEG2000-DMG), trometamolo, trometamolo
cloridrato, acido acetico, sodio acetato triidrato, saccarosio, acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Spikevax e contenuto della confezione
Spikevax 0,2 mg/mL dispersione per preparazione iniettabile
Spikevax è una dispersione di colore da bianco a biancastro, fornita in un flaconcino di vetro da 5 mL
con tappo di gomma e capsula di chiusura rimovibile in plastica rossa con sigillo in alluminio.
Confezione: 10 flaconcini multidose
Spikevax 0,1 mg/mL dispersione per preparazione iniettabile
Spikevax è una dispersione di colore da bianco a biancastro, fornita in un flaconcino di vetro da
2,5 mL con tappo di gomma e capsula di chiusura rimovibile in plastica blu con sigillo in alluminio.
Dimensioni della confezione: 10 flaconcini multidose.
Spikevax 50 microgrammi dispersione iniettabile in siringa preriempita
Spikevax è una dispersione di colore da bianco a biancastro, fornita in una siringa preriempita
(polimero olefinico ciclico) con tappo a stantuffo e capsula di chiusura (senza ago).
La siringa preriempita è confezionata in 5 blister trasparenti, contenenti ciascuno 2 siringhe
preriempite.
Dimensione della confezione: 10 siringhe preriempite
Titolare dell’autorizzazione all’immissione in commercio
MODERNA BIOTECH SPAIN, S.L.
C/ Julián Camarillo nº 31
28037 Madrid
Spagna
Produttori
Per i flaconcini multidose
Rovi Pharma Industrial Services, S.A.
Paseo de Europa, 50
28703, San Sebastián de los Reyes
Madrid
Spagna
Recipharm Monts
18 Rue de Montbazon
Monts, Francia 37260
Moderna Biotech Spain S.L.
C/ Julián Camarillo nº 31
28037 Madrid
Spagna
Per la siringa preriempita
Rovi Pharma Industrial Services, S.A.
Calle Julián Camarillo n°35
28037 Madrid
Spagna
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio.
België/Belgique/Belgien
Tél/Tel: 0800 81 460
Lietuva
Tel: 88 003 1114
България
Teл: 0800 115 4477
Luxembourg/Luxemburg
Tél/Tel: 800 85 499
Česká republika
Tel: 800 050 719
Magyarország
Tel: 06 809 87488
Danmark
Tlf.: 80 81 06 53
Malta
Tel: 8006 5066
Deutschland
Tel: 0800 100 9632
Nederland
Tel: 0800 409 0001
Eesti
Tel: 800 0044 702
Norge
Tlf: 800 31 401
Ελλάδα
Τηλ: 008004 4149571
Österreich
Tel: 0800 909636
España
Tel: 900 031 015
Polska
Tel: 800 702 406
France
Tél: 0805 54 30 16
Portugal
Tel: 800 210 256
Hrvatska
Tel: 08009614
Ireland
Tel: 1800 800 354
România
Tel: 0800 400 625
Slovenija
Tel: 080 083082
Ísland
Sími: 800 4382
Slovenská republika
Tel: 0800 191 647
Italia
Tel: 800 928 007
Suomi/Finland
Puh/Tel: 0800 774198
Κύπρος
Τηλ: 80091080
Sverige
Tel: 020 10 92 13
Latvija
Tel: 80 005 898
Eseguire la scansione con un dispositivo mobile per ottenere il foglio informativo in altre lingue.

Oppure visitare il sito https://www.ModernaCovid19Global.com
Informazioni più dettagliate su questo vaccino sono disponibili sul sito web dell’Agenzia europea per i
medicinali, https://www.ema.europa.eu .
Questo foglio è disponibile in tutte le lingue dell’Unione europea/dello Spazio economico europeo sul
sito web dell’Agenzia europea per i medicinali.
------------------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Tracciabilità
Al fine di migliorare la tracciabilità dei medicinali biologici, il nome e il numero di lotto del
medicinale somministrato devono essere chiaramente registrati.
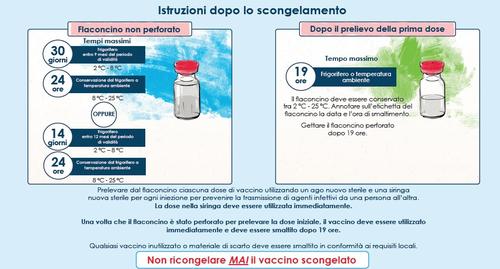
Conservazione e preparazione per la somministrazione
Spikevax deve essere somministrato da un operatore sanitario addestrato.
Una volta scongelato il vaccino è pronto per l’uso.
Non agitare né diluire.
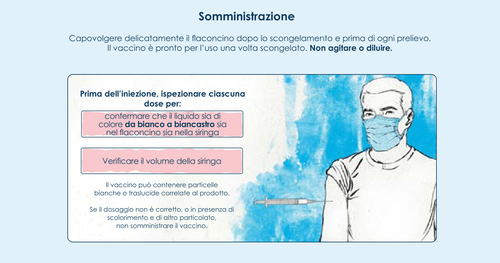
Il vaccino deve essere controllato visivamente per la presenza di particelle e scolorimento prima della
somministrazione.
Spikevax è una dispersione di colore da bianco a biancastro. Può contenere particelle bianche o
traslucide correlate al prodotto. Non somministrare il vaccino se presenta scolorimento o contiene altro
particolato.
Conservare i flaconcini e le siringhe preriempite in congelatore ad una temperatura compresa tra -
50 ºC e -15 ºC.
Tenere il flaconcino e la siringa preriempita nell’imballaggio esterno per proteggere il medicinale
dalla luce.
Spikevax 0,2 mg/mL dispersione per preparazione iniettabile (flaconcini multidose con capsula di
chiusura rimovibile rossa)
Da ogni flaconcino multidose può essere prelevato un massimo di dieci (10) dosi (da 0,5 mL ciascuna)
o un massimo di venti (20) dosi (da 0,25 mL ciascuna).
Si consiglia di perforare il tappo ogni volta in un punto diverso. Non perforare il flaconcino con
capsula di chiusura rimovibile rossa più di 20 volte.
Verificare che il flaconcino abbia la capsula di chiusura rimovibile rossa e che il nome del prodotto sia
Spikevax 0,2 mg/mL. Se il flaconcino ha la capsula di chiusura rimovibile blu e il nome del prodotto è
Spikevax bivalent Original/Omicron BA.1 o Spikevax bivalent Original/Omicron BA.4-5, si prega di
consultare il riassunto delle caratteristiche del prodotto per tale formulazione.
Scongelare ogni flaconcino multidose prima dell’uso seguendo le istruzioni riportate di seguito
(Tabella 3).
Tabella 3. Istruzioni per lo scongelamento dei flaconcini multidose prima dell’uso
| Configurazione | l Istruzioni per lo scongelamento e durata dello scongelamento | |||
| a t Temperatura I di scongelamento (in frigorifero) a | Durata dello scongelamen to | Temperatura di scongelament o (a temperatura ambiente) | Durata dello scongela mento | |
| i Flaconcino multidose | 2° – 8°C | 2 ore e 30 minuti | 15°C – 25°C | 1 ora |
Spikevax 0,1 mg/mL dispersione per preparazione iniettabile (flaconcini multidose con capsula di
chiusura rimovibile blu)
Da ogni flaconcino multidose possono essere prelevate cinque (5) dosi (da 0,5 mL ciascuna) o un
massimo di dieci (10) dosi (da 0,25 mL ciascuna).
Si consiglia di perforare il tappo ogni volta in un punto diverso.
Verificare che il flaconcino abbia la capsula di chiusura rimovibile blu e che il nome del prodotto sia
Spikevax 0,1 mg/mL. Se il flaconcino ha la capsula di chiusura rimovibile blu e il nome del prodotto è
Spikevax bivalent Original/Omicron BA.1 o Spikevax bivalent Original/Omicron BA.4-5, si prega di
consultare il riassunto delle caratteristiche del prodotto per tale formulazione.
Scongelare ogni flaconcino multidose prima dell’uso seguendo le istruzioni riportate di seguito
(Tabella 4).
Tabella 4. Istruzioni per lo scongelamento dei flaconcini multidose prima dell’uso
| i Configurazione z n | Istruzioni per lo scongelamento e durata dello scongelamento | |||
| a Temperatura di scongelamento (in frigorifero) | Durata dello scongelamen t o | Temperatura di scongelament o (a temperatura ambiente) | Durata dello s congelamento | |
| e Flaconcino multidose | 2° – 8°C | 2 ore e 30 minuti | 15°C – 25°C | 1 ora |

Spikevax 50 microgrammi dispersione iniettabile in siringa preriempita
Non agitare né diluire il contenuto della siringa preriempita.
Ogni siringa preriempita è esclusivamente monouso. Una volta scongelato, il vaccino è pronto per
l’uso.
Da ogni siringa preriempita può essere somministrata una (1) dose da 0,5 mL. Non utilizzare la siringa
preriempita per erogare un volume parziale di 0,25 mL.
Spikevax è fornito in una siringa preriempita monodose (senza ago) contenente 0,5 mL
(50 microgrammi) di mRNA e deve essere scongelato prima della somministrazione.
Durante la conservazione, ridurre al minimo l’esposizione a luce ambiente ed evitare l’esposizione alla
luce solare diretta e alla luce ultravioletta.
Scongelare ogni siringa preriempita prima dell’uso seguendo le istruzioni riportate di seguito. Le
siringhe possono essere scongelate nei blister (ogni blister contiene 2 siringhe preriempite) o nella
scatola, in frigorifero o a temperatura ambiente (Tabella 5).
Tabella 5. Istruzioni per lo scongelamento delle siringhe preriempite e delle scatole prima
dell’uso
| z n Configurazione e | Istruzioni per lo scongelamento e durata dello scongelamento | |||
| Temperatura di scongelamento (in frigorifero) (°C) | Durata dello scongelamento (minuti) | Temperatura di scongelamento (a temperatura ambiente) (°C) | Durata dello scongelamento (minuti) | |
| g Siringa preriempita nel blister |
| 55 |
| 45 |
| Scatola |
| 155 |
| 140 |
Verificare che il nome del prodotto della siringa preriempita sia Spikevax 50 microgrammi. Se il nome
del prodotto è Spikevax bivalent Original/Omicron BA.1 o Spikevax bivalent Original/Omicron BA.4-
5, si prega di consultare il riassunto delle caratteristiche del prodotto per tale formulazione.
Istruzioni per la manipolazione delle siringhe preriempite
- Non agitare.
- La siringa preriempita deve essere controllata visivamente per la presenza di particelle e scolorimento prima della somministrazione.
- Spikevax è una dispersione di colore da bianco a biancastro. Può contenere particelle bianche o traslucide correlate al prodotto. Non somministrare il vaccino se presenta scolorimento o contiene altro particolato.
- Gli aghi non sono inclusi nelle scatole delle siringhe preriempite.
- Usare un ago sterile della misura adatta per l’iniezione intramuscolare (aghi da 21 gauge o più sottili).
- Rimuovere la capsula di chiusura in posizione verticale, ruotando in senso antiorario fino a quando non si sgancia. Rimuovere la capsula di chiusura con un movimento lento e uniforme. Non tirare la capsula di chiusura mentre la si ruota.
- Inserire l’ago girando in senso orario fino a fissarlo saldamente alla siringa.
- Togliere il cappuccio dall’ago quando si è pronti per la somministrazione.
- Somministrare l’intera dose per via intramuscolare.
- Dopo lo scongelamento, non ricongelare.
Smaltimento
Il medicinale non utilizzato e i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
Dosaggio e programma
Tabella 6. Posologia di Spikevax per il ciclo primario, terza dose nei soggetti gravemente
immunocompromessi e dosi di richiamo
VaccinazioneSpikevax 0,2 mg/mL
dispersione per preparazione
iniettabile
Spikevax 0,1 mg/mL
dispersione per preparazione
iniettabile e Spikevax
50 microgrammi dispersione
per preparazione iniettabile
in siringa preriempita*
Ciclo primario
Per completare il ciclo
vaccinale si raccomanda di farsi
somministrare la seconda dose
dello stesso vaccino 28 giorni
dopo la prima dose.
Soggetti di età pari o superiore
a 12 anni
due iniezioni da 0,5 mL
Non pertinente†
Bambini di età compresa tra 6
e 11 anni
due iniezioni da 0,5 mL
Non pertinente Bambini di età compresa tra
6 mesi e 5 anni
due iniezioni da 0,25 mL*
Terza dose in soggetti
severamente
immunocompromessi
almeno 1 mese dopo la seconda
dose
Bambini di età compresa tra 6
e 11 anni
due iniezioni da 0,25 mL
Soggetti di età pari o superiore
a 12 anni
0,5 mL
Non pertinente‡
Bambini di età compresa tra 6
e 11 anni
0,25 mL
Bambini di età compresa tra 6
e 11 anni
0,5 mL
| Vaccinazione | Spikevax 0,2 mg/mL dispersione per preparazione iniettabile | Spikevax 0,1 mg/mL dispersione per preparazione o iniettabile e Spikevax 50 microgrammi dispersione c per preparazione iniettabile in siringa preriempita* |
| Non pertinente | a Bambini di età compresa tra m 6 mesi e 5 anni 0,25 mL | |
| Dose di richiamo può essere somministrata almeno 3 mesi dopo la seconda dose | Soggetti di età pari o superiore a 12 anni 0,25 mL | Soggetti di età pari o superiore r a 12 anni a 0,5 mL |
| Non pertinente | F Soggetti di età pari o superiore a 6 anni 0,25 mL* |
* Non utilizzare la siringa preriempita per erogare un volume parziale di 0,25 mL.
† Per il ciclo primario in soggetti di età pari o superiore a 12 anni, deve essere usato il flaconcino con
dosaggio 0,2 mg/mL.
‡ Per la terza dose in soggetti severamente immunocompromessi di età pari o superiore a 12 anni, deve
essere usato il flaconcino con dosaggio 0,2 mg/mL.
Come per tutti i vaccini iniettabili, devono essere sempre prontamente disponibili una supervisione
medica e trattamenti medici adeguati in caso di reazione anafilattica a seguito della somministrazione
di Spikevax.
I soggetti vaccinati devono essere tenuti sotto osservazione da un operatore sanitario per almeno
15 minuti dopo la vaccinazione.
Spikevax (tutte le diverse varianti) può essere somministrato in concomitanza con i vaccini
antinfluenzali (standard e ad alto dosaggio) e con il vaccino a subunità anti-herpes zoster (fuoco di
Sant’Antonio).
I diversi vaccini iniettabili devono essere somministrati in sedi di iniezione differenti.
Spikevax non deve essere miscelato nella stessa siringa con altri vaccini o medicinali.
Somministrazione
Il vaccino deve essere somministrato per via intramuscolare. Il sito preferito è la regione deltoidea del
braccio o, nei bambini piccoli, la parte anterolaterale della coscia. Non iniettare questo vaccino per via
intravascolare, sottocutanea o intradermica.
Flaconcini multidose
Siringhe preriempite
Usare un ago sterile della misura adatta per l’iniezione intramuscolare (da 21 gauge o più sottile).
Rimuovere la capsula di chiusura in posizione verticale, ruotando in senso antiorario fino a quando
non si sgancia. Rimuovere la capsula di chiusura con un movimento lento e uniforme. Non tirare la
capsula di chiusura mentre la si ruota. Inserire l’ago girando in senso orario fino a fissarlo saldamente
alla siringa. Togliere il cappuccio dall’ago quando si è pronti per la somministrazione. Somministrare
l’intera dose per via intramuscolare. Gettare via la siringa dopo l’uso. Esclusivamente monouso.
-

- Paese di registrazione
- Forma farmaceuticaDispersione per preparazione iniettabile, 0,5 ML
- Codice ATCJ07BN01
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a SPIKEVAX (EX COVID-19 VACCINE MODERNA)Forma farmaceutica: Dispersione per preparazione iniettabile, 30 mcgPrincipio attivo: covid-19, RNA-based vaccineProduttore: BIONTECH MANUFACTURING GMBHPrescrizione richiestaForma farmaceutica: Dispersione per preparazione iniettabile, 30 mcgPrincipio attivo: covid-19, RNA-based vaccineProduttore: BIONTECH MANUFACTURING GMBHPrescrizione richiestaForma farmaceutica: Dispersione per preparazione iniettabile, 30 mcgPrincipio attivo: covid-19, RNA-based vaccineProduttore: BIONTECH MANUFACTURING GMBHPrescrizione richiesta
Medici online per SPIKEVAX (EX COVID-19 VACCINE MODERNA)
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di SPIKEVAX (EX COVID-19 VACCINE MODERNA) — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per SPIKEVAX (EX COVID-19 VACCINE MODERNA) online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.














