
Come usare TRACLEER
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra traduzioneContenuto del foglietto illustrativo
Tracleer 62,5 mg compresse rivestite con film, 125 mg compresse rivestite con film
bosentan
Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
importanti informazioni per lei:
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista.
Contenuto di questo foglio:
- 1. Che cos’è Tracleer e a che cosa serve
- 2. Cosa deve sapere prima di prendere Tracleer
- 3. Come prendere Tracleer
- 4. Possibili effetti indesiderati
- 5. Come conservare Tracleer
- 6. Contenuto della confezione ed altre informazioni
1. Che cos’è Tracleer e a cosa serve
Le compresse di Tracleer contengono bosentan che blocca un ormone che esiste naturalmente
chiamato endotelina-1 (ET-1), che comporta un restringimento dei vasi sanguigni. Tracleer comporta,
quindi, una dilatazione dei vasi ed appartiene alla classe di medicinali denominata “antagonisti del
recettore dell’endotelina”.
Tracleer è usato per trattare:
- Ipertensione arteriosa polmonare(PAH): la PAH è una malattia caratterizzata da un severo restringimento dei vasi sanguigni del polmone con conseguente aumento di pressione nei vasi sanguigni che portano il sangue dal cuore ai polmoni (arterie polmonari). Questa pressione riduce la quantità di ossigeno che può passare nel sangue attraverso i polmoni, rendendo l’attività fisica più difficoltosa. Tracleer allarga le arterie polmonari, facilitando il pompaggio del sangue al loro interno da parte del cuore; ciò determina una riduzione della pressione sanguigna ed un’attenuazione dei sintomi.
Tracleer è usato per trattare pazienti affetti da PAH in classe III, per migliorare la capacità di esercizio
(possibilità di svolgere attività fisica) ed i sintomi. La “classe” riflette la gravità della malattia: “classe
III” comporta una marcata limitazione nell’attività fisica. Alcuni miglioramenti sono stati evidenziati
anche in pazienti PAH in classe II. “Classe II” comporta delle minori limitazioni nell’attività fisica. La
PAH per la quale Tracleer è indicato può essere:
- primaria (senza una causa identificabile o familiare);
- causata dalla sclerodermia (definita anche sclerosi sistemica, una malattia caratterizzata da un’anormale crescita del tessuto connettivo che sostiene la cute ed altri organi);
- causata da difetti congeniti (innati) del cuore con shunts (vie di passaggio anormali) che determinano un flusso anormale di sangue attraverso il cuore ed i polmoni.
- Ulcere digitali: (lesione delle dita di mani e piedi) in pazienti adulti con una condizione chiamata sclerodermia. Tracleer riduce il numero delle nuove ulcere delle dita di mani e piedi.
2. Cosa deve sapere prima di prendere Tracleer
Non prenda Tracleer:
- se è allergico al bosentano ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6)
- se ha disturbi epatici(chiedere al proprio medico)
- se è in stato di gravidanza o lo può diventarepoiché non usa metodi anticoncezionali affidabili. Per favore legga le informazioni riportate in “Contraccettivi” e in “Altri farmaci e Tracleer”
- se è in trattamento con ciclosporina A(un farmaco usato dopo un trapianto d’organo o per il trattamento della psoriasi)
In uno di questi casi, informi il suo medico.
Avvertenze e precauzioni
Esami richiesti dal medico prima del trattamento con Tracleer
- un esame del sangue per verificare la sua funzionalità epatica
- un esame del sangue per controllare la presenza di anemia (emoglobina bassa)
- un test di gravidanza se lei è una donna in età fertile In alcuni pazienti in terapia con Tracleer sono state riscontrate delle anormalità riguardo i test per la funzionalità epatica ed anemia (emoglobina bassa).
Esami che il suo dottore le prescriverà durante il trattamento
Durante il trattamento con Tracleer il medico provvederà a richiedere regolarmente esami del sangue,
in modo tale da controllare eventuali cambiamenti della funzionalità epatica e della concentrazione di
emoglobina.
Per tutti questi esami fare riferimento anche alla Carta Informativa del Paziente (contenuta nella sua
confezione di compresse di Tracleer). È importante che lei si sottoponga a questi esami del sangue ad
intervalli regolari durante l’intero periodo di somministrazione di Tracleer. Si consiglia di annotare
sulla Carta Informativa del Paziente la data dell’esame più recente e anche quella del prossimo esame
previsto (chiedere la data al medico), così da non dimenticare la data dell’esame successivo.
Esami del sangue per la funzionalità epatica
Verranno effettuati ogni mese per tutta la durata del trattamento con Tracleer. In seguito ad incremento
del dosaggio verrà effettuato un esame addizionale dopo 2 settimane.
Esami del sangue per l’anemia
Verranno effettuati ogni mese per i primi 4 mesi del trattamento e successivamente ogni 3 mesi, in
quanto i pazienti che assumono Tracleer possono sviluppare condizioni anemiche.
Se questi risultati dovessero essere anomali, il medico potrebbe decidere di ridurre la dose o
sospendere il trattamento con Tracleer ed effettuare ulteriori esami per determinarne la causa.
Bambini ed adolescenti
Tracleer non è raccomandato nei pazienti pediatrici con sclerosi sistemica ed ulcere digitali attive. Per
favore vedere anche il paragrafo 3. Come prendere Tracleer.
Altri farmaci e Tracleer
Si raccomanda di informare il medico o il farmacista nel caso lei stia assumendo o abbia recentemente
assunto altri medicinali, anche quelli acquistati senza prescrizione medica. È importante, soprattutto,
informare il medico se sta prendendo:
- ciclosporina A (un farmaco utilizzato dopo trapianti e per il trattamento della psoriasi) che non deve essere usato insieme a Tracleer.
- sirolimus o tacrolimus, che sono farmaci usati dopo trapianti, il cui uso insieme a Tracleer non è raccomandato.
- glibenclamide (un farmaco per il diabete), rifampicina (un farmaco per la tubercolosi), fluconazolo (un farmaco per il trattamento di infezioni da funghi), ketoconazolo (un farmaco usato per il trattamento della sindrome di Cushing) o nevirapina (un farmaco per l’HIV), in quanto l’uso di queste medicine insieme a Tracleer non è raccomandato.
- altri farmaci per il trattamento dell’infezione da HIV che possono richiedere un monitoraggio speciale se utilizzati insieme a Tracleer.
- contraccettivi ormonali, che non sono efficaci come unico metodo di contraccezione quando lei assume Tracleer. All’interno della confezione di compresse Tracleer troverà una Carta Informativa del Paziente che dovrà leggere attentamente. Il medico curante e/o il ginecologo stabilirà il metodo contraccettivo appropriato per lei.
- altri medicinali per il trattamento dell’ipertensione polmonare: sildenafil e tadalafil;
- warfarin (un agente anticoagulante);
- simvastatina (usata per trattare l’ipercolesterolemia).
Guida di veicoli e utilizzo di macchinari
Tracleer non altera o altera in modo trascurabile la capacità di guidare veicoli e di usare macchinari.
Tuttavia, Tracleer può indurre ipotensione (riduzione della sua pressione sanguigna) che può farla
sentire instabile e, influenzare la sua vista e la sua capacità di guidare veicoli o utilizzare macchinari.
Pertanto se lei avverte un senso di vertigine o le si offusca la vista durante il trattamento con Tracleer,
non guidi o non utilizzi strumenti o macchinari di alcun genere.
Donne in età fertile
NON assumere Tracleer se lei è in gravidanza o ha pianificato di esserlo.
Test di gravidanza
Tracleer può nuocere al nascituro concepito prima o durante il trattamento. Se lei è una donna in età
fertile, il suo medico le chiederà di effettuare un test di gravidanza prima di iniziare l’assunzione di
Tracleer e di effettuarlo, quindi, regolarmente durante il trattamento con Tracleer.
Contraccettivi
Se lei è una donna in età fertile, utilizzi un affidabile metodo di controllo della nascita (contraccettivo)
mentre prende Tracleer. Il medico o il ginecologo le consiglierà metodi contraccettivi affidabili mentre
prende Tracleer. Poiché Tracleer potrebbe rendere inefficace la contraccezione ormonale (ad esempio
contraccettivi orali, iniettabili, impiantabili o cerotti cutanei), questo metodo da solo non è affidabile.
Quindi, se lei usa contraccettivi ormonali deve usare un metodo di barriera (es. profilattico femminile,
diaframma, spugna contraccettiva oppure anche il suo partner deve utilizzare il profilattico).
All’interno della sua confezione di compresse Tracleer troverà una Carta Informativa del Paziente. Lei
dovrà riempire questa carta e portarla al suo medico alla prossima visita, in questo modo il medico
curante o il ginecologo potranno valutare se lei ha bisogno di affidabili metodi contraccettivi
addizionali o alternativi. Si raccomanda di effettuare un test di gravidanza ogni mese durante il
trattamento con Tracleer se lei è in età fertile.
Informi immediatamente il medico in caso di gravidanza subentrata durante il trattamento con Tracleer
e se si prevede di dare inizio ad una gravidanza nell’immediato futuro.
Allattamento
Tracleer passa nel latte materno. Si consiglia di interrompere l’allattamento al seno in caso venga
prescritto Tracleer in quanto non è escluso possa nuocere al suo bambino. Parli con il dottore se ha
domande su questo argomento.
Fertilità
Se lei è un uomo che assume Tracleer è possibile che questo medicinale riduca la conta degli
spermatozoi. Non si può escludere che questo potrebbe compromettere la sua possibilità di concepire
un figlio. Parli con il suo dottore se ha domande su questo argomento.
Tracleer contiene sodio
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per compressa, cioè è da considerarsi
essenzialmente ‘privo di sodio’.
3. Come prendere Tracleer
Il trattamento con Tracleer va iniziato e monitorato solo da un medico che ha esperienza nel
trattamento della PAH o della sclerosi sistemica. Prenda questo medicinale seguendo sempre
esattamente le istruzioni del medico. Se ha dubbi consulti il medico o il farmacista.
Tracleer con cibo e bevande
Tracleer può essere preso a digiuno o a stomaco pieno.
Dose raccomandata
Adulti
Negli adulti il trattamento ha inizio normalmente con l’assunzione di una compressa da 62,5 mg due
volte al giorno (mattina e sera) per le prime 4 settimane; in seguito il medico consiglierà solitamente di
assumere una compressa da 125 mg due volte al giorno a seconda della risposta a Tracleer riscontrata.
Bambini ed adolescenti
La dose raccomandata nei bambini è solo per la PAH. Per bambini di età uguale o maggiore a 1 anno
il trattamento con Tracleer ha inizio normalmente con l’assunzione di 2 mg per kg di peso corporeo
due volte al giorno (mattina e sera); il dosaggio successivo verrà consigliato dal medico.
Si prega di prendere nota che Tracleer è disponibile anche nella formulazione di compresse dispersibili
di 32 mg, che permettono una maggiore facilità di corretto dosaggio nei bambini e nei pazienti con
basso peso corporeo o con difficoltà a deglutire le compresse rivestite.
Se lei ha l’impressione che gli effetti del Tracleer siano troppo forti o troppo deboli, parli con il suo
medico allo scopo di valutare se vi è la necessità di cambiare la posologia.
Come prendere Tracleer
Assumere le compresse (mattina e sera) deglutendole con acqua. Le compresse possono essere assunte
con o senza cibo.
Se prende più Tracleer di quanto deve
In caso abbia assunto più compresse di quante prescritte, consulti immediatamente il medico.
Se si dimentica di prendere Tracleer
In caso si sia dimenticato di assumere Tracleer, prenda una compressa non appena si ricorda e poi
assuma le compresse agli orari normali. Non prenda una dose doppia per compensare eventuali
dimenticanze.
Se smette di prendere Tracleer
La sospensione improvvisa del trattamento con Tracleer potrebbe comportare un aggravamento dei
sintomi. Non sospenda tale trattamento a meno che ciò non venga richiesto dal medico. Il suo medico
potrebbe consigliarle di ridurre la dose nell’arco di alcuni giorni prima di sospendere definitivamente
il trattamento con Tracleer.
Se ha ulteriori domande sull’uso di questo medicinale si rivolga al medico o al farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Gli effetti indesiderati più gravi connessi con il Tracleer sono:
- Funzionalità del fegato anormale che può manifestarsi in più di 1 utilizzatore su 10
- Anemia (valori bassi negli esami del sangue) che può manifestarsi in 1 utilizzatore su 10. L’anemia può occasionalmente richiedere la trasfusione di sangue. I valori risultanti dagli esami del fegato e del sangue devono essere controllati durante il trattamento con Tracleer (vedere paragrafo 2). È importante che lei faccia questi controlli così come prescritto dal suo medico.
I segni di un non corretto funzionamento del suo fegato includono:
- nausea (impulso a vomitare)
- vomito
- febbre (temperatura elevata)
- dolore allo stomaco (addome)
- itterizia (ingiallimento della pelle o della sclera, ossia la parte bianca dell’occhio)
- urina di colore scuro
- prurito della pelle
- letargia o affaticamento (stanchezza o spossatezza inusuali)
- sindrome simil-influenzale (dolori alle articolazioni e ai muscoli con febbre)
Se nota uno di questi segni lo dica immediatamente al suo medico.
Altri effetti indesiderati:
Molto comuni(possono manifestarsi in più di 1 persona su 10):
- cefalea (mal di testa)
- edema (gonfiore delle gambe e delle caviglie o altri segni di ritenzione di liquidi)
Comuni(possono manifestarsi fino a 1 persona su 10):
- aspetto arrossato o arrossamento della pelle
- reazioni da ipersensibilità (che includono infiammazione della pelle, prurito e eruzione cutanea)
- malattia da reflusso gastroesofageo (reflusso acido)
- diarrea
- sincope (svenimento)
- palpitazioni (battiti del cuore veloci o irregolari)
- pressione sanguigna bassa
- congestione nasale
Non comuni(possono manifestarsi fino a 1 persona su 100):
- trombocitopenia (basso numero di piastrine nel sangue)
- neutropenia/leucopenia (basso numero di globuli bianchi)
- Valori elevati di funzionalità epatica associati a epatite (infiammazione del fegato) inclusa possibile esacerbazione dell’epatite sottostante e/o itterizia (ingiallimento della cute o della parte bianca dell’occhio)
Rari(possono manifestarsi fino a 1 persona su 1 000):
- anafilassi (reazione allergica generale), angioedema (gonfiore, più comune intorno ad occhi, labbra, lingua o gola)
- cirrosi (cicatrizzazione) del fegato, insufficienza epatica grave (grave alterazione della funzionalità del fegato), epatite autoimmune (infiammazione del fegato causata dal sistema di difesa dell’organismo che attacca le cellule del fegato), che può manifestarsi anche diversi mesi o anni dopo l'inizio del trattamento.
È stata inoltre riferita visione annebbiata, con una frequenza non nota (la frequenza non può essere
definita sulla base dei dati disponibili).
Effetti indesiderati aggiuntivi nei bambini e adolescenti
Gli effetti indesiderati che sono stati riportati nei bambini trattati con Tracleer sono gli stessi di quelli
degli adulti.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema
nazionale di segnalazione riportato nell’Allegato V. Segnalando gli effetti indesiderati lei può
contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Tracleer
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola e sul blister dopo
“Scad”.
Per i flaconi in polietilene bianco ad alta densità, utilizzare entro 30 giorni dalla prima apertura.
Per i blister in PVC/PE/PVDC/alluminio:
Non conservare a temperatura superiore ai 25 °C.
Per i flaconi in polietilene bianco ad alta densità:
Questo medicinale non richiede alcuna condizione particolare di conservazione.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista
come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione ed altre informazioni
Cosa contiene Tracleer
- Tracleer 62,5 mg compresse rivestite con film:Il principio attivo è il bosentan monoidrato. Ogni compressa contiene 62,5 mg di bosentan (monoidrato).
- Tracleer 125 mg compresse rivestite con film:Il principio attivo è il bosentan monoidrato. Ogni compressa contiene 125 mg di bosentan (monoidrato).
- Gli altri componentiall’interno della compressa sono: amido di mais, amido pregelatinizzato, sodio amido-glicolato (Tipo A), povidone, glicerolo dibeenato e magnesio stearato. Ilrivestimento in filmcontiene ipromellosa, glicerolo triacetato, talco, titanio diossido (E171), ferro ossido giallo (E172), ferro ossido rosso (E172) ed etilcellulosa.
Descrizione dell’aspetto di Tracleer e contenuto della confezione
Tracleer 62,5 mg compresse rivestite con film:
Tracleer 62,5 mg compresse rivestite con film sono compresse rivestite con film, rotonde, arancioni-
bianche con impresso la scritta “62,5” su un lato.
Blister PVC/PE/PVDC/alluminiocontenenti 14 compresse rivestite con film. Le scatole
contengono 14, 56 o 112 compresse rivestite con film (Tracleer 62,5 mg compresse rivestite con film).
Flaconi in polietilene ad alta densità bianchi con gel di silice come essiccante, contenenti 56
compresse rivestite con film. Gli astucci di cartone contengono 56 compresse rivestite con film
(Tracleer 62,5 mg compresse rivestite con film).
Non ingoiare l’essiccante.
Tracleer 125 mg compresse rivestite con film:
Tracleer 125 mg compresse rivestite con film sono compresse rivestite con film, ovali, arancioni-
bianche con impresso la scritta “125” su un lato.
Blister PVC/PE/PVDC/alluminiocontenenti 14 compresse rivestite con film. Le scatole
contengono 56 o 112 compresse rivestite con film (Tracleer 125 mg compresse rivestite con film).
Flaconi in polietilene ad alta densità bianchi con gel di silice come essiccante, contenenti 56
compresse rivestite con film. Gli astucci di cartone contengono 56 compresse rivestite con film
(Tracleer 125 mg compresse rivestite con film).
Non ingoiare l’essiccante.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Janssen-Cilag International NV
Turnhoutseweg 30
B-2340 Beerse
Belgio
Produttore
Janssen Pharmaceutica NV
Turnhoutseweg 30
B-2340 Beerse
Belgio
Per ulteriori informazioni su questo farmaco, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio.
België/Belgique/Belgien
Janssen-Cilag NV
Tel/Tél: +32 14 64 94 11
[email protected]
Lietuva
UAB “JOHNSON & JOHNSON”
Tel: +370 5 278 68 88
[email protected]
България
„Джонсън & Джонсън България” ЕООД
Тел.: +359 2 489 94 00
[email protected]
Luxembourg/Luxemburg
Janssen-Cilag NV
Tél/Tel: +32 14 64 94 11
[email protected]
Česká republika
Janssen-Cilag s.r.o.
Magyarország
Janssen-Cilag Kft.
Tel: +420 227 012 227 Tel.: +36 1 884 2858
[email protected]
Danmark
Janssen-Cilag A/S
Tlf: +45 4594 8282
[email protected]
Malta
AM MANGION LTD
Tel: +356 2397 6000
Deutschland
Janssen-Cilag GmbH
Tel: 0800 086 9247 / +49 2137 955 6955
[email protected]
Nederland
Janssen-Cilag B.V.
Tel: +31 76 711 1111
[email protected]
Eesti
UAB "JOHNSON & JOHNSON" Eesti filiaal
Tel: +372 617 7410
[email protected]
Norge
Janssen-Cilag AS
Tlf: +47 24 12 65 00
[email protected]
Ελλάδα
Janssen-Cilag Φαρμακευτική Μονοπρόσωπη
Österreich
Janssen-Cilag Pharma GmbH
Α.Ε.Β.Ε. Tel: +43 1 610 300
Tηλ: +30 210 80 90 000
España
Janssen-Cilag, S.A.
Tel: +34 91 722 81 00
[email protected]
Polska
Janssen-Cilag Polska Sp. z o.o.
Tel.: +48 22 237 60 00
France
Janssen-Cilag
Tél: 0 800 25 50 75 / +33 1 55 00 40 03
[email protected]
Portugal
Janssen-Cilag Farmacêutica, Lda.
Tel: +351 214 368 600
Hrvatska
Johnson & Johnson S.E. d.o.o.
Tel: +385 1 6610 700
[email protected]
România
Johnson & Johnson Rom ânia SRL
Tel: +40 21 207 1800
Ireland
Janssen Sciences Ireland UC
Tel: 1 800 709 122
[email protected]
Slovenija
Johnson & Johnson o.o.
Tel: +386 1 401 18 00
[email protected]
Ísland
Janssen-Cilag AB
c/o Vistor ehf.
Sími: +354 535 7000
[email protected]
Slovenská republika
Johnson & Johnson, s.r.o.
Tel: +421 232 408 400
Italia
Janssen-Cilag SpA
Tel: 800.688.777 / +39 02 2510 1
[email protected]
Suomi/Finland
Janssen-Cilag Oy
Puh/Tel: +358 207 531 300
[email protected]
Κύπρος
Βαρνάβας Χατζηπαναγής Λτδ
Τηλ: +357 22 207 700
Sverige
Janssen-Cilag AB
Tfn: +46 8 626 50 00
[email protected]
Latvija
UAB "JOHNSON & JOHNSON" filiāle Latvijā
Tel: +371 678 93561
[email protected]
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali: https://www.ema.europa.eu.
Tracleer 32 mg compresse dispersibili
bosentan
Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
importanti informazioni per lei:
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista.
Contenuto di questo foglio:
- 1. Che cos’è Tracleer e a che cosa serve
- 2. Cosa deve sapere prima di prendere Tracleer
- 3. Come prendere Tracleer
- 4. Possibili effetti indesiderati
- 5. Come conservare Tracleer
- 6. Contenuto della confezione ed altre informazioni
1. Che cos’è Tracleer e a che cosa serve
Le compresse di Tracleer contengono bosentan che blocca un ormone che esiste naturalmente
chiamato endotelina-1 (ET-1), che comporta un restringimento dei vasi sanguigni. Tracleer comporta,
quindi, una dilatazione dei vasi ed appartiene alla classe di medicinali denominata “antagonisti del
recettore dell’endotelina”.
Tracleer è usato per trattare:
- Ipertensione arteriosa polmonare(PAH): la PAH è una malattia caratterizzata da un severo restringimento dei vasi sanguigni del polmone con conseguente aumento di pressione nei vasi sanguigni che portano il sangue dal cuore ai polmoni (arterie polmonari). Questa pressione riduce la quantità di ossigeno che può passare nel sangue attraverso i polmoni, rendendo l’attività fisica più difficoltosa. Tracleer allarga le arterie polmonari, facilitando il pompaggio del sangue al loro interno da parte del cuore; ciò determina una riduzione della pressione sanguigna ed un’attenuazione dei sintomi.
Tracleer è usato per trattare pazienti affetti da PAH in classe III, per migliorare la capacità di esercizio
(possibilità di svolgere attività fisica) ed i sintomi. La “classe” riflette la gravità della malattia: “classe
III” comporta una marcata limitazione nell’attività fisica. Alcuni miglioramenti sono stati evidenziati
anche in pazienti PAH in classe II. “Classe II” comporta delle minori limitazioni nell’attività fisica. La
PAH per la quale Tracleer è indicato può essere:
- primaria (senza una causa identificabile o familiare);
- causata dalla sclerodermia (definita anche sclerosi sistemica, una malattia caratterizzata da un’anormale crescita del tessuto connettivo che sostiene la cute ed altri organi);
- causata da difetti congeniti (innati) del cuore con shunts (vie di passaggio anormali) che determinano un flusso anormale di sangue attraverso il cuore ed i polmoni.
- Ulcere digitali: (lesione delle dita di mani e piedi) in pazienti adulti con una condizione chiamata sclerodermia. Tracleer riduce il numero delle nuove ulcere delle dita di mani e piedi.
2. Cosa deve sapere prima di prendere Tracleer
Non prenda Tracleer:
- se è allergico al bosentano ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6)
- se ha disturbi epatici(chiedere al proprio medico)
- se è in stato di gravidanza o lo può diventarepoiché non usa metodi anticoncezionali affidabili. Per favore legga le informazioni riportate in “Contraccettivi” e in “Altri farmaci e Tracleer”
- se è in trattamento con ciclosporina A(un farmaco usato dopo un trapianto d’organo o per il trattamento della psoriasi)
In uno di questi casi, informi il suo medico.
Avvertenze e precauzioni
Esami richiesti dal medico prima del trattamento con Tracleer
- un esame del sangue per verificare la sua funzionalità epatica
- un esame del sangue per controllare la presenza di anemia (emogloblina bassa)
- un test di gravidanza se lei è una donna in età fertile In alcuni pazienti in terapia con Tracleer sono state riscontrate delle anormalità riguardo i test per la funzionalità epatica ed anemia (emoglobina bassa).
Esami che il suo dottore le prescriverà durante il trattamento
Durante il trattamento con Tracleer il medico provvederà a richiedere regolarmente esami del sangue,
in modo tale da controllare eventuali cambiamenti della funzionalità epatica e della concentrazione di
emoglobina.
Per tutti questi esami fare riferimento anche alla Carta Informativa del Paziente (contenuta nella sua
confezione di compresse di Tracleer). È importante che lei si sottoponga a questi esami del sangue ad
intervalli regolari durante l’intero periodo di somministrazione di Tracleer. Si consiglia di annotare
sulla Carta Informativa del Paziente la data dell’esame più recente e anche quella del prossimo esame
previsto (chiedere la data al medico), così da non dimenticare la data dell’esame successivo.
Esami del sangue per la funzionalità epatica
Verranno effettuati ogni mese per tutta la durata del trattamento con Tracleer. In seguito ad incremento
del dosaggio verrà effettuato un esame addizionale dopo 2 settimane.
Esami del sangue per l’anemia
Verranno effettuati ogni mese per i primi 4 mesi del trattamento e successivamente ogni 3 mesi, in
quanto i pazienti che assumono Tracleer possono sviluppare condizioni anemiche.
Se questi risultati dovessero essere anomali, il medico potrebbe decidere di ridurre la dose o
sospendere il trattamento con Tracleer ed effettuare ulteriori esami per determinarne la causa.
Bambini ed adolescenti
Tracleer non è raccomandato nei pazienti pediatrici con sclerosi sistemica ed ulcere digitali attive. Per
favore vedere anche il paragrafo 3. Come prendere Tracleer.
Altri farmaci e Tracleer
Si raccomanda di informare il medico o il farmacista nel caso lei stia assumendo o abbia recentemente
assunto altri medicinali, anche quelli acquistati senza prescrizione medica. È importante, soprattutto,
informare il suo medico se sta prendendo:
- ciclosporina A (un farmaco utilizzato dopo trapianti e per il trattamento della psoriasi) che non deve essere usato insieme a Tracleer.
- sirolimus o tacrolimus, che sono farmaci usati dopo trapianti, il cui uso insieme a Tracleer non è raccomandato.
- glibenclamide (un farmaco per il diabete), rifampicina (un farmaco per la tubercolosi), fluconazolo (un farmaco per il trattamento di infezioni da funghi), ketoconazolo (un farmaco usato per il trattamento della sindrome di Cushing) o nevirapina (un farmaco per l’HIV), l’uso di queste medicine insieme a Tracleer non è raccomandato.
- altri farmaci per il trattamento dell’infezione da HIV che possono richiedere un monitoraggio speciale se utilizzati insieme al Tracleer.
- contraccettivi ormonali, che non sono efficaci come unico metodo di contraccezione quando lei assume Tracleer. All’interno della confezione di compresse Tracleer troverà una Carta Informativa del Paziente che dovrà leggere attentamente. Il suo medico curante e/o il suo ginecologo stabilirà il metodo contraccettivo appropriato per lei.
- altri medicinali per il trattamento dell’ipertensione polmonare: sildenafil e tadalafil;
- warfarin (un agente anticoagulante);
- simvastatina (usata per trattare l’ipercolesterolemia).
Guida di veicoli e utilizzo di macchinari
Tracleer non altera o altera in modo trascurabile la capacità di guidare veicoli e di usare macchinari .
Tuttavia, Tracleer può indurre ipotensione (riduzione della sua pressione sanguigna) che può farla
sentire instabile e influenzare la sua vista e la sua capacità di guidare veicoli e utilizzare macchinari.
Pertanto se lei avverte un senso di vertigine o le si offusca la vista durante il trattamento con Tracleer,
non guidi o non utilizzi strumenti o macchinari di alcun genere.
Donne in età fertile
NON assumere Tracleer se lei è in gravidanza o ha pianificato di esserlo.
Test di gravidanza
Tracleer può nuocere al nascituro concepito prima o durante il trattamento. Se lei è una donna in età
fertile, il suo medico le chiederà di effettuare un test di gravidanza prima di iniziare l’assunzione di
Tracleer e di effettuarlo, quindi, regolarmente durante il trattamento con Tracleer.
Contraccettivi
Se lei è una donna in età fertile, utilizzi un affidabile metodo di controllo della nascita (contraccettivo)
mentre prende Tracleer. Il medico o il ginecologo le consiglierà metodi contraccettivi affidabili mentre
prende Tracleer. Poiché Tracleer potrebbe rendere inefficace la contraccezione ormonale (ad esempio
contraccettivi orali, iniettabili, impiantabili o cerotti cutanei), questo metodo da solo non è affidabile.
Quindi, se lei usa contraccettivi ormonali deve usare un metodo di barriera (es. profilattico femminile,
diaframma, spugna contraccettiva oppure anche il suo partner deve utilizzare il profilattico).
All’interno della sua confezione di compresse Tracleer troverà una Carta Informativa del Paziente. Lei
dovrà riempire questa carta e portarla al suo medico alla prossima visita, in questo modo il medico
curante o il ginecologo potranno valutare se lei ha bisogno di affidabili metodi contraccettivi
addizionali o alternativi. Si raccomanda di effettuare un test di gravidanza ogni mese durante il
trattamento con Tracleer se lei è in età fertile.
Informi immediatamente il medico in caso di gravidanza subentrata durante il trattamento con Tracleer
e se si prevede di dare inizio ad una gravidanza nell’immediato futuro.
Allattamento
Tracleer passa nel latte materno. Si consiglia di interrompere l’allattamento al seno in caso venga
prescritto Tracleer in quanto non è escluso possa nuocere al suo bambino. Parli con il dottore se ha
domande su questo argomento.
Fertilità
Se lei è un uomo che assume Tracleer è possibile che questo medicinale riduca la conta degli
spermatozoi. Non si può escludere che questo potrebbe compromettere la sua possibilità di concepire
un figlio. Parli con il suo dottore se ha domande su questo argomento.
Tracleer contiene aspartame e sodio
Questo medicinale contiene 3,7 mg di aspartame per compressa dispersibile. Aspartame è una fonte di
fenilalanina. Può esserle dannosa se è affetto da fenilchetonuria, una rara malattia genetica che causa
l’accumulo di fenilalanina perché il corpo non riesce a smaltirla correttamente.
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per compressa, cioè è da considerarsi
essenzialmente ‘privo di sodio’.
3. Come prendere Tracleer
Il trattamento con Tracleer va iniziato e monitorato solo da un medico che ha esperienza nel
trattamento della PAH o della sclerosi sistemica. Prenda questo medicinale seguendo sempre
esattamente le istruzioni del medico. Se ha dubbi consulti il medico o il farmacista.
Tracleer con cibo e bevande
Tracleer può essere preso a digiuno o a stomaco pieno.
Dose raccomandata
Adulti
Negli adulti il trattamento ha inizio normalmente con l’assunzione di una compressa da 62,5 mg due
volte al giorno (mattina e sera) per le prime 4 settimane; in seguito il medico consiglierà solitamente di
assumere una compressa da 125 mg due volte al giorno a seconda della risposta a Tracleer riscontrata.
Bambini ed adolescenti
La dose raccomandata nei bambini è solo per la PAH. Per bambini di età uguale o maggiore a 1 anno
il trattamento con Tracleer ha inizio normalmente con l’assunzione di 2 mg per kg di peso corporeo
due volte al giorno (mattina e sera); il dosaggio successivo verrà consigliato dal medico.
Se necessario la compressa dispersibile può essere divisa lungo le linee intagliate in quattro parti
uguali.
Se lei ha l’impressione che gli effetti del Tracleer siano troppo forti o troppo deboli, parli con il suo
medico allo scopo di valutare se vi è la necessità di cambiare la posologia.
Come prendere Tracleer
Assumere le compresse (mattina e sera) deglutendole con acqua. Le compresse possono essere assunte
con o senza cibo.
La compressa dispersibile è contenuta in un blister a prova di bambino.
Per rimuovere la compressa dispersibile:
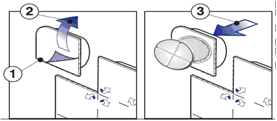
- 1. Separare la singola cavità del blister lungo le perforazioni.
- 2. Rimuovere gli strati superiori.
- 3. Fare uscire la compressa attraverso la pellicola.
Ogni compressa dispersibile di Tracleer può essere disciolta in acqua per ottenere un farmaco liquido.
A tale scopo collocare la compressa in un cucchiaio con un po’ d’acqua, utilizzando acqua sufficiente
a coprire l’intera compressa. Aspettare per circa un minuto fino a quando la compressa si è
completamente disciolta poi deglutire tutto il liquido. Per assicurarsi di avere assunto tutto il farmaco,
aggiungere ancora un po’ d’acqua nel cucchiaio e ingerirlo. Se possibile bere un bicchiere d’acqua per
assicurarsi di aver preso tutta la medicina.
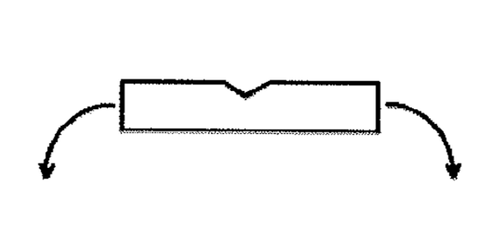
Se necessario la compressa dispersibile può essere divisa spezzandola lungo le linee intagliate sulla
superficie. Tenere la compressa tra il pollice e l’indice sui due lati di una delle linee, con la linea
rivolta verso l’alto e spezzare la compressa lungo la linea (vedere figura seguente).
Se prende più Tracleer di quanto deve
In caso abbia assunto più compresse di quante prescritte, consulti immediatamente il medico.
Se si dimentica di prendere Tracleer
In caso si sia dimenticato di assumere Tracleer, prenda una compressa non appena si ricorda e poi
assuma le compresse agli orari normali. Non prenda una dose doppia per compensare eventuali
dimenticanze.
Se smette di prendere Tracleer
La sospensione improvvisa del trattamento con Tracleer potrebbe comportare un aggravamento dei
sintomi. Non sospenda tale trattamento a meno che ciò non venga richiesto dal medico. Il suo medico
potrebbe consigliarle di ridurre la dose nell’arco di alcuni giorni prima di sospendere definitivamente
il trattamento con Tracleer.
Se ha ulteriori domande sull’uso di questo medicinale si rivolga al medico o al farmacista.
4Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le
persone li manifestino.
Gli effetti indesiderati più gravi connessi con il Tracleer sono:
- Funzionalità del fegato anormale che può manifestarsi in più di 1 utilizzatore su 10
- Anemia (valori bassi negli esami del sangue) che può manifestarsi in 1 utilizzatore su 10. L’anemia, può occasionalmente, richiedere la trasfusione di sangue. I valori risultanti dagli esami del fegato e del sangue devono essere controllati durante il trattamento con Tracleer (vedere paragrafo 2). E’ importante che lei faccia questi controlli così come prescritto dal suo medico.
I segni di un non corretto funzionamento del suo fegato includono:
- nausea (impulso a vomitare)
- vomito
- febbre (temperatura elevata)
- dolore allo stomaco (addome)
- itterizia (ingiallimento della pelle o della sclera, ossia la parte bianca dell’occhio)
- urina di colore scuro
- prurito della pelle
- letargia o affaticamento (stanchezza o spossatezza inusuali)
- sindrome simil-influenzale (dolori alle articolazioni e ai muscoli con febbre)
Se nota uno di questi segni lo dica immediatamente al suo medico.
Altri effetti indesiderati:
Molto comuni(possono manifestarsi in più di 1 persona su 10):
- cefalea (mal di testa)
- edema (gonfiore delle gambe e delle caviglie o altri segni dovuti a ritenzione dei liquidi)
Comuni(possono manifestarsi fino a 1 persona su 10):
- aspetto arrossato o arrossamento della pelle
- reazioni da ipersensibilità (che includono infiammazione della pelle, prurito e eruzione cutanea)
- malattia da reflusso gastroesofageo (reflusso acido)
- diarrea
- sincope (svenimento)
- palpitazioni (battiti del cuore veloci o irregolari)
- pressione sanguigna bassa
- congestione nasale
Non comuni(possono manifestarsi fino a 1 persona su 100):
- trombocitopenia (basso numero di piastrine nel sangue)
- neutropenia/leucopenia (basso numero di globuli bianchi)
- Valori elevati di funzionalità epatica associati a epatite (infiammazione del fegato) inclusa possibile esacerbazione dell’epatite sottostante e/o itterizia (ingiallimento della cute o della parte bianca dell’occhio)
Rari(possono manifestarsi fino a 1 persona su 1 000):
- anafilassi (reazione allergica generalizzata), angioedema (gonfiore, più comune intorno ad occhi, labbra, lingua o gola)
- cirrosi (cicatrizzazione) del fegato, insufficienza epatica (grave alterazione della funzionalità del fegato), epatite autoimmune (infiammazione del fegato causata dal sistema di difesa dell’organismo che attacca le cellule del fegato) che può manifestarsi anche vari mesi o anni dopo l'inizio del trattamento.
È stata inoltre riferita visione offuscata, con una frequenza non nota (la frequenza non può essere
definita sulla base dei dati disponibili).
Effetti indesiderati aggiuntivi nei bambini e adolescenti
Gli effetti indesiderati che sono stati riportati nei bambini trattati con Tracleer sono gli stessi di quelli
degli adulti.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema
nazionale di segnalazione riportato nell’Allegato V. Segnalando gli effetti indesiderati lei può
contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Tracleer
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola e sul blister dopo
“Scad”.
Non conservare a temperatura superiore a 25 °C
Le parti restanti di una compressa dispersibile divisa possono essere conservate a temperatura ambiente e
devono essere consumate entro 7 giorni.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista
come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione ed altre informazioni
Cosa contiene Tracleer
- Il principio attivo è il bosentan sotto forma di monoidrato. Ogni compressa dispersibile contiene 32 mg di bosentan (monoidrato).
- Gli altri componenti sono: cellulosa microcristallina, calcio fosfato dibasico anidro, croscarmellosa sodica, silice colloidale anidra, acido tartarico, aroma tutti frutti, aspartame (E951, per favore legga ulteriori informazioni alla fine del paragrafo 2), acesulfame potassico, magnesio stearato.
Descrizione dell’aspetto di Tracleer e contenuto della confezione
Tracleer 32 mg compresse dispersibili. Compresse a forma di quadrifoglio di colore da giallo pallido a
biancastro, divise in quattro su un lato e con “32” impresso sull’altro lato.
Blister peel-push contenenti 14 compresse disperdibili. Astucci di cartone contenenti 56 compresse
dispersibili.
Titolare dell’autorizzazione all’immissione in commercio
Janssen-Cilag International NV
Turnhoutseweg 30
B-2340 Beerse
Belgio
Produttore
Janssen Pharmaceutica NV
Turnhoutseweg 30
B-2340 Beerse
Belgio
Per ulteriori informazioni su questo farmaco, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio.
België/Belgique/Belgien
Janssen-Cilag NV
Tel/Tél: +32 14 64 94 11
[email protected]
Lietuva
UAB “JOHNSON & JOHNSON”
Tel: +370 5 278 68 88
[email protected]
БългарияLuxembourg/Luxemburg
„Джонсън & Джонсън България” ЕООД
Тел.: +359 2 489 94 00
[email protected]
Janssen-Cilag NV
Tél/Tel: +32 14 64 94 11
[email protected]
Česká republika
Janssen-Cilag s.r.o.
Tel: +420 227 012 227
Magyarország
Janssen-Cilag Kft.
Tel.: +36 1 884 2858
[email protected]
Danmark
Janssen-Cilag A/S
Tlf: +45 4594 8282
[email protected]
Malta
AM MANGION LTD
Tel: +356 2397 6000
Deutschland
Janssen-Cilag GmbH
Tel: 0800 086 9247 / +49 2137 955 6955
[email protected]
Nederland
Janssen-Cilag B.V.
Tel: +31 76 711 1111
[email protected]
Eesti
UAB "JOHNSON & JOHNSON" Eesti filiaal
Tel: +372 617 7410
[email protected]
Norge
Janssen-Cilag AS
Tlf: +47 24 12 65 00
[email protected]
Ελλάδα
Janssen-Cilag Φαρμακευτική Μονοπρόσωπη
Α.Ε.Β.Ε.
Tηλ: +30 210 80 90 000
Österreich
Janssen-Cilag Pharma GmbH
Tel: +43 1 610 300
España
Janssen-Cilag, S.A.
Tel: +34 91 722 81 00
[email protected]
Polska
Janssen-Cilag Polska Sp. z o.o.
Tel.: +48 22 237 60 00
France
Janssen-Cilag
Tél: 0 800 25 50 75 / +33 1 55 00 40 03
[email protected]
Portugal
Janssen-Cilag Farmacêutica, Lda.
Tel: +351 214 368 600
Hrvatska
Johnson & Johnson S.E. d.o.o.
Tel: +385 1 6610 700
[email protected]
România
Johnson & Johnson România SRL
Tel: +40 21 207 1800
Ireland
[email protected]
Slovenija
Ísland
Janssen-Cilag AB
c/o Vistor ehf.
Sími: +354 535 7000
[email protected]
Slovenská republika
| Janssen Sciences Ireland UC | |
| Tel: 1 800 709 122 | n |
| Johnson & Johnson o. | o. |
| Tel: +386 1 401 18 00 | |
| [email protected] | |
| Johnson & Johnson, s.r.o. | |
| Tel: +421 232 408 400 | |
Italia
Janssen-Cilag SpA
Tel: 800.688.777 / +39 02 2510 1
Suomi/Finland
Janssen-Cilag Oy
Puh/Tel: +358 207 531 300
[email protected] [email protected]
Κύπρος
Βαρνάβας Χατζηπαναγής Λτδ
Τηλ: +357 22 207 700
Sverige
Janssen-Cilag AB
Tfn: +46 8 626 50 00
[email protected]
Latvija
UAB "JOHNSON & JOHNSON" filiāle Latvijā
Tel: +371 678 93561
[email protected]
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali: https://www.ema.europa.eu.
ALLEGATO IV
CONCLUSIONI SCIENTIFICHE E MOTIVAZIONI PER LA VARIAZIONE DEI TERMINI
DELLE AUTORIZZAZIONI ALL’IMMISSIONE IN COMMERC
Conclusioni scientifiche
Tenendo conto della valutazione del Comitato per la valutazione dei rischi in farmacovigilanza
( Pharmacovigilance and Risk Assessment Committee, PRAC) dei Rapporti periodici di aggiornamento
sulla sicurezza ( Periodic Safety Update Report, PSUR) per bosentan, le conclusioni scientifiche sono
le seguenti:
Sulla base dei dati disponibili sull’epatite autoimmune, derivati dagli studi clinici, dalla letteratura,
dalle segnalazioni spontanee, inclusa in alcuni casi, una stretta correlazione temporale, da un
miglioramento dopo la sospensione e/o ricomparsa quando il farmaco è stato risomministrato
(de-challengee/o re-challengepositivo ), il PRAC Rapporteur ritiene che esista almeno una
ragionevole possibilità di una relazione causale tra bosentan ed epatite autoimmune.
Il PRAC Rapporteur ha concluso che le informazioni sul prodotto dei medicinali contenenti bosentan
debbano essere, di conseguenza, modificate.
Avendo esaminato la raccomandazione del PRAC, il Comitato dei medicinali per uso umano
( Committee for Human Medicinal Products, CHMP) concorda con le relative conclusioni generali e
con le motivazioni della raccomandazione.
Motivazioni della variazione dei termini delle autorizzazioni all’immissione in commercio
Sulla base delle conclusioni scientifiche su bosentan, il CHMP ritiene che il rapporto beneficio/rischio
dei medicinali contenenti bosentan sia invariato, fatte salve le modifiche proposte alle informazioni sul
prodotto.
Il CHMP raccomanda la variazione dei termini delle autorizzazioni all'immissione in commercio.
- Paese di registrazione
- Forma farmaceuticaCompressa rivestita con film, 62,5 MG
- Codice ATCC02KX01
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a TRACLEERForma farmaceutica: Compressa rivestita con film, 62,5 MGPrincipio attivo: bosentanProduttore: Abdi Farma GmbHPrescrizione richiestaForma farmaceutica: Compressa rivestita con film, 62,5 MGPrincipio attivo: bosentanProduttore: ACCORD HEALTHCARE, S.L.U.Prescrizione richiestaForma farmaceutica: Compressa rivestita con film, 62,5 MGPrincipio attivo: bosentanProduttore: AUROBINDO PHARMA (ITALIA) S.R.L.Prescrizione richiesta
Medici online per TRACLEER
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di TRACLEER — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per TRACLEER online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.









