
Come usare REFIXIA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Refixia 500 UI polvere e solvente per soluzione iniettabile, 1 000 UI polvere e solvente per soluzione iniettabile, 2 000 UI polvere e solvente per soluzione iniettabile, 3 000 UI polvere e solvente per soluzione iniettabile
nonacog beta pegilato
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Refixia e a cosa serve
- 2. Cosa deve sapere prima di usare Refixia
- 3. Come usare Refixia
- 4. Possibili effetti indesiderati
- 5. Come conservare Refixia
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Refixia e a cosa serve
Cos’è Refixia
Refixia contiene il principio attivo nonacog beta pegilato. Si tratta di una versione ad azione
prolungata del fattore IX. Il fattore IX è una proteina naturalmente presente nel sangue che aiuta a
fermare i sanguinamenti.
A cosa serve Refixia
Refixia viene utilizzato in pazienti di tutte le fasce di età con emofilia B (deficit congenito di
fattore IX) per il trattamento e la prevenzione di eventi emorragici (sanguinamenti).
Nei pazienti con emofilia B, il fattore IX è mancante o non funziona correttamente. Refixia sostituisce
questo fattore IX che funziona male o è assente e aiuta il sangue a formare coaguli nel sito
dell’emorragia (il sanguinamento).
2. Cosa deve sapere prima di usare Refixia
Non usi Refixia
- se è allergico al principio attivo o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6).
- se è allergico alle proteine di criceto.
Se non è sicuro che quanto sopra riportato si applichi a lei, contatti il medico prima di usare questo
medicinale.
Avvertenze e precauzioni
Tracciabilità
È importante tenere un registro dei numeri di lotto di Refixia. Quindi, ogni volta che prende una nuova
confezione del medicinale, annoti la data e il numero di lotto (che si trova sulla confezione dopo
Lotto) e tenga queste informazioni in un posto sicuro.
Reazioni allergiche e sviluppo di inibitori
Esiste il rischio, sebbene raro, che possa sviluppare una grave e improvvisa reazione allergica (per es.
reazione anafilattica) a Refixia. Interrompa l’iniezione e si rivolga immediatamente al medico o al
pronto soccorso se manifesta segni di una reazione allergica, quali eruzione cutanea, orticaria, ponfi,
prurito generalizzato, arrossamento e/o gonfiore delle labbra, della lingua, del viso o delle mani,
difficoltà a deglutire o nella respirazione, respiro corto, respiro sibilante, senso di oppressione al
torace, pelle pallida e fredda, accelerazione del battito cardiaco e/o capogiri.
Il medico potrebbe dover trattare tempestivamente queste reazioni e potrebbe anche eseguire un esame
del sangue per controllare se lei ha sviluppato inibitori del fattore IX (anticorpi neutralizzanti) verso il
medicinale, perché gli inibitori potrebbero svilupparsi insieme alle reazioni allergiche. Se presenta
questi inibitori, potrebbe presentare un rischio più elevato di sviluppare reazioni allergiche improvvise
e gravi (per es. reazione anafilattica) durante il trattamento futuro con il fattore IX.
A causa del rischio di reazioni allergiche al fattore IX, il trattamento iniziale con Refixia deve essere
somministrato in un centro medico o in presenza di personale medico-sanitario in un luogo dove sia
possibile fornire le cure mediche appropriate in caso di reazione allergica, se necessario.
Si rivolga immediatamente al medico se l’emorragia non si arresta come atteso o se deve aumentare
significativamente la quantità di Refixia per fermare un’emorragia. Il medico eseguirà un esame del
sangue per controllare se lei ha sviluppato inibitori (anticorpi neutralizzanti) verso Refixia. Il rischio di
sviluppare inibitori è massimo nelle persone a cui non sono mai stati somministrati medicinali
contenenti fattore IX, tipicamente nei bambini piccoli.
Coaguli di sangue
Si rivolga al medico se una qualsiasi di queste situazioni la riguarda, perché potrebbe essere a maggior
rischio di sviluppare coaguli di sangue durante il trattamento con Refixia:
- è stato recentemente sottoposto a un intervento chirurgico
- soffre di altre malattie gravi, per es. malattia al fegato, al cuore o tumore
- presenta fattori di rischio per la malattia al cuore, per es. pressione sanguigna elevata, obesità o fumo.
Disturbo renale (sindrome nefrosica)
Esiste un raro rischio di sviluppare un disturbo renale specifico, chiamato ‘sindrome nefrosica’, dopo
la somministrazione di dosi elevate di fattore IX in pazienti con emofilia B che hanno sviluppato
inibitori del fattore IX e presentano una storia di reazioni allergiche.
Problemi correlati all’uso del catetere
Se ha un sistema di accesso venoso centrale (CVC), potrebbe sviluppare infezioni o coaguli di sangue
nel sito di cateterizzazione.
Altri medicinali e Refixia
Informi il medico se sta usando, ha recentemente usato o potrebbe usare qualsiasi altro medicinale.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico prima di usare Refixia.
Guida di veicoli e utilizzo di macchinari
Refixia non altera la capacità di guidare veicoli e di usare macchinari.
Refixia contiene sodio
Questo medicinale contiene meno di 1 mmol di sodio (23 mg) per flaconcino, cioè essenzialmente
‘senza sodio’. In caso di trattamento con più flaconcini, deve essere preso in considerazione il
contenuto di sodio totale.
3. Come usare Refixia
Il trattamento con Refixia deve essere iniziato da un medico esperto nel trattamento di pazienti con
emofilia B. Usi questo medicinale seguendo sempre esattamente le istruzioni del medico. Se ha dubbi
sull’uso di Refixia consulti il medico.
Il medico determinerà la dose giusta per lei, sulla base del peso corporeo e dello scopo del medicinale.
Prevenzione delle emorragie
La dose abituale di Refixia è 40 unità internazionali (UI) per kg di peso corporeo, iniettate una volta
alla settimana. Il medico può scegliere una dose differente o modificare quanto spesso le iniezioni
devono essere somministrate sulla base delle sue necessità.
Trattamento delle emorragie
La dose abituale di Refixia è 40 unità internazionali (UI) per kg di peso corporeo. A seconda della
sede e della gravità dell’emorragia, può aver bisogno di una dose più elevata (80 UI per kg) o di
ulteriori iniezioni. Si rivolga al medico per conoscere la dose e il numero di iniezioni di cui avrà
bisogno.
Uso nei bambini e negli adolescenti
Refixia può essere utilizzato in bambini e adolescenti di tutte le età. Anche nei bambini e negli
adolescenti la dose è calcolata in base al peso corporeo ed è identica a quella per gli adulti.
Come viene somministrato Refixia
Refixia è disponibile in polvere e solvente che compongono una soluzione (ricostituzione) e viene
somministrato con un’iniezione in vena. Per maggiori informazioni vedere ‘Istruzioni su come usare
Refixia’.
Se usa più Refixia di quanto deve
Se usa più Refixia di quanto deve, informi il medico.
Si rivolga immediatamente al medico se deve aumentare significativamente la quantità di Refixia per
fermare un’emorragia. Per maggiori informazioni, vedere paragrafo 2 ‘Reazioni allergiche e sviluppo
di inibitori’.
Se dimentica di usare Refixia
Se dimentica una dose, inietti la dose saltata non appena se ne ricorda. Non inietti una dose doppia per
compensare la dimenticanza della dose. Se ha dubbi consulti il medico.
Se interrompe il trattamento con Refixia
Se interrompe il trattamento con Refixia può non essere più protetto contro le emorragie e i
sanguinamenti successivi possono non fermarsi. Non interrompa il trattamento con Refixia senza aver
prima consultato il medico.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Con questo medicinale sono possibili reazioni allergiche.
Nel caso in cui si verifichino reazioni allergiche (per es. reazioni anafilattiche) gravi e improvvise,
deve interrompere immediatamente l’iniezione. Se avverte uno dei segni precoci di una reazione
allergica grave (reazione anafilattica), deve contattare il medico o il pronto soccorso immediatamente:
- difficoltà a deglutire o respirare
- respiro corto o sibilante
- oppressione al petto
- arrossamento e/o gonfiore delle labbra, della lingua, del viso o delle mani
- eruzione cutanea, orticaria, ponfi o prurito
- pelle pallida e fredda, accelerazione del battito cardiaco e/o capogiri (bassa pressione sanguigna).
In bambini non trattati in precedenza con farmaci a base di fattore IX, possono formarsi comunemente
(fino a 1 paziente su 10) degli inibitori (vedere paragrafo 2). Se ciò accade, il farmaco potrebbe
smettere di funzionare correttamente e il bambino potrebbe soffrire di emorragie persistenti. In tal
caso, è necessario contattare immediatamente il medico.
Con Refixia sono stati osservati i seguenti effetti indesiderati:
Effetti indesiderati comuni(possono verificarsi in fino a 1 persona su 10)
- reazioni allergiche (ipersensibilità). Potrebbero diventare gravi ed essere potenzialmente letali (reazioni anafilattiche).
- prurito
- reazioni cutanee nel sito di iniezione
- nausea
- stanchezza
- eruzione cutanea
- bambini non trattati in precedenza con farmaci a base di fattore IX: anticorpi neutralizzanti (inibitori), reazioni anafilattiche.
Effetti indesiderati non comuni(possono verificarsi in fino a 1 persona su 100)
- palpitazioni
- vampate.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Lei può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’Allegato V. Segnalando gli effetti
indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Refixia
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi Refixia dopo la data di scadenza che è riportata sulla scatola e sulle etichette del flaconcino e
della siringa preriempita dopo ‘Scad.’. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2 °C – 8 °C). Non congelare. Conservare il flaconcino nella confezione
esterna per proteggere il medicinale dalla luce.
Refixia può essere tenuto fuori dal frigorifero per un periodo massimo di 1 anno e conservato a
temperatura ambiente (fino a 30 °C). Registri sulla confezione la data in cui Refixia viene estratto dal
frigorifero e conservato a temperatura ambiente. Questa nuova data di scadenza non deve mai superare
quella riportata inizialmente sulla confezione esterna. Eliminare il medicinale se non viene usato prima
della nuova data di scadenza. Dopo la conservazione a temperatura ambiente il medicinale non deve
essere rimesso in frigorifero.
Usare la preparazione iniettabile immediatamente dopo aver preparato la soluzione (ricostituzione). Se
non può essere usata immediatamente, usarla entro 24 ore se conservata in frigorifero a 2 °C – 8 °C o
entro 4 ore se conservata fuori dal frigorifero a una temperatura massima di 30 °C.
La polvere nel flaconcino appare da bianca a biancastra. Non usi la polvere se il colore ha subìto
cambiamenti.
La soluzione ricostituita è limpida e incolore o leggermente gialla. Non usi la soluzione ricostituita se
nota particelle o alterazioni del colore.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Refixia
- Il principio attivo è nonacog beta pegilato (fattore IX della coagulazione umano pegilato (rDNA)). Ciascun flaconcino di Refixia contiene nominalmente 500 UI, 1 000 UI, 2 000 UI o 3 000 UI di nonacog beta pegilato corrispondente rispettivamente a circa 125 UI/mL, 250 UI/mL, 500 UI/mL o 750 UI/ml dopo la ricostituzione con il solvente istidina.
- Gli altri componenti della polvere sono cloruro di sodio, istidina, saccarosio, polisorbato 80, mannitolo, idrossido di sodio e acido cloridrico. Vedere paragrafo 2 “Refixia contiene sodio”.
- I componenti del solvente sterilizzato sono istidina, acqua per preparazioni iniettabili, idrossido di sodio e acido cloridrico.
Descrizione dell’aspetto di Refixia e contenuto della confezione
- Refixia è fornito come polvere e solvente per soluzione iniettabile (500 UI, 1 000 UI, 2 000 UI o 3 000 UI di polvere in un flaconcino e 4 mL di solvente in una siringa preriempita, uno stantuffo e un adattatore per flaconcino - confezione da 1).
- La polvere è da bianca a biancastra e il solvente è limpido e incolore.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Novo Nordisk A/S
Novo Allé
DK-2880 Bagsværd, Danimarca
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, http://www.ema.europa.eu .
Istruzioni su come usare Refixia
Legga attentamente queste istruzioni prima di usare Refixia.
Refixia è fornito in polvere. Prima dell’iniezione, deve essere preparata una soluzione
(ricostituzione) con il solvente fornito nella siringa. Il solvente è una soluzione di istidina. La
soluzione ricostituita deve essere iniettata in vena (iniezione endovenosa). Il materiale contenuto in
questa confezione è stato progettato per ricostituire ed iniettare Refixia.
Avrà bisogno anche di un set di infusione (tubicino ed ago a farfalla), tamponi sterili imbevuti di
alcool, garze e cerotti. Questi non sono inclusi nella confezione di Refixia.
Non usi il materiale senza una formazione adeguata da parte del medico o dell’infermiere.
Lavi sempre le mani e si assicuri che l’area attorno a lei sia pulita.
Quando prepara e inietta un medicinale direttamente in vena, è importante usare una tecnica
asettica e in assenza di germi.Una tecnica non corretta può introdurre germi che possono infettare
il sangue.
Non apra il materiale fino a quando non è pronto ad usarlo.
Non utilizzi il materiale se è caduto o se è danneggiato.Utilizzi invece una nuova confezione.
Non utilizzi il materiale se è scaduto.Utilizzi, invece, una nuova confezione. La data di scadenza
è stampata sulla confezione esterna, sul flaconcino, sull’adattatore per flaconcino e sulla siringa
preriempita.
Non utilizzi il materiale se sospetta che sia stato contaminato.Utilizzi, invece, una nuova
confezione.
Non getti uno qualsiasi degli elementi fino a quando non ha iniettato la soluzione ricostituita.
Il materiale è solo monouso.
Contenuto
La confezione contiene:
- 1 flaconcino con Refixia polvere
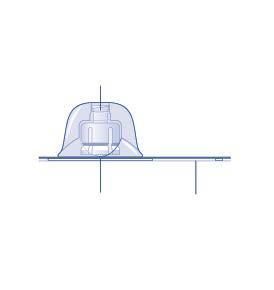
- 1 adattatore per flaconcino
- 1 siringa preriempita con solvente
- 1 stantuffo (posto sotto la siringa)
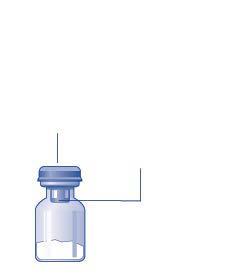
Descrizione generale
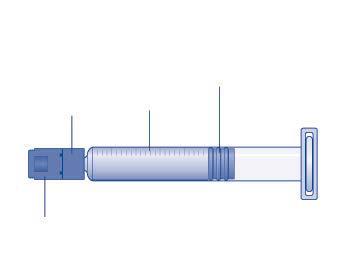
Siringa preriempita con solvente
Stantuffo
Punta della siringa
(sotto il cappuccio
della siringa)
Scala
Cappuccio della
siringa
o Stantuffo c Filettatura Estremità larga a m 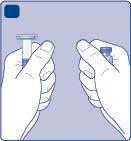 | |
| r a A F l e d a |
i z
| B |
| C o c a m r a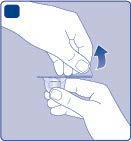 |
| F D l e d |
| a E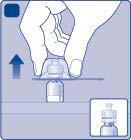 |
t
| F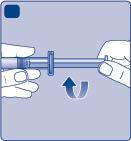 |
| G o c a m |
| r a H F l e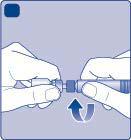 |
| d I a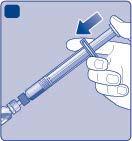 |
i l
| J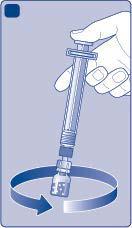 |
| n e Refixia deve essere usato immediatamente dopo la ricostituzione. Se non utilizzato, il medicinale può non essere più sterile e può causare delle infezioni. g Se non può usare immediatamente la soluzione ricostituita di Refixia, questa deve essere usata A entro 4 ore se conservata a temperatura ambiente (fino a 30 °C) e entro 24 ore se conservata in frigorifero (2 °C - 8 °C). Conservi il medicinale ricostituito nel flaconcino. Non congeli la soluzione ricostituita di Refixia né la conservi nella siringa. | |
Tenga la soluzione ricostituita di Refixia al riparo dalla luce. o Se la sua dose richiede più di un flaconcino, ripeta i punti da A a J con gli altri flaconcini, adattatori e siringhe preriempite, fino al raggiungimento della dose necessaria.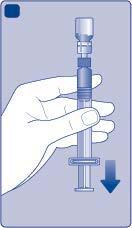 | |
| c a K m r a F l e d a |
I
| L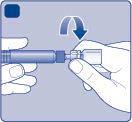 |
n
| |
le siringhe preriempite. Questa incompatibilità può impedire la somministrazione del medicinale e/o danneggiare il connettore senza ago. o Iniettare la soluzione attraverso un sistema di accesso venoso centrale (CVC) come un catetere c venoso centrale o un port sottocutaneo:
| |
Smaltimento
| r a M F l e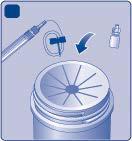 |
| d Non smonti il materiale prima dello smaltimento. a Non riusi il materiale. | |
-

- Paese di registrazione
- Forma farmaceuticaPolvere e solvente per soluzione iniettabile, 500 UI
- Codice ATCB02BD04
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a REFIXIAForma farmaceutica: Polvere e solvente per soluzione per infusione endovenosa, 500 U.I.Principio attivo: coagulation factor IXProduttore: KEDRION S.P.A.Prescrizione richiestaForma farmaceutica: Polvere e solvente per soluzione per infusione endovenosa, 500 UI/10 MLPrincipio attivo: coagulation factor IXProduttore: GRIFOLS ITALIA S.P.A.Prescrizione richiestaForma farmaceutica: Polvere e solvente per soluzione iniettabile, 250 IUPrincipio attivo: coagulation factor IXProduttore: SWEDISH ORPHAN BIOVITRUM AB (PUBL)Prescrizione richiesta
Medici online per REFIXIA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di REFIXIA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per REFIXIA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.











