
Come usare NUMETA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
- NUMETA G13E, emulsione per infusione
- Numeta G13E è stato ideato per rispondere alle esigenze nutrizionali dei neonati
- Numeta G13E potrebbe non essere adeguato per alcuni neonati pretermine, in quanto la
- Numeta G13E si presenta sotto forma di sacca a tre compartimenti. Ogni sacca contiene
- NUMETA G16E, emulsione per infusione
- Numeta G16E per rispondere alle esigenze individuali del bambino se presenta le seguenti
- NUMETA G19E, emulsione per infusione
- Numeta G19E è stato ideato per rispondere alle esigenze nutrizionali dei bambini con età
- Numeta G19E si presenta sotto forma di sacca a tre compartimenti. Ogni sacca contiene
NUMETA G13E, emulsione per infusione
Legga attentamente questo foglio prima di utilizzare questo medicinale perché
contiene importanti informazioni per Lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al pediatra, al farmacista, o all’infermiere.
- Se il suo bambino ha uno qualsiasi degli effetti indesiderati, informi il pediatra o l’infermiere. Questo potrebbe includere qualsiasi effetto indesiderato non elencato in questo foglio. Vedere il paragrafo 4.
Contenuto di questo foglio:
- 1. Che cos'è Numeta G13E e a che cosa serve
- 2. Cosa sapere prima che al suo bambino sia somministrato Numeta G13E
- 3. Come viene somministrato Numeta G13E
- 4. Possibili effetti indesiderati
- 5. Come conservare Numeta G13E
- 6. Contenuto della confezione ed altre informazioni
1. Che cos'è Numeta G13E e a che cosa serve
Numeta G13E è un'emulsione per nutrizione appositamente studiata per i neonati
pretermine. Viene somministrata attraverso un tubo inserito nella vena del suo bambino,
quando non riesce ad assumere tutto il nutrimento necessario per bocca.
Numeta si presenta in sacca a 3 compartimenti nella quale ciascun compartimento separato
contiene:
una soluzione di glucosio al 50%
una soluzione pediatrica di amminoacidi al 5,9%, con elettroliti
un'emulsione di lipidi (grassi) al 12,5%
Due o tre di queste soluzioni vengono miscelate nella sacca prima di essere somministrate
al suo bambino, in base alle sue necessità.
Numeta G13E deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che al suo bambino sia somministrato Numeta G13E
Al suo bambino non deve essere dato Numeta G13E nei seguenti casi:
Con le soluzioni di glucosio e amminoacidi/elettroliti miscelate nella sacca ("2 in 1"):
- Se il suo bambino è allergico alle uova, alla soia, alle arachidi o a qualsiasi altro componente di questo medicinale o componente del contenitore (elencati nel paragrafo 6)
- Se l'utilizzo di componenti delle proteine crea problemi all'organismo del suo bambino.
- Se il suo bambino presenta nel sangue alte concentrazioni di uno qualsiasi degli elettroliti inclusi in Numeta G13E
- Numeta G13E (o altre soluzioni contenenti calcio) non deve essere somministrato contemporaneamente al ceftriaxone (un antibiotico), anche in caso di utilizzo di linee di infusione separate. C’è il rischio fatale di formazioni di particelle nel flusso sanguigno del neonato
- Se il suo bambino soffre di iperglicemia (livelli di zuccheri nel sangue particolarmente alti)
Con le soluzioni di glucosio, amminoacidi/elettroliti e lipidi miscelate nella sacca ("3
in 1"):
Tutte le situazioni menzionate in “2 in 1” più la seguente:
- Se il suo bambino ha livelli di grassi nel sangue particolarmente elevati.
In tutti i casi, il medico deciderà se il suo bambino dovrà ricevere questo medicinale sulla
base di fattori quali età, peso e condizione clinica. Il medico terrà conto anche dei risultati
degli esami eseguiti.
Avvertenze e precauzioni
Parli con il pediatra o con l’infermiere prima che diano Numeta G13E.
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione. L’esposizione di Numeta G13E alla luce
ambientale, specialmente dopo aggiunta di oligoelementi e/o vitamine, genera perossidi e
altri prodotti di degradazione che possono essere ridotti con la protezione dall’esposizione
alla luce.
Reazioni Allergiche
L'infusione deve essere interrotta immediatamente in caso di sviluppo di segni o sintomi di
reazione allergica (ad esempio febbre, sudorazione, brividi, mal di testa, eruzioni cutanee
o difficoltà respiratoria). Questo medicinale contiene olio di semi di soia che, raramente,
può causare gravi reazioni di ipersensibilità. È stato osservato raramente che alcuni soggetti
allergici alle proteine delle arachidi sono allergici anche alle proteine dei semi di soia.
Numeta G13E contiene glucosio prodotto dall'amido di mais. Pertanto, Numeta G13E deve
essere utilizzato con cautela nei pazienti con allergia nota al mais o ai prodotti derivati dal
mais.
Rischio di formazione di particelle con ceftriaxone (antibiotico):
Un determinato antibiotico chiamato ceftriaxone non deve essere miscelato o
somministrato contemporaneamente a soluzioni contenenti calcio (incluso Numeta G13E)
somministrate con una una flebo in vena.
Il medico lo sa e non li somministrerà insieme, neanche attraverso diverse linee di infusione
o diversi siti di infusione.
Formazione di piccole particelle nei vasi sanguigni dei polmoni:
Anche la difficoltà respiratoria può essere un segno che si sono formate piccole particelle,
che bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Se il suo
bambino accusa difficoltà respiratorie, si rivolga al pediatra o infermiere. Essi decideranno
quali azioni intraprendere.
Infezioni e Sepsi
Il medico controllerà accuratamente il suo bambino per qualsiasi segnale di infezione.
Il rischio di infezione può essere ridotto usando una “tecnica asettica” (tecnica priva di germi)
durante il posizionamento e la manutenzione del catetere, come anche nella preparazione della
formula nutrizionale.
A volte, i bambini possono sviluppare infezione e sepsi (presenza di batteri nel sangue)
quando viene inserito un tubo in vena (catetere endovenoso). Alcuni medicinali e alcune
malattie possono aumentare il rischio di sviluppare un'infezione o la sepsi. I pazienti che
necessitano di nutrizione parenterale (somministrazione di nutrimento attraverso un tubo
inserito in vena) possono essere maggiormente soggetti allo sviluppo di un'infezione a
causa delle loro condizioni mediche.
Sindrome da sovraccarico di grassi
La sindrome da sovraccarico di grassi è stata riportata con medicinali simili. Una ridotta o
limitata capacità di rimuovere i lipidi presenti in Numeta G13E o un sovradosaggio
possono provocare una "sindrome da sovraccarico di grassi". (Vedere il paragrafo 3 ed il
paragrafo 4).
Alterazioni nei parametri chimici del sangue
Il medico controllerà e verificherà i fluidi, la composizione chimica del sangue ed altri
parametri del sangue del suo bambino durante il trattamento con Numeta G13E. A volte,
la rialimentazione di pazienti gravemente malnutriti può determinare alcune alterazioni dei
livelli chimici del sangue che necessitano di essere corrette. Inoltre, si possono verificare
gonfiore e presenza di quantità eccessive di fluidi nei tessuti. Si raccomanda di iniziare la
nutrizione parenterale lentamente e con la massima attenzione.
Monitoraggio e aggiustamenti:
Il medico manterrà il suo bambino sotto stretto controllo e aggiusterà il dosaggio di
Numeta G13E per rispondere alle esigenze individuali del bambino, specialmente se
presenta le seguenti condizioni:
- condizioni post-traumatiche gravi
- diabete mellito grave
- shock
- attacco cardiaco
- infezione grave
- alcuni tipi di coma
Utilizzare con cautela:
Numeta G13E deve essere utilizzato con cautela se il suo bambino ha:
- edema polmonare (fluido nei polmoni) o insufficienza cardiaca;
- gravi problemi epatici;
- problemi nell'utilizzo corretto degli elementi nutritivi;
- iperglicemia;
- problemi renali;
- gravi disturbi metabolici (incapacità dell'organismo di scomporre le sostanze in modo normale);
- patologie della coagulazione del sangue. Lo stato dei fluidi del suo bambino, i valori di funzionalità epatica e/o i valori del sangue verranno attentamente controllati. Vi sono informazioni limitate sulla somministrazione di questo medicinale nei neonati pretermine (prematuri) di meno di 28 settimane di età gestazionale.
Altri medicinali e NumetaG13E
Informi il medico se il suo bambino sta assumendo o utilizzando, o ha recentemente assunto
o potrebbe assumere qualsiasi altro medicinale.
- Numeta G13E non deve non deve essere somministrato contemporaneamentea:ceftriaxone(un antibiotico) neanche attraverso linee d’infusione separate a causa del rischio di formazione di particelle.
- sanguetramite lo stesso set d'infusione a causa del rischio di pseudoagglutinazione (formazione di grumi di globuli rossi).
- Ampicillina, fosfenitoina o furosemideattraverso la stessa linea d’infusione a causa del rischio di formazione di particelle.
Cumarina e warfarin (Anticoagulanti):
Il medico visiterà con cura il suo bambino se sta assumendo cumarina o warfarin. Questi
farmaci sono anticoagulanti che impediscono la coagulazione del sangue. L’olio di oliva e
l’olio di soia hanno un contenuto naturale di vitamina K1. La vitamina K1 può interferire
con i medicinali quali la cumarina e la warfarin.
Analisi di laboratorio
I lipidi contenuti in questa emulsione possono interferire con i risultati di determinati test
di laboratorio. I test di laboratorio possono essere eseguiti dopo un periodo di 5-6 ore
dall'uso dei lipidi quando non vengono somministrati lipidi aggiuntivi
Interazioni di Numeta G13E con medicinali che possono alterare i livelli/metabolismo
del potassio
Numeta G13E contiene potassio. Alte concentrazioni di potassio nel sangue possono
causare un ritmo cardiaco anormale. Prestare particolare attenzione in pazienti che
assumono diuretici (medicinali che riducono la ritenzione dei fluidi), ACE-inibitori
(medicinali per la pressione alta) o antagonisti del recettore dell’angiotensina II (medicinali
per la pressione alta) o immunosoppressori (medicinali che possono abbassare le normali
difese immunitarie del corpo). Queste tipologie di medicinali possonoaumentare i livelli di
potassio.
3. Come viene somministrato Numeta G13E
Al suo bambino deve sempre essere somministrato Numeta G13E esattamente come
indicato dal medico. Controlli con il medico se non è sicuro.
Gruppi di età
Numeta G13E è stato ideato per rispondere alle esigenze nutrizionali dei neonati
pretermine.
Numeta G13E potrebbe non essere adeguato per alcuni neonati pretermine, in quanto la
loro condizione clinica potrebbe richiedere formulazioni personalizzate per soddisfarele
loro esigenze nutrizionali specifiche. Il medico deciderà se questo medicinale è adatto per
il suo bambino.
Somministrazione
Questo medicinale è una emulsione per infusione. Viene data tramite un tubo di plastica in
una vena del braccio o in una grande vena del torace del suo bambino.
Il pediatra potrebbe decidere di non somministrare lipidi al bambino. La sacca di Numeta
G13E è ideata in modo da permettere la rottura della sola membrana di separazione che
separa il compartimento degli amminoacidi/elettroliti e il compartimento del glucosio. In
questo caso, la membrana di separazione tra il compartimento degli amminoacidi e il
compartimento dei lipidi rimane intatta. Il contenuto della sacca può quindi essere infuso
senza lipidi.
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione (vedere il paragrafo 2).
Dosaggio e durata del trattamento
Il medico deciderà la dose e per quanto tempo sarà somministrata. Il dosaggio dipende
dalle esigenze nutrizionali del suo bambino. Il dosaggio si baserà sul peso del suo bambino,
sullo stato clinico e sulla capacità del suo corpo di scomporre e utilizzare i costituenti di
Numeta G13E. Potranno essere anche dati nutrienti o proteine aggiuntive per via
orale/enterale.
Se al suo bambino viene dato troppo Numeta G13E
Sintomi
Dosi eccessive di questo medicinale, o una somministrazione troppo veloce possono
causare quanto segue:
- nausea (sentirsi male)
- vomito
- brividi
- squilibri elettrolitici (quantità anomale di elettroliti nel sangue)
- segni di ipervolemia (aumento del volume ematico in circolo, eccesso di liquidi nei vasi sanguigni)
- acidosi (aumento dell'acidità del sangue) In tali situazioni interrompere immediatamente l'infusione. Il medico deciderà se sono necessarie ulteriori misure. Un sovradosaggio dei grassi contenuti in Numeta G13E può provocare una "sindrome da sovraccarico di grassi", che solitamente è reversibile dopo l'interruzione dell'infusione. Nei neonati e nei bambini piccoli (lattanti), la sindrome da sovraccarico di grassi è stata associata a disturbi respiratori che portano a una riduzione dell'ossigeno nel corpo
(difficoltà respiratoria) e a condizioni che portano ad un aumento dell'acidità del sangue
(acidosi).
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la condizione del
suo bambino e controllerà i suoi livelli del sangue durante il trattamento.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati, sebbene non
tutti i bambini li manifestino.
Se nota cambiamenti nello stato di salute del suo bambino, durante o dopo il trattamento,
lo comunichi prontamente al medico o all'infermiere.
Gli esami che effettuerà il medico mentre il suo bambino assume il medicinale riducono i
rischi di effetti indesiderati.
In caso di comparsa di segni di reazione allergica, l’infusione deve essere interrotta e
bisogna contattare immediatamente il medico. Ciò può essere grave ed i segni possono
includere:
- sudorazione
- brividi
- mal di testa
- eruzioni cutanee
- difficoltà respiratorie Altri effetti indesiderati che sono stati osservati sono: Comuni(possono interessare fino a 1 su 10 persone):
- Un livello basso di fosfati nel sangue (ipofosfatemia)
- Un livello elevato di zuccheri nel sangue (iperglicemia)
- Un livello elevato di calcio nel sangue (ipercalcemia)
- Un livello elevato di trigliceridi nel sangue (ipertrigliceridemia)
- Un'alterazione elettrolitica (iponatriemia) Non comuni (possono interessare fino a 1 su 100 persone):
- Un livello elevato di lipidi nel sangue (iperlipidemia).
- Una condizione in cui la bile non riesce a scorrere dal fegato al duodeno (colestasi). Il duodeno fa parte dell'intestino.
Non nota: la frequenza non può essere stimata sulla base dei dati disponibili(Queste
reazioni avverse sono state segnalate solo per Numeta G13E e G16E quando
somministrati per via periferica con diluizione insufficiente). :
- Necrosi cutanea
- Lesione dei tessuti molli
- Stravaso
Sono stati segnalati i seguenti effetti indesiderati con altri medicinali per nutrizione
parenterale:
La ridotta o limitata capacità di rimuovere i lipidi contenuti in Numeta può risultare in
una “sindrome da sovraccarico di grassi”. I seguenti segni e sintomi di questa sindrome
sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
o peggioramento improvviso e inatteso della condizione medica del paziente
o livelli elevati di grassi nel sangue (iperlipidemia)
o febbre
o infiltrazione di grasso nel fegato (epatomegalia)
o deterioramento della funzionalità del fegato
o riduzione dei globuli rossi che può rendere pallida la pelle e causare senso di
debolezza o affanno (anemia)
o bassa conta dei globuli bianchi, che può aumentare il rischio di infezione
(leucopenia)
o bassa conta delle piastrine, che può aumentare il rischio di ecchimosi e/o
sanguinamento (trombocitopenia)
o alterazioni della coagulazione che compromettono la capacità del sangue di
coagularsi
o Disturbi respiratori che comportano una riduzione dell'ossigeno nel corpo
(difficoltà respiratoria)
o Condizioni che portano ad un aumento dell'acidità del sangue (acidosi)
o coma, che richiede il ricovero ospedaliero
- Formazione di particelle che può provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) o difficoltà respiratorie.
Segnalazione di effetti indesiderati
Se il suo bambino manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati
in questo foglio, si rivolga al medico o all'infermiere.
Lei può inoltre segnalare gli effetti indesiderati direttamente (vedere i dettagli di seguito).
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla
sicurezza di questo medicinale.
Gli effetti indesiderati possono, inoltre, essere segnalati direttamente tramite il sistema
nazionale di segnalazione all’indirizzo https://www.aifa.gov.it/content/segnalazioni-
reazioni-avverse.
5. Come conservare Numeta G13E
Tenere il medicinale fuori dalla vista e dalla portata dei bambini quando non viene
somministrato.
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione (vedere il paragrafo 2).
Non usi questo medicinale dopo la data di scadenza che è riportata sulla sacca e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del
mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico o nei rifiuti domestici. Chieda al
farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere
l’ambiente.
6. Contenuto della confezione ed altre informazioni
Descrizione dell'aspetto di Numeta G13 e contenuto della confezione
Numeta G13E si presenta sotto forma di sacca a tre compartimenti. Ogni sacca contiene
una combinazione sterile di una soluzione di glucosio, una soluzione pediatrica di
amminoacidi, con elettroliti, e un'emulsione lipidica, come descritto di seguito.
| Dimensioni contenitore | Soluzione di glucosio al 50% | Soluzione di amminoacidi al 5,9% con elettroliti | m Emulsione di r lipidi al 12,5% |
| 300 mL | 80 mL | 160 mL | a 60 mL |
Aspetto prima della ricostituzione:
Le soluzioni nei compartimenti di amminoacidi e glucosio sono limpide, incolori
o leggermente gialle
Il compartimento dell'emulsione di lipidi contiene un liquido uniforme di color
bianco latte
Aspetto dopo la ricostituzione:
- La soluzione per infusione “2 in 1” (amminoacidi/elettroliti e glucosio) per infusione è limpida, incolore o leggermente gialla L’emulsione per infusione “3 in 1” è uniforme di color bianco latte
La sacca a tre compartimenti è una sacca in plastica multistrato.
Per impedire il contatto con l'aria, la sacca di Numeta G13E è confezionata in un involucro
esterno con barriera per l'ossigeno, che contiene anche un assorbitore di ossigeno e un
indicatore di ossigeno.
Confezioni:
sacca da 300 ml: 10 unità per scatola in cartone
1 sacca da 300 ml
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Via Del Serafico 89
00142 Roma
Italia
Produttore responsabile del rilascio lotti:
Baxter SA
Boulevard René Branquart 80
7860 Lessines
(Belgio)
Questo medicinale è autorizzato negli Stati Membri dello Spazio Economico
Europeo con le seguenti denominazioni:
| Austria Germany | m Numeta G 13 % E Emulsion zur Infusion |
| Belgium Luxembourg | r a NUMETZAH G13%E, émulsion pour perfusion |
| France | F NUMETAH G13%E PREMATURES, emulsion pour perfusion |
| Denmark Norway Sweden | l e Numeta G13E |
| Czech Republic | d Numeta G 13 % E |
| Greece | a NUMETA Preterm G 13 E |
| Netherlands | n Numeta G13%E emulsie voor infusie |
| Ireland Malta United Kingdom | a i Numeta G13%E Preterm, Emulsion for Infusion |
| Italy | l a Numeta G13E emulsione per infusione t |
| Finland | I Numeta G13E infuusioneste, emulsio |
| a i Poland | Numeta G 13 % E Preterm |
| z n Portugal | Numeta G13%E |
| e g Spain | Numeta G13%E, emulsión para perfusión |
Le informazioni seguenti sono destinate esclusivamente ai professionisti medici o
operatori sanitari*
*Si tenga presente che in alcuni casi questo medicinale può essere somministrato a casa
dai genitori o da altre persone che ne hanno cura. In questi casi i genitori o chi ne ha cura
devono leggere queste informazioni.
Non effettuare aggiunte alla sacca prima di verificarne la compatibilità. Si potrebbero
formare particelle o si potrebbe rompere l’emulsione lipidica. Ciò porterebbe al blocco dei
vasi sanguigni.
Numeta G13E deve essere a temperatura ambiente prima dell'uso.
Prima di usare Numeta G13E, preparare la sacca come mostrato di seguito.
Verificare che la sacca non sia danneggiata. Usare la sacca solo se non è danneggiata.
L'aspetto di una sacca integra è così:
- Le membrane di separazione non permanenti sono intatte. Questo indica l'assenza di miscelazione del contenuto dei tre compartimenti.
- Le soluzioni di amminoacidi e di glucosio sono limpide, incolori o leggermente gialle, senza particelle visibili.
- L'emulsione di lipidi è un liquido uniforme di color bianco latte.
Prima di aprire l'involucro esterno, controllare il colore dell'indicatore di ossigeno.
Confrontarlo con il colore di riferimento stampato accanto al simbolo OK
nell'area stampata dell'etichetta dell'indicatore.
Non usare la sacca se il colore dell'indicatore di ossigeno non corrisponde al
colore di riferimento stampato accanto al simbolo OK.
Le figure 1 e 2 illustrano come rimuovere l'involucro esterno di protezione. Gettare
l'involucro esterno, l’indicatore di ossigeno e l'assorbitore di ossigeno








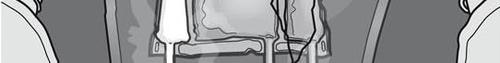

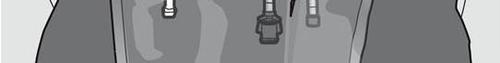





Figura 1 Figura 2
Preparazione dell’emulsione miscelata:
assicurarsi che il medicinale sia a temperatura ambiente quando si rompono le
membrane di separazione non permanenti.
Porre la sacca su una superficie piana e pulita.
Attivazione della sacca a 3 compartimenti (miscelazione delle 3 soluzioni mediante
rottura delle 2 membrane non permanenti)
Step 1: Iniziare arrotolando la sacca dal lato dell'occhiello a D
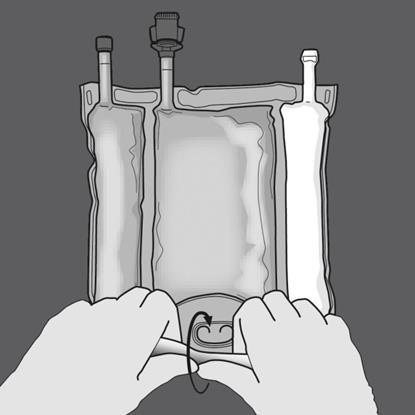
Step 2: Fare pressione finché le membrane di separazione non siano aperte.
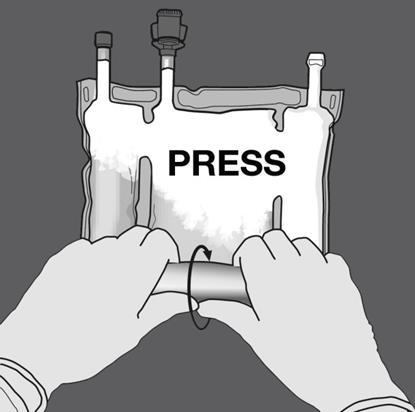
Step 3: Cambiare direzione arrotolando la sacca verso l’occhiello a D. Continuare fino a
che la membrana è completamente aperta.
Procedere allo stesso modo per completare l'apertura della seconda membrana.
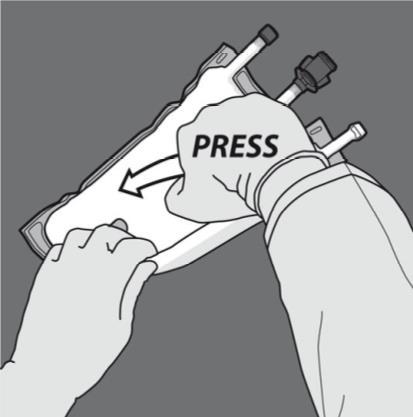
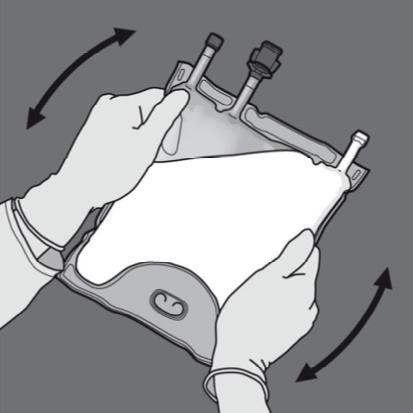
Step 4: Capovolgere la sacca almeno tre volte per miscelare completamente il contenuto.
L'aspetto della soluzione miscelata dovrebbe essere simile a un’emulsione di color bianco
latte
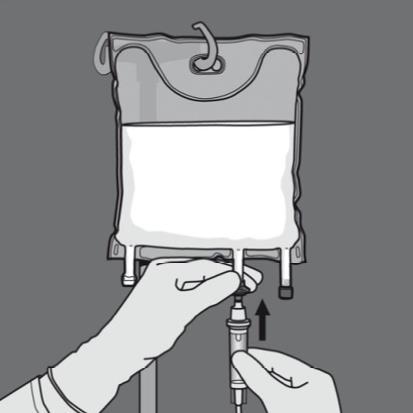
Step 5: Rimuovere il cappuccio protettivo dal punto di somministrazione e inserire il set
di infusione per via endovenosa
Attivazione della sacca a due compartimenti (miscelazione delle 2 soluzioni attraverso la
rottura della membrana non permanente tra il compartimento degli amminoacidi e il
compartimento con glucosio)
Step 1:
Per miscelare solo 2 soluzioni, arrotolare la sacca dall’angolo superiore (estremità con
l’occhiello) della membrana che separa le soluzioni.
Fare pressione per aprire la membrana che separa i compartimenti di glucosio e
amminoacidi.







Step 2: Posizionare la sacca in modo che il compartimento contenente l’emulsione lipidica
sia il più vicino all’operatore.
Arrotolare la sacca proteggendo il compartimento dell’emulsione lipidica con i palmi delle
mani
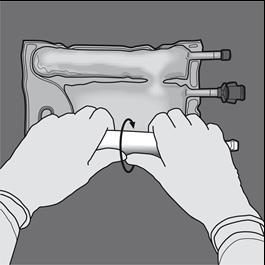
Step 3: Con una mano, fare pressione arrotolando la sacca verso i punti di iniezione.
















Step 4:
Cambiare direzione arrotolando la sacca verso il lato superiore (estremità con
l’occhiello).
Premere con l’altra mano, continuando fino a che la membrana che separa le soluzioni di
amminoacidi e glucosio è completamente aperta.
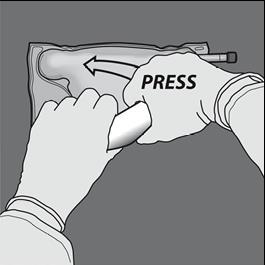
Step 5: Capovolgere la sacca almeno tre volte per miscelare completamente il contenuto.
L'aspetto della soluzione miscelata dovrebbe essere chiaro, incolore o leggermente giallo.
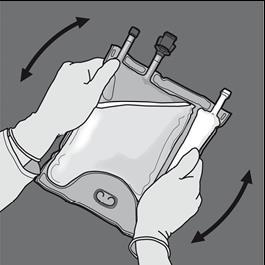
Step 6: Rimuovere il cappuccio protettivo dal punto di somministrazione e inserire il set
di infusione per via endovenosa.
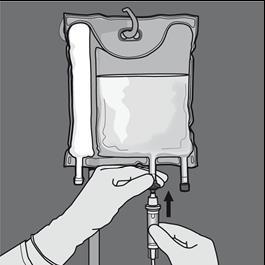
La velocità del flusso deve essere aumentata gradualmente durante la prima ora. La
velocità di somministrazione del flusso deve essere regolata in base ai fattori seguenti:
dose da somministrare
i volumi da assumere quotidianamente
la durata dell'infusione
Modo di somministrazione
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione.
E’ raccomandato l’utilizzo di un filtro da 1,2 micron per la somministrazione di Numeta
G13E.
Per la sua alta osmolarità, Numeta G13E non diluito può essere somministrato solo
attraverso una vena centrale. Tuttavia, una sufficiente diluizione di Numeta G13E con
acqua per preparazioni iniettabili riduce l'osmolarità e permette l'infusione periferica.
La formula che segue indica l’effetto della diluizione sull'osmolarità delle sacche.

La tabella che segue mostra esempi di osmolarità per miscelazioni di 2CB attivati e 3CB
attivati dopo l'aggiunta di acqua per preparazioni iniettabili:
| a Amminoacidi e glucosio (2CB attivati) | Amminoacidi, glucosio e lipidi (3CB attivati) | |
| Volume iniziale nella sacca (mL) | i 240 | 300 |
| Osmolarità iniziale (appross. mOsm/L) | l a 1400 | 1150 |
| Volume di acqua aggiunta (mL) | t 240 | 300 |
| I Volume finale dopo l'aggiunta (mL) | 480 | 600 |
| a Osmolarità dopo l'aggiunta (mOsm/L appross.) | 700 | 575 |
Aggiunte di additivi:
L’esposizione alla luce di soluzioni per nutrizione parenterale endovenosa, specialmente
dopo aggiunta di oligoelementi e/o vitamine, può avere effetti avversi sull’esito clinico nei
neonati a causa della generazione di perossidi e altri prodotti di degradazione. Quando
impiegata in neonati e bambini di età inferiore a 2 anni, Numeta G13E deve essere protetta
dalla luce ambientale fino al completamento della somministrazione.
Additivi compatibili possono essere aggiunti attraverso il sito di iniezione nella miscela
ricostituita (dopo l'apertura delle membrane non permanenti e dopo la miscelazione del
contenuto dei due o tre compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che
la miscela sia ricostituita (prima dell'apertura delle membrane di separazione non
permanenti e prima della miscelazione delle soluzioni e dell'emulsione).
Eventuali aggiunte di soluzioni di oligoelementi (identificati come TE1 e TE4), vitamine (
identificate come liofilizzato V1 e emulsione V2), e elettroliti disponibili in commercio in
quantità definite sono mostrate nelle tabelle 1-4.
- 1.Compatibilità con TE4, V1 e V2
Tabella 1: Compatibilità della sacca 3-in-1 (3CB attivati) con e senza diluizione con acqua
| i Per 300 mL (3 in 1 miscela con lipidi) | ||||||
| l Miscela non diluita | Miscela diluita | |||||
| Aggiunte | Livello incluso | a Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 6,6 | t 5,0 | 11,6 | 6,6 | 5,0 | 11,6 |
| Potassio (mmol) | I 6,2 | 4,2 | 10,4 | 6,2 | 4,2 | 10,4 |
| Magnesio (mmol) | 0,47 | 0,83 | 1,3 | 0,47 | 0,83 | 1,3 |
| Calcio (mmol) | 3,8 | 3,5 | 7,3 | 3,8 | 3,5 | 7,3 |
| Fosfato* (mmol) | a 3,8 | 2,5 | 6,3 | 3,8 | 2,5 | 6,3 |
| Oligoelementi e vitamine | i | 15 mL TE4 + 1,5 fiala V1 + 25 mL V2 | 15 mL TE4 + 1,5 fiala V1 + 25 mL V2 | 15 mL TE4 + 1,5 fiala V1 + 25 mL V2 | 15 mL TE4 + 1,5 fiala V1 + 25 mL V2 | |
| Acqua per soluzioni iniettabili | z | 300 mL | 300 mL | |||
Tabella 2: Compatibilità della sacca 2-in-1 (2CB attivati) con e senza diluizione con acqua
| Per 240 mL (2 in 1 miscela senza lipidi) | ||||||
| Miscela non diluita | a Miscela diluita | |||||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | m Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 6,4 | 17,6 | 24 | 6,4 | 0,0 | 6,4 |
| Potassio (mmol) | 6,2 | 17,8 | 24 | r 6,2 | 0,0 | 6,2 |
| Magnesio (mmol) | 0,47 | 2,13 | 2,6 | 0,47 | 0,0 | 0,47 |
| Calcio (mmol) | 3,8 | 3,5 | 7,3 | a 3,8 | 0,0 | 3,8 |
| Fosfato* (mmol) | 3,2 | 4,0 | 7,2 | 3,2 | 0,0 | 3,2 |
| Oligoelementi e vitamine | 2,5 mL TE4 + ¼ fiala V1 | 2,5 mL TE4 + ¼ fiala V1 | F | 2,5 mL TE4 + ¼ fiala V1 | 2,5 mL TE4 + ¼ fiala V1 | |
| Acqua per soluzioni iniettabili | l | 240 mL | 240 mL | |||
- 2.Compatibilità con TE1, V1 e V2Tabella 3: Compatibilità della sacca 3-in-1 (3CB attivati) con e senza diluizione con acqua
| Per 300 mL (3 in 1 miscela con lipidi) | ||||||
| Miscela non diluita | Miscela diluita | |||||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | a Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 6,6 | n 5,0 | 11,6 | 6,6 | 0,0 | 6,6 |
| Potassio (mmol) | 6,2 | 4,2 | 10,4 | 6,2 | 0,0 | 6,2 |
| Magnesio (mmol) | 0,47 | a 0,83 | 1,3 | 0,47 | 0,0 | 0,47 |
| Calcio (mmol) | 3,8 | i 1,9 | 5,7 | 3,8 | 0,0 | 3,8 |
| Fosfato* (mmol) | 3,8 | 2,5 | 6,3 | 3,8 | 0,0 | 3,8 |
| Oligoelementi e vitamine | l a 2,5 mL TE1 + ¼ fiala V1 + 2,5 mL V2 | 2,5 mL TE1 + ¼ fiala V1 + 2,5 mL V2 | 2,5 mL TE1 + ¼ fiala V1 + 2,5 mL V2 | 2,5 mL TE1 + ¼ fiala V1 + 2,5 mL V2 | ||
| Acqua per soluzioni iniettabili | t | 300 mL | 300 mL | |||
Tabella 4: Compatibilità della sacca 2-in-1 (2CB attivati) con e senza diluizione con acqua
| Per 240 mL (2 in 1 miscela senza lipidi) | ||||||
| i Miscela non diluita | Miscela diluita | |||||
| Aggiunte | z Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| n Sodio (mmol) | 6,4 | 17,6 | 24 | 6,4 | 0,0 | 6,4 |
| Potassio (mmol) | 6,2 | 17,8 | 24 | 6,2 | 0,0 | 6,2 |
| e Magnesio (mmol) | 0,47 | 2,13 | 2,6 | 0,47 | 0,0 | 0,47 |
| Calcio (mmol) | 3,8 | 3,5 | 7,3 | 3,8 | 0,0 | 3,8 |
| g Fosfato* (mmol) | 3,2 | 4,0 | 7,2 | 3,2 | 0,0 | 3,2 |
| Oligoelementi e vitamine | 2,5 mL TE1 + ¼ fiala V1 | 2,5 mL TE1 + ¼ fiala V1 | 2,5 mL TE1 + ¼ fiala V1 | 2,5 mL TE1 + ¼ fiala V1 | ||
| A Acqua per soluzioni iniettabili | 240 mL | 240 mL | ||||
La composizione delle preparazioni di vitamine e oligoelementi sono illustrate nelle tabelle 5 e 6.
Tabella 5: Composizione del preparato commerciale di oligoelementi utilizzato:
| Composizione per fiala | TE1 (10 ml) | TE4 (10 ml) |
| Zinco | 38,2 µmol o 2,5 mg | 15,3 µmol o 1 mg |
| Selenio | 0,253 µmol o 0,02 mg | 0,253 µmol o 0,02 mg |
| Rame | 3,15 µmol or 0,2 mg | 3,15 µmol o 0,2 mg |
| Iodio | 0,0788 µmol o 0,01 mg | 0,079 µmol o 0,01 mg |
| Fluoro | 30 µmol o 0,57 mg | |
| Manganese | 0,182 µmol o 0,01 mg | 0,091 µmol o 0,005 mg |
Tabella 6: Composizione del preparato commerciale di vitamine utilizzato:
Per eseguire un'aggiunta:
- Operare in condizioni asettiche
- Preparare il punto d'iniezione della sacca
- Forare il punto di iniezione e iniettare le aggiunte mediante un ago per iniezione o un dispositivo di ricostituzione
- Miscelare il contenuto della sacca e le aggiunte
| Composizione per fiala | V1 | a V2 |
| Vitamina B1 | 2,5 mg | n |
| Vitamina B2 | 3,6 mg | |
| Nicotinamide | a 40 mg | |
| Vitamina B6 | 4,0 mg | |
| Acido Pantotenico | i 15,0 mg | |
| Biotina | l 60 µg | |
| Acido Folico | a 400 µg | |
| Vitamina B12 | 5,0 µg | |
| Vitamina C | t 100 mg | |
| Vitamina A | I | 2300 IU |
| Vitamina D | 400 IU | |
| Vitamina E | 7 IU | |
| Vitamina K | a | 200 µg |
Preparazione dell'infusione:
- Operare in condizioni asettiche
- Sospendere la sacca
- Rimuovere la protezione in plastica dal punto di somministrazione
- Inserire saldamente lo spike del set di infusione nel punto di somministrazione
Somministrazione dell'infusione:
- Solo per uso singolo
- Somministrare il medicinale solo dopo l'apertura delle membrane di separazione non permanenti tra i due o tre compartimenti e la miscelazione del contenuto dei due o tre compartimenti
- Assicurarsi che l'emulsione finale per infusione dei 3 compartimenti attivati non mostri alcuna prova di separazione delle fasi o che la soluzione per infusione finale dei 2 compartimenti attivati non mostri alcuna presenza di particelle
- Dopo la rottura delle membrane non permanenti, il contenuto si deve usare immediatamente. Numeta G13E non deve essere conservato per un'infusione successiva
- Non collegare eventuali sacche parzialmente utilizzate
- Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa a causa di possibili residui gassosi contenuti nella sacca principale
- E’ raccomandato l’utilizzo di un filtro da 1,2 micron per la somministrazione di Numeta G13E
- Quando impiegata in neonati e bambini di età inferiore a 2 anni, proteggere dall’esposizione alla luce fino al completamento della somministrazione. L’esposizione di Numeta G13E alla luce ambientale, specialmente dopo aggiunta di oligoelementi e/o vitamine, genera perossidi e altri prodotti di degradazione che possono essere ridotti con la protezione dall’esposizione alla luce. Qualsiasi eventuale prodotto non utilizzato, rifiuti derivati e tutti i dispositivi usa e getta necessari devono essere smaltiti correttamente e non riutilizzati
Periodo di validità dopo la ricostituzione
Utilizzare il medicinale immediatamente dopo l'apertura delle membrane non permanenti
tra i due o tre compartimenti. Gli studi di stabilità delle miscele sono stati condotti per 7
giorni a una temperatura compresa tra 2°C e 8°C, seguiti da 48 ore a 30°C.
Periodo di validità dopo l'integrazione (elettroliti, oligoelementi, vitamine, acqua):
Per specifiche miscelazioni, la stabilità fisica della formulazione Numeta è stata dimostrata
a una temperatura compresa tra 2 °C e 8 °C per 7 giorni, seguita da 48 ore a 30°C. Le
informazioni su queste aggiunte sono specificate nel paragrafo 6.6 dell’RCP (Riassunto
delle Caratteristiche del Prodotto).
Da un punto di vista microbiologico, il medicinale deve essere utilizzato immediatamente.
In caso contrario, i tempi e le condizioni di conservazione dopo la miscelazione e prima
dell’uso sono responsabilità dell'utente e non devono superare le 24 ore, a temperatura
compresa tra 2°C e 8°C, a meno che la ricostituzione /diluizione/integrazione non sia
avvenuta in condizioni asettiche controllate e convalidate.
Non usare Numeta G13E se la sacca è danneggiata. Questo è l'aspetto di una sacca
danneggiata:
- le membrane di separazione non permanenti sono rotte
- uno dei compartimenti contiene una miscela delle soluzioni
- le soluzioni di amminoacidi e di glucosio non sono limpide, incolori o leggermente gialle e/o contengono particelle visibili
- l'emulsione di lipidi non è un liquido uniforme di color bianco latte.
I medicinali non devono essere gettati nell’acqua di scarico e nei rifiuti domestici. Chieda
al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere
l’ambiente.
Cosa contiene Numeta G13E:
I principi attivi sono:
| o Composizione | ||
| Principio attivo | 2CB attivati (240 ml) | c 3CB attivati (300 ml) |
| Compartimento Amminoacidi | a | |
| Alanina | 0,75 g | 0,75 g |
| Arginina | m 0,78 g | 0,78 g |
| Acido aspartico | 0,56 g | 0,56 g |
| Cisteina | r 0,18 g | 0,18 g |
| Acido glutammico | a 0,93 g | 0,93 g |
| Glicina | F 0,37 g | 0,37 g |
| Istidina | 0,35 g | 0,35 g |
| Isoleucina | 0,62 g | 0,62 g |
| l Leucina | 0,93 g | 0,93 g |
| e Lisina monoidrata (come lisina) | 1,15 g (1,03 g) | 1,15 g (1,03 g) |
| d Metionina | 0,22 g | 0,22 g |
| a Ornitina cloridrata (come ornitina) | 0,30 g (0,23 g) | 0,30 g (0,23 g) |
| Fenilalanina | 0,39 g | 0,39 g |
| n Prolina | 0,28 g | 0,28 g |
| a Serina | 0,37 g | 0,37 g |
| i Taurina | 0,06 g | 0,06 g |
| l Treonina | 0,35 g | 0,35 g |
| Triptofano | 0,19 g | 0,19 g |
| a Tirosina | 0,07 g | 0,07 g |
| t Valina | 0,71 g | 0,71 g |
| I Potassio acetato | 0,61 g | 0,61 g |
| Calcio cloruro biidrato | 0,55 g | 0,55 g |
| a Magnesio acetato tetraidrato | 0,10 g | 0,10 g |
| i Sodio glicerofosfato idrato | 0,98 g | 0,98 g |
| z Compartimento Glucosio | ||
| n Glucosio monoidrato (come glucosio anidro) | 44,00 g (40,00 g) | 44,00 g (40,00 g) |
| Compartimento Lipidi | ||
| e Olio di oliva purificato (circa 80%) + olio di soia purificato (circa 20%) | 7,5 g | |
La soluzione/emulsione ricostituita fornisce quanto segue:
| c Composizione | ||||
| 2CB attivati | 3CB attivati | |||
| Per unità di volume (ml) Azoto (g) Amminoacidi (g) Glucosio (g) Lipidi (g) Energia Calorie totali (kcal) Calorie non proteiche (kcal) Calorie da glucosio (kcal) Calorie lipidiche (kcal)a Calorie non proteiche/azoto (kcal/g N) Calorie lipidiche/ calorie non proteiche (%) Calorie lipidiche /calorie totali (%) Elettroliti Sodio (mmol) Potassio (mmol) Magnesio (mmol) i Calcio (mmol) l Fosfato (mmol)b a Acetato (mmol) t Malato (mmol) Cloruro (mmol) | 240 1,4 9,4 40,0 0 198 160 160 0 113 ND a ND n 6,4 6,2 a 0,47 3,8 3,2 7,2 3,2 9,3 | 100 0,59 3,9 16,7 0 82 67 l 67 e 0 d 113 ND ND 2,7 2,6 0,20 1,6 1,3 3,0 1,3 3,9 | m 300 1,4 9,4 r 40,0 a 7,5 F 273 235 160 75 165 32 28 6,6 6,2 0,47 3,8 3,8 7,2 3,2 9,3 | a 100 0,47 3,1 13,3 2,5 91 78 53 25 165 32 28 2,2 2,1 0,16 1,3 1,3 2,4 1,1 3,1 |
| I pH (appross.) Osmolarità appross. (mOsm/L) | 5,5 1400 | 5,5 1400 | 5,5 1150 | 5,5 1150 |
Gli eccipienti sono:
NUMETA G16E, emulsione per infusione
Legga attentamente questo foglio prima di utilizzare questo medicinale perché
contiene importanti informazioni per Lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al suo pediatra, al farmacista, o all’infermiere.
- Se il suo bambino ha uno qualsiasi degli effetti indesiderati, informi il suo pediatra o l’infermiere. Questo potrebbe includere qualsiasi effetto indesiderato non elencato in questo foglietto. Vedere il paragrafo 4. Contenuto di questo foglio:
- 1.Che cos'è Numeta G16E e a che cosa serve
- 2. Cosa sapere prima che al suo bambino sia dato Numeta G16E
- 3. Come viene dato Numeta G16E
- 4. Possibili effetti indesiderati
- 5. Come conservare Numeta G16E
- 6. Contenuto della confezione ed altre informazioni
1. Che cos'è Numeta G16E e a che cosa serve
Numeta G16E è un’emulsione per nutrizione appositamente studiata per neonati a termine
e bambini fino a 2 anni. È somministrato attraverso un tubo che è posizionato nella vena
del suo bambino, quando il suo bambino non è in grado di prendere il suo nutrimento per
bocca.
Numeta si presenta in sacca a 3 compartimenti nella quale ciascun compartimento separato
contiene:
una soluzione di glucosio al 50%
una soluzione pediatrica di amminoacidi al 5,9%, con elettroliti
un'emulsione di lipidi (grassi) al 12,5%
A seconda delle esigenze del suo bambino, 2 o 3 di queste soluzioni sono miscelate insieme
nella sacca prima che venga dato al suo bambino.
Numeta deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che al suo bambino sia dato Numeta G16E
Al suo bambino non deve essere dato Numeta G16E nei seguenti casi:
Con 2 soluzioni miscelate nella sacca (2 in 1):
- Se il suo bambino è allergico alle proteine dell'uovo, alla soia, alle arachidi o ad uno qualsiasi dei componenti dei compartimenti di glucosio o amminoacidi (elencati nel paragrafo 6).
- Se il corpo del suo bambino ha problemi a formare "mattoncini" di proteine.
- Se il suo bambino ha nel sangue elevate concentrazioni di uno qualsiasi degli elettroliti inclusi in Numeta G16E.
- Se il suo bambino è neonato (≤28 giorni di età) Numeta G16E (o altre soluzioni contenenti calcio) non deve essere somministrato in contemporanea con ceftriaxone (un antibiotico), anche in caso di utilizzo di linee di infusione separate. C’è il rischio fatale di formazioni di particelle nel flusso sanguigno del neonato.
- Se il suo bambino soffre di iperglicemia (livelli di zuccheri nel sangue particolarmente alti).
Con 3 soluzioni miscelate nella sacca (3 in 1):
- Tutte le situazioni menzionate in “2 in 1” più la seguente:
- Se il suo bambino ha livelli di grassi nel sangue particolarmente elevati. In tutti i casi, il suo medico deciderà se il suo bambino dovrà ricevere questo medicinale sulla base di fattori quali età, peso e condizione clinica. Il suo medico terrà conto anche dei risultati degli esami eseguiti. Avvertenze e precauzioniParli con il suo pediatra o con l’infermiere prima che diano Numeta G16E. Quando impiegata in neonati e ambini di età inferiore a 2 anni, la soluzione (nelle sacche e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al completamento della somministrazione. L’esposizione di Numeta G16E alla luce ambientale, specialmente dopo aggiunta di oligoelementi e/o vitamine, genera perossidi e altri prodotti di degradazione che possono essere ridotti con la protezione dall’esposizione alla luce. Reazioni Allergiche:L'infusione deve essere interrotta immediatamente in caso di sviluppo di segni o sintomi di reazione allergica (ad esempio febbre, sudorazione, brividi, cefalea, rash cutanei o difficoltà respiratoria). Questo medicinale contiene olio di semi di soia che, raramente, può causare gravi reazioni di ipersensibilità. È stato osservato raramente che alcuni soggetti allergici alle proteine delle arachidi sono allergici anche alle proteine dei semi di soia. Numeta G16E contiene glucosio prodotto dall'amido di mais. Pertanto, Numeta G16E deve essere utilizzato con cautela nei pazienti con allergia nota al mais o ai prodotti derivati dal mais. Rischio di formazione di particelle con ceftriaxone (antibiotico):Un antibiotico che si chiama ceftriaxone non deve essere miscelato o somministrato contemporaneamente a qualsiasi soluzione contenente calcio (compreso Numeta G16E) somministrato a voi con una flebo in vena. Il medico lo sa e non ve li darà insieme, neanche attraverso diverse linee di infusione o diversi siti di infusione.
Tuttavia, il medico può dare il calcio e il ceftriaxone in sequenza uno dopo l'altro se sono
utilizzate linee di infusione in siti di infusione diversi o se le linee di infusione sono
sostituite o sono state accuratamente lavate con una soluzione salina fisiologica tra le
infusioni per evitare la precipitazione.
Formazione di piccole particelle nei vasi sanguigni dei polmoni:
Anche le difficoltà respiratorie potrebbero essere un segnale di formazione di piccole
particelle che bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Se il
suo bambino presenta una qualsiasi difficoltà di respirazione, informi il pediatra o
l'infermiere. Essi decideranno quali azioni intraprendere.
Infezioni e Sepsi:
Il suo medico controllerà accuratamente il suo bambino per qualsiasi segnale di infezione.
Il rischio di infezione può essere ridotto usando una “tecnica asettica” (tecnica priva di
germi) durante il posizionamento e la manuntenzione del catetere come anche nella
preparazione della formula nutrizionale.
A volte, i bambini possono sviluppare un'infezione e sepsi (presenza di batteri nel sangue)
quando viene inserito un tubo in vena (catetere endovenoso). Alcuni medicinali e alcune
malattie possono aumentare il rischio di sviluppare un'infezione o la sepsi. I pazienti che
necessitano di nutrizione parenterale (somministrazione di nutrimento attraverso un tubo
inserito in vena) possono essere maggiormente soggetti allo sviluppo di un'infezione a
causa delle loro condizioni mediche.
Sindrome da sovraccarico di grassi:
La sindrome da sovraccarico di grassi è stata riportata con prodotti simili. Una ridotta o
limitata capacità di rimuovere i lipidi presenti in Numeta G16E o un sovradosaggio
possono provocare una "sindrome da sovraccarico di grassi". (Vedere il paragrafo 3 ed il
paragrafo 4 -).
Alterazioni nei parametri chimici del sangue:
Il suo medico controllerà e valuterà i fluidi, la composizione chimica del sangue ed altri
parametri del sangue del suo bambino, dato che, a volte, la rialimentazione di pazienti
gravemente malnutriti può determinare alcuni cambiamenti dei livelli chimici del sangue.
Inoltre, si possono verificare gonfiore e presenza di quantità eccessive di fluidi nei tessuti.
Si consiglia di iniziare la nutrizione parenterale lentamente e con la massima attenzione.
Livello elevato di magnesio nel sangue:
La quantità di magnesio contenuta in Numeta G16E potrebbe causare l’aumento del livello
di magnesio nel sangue. I segni di questo problema possono includere debolezza, riflessi
lenti, nausea, vomito, livelli bassi di calcio nel sangue, difficoltà respiratoria, pressione
arteriosa bassa e battito cardiaco irregolare. Poiché potrebbe essere difficile rilevare tali
segni, il medico potrebbe controllare i valori del sangue del bambino, in particolare se il
bambino presenta fattori di rischio per un livello elevato di magnesio nel sangue, compresa
una funzionalità renale ridotta. Se il livello di magnesio nel sangue è elevato, l’infusione
verrà interrotta o ridotta.
Monitoraggio e Aggiustamenti:
Il suo medico manterrà il suo bambino sotto stretto controllo e aggiusterà il dosaggio di
Numeta G16E per rispondere alle esigenze individuali del bambino se presenta le seguenti
condizioni:
- condizioni post-traumatiche gravi
- diabete mellito grave
- shock
- infarto
- infezione grave
- alcuni tipi di coma
Utilizzare con attenzione:
Numeta deve essere usato con attenzione se il suo bambino ha:
- Edema polmonare (fluido nei polmoni) o insufficienza cardiaca.
- Gravi problemi epatici.
- Problemi con l’utilizzo dei nutrienti.
- Elevate concentrazioni di zucchero nel sangue.
- Problemi renali.
- Scompensi metabolici gravi (quando il corpo non riesce a suddividere le sostanze in modo normale).
- Disordini della coagulazione. Lo stato dei fluidi del suo bambino, i valori di funzionalità epatica e/o i valori del sangue verranno attentamente controllati.
Altri medicinali e Numeta G16E
Informi il suo medico se il suo bambino stà prendendo o utilizzando, o ha recentemente
preso o potrebbe utilizzare qualsiasi altra medicina.
Numeta non deve essere dato nello stesso tempo con:
- ceftriaxone(un antibiotico) neanche attraverso linee d’infusione separate a causa del rischio di formazione di precipitato (particelle).
- sangueper mezzo dello stesso set d'infusione a causa del rischio di pseudoagglutinazione (formazione di grumi di globuli rossi).
- Ampicillina, fosfenitoina o furosemideattraverso la stessa linea d’infusione a causa del rischio di formazione di particelle.
Cumarina e warfarina (Anticoagulanti):
Il suo medico guarderà attentamente il suo bambino se sta assumendo cumarina o
warfarina. L'olio di oliva e l'olio di semi di soia hanno un contenuto naturale di vitamina
K1. La vitamina K1 può interferire con i medicinali quali la cumarina e la warfarina. Questi
farmaci sono anticoagulanti che impediscono la coagulazione del sangue.
Analisi di laboratorio:
I lipidi contenuti in questa emulsione possono interferire con i risultati di determinati test
di laboratorio. I test di laboratorio possono essere eseguiti dopo un periodo di 5-6 ore
dall'uso dei lipidi quando non vengono somministrati lipidi aggiuntivi.
Interazioni di Numeta G16E su farmaci che possono alterare i livelli/metabolismo del
potassio:
Numeta contiene potassio. Alte concentrazioni di potassio nel sangue possono causare un ritmo
cardiaco anormale. Prestare particolare attenzione in pazienti che assumono diuretici (farmaci che
riducono la ritenzione dei fluidi), ACE-inibitori (farmaci per la pressione alta) o antagonisti del
recettore dell’angiotensina II (farmaci per la pressione alta) o immunosoppressori (farmaci che
possono abbassare le normali difese immunitarie del corpo). Queste tipologie di farmaci possono
aumentare i livelli di potassio.
3. Come viene somministrato Numeta G16E
Al suo bambino deve sempre essere somministrato Numeta G16E esattamente come
indicato dal medico. Controlli con il suo medico se non è sicuro.
Gruppi di età
Numeta G16E è stato ideato per rispondere alle esigenze nutrizionali dei neonati a termine
e dei bambini fino a 2 anni.
Il suo dottore deciderà se questo medicinale è adatto al suo bambino.
Somministrazione
Questo medicinale è una emulsione per infusione. Viene somministrato tramite un tubo di
plastica in una vena del braccio o in una grande vena del torace del suo bambino.
Il suo pediatra potrebbe decidere di non somministrare lipidi al suo bambino. La sacca di
Numeta G16E è ideata in modo da permettere la rottura della sola membrana di separazione
tra il compartimento di amminoacidi/elettroliti e quello di glucosio se necessario. La
membrana di separazione tra il compartimento di amminoacidi e quello di lipidi rimane
intatta in questo caso. Il contenuto della sacca può così essere infuso senza lipidi.
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione (vedere il paragrafo 2).
Dosaggio e durata del trattamento
Il suo pediatra deciderà il dosaggio e la durata del trattamento. Il dosaggio dipende dalle
esigenze nutrizionalidel suo bambino. Il dosaggio si baserà sul peso del suo bambino, sullo
stato clinico e sulla capacità del corpo del suo bambino di metabolizzare e di utilizzare i
costituenti di Numeta G16E. Potranno essere anche dati nutrienti o proteine aggiuntive per
via orale/enterale.
Se al suo bambino viene dato troppo Numeta G16E
Sintomi
Il sovradosaggio di questo medicinale o una somministrazione troppo veloce può risultare
in:
- nausea (sentirsi male)
- vomito
- brividi
- squilibri elettrolitici (quantità anomale di elettroliti nel sangue)
- segni di ipervolemia (aumento del volume ematico in circolo)
- acidosi (aumento dell'acidità del sangue)
In tali situazioni interrompere immediatamente l'infusione. Il medico del suo bambino
deciderà se sono necessarie ulteriori misure.
Un sovradosaggio dei grassi contenuti in Numeta G16E può provocare una "sindrome da
sovraccarico di grassi", che solitamente è reversibile dopo l'interruzione dell'infusione. Nei
neonati e nei bambini piccoli (lattanti), la sindrome da sovraccarico di grassi è stata
associata a disturbi respiratori che portano a una riduzione dell'ossigeno nel corpo
(difficoltà respiratoria) e a condizioni che portano ad un aumento dell'acidità del sangue
(acidosi).
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la condizione del
suo bambino e controllerà i suoi livelli del sangue durante il trattamento.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati, sebbene non
tutti i bambini li manifestino.
Se nota cambiamenti nello stato di salute del suo bambino, durante o dopo il trattamento,
lo comunichi prontamente al suo medico o all'infermiere.
Gli esami che effettuerà il medico mentre il suo bambino assume il medicinale riducono i
rischi di effetti indesiderati.
In caso di comparsa di segni di reazione allergica, l’infusione deve essere interrotta e
bisogna contattare immediatamente il medico. Ciò può essere grave ed i segni possono
includere:
- sudorazione
- brividi
- cefalea
- rash cutanei
- difficoltà respiratorie Altri effetti indesiderati che sono stati osservati sono:
Comuni(possono interessare fino a 1 su 10 persone):
- Un livello basso di fosfati nel sangue (ipofosfatemia)
- Un livello elevato di zuccheri nel sangue (iperglicemia)
- Un livello elevato di calcio nel sangue (ipercalcemia)
- Un livello elevato di trigliceridi nel sangue (ipertrigliceridemia)
- Un'alterazione elettrolitica (iponatriemia)
Non comuni (possono interessare fino a 1 su 100 persone):
- Un livello elevato di lipidi nel sangue (iperlipidemia).
- Una condizione in cui la bile non riesce a scorrere dal fegato al duodeno (colestasi). Il duodeno fa parte dell'intestino.
Non nota: la frequenza non può essere stimata sulla base dei dati disponibili(Queste
reazioni avverse sono state segnalate solo per Numeta G13E e G16E quando
somministrate per via periferica con diluizione insufficiente). :
- Necrosi cutanea
- Lesione dei tessuti molli
- Stravaso
I seguenti effetti indesiderati sono stati riportati con altri prodotti per la nutrizione
parenterale:
La ridotta o limitata capacità di rimuovere i lipidi contenuti in Numeta può risultare in
una “sindrome da sovraccarico di grassi”. I seguenti segni e sintomi di questa sindrome
sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
o aggravamento improvviso e inatteso della condizione medica del paziente
o livelli elevati di grassi nel sangue (iperlipidemia)
o febbre
o infiltrazione di grasso nel fegato (epatomegalia)
o deterioramento della funzionalità del fegato
o riduzione dei globuli rossi che può rendere pallida la pelle e causare senso di
debolezza o affanno (anemia)
o bassa conta dei globuli bianchi, che può aumentare il rischio di infezione
(leucopenia)
o bassa conta delle piastrine, che può aumentare il rischio di ecchimosi e/o
sanguinamento (trombocitopenia)
o alterazioni della coagulazione che compromettono la capacità del sangue di
coagularsi
o Disturbi respiratori che comportano una riduzione dell'ossigeno nel corpo
(difficoltà respiratoria)
o Condizioni che portano ad un aumento dell'acidità del sangue (acidosi)
o coma, che richiede il ricovero
Formazione di piccole particelle che possono portare al blocco dei vasi sanguigni nei
polmoni (precipitati vascolari polmonari), o difficoltà respiratorie.
Segnalazione degli effetti indesiderati
Se il suo bambino presenta uno qualsiasi degli effetti indesiderati, informi il suo medico o
l’infermiere. Questo include qualsiasi possibile effetto indesiderato non elencato in questo
foglio.
Lei può inoltre segnalare gli effetti avversi direttamente (vedere i dettagli di seguito).
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla
sicurezza di questo medicinale. Gli effetti indesiderati possono, inoltre, essere segnalati
direttamente tramite il sistema nazionale di segnalazione all’indirizzo
https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
5. Come conservare Numeta G16E
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini quando non viene
somministrato.
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione (vedere il paragrafo 2).
Non usi questo medicinale dopo la data di scadenza che è riportata sulla sacca e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del
mese.
Non congelare.
Conservare nell'involucro esterno.
I medicinali non devono essere gettati nell’acqua di scarico o nei rifiuti domestici. Chieda
al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere
l’ambiente.
6. Contenuto della confezione ed altre informazioni
Descrizione dell'aspetto di Numeta G16E e contenuto della confezione
Numeta si presenta sotto forma di sacca a tre compartimenti. Ogni sacca contiene una
combinazione sterile di una soluzione di glucosio, una soluzione pediatrica di
amminoacidi, con elettroliti, e un'emulsione lipidica, come descritto di seguito.
| Dimensioni contenitore | a Soluzione di glucosio al 50% i | Soluzione di amminoacidi al 5,9% con elettroliti | Emulsione di lipidi al 12,5% |
| 500 mL | z 155 mL | 221 mL | 124 mL |
Aspetto prima della ricostituzione:
- Le soluzioni nei compartimenti di amminoacidi e glucosio sono limpide, incolori o leggermente gialle
- Il compartimento dell'emulsione di lipidi contiene un liquido uniforme di color bianco latte
Aspetto dopo la ricostituzione:
- La soluzione per infusione “2 in 1” è limpida, incolore o leggermente gialla
- L’emulsione per infusione “3 in 1” è uniforme di color bianco latte
La sacca a tre compartimenti è una sacca in plastica multistrato.
Per impedire il contatto con l'aria, la sacca di Numeta è confezionata in un involucro
esterno con barriera per l'ossigeno, che contiene anche un assorbitore di ossigeno e un
indicatore di ossigeno.
Confezioni:
sacca da 500 ml: 6 unità per scatola in cartone
1 sacca da 500 ml
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Via Del Serafico 89
00142 Roma
Produttore:
Baxter S.A.
Boulevard Rene Branquart, 80
7860 Lessines
Belgio
Questo medicinale è autorizzato negli Stati Membri dello Spazio Economico
Europeo con le seguenti denominazioni:
| Austria a Germany | I Numeta G 16 % E Emulsion zur Infusion |
| i z Belgium Luxembourg | NUMETZAH G16%E émulsion pour perfusion |
| n France | NUMETAH G16%E émulsion pour perfusion |
| e Denmark g Norway A Sweden | Numeta G16E |
| Czech Republic Greece | o c Numeta G 16 % E |
| Netherlands | a Numeta G16%E emulsie voor infusie |
| Ireland United Kingdom | m Numeta G16%E, Emulsion for Infusion r |
| Italy | a Numeta G16%E emulsione per infusione |
| Finland | F Numeta G16E infuusioneste, emulsio |
| Poland | l Numeta G 16 % E |
| Portugal | e Numeta G16%E |
| Spain | d Numeta G16%E, emulsión para perfusión |
Le informazioni seguenti sono destinate esclusivamente ai professionisti medici o
operatori sanitari*
*Si tenga presente che in alcuni casi questo prodotto può essere somministrato a casa dai
genitori o da altre persone che ne hanno cura. In questi casi i genitori/o chi ne ha cura
devono leggere queste informazioni.
Non effettuare aggiunte alla sacca prima di verificarne la compatibilità. Si potrebbero
formare particelle o si potrebbe rompere l’emulsione lipidica. Ciò porterebbe al blocco dei
vasi sanguigni.
Numeta G16E deve essere a temperatura ambiente prima dell'uso.
Prima di usare Numeta G16E, prepare la sacca come mostrato di seguito.
Verificare che la sacca non sia danneggiata. Usare la sacca solo se non è danneggiata.
L'aspetto di una sacca integra è così:
- Le membrane di separazione non permanenti sono intatte. Questo indica l'assenza di miscelazione del contenuto dei tre compartimenti
- Le soluzioni di amminoacidi e di glucosio sono limpide, incolori o leggermente gialle, senza particelle visibili
- L'emulsione di lipidi è un liquido uniforme di color bianco latte
Prima di aprire l'involucro esterno, controllare il colore dell'indicatore di ossigeno..
- Confrontarlo con il colore di riferimento stampato accanto al simbolo OK nell'area stampata dell'etichetta dell'indicatore.
- Non usare la sacca se il colore dell'indicatore di ossigeno non corrisponde al colore di riferimento stampato accanto al simbolo OK.
Le Figure 1 e 2 illustrano come rimuovere l'involucro esterno di protezione. Gettare
l'involucro esterno, l’indicatore di ossigeno e l'assorbitore di ossigeno.









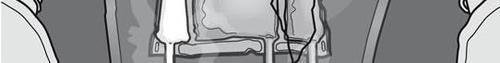

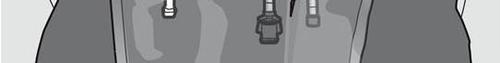




Figura 1 Figura 2
Preparazione dell’emulsione miscelata:
- assicurarsi che il medicinale sia a temperatura ambiente quando si rompono le membrane di separazione non permanenti.
- Porre la sacca su una superficie piana e pulita.
Attivazione della sacca a 3 compartimenti (miscelazione delle 3 soluzioni mediante
rottura delle 2 membrane non permanenti)
Step 1: Iniziare arrotolando la sacca dal lato dell'occhiello a D.
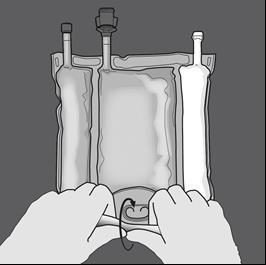
Step 2: Fare pressione finché le membrane di separazione non siano aperte.
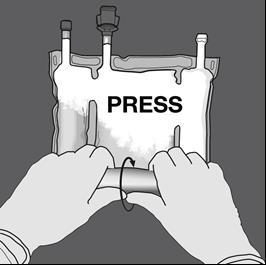
Step 3: Cambiare direzione arrotolando la sacca la sacca verso l'occhiello a D.
Continuare finché la membrana non è completamente aperta.
Procedere nello stesso modo per completare l’apertura della seconda membrana.
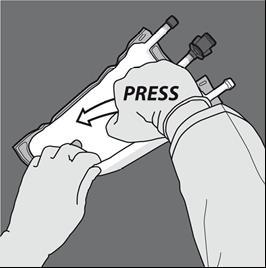
Step 4: Capovolgere la sacca almeno tre volte per mescolare completamente il contenuto.
L'aspetto della soluzione mescolata dovrebbe essere simile a un’emulsione di color bianco
latte.







Step 5: Rimuovere il cappuccio protettivo dal punto di somministrazione e inserire il set di
infusione.








Attivazione di 2 compartimenti (miscelazione delle 2 soluzioni attraverso la rottura della
membrana non permanente tra il compartimento degli amminoacidi e il compartimento con
glucosio)
Step 1: Per miscelare soltanto 2 soluzioni, arrotolare la sacca dall'angolo superiore
(estremità con l’occhiello) della membrana che separa le soluzioni.
Fare pressione per aprire la membrana che separa i compartimenti delle soluzioni di
glucosio e amminoacidi.







Step 2: Posizionare la sacca in modo che il compartimento contenente l'emulsione lipidica
sia il più vicinoall'operatore.
Arrotolare la sacca proteggendo il compartimento dell'emulsione lipidica con i palmi delle
mani.
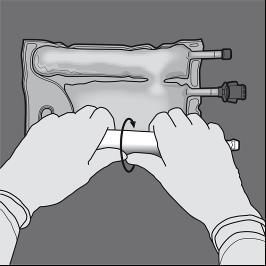
Step 3: Con una mano, fare pressione e arrotolare la sacca verso i punti di iniezione.
















Step 4: Cambiare direzione arrotolando la sacca verso il lato superiore (estremità con
l’occhiello).
Premendo con l'altra mano, continuando fino a che la membrana che separa le soluzioni di
amminoacidi e glucosio è completamente aperta.








Step 5: Capovolgere la sacca almeno tre volte per mescolare completamente il contenuto.
L'aspetto della soluzione mescolata dovrebbe essere chiaro, incolore o leggermente giallo.








Step 6: Rimuovere il cappuccio protettivo dal punto di somministrazione e inserire il set di
infusione.








La velocità del flusso deve essere aumentata gradualmente durante la prima ora. La velocità
di somministrazione del flusso deve essere regolata in base ai fattori seguenti:
- dose da somministrare
- i volumi da assumere quotidianamente
- la durata dell'infusione.
Modo di somministrazione
Quando impiegata in neonati e bambini di età inferiore a 2 anni, la soluzione (nelle sacche
e nei set per la somministrazione) deve essere protetta dall’esposizione alla luce fino al
completamento della somministrazione.
E’ raccomandato l’utilizzo di un filtro da 1,2 micron per la somministrazione di Numeta
G16E.
Per la sua alta osmolarità, Numeta G16E non diluito può essere somministrato solo
attraverso una vena centrale. Tuttavia, una sufficiente diluizione di Numeta G16E con
acqua per preparazioni iniettabili riduce l'osmolarità e permette l'infusione periferica.
La formula che segue indica l’effetto della diluizione sull'osmolarità delle sacche.

La tabella che segue mostra esempi di osmolarità per miscelazioni di 2CB attivati e 3CB
attivati dopo l'aggiunta di acqua per preparazioni iniettabili:
| Amminoacidi e Glucosio (2CB attivati) | m Amminoacidi, Glucosio e Lipidi (3CB attivati) | |
| Volume iniziale nella sacca (mL) | 376 | 500 |
| Osmolarità iniziale (appross. mOsm/L) | 1585 | r a 1230 |
| Volume di acqua aggiunta (mL) | 376 | 500 |
| Volume finale dopo l'aggiunta (mL) | 752 | F 1000 |
| Osmolarità dopo l'aggiunta (mOsm/L appross.) | e 792,5 | l 615 |
Aggiunte di additivi:
L’esposizione alla luce di soluzioni per nutrizione parenterale endovenosa, specialmente
dopo l’aggiunta di oligoelementi e/o vitamine, può avere effetti avversi sull’esito clinico
nei neonati, a causa della generazione di perossidi e altri prodotti di degradazione. Quando
impiegata in neonati e bambini di età inferiore a 2 anni, Numeta G16E deve essere protetta
dalla luce ambientale fino al completamento della somministrazione.
Additivi compatibili possono essere aggiunti attraverso il sito di iniezione nella miscela
ricostituita (dopo l'apertura delle membrane non permanenti e dopo la miscelazione del
contenuto dei due o tre compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che
la miscela sia ricostituita (prima dell'apertura delle membrane di separazione non
permanenti e prima della miscelazione delle soluzioni e dell'emulsione).
Eventuali aggiunte di soluzioni di oligoelementi (identificati come TE1, TE2 e TE4),
vitamine (identificate come liofilizzato V1 e emulsione V2), e elttroliti disponibili in
commercio in quantità definite sono mostrate nelle tabelle 1-6.
- 1.Compatibilità con TE4, V1 e V2
Tabella 1: Compatibilità della sacca 3-in-1 (3CB attivati) con e senza diluizione con acqua
| a Per 500 mL (3 in 1 miscela con lipidi) | ||||||
| Miscela non diluita | Miscela diluita | |||||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | Livello r incluso | m Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 12,0 | 25,6 | 37,6 | a 12,0 | 25,6 | 37,6 |
| Potassio (mmol) | 11,4 | 26,2 | 37,6 | F 11,4 | 26,2 | 37,6 |
| Magnesio (mmol) | 1,6 | 3,6 | 5,2 | 1,6 | 3,6 | 5,2 |
| Calcio (mmol) | 3,1 | 16,4 | l 19,5 | 3,1 | 8,2 | 11,3 |
| Fosfato* (mmol) | 4,4 | 6,9 | e 11,3 | 4,4 | 6,9 | 11,3 |
| Oligoelementi e vitamine | 10 mL TE4 + 1 fiala V1 + 30 mL V2 | d 10 mL TE4 + 1 fiala V1 + 30 mL V2 | 5 mL TE4 + ½ fiala V1 + 5 mL V2 | 5 mL TE4 + ½ fialaV1 + 5 mL V2 | ||
| Acqua per soluzioni iniettabili | a | 350 mL | 350 mL | |||
Tabella 2: Compatibilità della sacca 2-in-1 (2CB attivati) con e senza diluizione
| l Per 376 mL (2 in 1 miscela senza lipidi) | ||||||
| a Miscela non diluita | Miscela diluita | |||||
| Aggiunte | Livello I incluso | t Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | a 11,6 | 26,0 | 37,6 | 11,6 | 0,0 | 11,6 |
| Potassio (mmol) | i 11,4 | 26,2 | 37,6 | 11,4 | 0,0 | 11,4 |
| Magnesio (mmol) | z 1,6 | 3,6 | 5,2 | 1,6 | 0,0 | 1,6 |
| Calcio (mmol) | 3,1 | 8,2 | 11,3 | 3,1 | 0,0 | 3,1 |
| n Fosfato* (mmol) | 3,2 | 8,1 | 11,3 | 3,2 | 0,0 | 3,2 |
| e Oligoelementi e g vitamine | 5 mL TE4 + ½ fiala V1 | 5 mL TE4 + ½ fiala V1 | 5 mL TE4 + ½ fiala V1 | 5 mL TE4 + ½ fiala V1 | ||
| Acqua per soluzioni iniettabili | 450 mL | 450 mL | ||||
- 2.Compatibilità con TE1, V1 e V2
Tabella 3: Compatibilità della sacca 3-in-1 (3CB attivati) con e senza diluizione con acqua
| Per 500 mL (3 in 1 miscela con lipidi) | ||||||
| Miscela non diluita | m Miscela diluita | |||||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | r Livello a incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 12,0 | 4,0 | 16,0 | F 12,0 | 0,0 | 12,0 |
| Potassio (mmol) | 11,4 | 6,2 | 17,6 | 11,4 | 0,0 | 11,4 |
| Magnesio (mmol) | 1,6 | 0 | l 1,6 | 1,6 | 0,0 | 1,6 |
| Calcio (mmol) | 3,1 | 2,1 | e 5,2 | 3,1 | 0,0 | 3,1 |
| Fosfato* (mmol) | 4,4 | 2,0 | d 6,4 | 4,4 | 0,0 | 4,4 |
| Oligoelementi e vitamine | 5 mL TE1 + ½ fiala V1 + 5 mL V2 | 5 mL TE1 + a ½ fiala V1 + 5 mL V2 | 5 mL TE1 + ½ fiala V1 + 5 mL V2 | 5 mL TE1 + ½ fialaV1 + 5 mL V2 | ||
| Acqua per soluzioni iniettabili | n | 350 mL | 350 mL | |||
Tabella 4: Compatibilità della sacca 2-in-1 (2CB attivati) con e senza diluizione con acqua
| t Per 376 mL (2 in 1 miscela senza lipidi) | ||||||
| I Miscela non diluita | Miscela diluita | |||||
| Aggiunte | Livello a incluso | Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | i 11,6 | 26,0 | 37,6 | 11,6 | 0,0 | 11,6 |
| Potassio (mmol) | z 11,4 | 26,2 | 37,6 | 11,4 | 0,0 | 11,4 |
| n Magnesio (mmol) | 1,6 | 3,6 | 5,2 | 1,6 | 0,0 | 1,6 |
| e Calcio (mmol) | 3,1 | 8,2 | 11,3 | 3,1 | 0,0 | 3,1 |
| g Fosfato* (mmol) | 3,2 | 8,1 | 11,3 | 3,2 | 0,0 | 3,2 |
| A Oligoelementi e vitamine | 5 mL TE1 + ½ fiala V1 | 5 mL TE1 + ½ fiala V1 | 5 mL TE1 + ½ fiala V1 | 5 mL TE1 + ½ fiala V1 | ||
| Acqua per soluzioni iniettabili | o 450 mL c | 450 mL |
3Compatibilità con TE2, V1 e V2
Tabella 5: Compatibilità della sacca 3-in-1 (3CB attivati) con e senza diluizione con acqua
| Per 500 mL (3 in 1 miscela con lipidi) | ||||||
| Miscela non diluita | r Miscela diluita | |||||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | a Livello F incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 12,0 | 4,0 | 16,0 | 12,0 | 0,0 | 12,0 |
| Potassio (mmol) | 11,4 | 6,2 | l 17,6 | 11,4 | 0,0 | 11,4 |
| Magnesio (mmol) | 1,6 | 0 | e 1,6 | 1,6 | 0,0 | 1,6 |
| Calcio (mmol) | 3,1 | 2,1 | d 5,2 | 3,1 | 0,0 | 3,1 |
| Fosfato* (mmol) | 4,4 | 2,0 | 6,4 | 4,4 | 0,0 | 4,4 |
| Oligoelementi e vitamine | 5 mL TE2 + n ½ fiala V1 + 5 mL V2 | a 5 mL TE2 + ½ fiala V1 + 5 mL V2 | 5 mL TE2 + ½ fiala V1 + 5 mL V2 | 5 mL TE2 + ½ fialaV1 + 5 mL V2 | ||
| Acqua per soluzioni iniettabili | a
| 350 mL | 350 mL | |||
Tabella 6: Compatibilità della sacca 2-in-1 (2CB attivati) con e senza diluizione con acqua
| I Per 376 mL (2 in 1 miscela senza lipidi) | ||||||
| a Miscela non diluita | Miscela diluita | |||||
| Aggiunte | i Livello z incluso | Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| n Sodio (mmol) | 11,6 | 26,0 | 37,6 | 11,6 | 0,0 | 11,6 |
| e Potassio (mmol) | 11,4 | 26,2 | 37,6 | 11,4 | 0,0 | 11,4 |
| Magnesio (mmol) | 1,6 | 3,6 | 5,2 | 1,6 | 0,0 | 1,6 |
| g Calcio (mmol) | 3,1 | 8,2 | 11,3 | 3,1 | 0,0 | 3,1 |
| A Fosfato* (mmol) | 3,2 | 8,1 | 11,3 | 3,2 | 0,0 | 3,2 |
| Oligoelementi e vitamine | 5 mL TE2 + ½ fiala V1 | 5 mL TE2 + ½ fiala V1 | o 5 mL TE2 + c ½ fiala V1 | 5 mL TE2 + ½ fiala V1 | ||
| Acqua per soluzioni iniettabili | a 450 mL | 450 mL |
La composizione delle preparazioni di vitamine e oligoelementi sono illustrate nelle tabelle 7 e 8.
Tabella 7:Composizione del preparato commerciale di oligoelementi utilizzato:
| Composizione per 10mL | TE1 | TE2 | a F TE4 |
| Ferro | 8,9 µmol o 0,5 mg |
| |
| Zinco | 38,2 µmol o 2,5 mg | 15,3 µmol o 1 mg | e 15,3 µmol o d 1mg |
| Selenio | 0,253 µmol o 0,02 mg | 0,6 µmol o a 0,05 mg | 0,253 µmol o 0,02 mg |
| Rame | 3,15 µmol o 0, 2mg | n 4,7 µmol o 0,3 mg | 3,15 µmol o 0,2 mg |
| Iodio | 0,0788 µmol o 0,01 mg | a 0,4 µmol o i l 0,05 mg | 0,079 µmol o 0,01 mg |
| Fluoro | a 30 µmol o t 0,57 mg | 26,3 µmol o 0,5 mg | |
| Molibdeno | I | 0,5 µmol o 0,05 mg | |
| Manganese | a 0,182 µmol o i 0,01 mg | 1,8 µmol o 0,1 mg | 0,091 µmol o 0,005 mg |
| Cobalto n | z | 2,5 µmol o 0,15 mg | |
| e Cromo | 0,4 µmol o 0,02 mg |
Tabella 8: Composizione del preparato commerciale di vitamine utilizzato:
| Composizione per fiala | V1 | V2 |
| Vitamina B1 | 2,5 mg | |
| Vitamina B2 | 3,6 mg | |
| Nicotinamide | 40 mg | |
| Vitamina B6 | 4,0 mg | |
| Acido Pantotenico | 15,0 mg | |
| Biotina | 60 µg | |
| Acido Folico | 400 µg | l |
| Vitamina B12 | 5,0 µg | e |
| Vitamina C | 100 mg | d |
| Vitamina A | 2300 IU | |
| Vitamina D | a 400 IU | |
| Vitamina E | n 7 IU | |
| Vitamina K | a | 200 µg |
Per eseguire un'aggiunta:
- Operare in condizioni asettiche
- Preparare il punto d'iniezione della sacca
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione
- Miscelare il contenuto della sacca e le aggiunte
Preparazione dell'infusione:
- Operare in condizioni asettiche
- Sospendere la sacca
- Rimuovere la protezione in plastica dal punto di somministrazione
- Inserire saldamente lo spike del set di infusione nel punto di somministrazione
Somministrazione dell'infusione:
- Solo per uso singolo
- Somministrare il prodotto solo dopo l'apertura delle membrane di separazione non permanenti tra i due o tre compartimenti e la miscelazione del contenuto dei due o tre compartimenti
- Assicurarsi che l'emulsione finale per infusione dei 3 compartimenti attivati non mostri alcuna prova di separazione delle fasi o che la soluzione per infusione finale dei 2 compartimenti attivati non mostri alcuna presenza di particelle
- Dopo la rottura delle membrane non permanenti, il contenuto si deve usare immediatamente. Numeta G16E non deve essere conservato per un'infusione successiva. Non collegare eventuali sacche parzialmente utilizzate
- Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa a causa di possibili residui gassosi contenuti nella sacca principale
- E’ raccomandato l’utilizzo di un filtro da 1,2 micron per la somministrazione di Numeta G16E
- Quando impiegata in neonati e bambini di età inferiore ai 2 anni, proteggere dall’esposizione alla luce fino al completamento della somministrazione. L’esposizione di Numeta G16E alla luce ambientale, specialmente dopo aggiunta di oligoelementi e/o vitamine, genera perossidi e altri prodotti di degradazione che possono essere ridotti attraverso la protezione dall’esposizione alla luce.
- Qualsiasi eventuale prodotto non utilizzato, rifiuti derivati e tutti i dispositivi usa e getta necessari devono essere smaltiti correttamente e non riutilizzati Periodo di validità dopo la miscelazione delle soluzioni Utilizzare il prodotto immediatamente dopo l'apertura delle membrane non permanenti tra i due o tre compartimenti. Gli studi di stabilità delle miscele sono stati condotti per 7 giorni a una temperatura compresa tra 2°C e 8°C, seguiti da 48 ore a 30°C.
Periodo di validità dopo l’integrazione (elettroliti, oligoelementi, vitamine, acqua):
Per specifiche miscele, i dati di stabilità in uso della formulazione di Numeta sono stati dimostrati
per 7 giorni a una temperatura compresa tra 2°C e 8°C, seguiti da 48 ore a 30°C.
Da un punto di vista microbiologico, il prodotto deve essere utilizzato immediatamente. Se non
utilizzato immediatamente, i tempi e le condizioni di conservazione all’utilizzo sono responsabilità
dell'utente e non devono essere superiori alle 24 ore, a temperature comprese tra 2°C e 8°C, a meno
che la ricostituzione/diluizione/supplementazione non sia avvenuta in condizioni asettiche
controllate e convalidate.
Non usare Numeta G16E se la sacca è danneggiata. Questo è l'aspetto di una sacca danneggiata:
- le membrane di separazione non permanenti sono rotte
- uno dei compartimenti contiene una miscela delle soluzioni
- le soluzioni di amminoacidi e di glucosio non sono limpide, incolori o leggermente gialle e/o contengono particelle visibili
- l'emulsione di lipidi non è un liquido uniforme di color bianco latte.
I medicinali non devono essere gettati nell’acqua di scarico e nei rifiuti domestici. Chieda al
farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
Cosa contiene Numeta G16E
I principi attivi sono:
| a Composizione | ||
| Principio attivo | 2CB attivati (376 mL) | m 3CB attivati (500 mL) |
| Compartimento Amminoacidi | ||
| Alanina | 1,03 g | r 1,03 g |
| Arginina | 1,08 g | a 1,08 g |
| Acido aspartico | F 0,77 g | 0,77 g |
| Cisteina | 0,24 g | 0,24 g |
| Acido glutammico | l 1,29 g | 1,29 g |
| Glicina | e 0,51 g | 0,51 g |
| Istidina | 0,49 g | 0,49 g |
| Isoleucina | d 0,86 g | 0,86 g |
| Leucina | 1,29 g | 1,29 g |
| n Lisina monoidrata (come lisina) | a 1,59 g (1,42 g) | 1,59 g (1,42 g) |
| Metionina | 0,31 g | 0,31 g |
| a i Ornitina cloridrata (come ornitina) | 0,41 g (0,32 g) | 0,41 g (0,32 g) |
| l Fenilalanina | 0,54 g | 0,54 g |
| a Prolina | 0,39 g | 0,39 g |
| t Serina | 0,51 g | 0,51 g |
| I Taurina | 0,08 g | 0,08 g |
| a Treonina | 0,48 g | 0,48 g |
| Triptofano | 0,26 g | 0,26 g |
| i Tirosina | 0,10 g | 0,10 g |
| z Valina | 0,98 g | 0,98 g |
| n Sodio cloruro | 0,30 g | 0,30 g |
| e Potassio acetato | 1,12 g | 1,12 g |
| Calcio cloruro biidrato | 0,46 g | 0,46 g |
| g Magnesio acetato tetraidrato | 0,33 g | 0,33 g |
| A Sodio glicerofosfato idrato | 0,98 g | 0,98 g |
| Compartimento glucosio | ||
| o Composizione | ||
| Principio attivo | 2CB attivati (376 mL) | c 3CB attivati (500 mL) |
| Glucosio monoidrato (come glucosio anidro) | 85,25 g (77,50 g) | a 85,25 g (77,50 g) |
| m Compartimento Lipidi | ||
| Olio di oliva purificato (circa 80%) + olio di soia purificato (circa 20%) | r 15,5 g | |
La soluzione/emulsione ricostituita fornisce quanto segue:
| Composizione | ||||
| l 2CB attivati | 3CB attivati | |||
| Per unità di volume (mL) Azoto (g) Amminoacidi (g) Glucosio (g) Lipidi (g) Energia Calorie totali (kcal) i Calorie non proteiche (kcal) l Calorie da glucosio (kcal) a Calorie lipidiche (kcal)a t Calorie non proteiche/azoto (kcal/g N) I Calorie lipidiche (calorie non proteiche %) Calorie lipidiche (calorie totali %) a Electrolytes i Sodio (mmol) z Potassio (mmol) n Magnesio (mmol) Calcio (mmol) e Fosfatob (mmol) g Acetato (mmol) Malato (mmol) Cloruro (mmol) | 376 2,0 13,0 a 77,5 n 0 a 362 310 310 0 158 NA NA 11,6 11,4 1,6 3,1 3,2 14,5 4,3 13,8 | e d 100 0,52 3,5 20,6 0 96 82 82 0 158 N/A N/A 3,1 3,0 0,41 0,82 0,85 3,9 1,1 3,7 | 500 2,0 13,0 77,5 15,5 517 465 310 155 237 33 30 12,0 11,4 1,6 3,1 4,4 14,5 4,3 13,8 | 100 0,39 2,6 15,5 3,1 103 93 62 31 237 33 30 2,4 2,3 0,31 0,62 0,87 2,9 0,86 2,8 |
| A pH (appross.) | 5,5 | 5,5 | 5,5 | 5,5 |
Gli altri componenti sono:
Acido L-malico
Acido cloridrico
Fosfolipidi di uovo per
preparazioni iniettabili
Glicerolo
Sodio oleato
Sodio idrossido
Acqua per preparazioni iniettabili
per la regolazione del pH
| o Composizione | ||||
| 2CB attivati | c 3CB attivati | |||
| Per unità di volume (mL) Osmolarità appross. (mOsm/L) | 376 1585 | 100 1585 | 500 1230 | a 100 1230 |
NUMETA G19E, emulsione per infusione
Legga attentamente questo foglio prima di utilizzare questo medicinale perché
contiene importanti informazioni per Lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al suo pediatra, al farmacista, o all’infermiere.
- Se il suo bambino ha uno qualsiasi degli effetti indesiderati, informi il suo pediatra o l’infermiere. Questo potrebbe includere qualsiasi effetto indesiderato non elencato in questo foglietto. Vedere il paragrafo 4.
Contenuto di questo foglio:
- 1. Che cos'è Numeta G19E e a che cosa serve
- 2. Cosa sapere prima che al suo bambino sia dato Numeta G19E
- 3. Come viene dato Numeta G19E
- 4. Possibili effetti indesiderati
- 5. Come conservare Numeta G19E
- 6. Contenuto della confezione ed altre informazioni
1. Che cos'è Numeta G19E e a che cosa serve
Numeta G19E è un’emulsione per nutrizione appositamente studiata per bambini con età
superiore ai 2 anni e adolescenti fino a 18 anni di età. È somministrata attraverso un tubo
inserito nella vena del suo bambino, quando non riesce ad assumeretutto il nutrimento
necessario per bocca.
Numeta si presenta in sacca a 3 compartimenti nella quale ciascun compartimento separato
contiene:
una soluzione di glucosio al 50%
una soluzione pediatrica di amminoacidi al 5,9%, con elettroliti
un'emulsione di lipidi (grassi) al 12,5%
A seconda delle esigenze del suo bambino, 2 o 3 di queste soluzioni sono miscelate insieme
nella sacca prima che venga somministrato al suo bambino.
Numeta G19E deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che al suo bambino sia somministrato Numeta G19E
Al suo bambino non deve essere dato Numeta G19E nei seguenti casi:
Con 2 soluzioni miscelate nella sacca (2 in 1):
- Se il suo bambino è allergico alle proteine dell'uovo, alla soia, alle arachidi o ad uno qualsiasi degli eccipienti dei compartimenti di glucosio o amminoacidi (elencati nel paragrafo 6).
- Se il corpo del suo bambino ha problemi a formare "mattoncini" di proteine.
- Se il suo bambino ha nel sangue elevate concentrazioni di uno qualsiasi degli elettroliti inclusi in Numeta G19E.
- Se il suo bambino soffre di iperglicemia (livelli di zuccheri nel sangue particolarmente alti).
Con 3 soluzioni miscelate nella sacca (3 in 1):
- Tutte le situazioni menzionate in “2 in 1” più la seguente:
- Se il suo bambino ha livelli di grassi nel sangue particolarmente elevati.
In tutti i casi, il suo medico deciderà se il suo bambino dovrà ricevere questo medicinale
sulla base di fattori quali età, peso e condizione clinica. Il suo medico terrà conto anche
dei risultati degli esami eseguiti.
Avvertenze e precauzioni
Parli con il suo pediatra o con l’infermiere prima che diano Numeta G19E.
Reazioni Allergiche:
L'infusione deve essere interrotta immediatamente in caso di sviluppo di segni o sintomi di
reazione allergica (ad esempio febbre, sudorazione, brividi, cefalea, rashcutanei o difficoltà
respiratoria). Questo medicinale contiene olio di semi di soia che, raramente, può causare
gravi reazioni di ipersensibilità. È stato osservato raramente che alcuni soggetti allergici
alle proteine delle arachidi sono allergici anche alle proteine dei semi di soia.
Numeta G19E contiene glucosio prodotto dall'amido di mais. Pertanto, Numeta G19E deve
essere utilizzato con cautela nei pazienti con allergia nota al mais o ai prodotti derivati dal
mais
Rischio di formazione di particelle con ceftriaxone (antibiotico):
Un antibiotico che si chiama ceftriaxone non deve essere miscelato o somministrato
contemporaneamente a qualsiasi soluzione contenente calcio (compreso Numeta G19E)
somministrate con una flebo in vena.
Il medico lo sa e non li somministrerà insieme, neanche attraverso diverse linee di infusione
o diversi siti di infusione.
Tuttavia, il medico può somministrare il calcio e il ceftriaxone in sequenza uno dopo l’altro
se sono utilizzate linee di infusione in siti di infusione diversi o se le linee di infusione sono
sostituite o sono state accuratamente lavate con una soluzione salina fisiologica tra le
infusioni per evitare la precipitazione.
Formazione di piccole particelle nei vasi sanguigni dei polmoni:
Anche le difficoltà respiratorie potrebbero essere un segnale di formazione di piccole
particelle che bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Se il
suo bambino presenta una qualsiasi difficoltà respiratoria, informi il pediatra o l’infermiere.
Essi decideranno quali azioni intraprendere.
Infezioni e Sepsi:
Il suo medico controllerà accuratamente il suo bambino per qualsiasi segnale di infezione.
Il rischio di infezione può essere ridotto usando una “tecnica asettica” (tecnica priva di germi)
durante il posizionamento e la manuntenzione del catetere come anche nella preparazione
della formula nutrizionale.
A volte, i bambini possono sviluppare un'infezione e sepsi (presenza di batteri nel sangue)
quando viene inserito un tubo in vena (catetere endovenoso). Alcuni medicinali e alcune
malattie possono aumentare il rischio di sviluppare un'infezione o la sepsi. I pazienti che
necessitano di nutrizione parenterale (somministrazione di nutrimento attraverso un tubo
inserito in vena) possono essere maggiormente soggetti allo sviluppo di un'infezione a
causa delle loro condizioni mediche.
Sindrome da sovraccarico di grassi:
La sindrome da sovraccarico di grassi è stata riportata con prodotti simili. Una ridotta o
limitata capacità di rimuovere i lipidi presenti in Numeta G19E o un sovradosaggio
possono provocare una "sindrome da sovraccarico di grassi". (Vedere il paragrafo 3 ed il
paragrafo 4).
Alterazioni nei parametri chimici del sangue:
Il suo medico controllerà e valuterà i fluidi, la composizione chimica del sangue ed altri
parametri del sangue del suo bambino, dato che, a volte, la rialimentazione di pazienti
gravemente malnutriti può determinare alcuni cambiamenti dei livelli chimici del sangue.
Inoltre, si possono verificare gonfiore e presenza di quantità eccessive di fluidi nei tessuti.
Si consiglia di iniziare la nutrizione parenterale lentamente e con la massima attenzione.
Monitoraggio e Aggiustamenti:
Il suo medico manterrà il suo bambino sotto stretto controllo e aggiusterà il dosaggio di
Numeta G19E per rispondere alle esigenze individuali del bambino se presenta le seguenti
condizioni:
- condizioni post-traumatiche gravi
- diabete mellito grave
- shock
- infarto
- infezione grave
- alcuni tipi di coma
Utilizzare con attenzione:
Numeta deve essere usato con attenzione se il suo bambino ha:
- Edema polmonare (fluido nei polmoni) o insufficienza cardiaca
- Gravi problemi epatici
- Problemi con l’utilizzo dei nutrienti
- Elevate concentrazioni di zucchero nel sangue
- Problemi renali
- Scompensi metabolici gravi (quando il corpo non riesce a suddividere le sostanze in modo normale)
- Disordini della coagulazione Lo stato dei fluidi del suo bambino, i valori di funzionalità epatica e/o i valori del sangue verranno attentamente controllati.
Altri medicinali e Numeta G19E
Informi il suo medico se il suo bambino sta prendendo o utilizzando, o ha recentemente
preso o potrebbe utilizzare qualsiasi altra medicina.
Numeta non deve essere somministrato contemporaneamente a:
- ceftriaxone(un antibiotico) neanche attraverso linee d’infusione separate a causa del rischio di formazione di particelle.
- sangueper mezzo dello stesso set d'infusione a causa del rischio di pseudoagglutinazione (formazione di grumi di globuli rossi).
- Ampicillina, fosfenitoina o furosemideattraverso la stessa linea d’infusione a causa del rischio di formazione di particelle
Cumarina e warfarina (Anticoagulanti):
Il suo medico visiterà attentamente il suo bambino se sta assumendo cumarina o
warfarina. L'olio di oliva e l'olio di semi di soia hanno un contenuto naturale di vitamina
K1. La vitamina K1 può interferire con i medicinali quali la cumarina e la warfarina.
Questi farmaci sono anticoagulanti che impediscono la coagulazione del sangue.
Analisi di laboratorio:
I lipidi contenuti in questa emulsione possono interferire con i risultati di determinati test
di laboratorio. I test di laboratorio possono essere eseguiti dopo un periodo di 5-6 ore
dall'uso dei lipidi quando non vengono somministrati lipidi aggiuntivi.
Interazioni di Numeta G19E con farmaci che possono alterare i livelli/metabolismo
del potassio:
Numeta G19E contiene potassio. Alte concentrazioni di potassio nel sangue possono
causare un ritmo cardiaco anormale. Prestare particolare attenzione in pazienti che
assumono diuretici (farmaci che riducono la ritenzione dei fluidi), ACE-inibitori (farmaci
per la pressione alta) o antagonisti del recettore dell’angiotensina II (farmaci per la
pressione alta) o immunosoppressori (farmaci che possono abbassare le normali difese
immunitarie del corpo). Queste tipologie di farmaci possono aumentare i livelli di potassio.
Gravidanza, allattamento e fertilità
Non vi sono dati adeguati riguardanti l'uso di Numeta nelle donne in gravidanza o in
allattamento. Prima di prescrivere Numeta il suo medico deve analizzare con attenzione i
potenziali rischi e benefici per ciascun specifico paziente.
3. Come viene dato Numeta G19E
Al suo bambino deve sempre essere dato Numeta G19 E esattamente come indicato dal
medico. Controlli con il suo medico se non è sicuro.
Gruppi di età
Numeta G19E è stato ideato per rispondere alle esigenze nutrizionali dei bambini con età
superiore ai 2 anni e degli adolescenti fino a 18 anni di età.
Il suo dottore deciderà se questo medicinale è adatta al suo bambino.
Somministrazione
Questo medicinale è una emulsione per infusione. Viene data tramite un tubo di plastica in
una vena del braccio o in una grande vena del torace del suo bambino.
Il suo pediatra potrebbe decidere di non somministrare lipidi al suo bambino. La sacca di
Numeta G19E è ideata in modo da permettere la rottura della sola membrana di separazione
tra il compartimento di amminoacidi/elettroliti e quello di glucosio se necessario. La
membrana di separazione tra il compartimento di amminoacidi e quello di lipidi rimane
intatta in questo caso. Il contenuto della sacca può così essere infuso senza lipidi.
Dosaggio e durata del trattamento
Il suo pediatra deciderà il dosaggio e la durata del trattamento. Il dosaggio dipende dalle
esigenze nutrizionali del suo bambino. Il dosaggio si baserà sul peso del suo bambino, sullo
stato clinico e sulla capacità del corpo del suo bambino di metabolizzare e di utilizzare i
costituenti di Numeta G19E. Potranno essere anche dati nutrienti o proteine aggiuntive per
via orale/enterale.
Se al suo bambino viene dato troppo Numeta G19E
Sintomi
Il sovradosaggio di questo medicinale o una somministrazione troppo veloce possono
causare quanto segue:
- nausea (sentirsi male)
- vomito
- brividi
- squilibri elettrolitici (quantità anomale di elettroliti nel sangue)
- segni di ipervolemia (aumento del volume ematico in circolo)
- acidosi (aumento dell'acidità del sangue)
In tali situazioni interrompere immediatamente l'infusione. Il medico del suo bambino
deciderà se sono necessarie ulteriori misure.
Un sovradosaggio dei grassi contenuti in Numeta G19E può provocare una "sindrome da
sovraccarico di grassi", che solitamente è reversibile dopo l'interruzione dell'infusione. Nei
neonati e nei bambini piccoli (lattanti), la sindrome da sovraccarico di grassi è stata
associata a disturbi respiratori che portano a una riduzione dell'ossigeno nel corpo
(difficoltà respiratoria) e a condizioni che portano ad un aumento dell'acidità del sangue
(acidosi).
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la condizione del
suo bambino e controllerà i suoi livelli del sangue durante il trattamento.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutti
i bambini li manifestino.
Se nota cambiamenti nello stato di salute del suo bambino, durante o dopo il trattamento,
lo comunichi prontamente al suo medico o all'infermiere.
Gli esami che effettuerà il medico mentre il suo bambino assume il medicinale riducono i
rischi di effetti indesiderati.
In caso di comparsa di segni di reazione allergica, l’infusione deve essere interrotta e
bisogna contattare immediatamente il medico. Ciò può essere grave ed i segni possono
includere:
- sudorazione
- brividi
- cefalea
- rash cutanei
- difficoltà respiratorie
Altri effetti indesiderati che sono stati osservati sono:
Comuni(possono interessare fino a 1 su 10 persone):
- Un livello basso di fosfati nel sangue (ipofosfatemia)
- Un livello elevato di zuccheri nel sangue (iperglicemia)
- Un livello elevato di calcio nel sangue (ipercalcemia)
- Un livello elevato di trigliceridi nel sangue (ipertrigliceridemia)
- Un'alterazione elettrolitica (iponatriemia)
Non comuni (possono interessare fino a 1 su 100 persone):
- Un livello elevato di lipidi nel sangue (iperlipidemia).
- Una condizione in cui la bile non riesce a scorrere dal fegato al duodeno (colestasi). Il duodeno fa parte dell'intestino.
Non nota: la frequenza non può essere stimata sulla base dei dati disponibili(Queste
reazioni avverse sono state segnalate solo per Numeta G13E e G16E quando
somministrate per via periferica con diluizioni insufficienti). :
- Necrosi cutanea
- Lesione dei tessuti molli
- Stravaso
I seguenti effetti indesiderati sono stati riportati con altri prodotti per la nutrizione
parenterale:
La ridotta o limitata capacità di rimuovere i lipidi contenuti in Numeta può risultare in
una “sindrome da sovraccarico di grassi”. I seguenti segni e sintomi di questa sindrome
sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
o aggravamento improvviso e inatteso della condizione medica del paziente
o livelli elevati di grassi nel sangue (iperlipidemia)
o febbre
o infiltrazione di grasso nel fegato (epatomegalia)
o deterioramento della funzionalità del fegato
o riduzione dei globuli rossi che può rendere pallida la pelle e causare senso di
debolezza o affanno (anemia)
o bassa conta dei globuli bianchi, che può aumentare il rischio di infezione
(leucopenia)
o bassa conta delle piastrine, che può aumentare il rischio di ecchimosi e/o
sanguinamento (trombocitopenia)
o alterazioni della coagulazione che compromettono la capacità del sangue di
coagularsi
o Disturbi respiratori che comportano una riduzione dell'ossigeno nel corpo
(difficoltà respiratoria)
o Condizioni che portano ad un aumento dell'acidità del sangue (acidosi)
o coma, che richiede il ricovero
Formazione di piccole particelle che possono portare al blocco dei vasi sanguigni nei
polmoni (precipitati vascolari polmonari), o difficoltà respiratorie.
Segnalazione degli effetti indesiderati
Se il suo bambino presenta uno qualsiasi degli effetti indesiderati, informi il suo medico o
l’infermiere. Questo include qualsiasi possibile effetto indesiderato non elencato in questo
foglio. Lei può inoltre segnalare gli effetti indesiderati direttamente (vedere i dettagli di
seguito). Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori
informazioni sulla sicurezza di questo medicinale.
Gli effetti indesiderati possono, inoltre, essere segnalati direttamente tramite il sistema
nazionale di segnalazione all’indirizzo https://www.aifa.gov.it/content/segnalazioni-
reazioni-avverse.
5. Come conservare Numeta G19E
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini quando non viene
somministrato.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla sacca e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del
mese.
Non congelare.
Conservare nell'involucro esterno.
I medicinali non devono essere gettati nell’acqua di scarico o nei rifiuti domestici. Chieda
al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere
l’ambiente.
6. Contenuto della confezione ed altre informazioni
Descrizione dell'aspetto di Numeta G19E e contenuto della confezione
Numeta G19E si presenta sotto forma di sacca a tre compartimenti. Ogni sacca contiene
una combinazione sterile di una soluzione di glucosio, una soluzione pediatrica di
amminoacidi con elettroliti e un'emulsione lipidica, come descritto di seguito.
| Dimensioni contenitore | Soluzione di glucosio al 50% | Soluzione di amminoacidi al 5,9% con elettroliti | a m Emulsione di lipidi al 12,5% |
| 1000 mL | 383 mL | 392 mL | 225 mL |
Aspetto precedente la ricostituzione:
- Le soluzioni nei compartimenti di amminoacidi e glucosio sono limpide, incolori o leggermente gialle
- Il compartimento dell'emulsione di lipidi contiene un liquido uniforme di color bianco latte Aspetto dopo la ricostituzione:
- La soluzione per infusione “2 in 1” è limpida, incolore o leggermente gialla
- L’emulsione per infusione “3 in 1” è uniforme di color bianco latte La sacca a tre compartimenti è una sacca in plastica multistrato. Per impedire il contatto con l'aria, la sacca di Numeta è confezionata in un involucro esterno con barriera per l'ossigeno, che contiene un assorbitore di ossigeno e un indicatore di ossigeno.
Confezioni:
sacca da 1000 mL: 6 unità per scatola in cartone
1 sacca da 1000 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Via del Serafico 89
00142 Roma
Produttore:
Baxter S.A.
Boulevard Rene Branquart, 80
7860 Lessines
Belgio
Questo medicinale è autorizzato negli Stati Membri dello Spazio Economico Europeo con
le seguenti denominazioni:
| Austria Germany | m Numeta G 19 % E Emulsion zur Infusion |
| Belgium Luxembourg | r a NUMETZAH G19%E, émulsion pour perfusion |
| France | F NUMETAH G 19 %E émulsion pour perfusion |
| Denmark Norway Sweden | l e Numeta G19E |
| Czech Republic Greece | d Numeta G 19 % E |
| Netherlands | a Numeta G19%E emulsie voor infusie |
| Ireland United Kingdom | n a Numeta G19%E, Emulsion for Infusion i |
| Italy | l a Numeta G19%E emulsione per infusione |
| Finland | t I Numeta G19E infuusioneste, emulsio |
| a Poland | Numeta G 19 % E |
| i Portugal | Numeta G19%E |
| z n Spain | Numeta G19%E, emulsión para perfusión |
Le informazioni seguenti sono destinate esclusivamente ai professionisti medici o
operatori sanitari*
*Si tenga presente che in alcuni casi questo prodotto può essere somministrato a casa dai
genitori o da altre persone che ne hanno cura. In questi casi i genitori/o chi ne ha cura
devono leggere queste informazioni.
Non effettuare aggiunte alla sacca prima di verificarne la compatibilità. Si potrebbero
formare particelle o si potrebbe rompere l’emulsione lipidica. Ciò porterebbe al blocco dei
vasi sanguigni.
Numeta G19E deve essere a temperatura ambiente prima dell'uso.
Prima di usare Numeta G19E, prepare la sacca come mostrato di seguito.
Verificare che la sacca non sia danneggiata. Usare la sacca solo se non è danneggiata
L'aspetto di una sacca integra è così:
- Le membrane di separazione non permanenti sono intatte. Questo indica l'assenza di miscelazione del contenuto dei tre compartimenti.
- Le soluzioni di amminoacidi e di glucosio sono limpide, incolori o leggermente gialle, senza particelle visibili.
- L'emulsione di lipidi è un liquido uniforme di color bianco latte.
Prima di aprire l'involucro esterno, controllare il colore dell'indicatore di ossigeno.
- Confrontarlo con il colore di riferimento stampato accanto al simbolo OK nell'area stampata dell'etichetta dell'indicatore.
- Non usare la sacca se il colore dell'indicatore di ossigeno non corrisponde al colore di riferimento stampato accanto al simbolo OK. Le figure 1 e 2 illustrano come rimuovere l'involucro esterno di protezione. Gettare l'involucro esterno, l’indicatore di ossigeno e l'assorbitore di ossigeno.









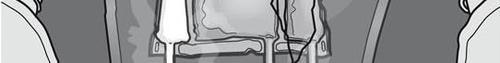

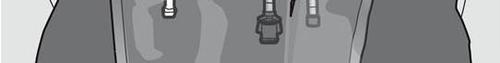




Figura 1 Figura 2
Preparazione dell’emulsione miscelata:
- Assicurarsi che il medicinale sia a temperatura ambiente quando si rompono le membrane di separazione non permanenti.
Porre la sacca su una superficie piana e pulita.
Attivazione della sacca a 3 compartimenti (miscelazione delle 3 soluzioni mediante
rottura delle 2 membrane non permanenti)
Step 1: Iniziare arrotolando la sacca dal lato dell’occhiello a D.
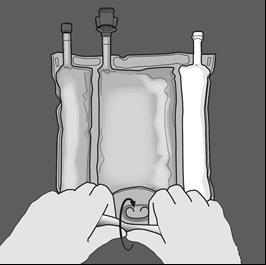
Step 2: Fare pressione finché le membrane di separazione non siano aperte.
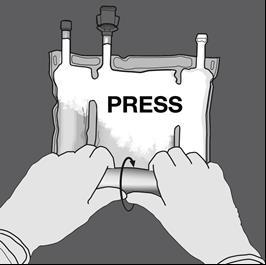
Step 3:
Cambiare direzione arrotolando la sacca verso l’occhiello a D. Continuare finché la
membrana non è completamente aperta.
Procedere nello stesso modo per completare l’apertura della seconda membrana.
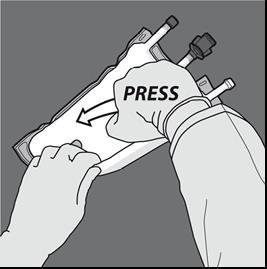
Step 4: Capovolgere la sacca almeno tre volte per mescolare completamente il contenuto.
L'aspetto della soluzione mescolata dovrebbe essere simile a un’emulsione di color
bianco latte.







Step 5: Rimuovere il cappuccio protettivo dal punto di somministrazione e inserire il set di
infusione.








Attivazione di 2 compartimenti (miscelazione delle 2 soluzioni attraverso la rottura della
membrana non permanente tra il compartimento degli amminoacidi e il compartimento con
glucosio)
Step 1: Per miscelare soltanto 2 soluzioni, arrotolare la sacca dall'angolo superiore
(estremità con l’occhiello) della membrana che separa le soluzioni. Fare pressione per
aprire la membrana che separa i compartimenti delle soluzioni di glucosio e amminoacidi.







Step 2: Posizionare la sacca in modo che il compartimento contenente l'emulsione lipidica
sia il più vicino all'operatore. Arrotolare la sacca proteggendo il compartimento
dell'emulsione lipidica con i palmi delle mani.
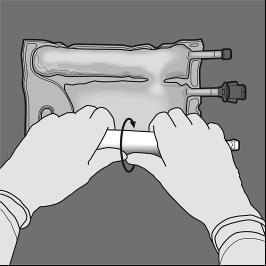
Step 3: Con una mano, fare pressione e arrotolare la sacca verso i punti di iniezione.
















Step 4: Cambiare direzione arrotolando la sacca verso la parte alta (estremità con
l’occhiello).
Premere con l'altra mano, continuando fino a che la membrana che separa le soluzioni di
amminoacidi e glucosio è completamente aperta.








Step 5: Capovolgere la sacca almeno tre volte per mescolare completamente il contenuto.
L'aspetto della soluzione mescolata dovrebbe essere chiaro, incolore o leggermente giallo.








Step 6: Rimuovere il cappuccio protettivo dal punto di somministrazione e inserire il set di
infusione.








La velocità del flusso deve essere aumentata gradualmente durante la prima ora. La
velocità di somministrazione del flusso deve essere regolata in base ai fattori seguenti:
- dose da somministrare
- i volumi da assumere quotidianamente
- la durata dell'infusione
Modo di somministrazione
La soluzione (nelle sacche e nei set per la somministrazione) deve essere protetta
dall’esposizione alla luce dal momento della miscelazione fino alla somministrazione.
E’ raccomandato l’utilizzo di un filtro da 1,2 micron per la somministrazione di Numeta G19E.
Per la sua alta osmolarità, Numeta G19E non diluito può essere somministrato solo
attraverso una vena centrale. Tuttavia, una sufficiente diluizione di Numeta G19E con
acqua per preparazioni iniettabili riduce l'osmolarità e permette l'infusione periferica.
La formula che segue indica l’effetto della diluizione sull'osmolarità delle sacche.

La tabella che segue mostra esempi di osmolarità per miscelazioni di 3CB attivati dopo
l'aggiunta di acqua per preparazioni iniettabili:
| Amminoacidi, glucosio e lipidi (3CB attivati) | |
| Volume iniziale nella sacca (mL) | 1000 |
| Osmolarità iniziale (appross. mOsm/L) | 1460 |
| Volume di acqua aggiunta (mL) | 1000 |
| Volume finale dopo l'aggiunta (mL) | 2000 |
| Osmolarità dopo l'aggiunta (mOsm/L appross.) | 730 |
Aggiunte di additivi:
Miscele contenenti oligoelementi e vitamine, devono essere protette dalla luce, dal
momento della miscelazione fino alla somminisrazione. L’esposizione alla luce ambientale
genera perossidi e altri prodotti di degradazione che possono essere ridotti dalla
fotoprotezione.
Additivi compatibili possono essere aggiunti attraverso il sito di iniezione nella miscela
ricostituita (dopo l'apertura delle membrane non permanenti e dopo la miscelazione del
contenuto dei due o tre compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che
la miscela sia ricostituita (prima dell'apertura delle membrane di separazione non
permanenti e prima della miscelazione delle soluzioni e dell'emulsione).
Eventuali aggiunte di soluzioni di oligoelementi (identificati come TE1,TE2 e TE4),
vitamine (identificate come liofilizzato V1 e emulsione V2), e elettroliti disponibili in
commercio in quantità definite sono mostrate nelle tabelle 1-6.
- 3.Compatibilità con TE4, V1 e V2
Tabella 1: Compatibilità della sacca 3-in-1 (3CB attivati) con e senza diluizione con acqua
| n Per 1000 mL (3 in 1 miscela con lipidi) | ||||||
| e | Miscela non diluita | Miscela diluita | ||||
| g Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| A Sodio (mmol) | 45,8 | 105 | 151 | 45,8 | 105 | 151 |
| Potassio (mmol) | 32,0 | 118 | 150 | 32,0 | o 118 | 150 |
| Magnesio (mmol) | 2,6 | 7,8 | 10,4 | 2,6 | c 7,8 | 10,4 |
| Calcio (mmol) | 3,8 | 20,5 | 24,3 | 3,8 | a 20,5 | 24,3 |
| Fosfato* (mmol) | 9,4 | 14,6 | 24,0 | 9,4 | 14,6 | 24,0 |
| Oligoelementi e vitamine | 34 mL TE4 + 3,4 fiale V1 + 38 mL V2 | 34 mL TE4 + 3,4 fiale V1 + 38 mL V2 |
| m 34 mL TE4 + 3,4 fiale V1 + 38 mL V2 | 34 mL TE4 + 3,4 fiale V1 + 38 mLV2 | |
| Acqua per soluzioni iniettabili | a | 1450 mL | 1450 mL |
Tabella 2: Compatibilità della sacca 2-in-1 (2CB attivati)
| e Per 775 mL (2 in 1 miscela senza lipidi) | |||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | d Livello toale massimo |
| Sodio (mmol) | 45,1 | 32,0 | a 77,1 |
| Potassio (mmol) | 32,0 | n 45,6 | 77,6 |
| Magnesio (mmol) | 2,6 | a 5,2 | 7,8 |
| Calcio (mmol) | 3,8 | i 19,4 | 23,2 |
| Fosfato* (mmol) | 7,2 | l 16,0 | 23,2 |
| Oligoelmenti e vitamine | a 10 mL TE4 + 1 t fiala V1 | 10 mL TE4 + 1 fiala V1 | |
- 4.Compatibilità con TE1, V1 e V2Tabella 3: Compatibilità della sacca 3-in-1 (3CB attivati)
| Per 1000 mL (3 in 1 miscela con lipidi) | |||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 45,8 | 0 | 45,8 |
| Potassio (mmol) | 32,0 | 0 | r 32,0 |
| Magnesio (mmol) | 2,6 | 0 | a 2,6 |
| Calcio (mmol) | 3,8 | 6,4 | 10,2 |
| Fosfato* (mmol) | 9,4 | 0 | F 9,4 |
| Oligoelementi e vitamine | 15 mL TE1 + 1 fiala V1 + 10 mL V2 | l 15 mL TE1 e + 1 fiala V1 + 10 mL V2 | |
Tabella 4: Compatibilità della sacca 2-in-1 (2CB attivati)
| Per 775 mL (2 in 1 miscela senza lipidi) | |||
| Aggiunte | Livello incluso | a n Aggiunta ulteriore massima | Livello totale massimo |
| Sodio (mmol) | 45,1 | a 32,0 | 77,1 |
| Potassio (mmol) | 32,0 | i 45,6 | 77,6 |
| Magnesio (mmol) | 2,6 | l 5,2 | 7,8 |
| Calcio (mmol) | 3,8 | a 19,4 | 23,2 |
| Fosfato* (mmol) | 7,2 | t 16,0 | 23,2 |
| Oligoelementi e vitamine | I | 10 mL TE1 + 1 fiala V1 | 10 mL TE1 + 1 fiala V1 |
- 5.Compatibilità con TE2, V1 e V2
Tabella 5: Compatibilità della sacca 2-in-1 (2CB attivati)
| n Per 775 mL (2 in 1 miscela senza lipidi) | |||
| e Aggiunte | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| g Sodio (mmol) | 45,1 | 32,0 | 77,1 |
| A Potassio (mmol) | 32,0 | 45,6 | 77,6 |
| Magnesio (mmol) | 2,6 | 5,2 | 7,8 |
| Calcio (mmol) | 3,8 | 19,4 | 23,2 |
| Fosfato* (mmol) | 7,2 | 16,0 | 23,2 |
| Oligoelementi e vitamine | 15 mL TE2 + 1 fiala V1 | 15 mL TE2 + 1 fiala V1 |
Tabella 6: Compatibilità della sacca 3-in-1 (3CB attivati)
| a Per 1000 mL (3 in 1 miscela con lipidi) | |||
| Aggiunte | Livello incluso | Aggiunta ulteriore massima | F Livello totale massimo |
| Sodio (mmol) | 45,8 | 0 | l 45,8 |
| Potassio (mmol) | 32,0 | 0 | e 32,0 |
| Magnesio (mmol) | 2,6 | 0 | 2,6 |
| Calcio (mmol) | 3,8 | 6,4 | d 10,2 |
| Fosfato* (mmol) | 9,4 | 0 | 9,4 |
| Oligoelementi e vitamine | a n 15 mL TE2 + 1 fiala V1 + 10 mL V2 | 15 mL TE2 + 1 fiala V1 + 10 mL V2 | |
La composizione dei preparati di vitamine e oligoelementi sono illustrati nelle tabelle 7 e
8
Tabella 7: Composizione del preparato commerciale di oligoelementi utilizzato
| Composizione per 10mL | TE1 | TE2 | TE4 |
| Ferro | 8,9 µmol o 0,5 mg | r
| |
| Zinco | 38,2 µmol o 2,5 mg | 15,3 µmol o 1 mg | F 15,3 µmol o 1 mg |
| Selenio | 0,253 µmol o 0,02 mg | 0,6 µmol o 0,05 mg | l 0,253 µmol o e 0,02 mg |
| Rame | 3,15 µmol o 0,2 mg | d 4,7 µmol o 0,3 mg | 3,15 µmol o 0,2 mg |
| Iodio | 0,0788 µmol o 0,01 mg | a 0,4 µmol o 0,05 mg | 0,079 µmol o 0,01 mg |
| Fluoro | 30 µmol o 0,57 mg | n 26,3 µmol o a 0,5 mg | |
| Molibdeno |
| i 0,5 µmol o 0,05 mg | |
| Manganese | a 0,182 µmol o t I 0,01 mg | 1,8 µmol o 0,1 mg | 0,091 µmol o 0,005 mg |
| Cromo |
| 0,4 µmol o 0,02 mg | |
| Cobalto | i
| 2,5 µmol o 0,15 mg |
Tabella 8:Composizione del preparato comerciale di vitamine utilizzato:
| e Composizione per fiala | V1 | V2 |
| g Vitamina B1 | 2,5 mg | |
| A Vitamina B2 | 3,6 mg | |
| Nicotinamide | 40 mg |
Per eseguire un'aggiunta:
- Operare in condizioni asettiche
- Preparare il punto d'iniezione della sacca
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione
- Miscelare il contenuto della sacca e le aggiunte
Preparazione dell'infusione:
- Operare in condizioni asettiche
- Sospendere la sacca
- Rimuovere la protezione in plastica dal punto di somministrazione
- Inserire saldamente lo spike del set di infusione nel punto di somministrazione
Somministrazione dell'infusione:
- Solo per uso singolo
- Somministrare il prodotto solo dopo l'apertura delle membrane di separazione non permanenti tra i due o tre compartimenti e la miscelazione del contenuto dei due o tre compartimenti
- Assicurarsi che l'emulsione finale per infusione dei 3 compartimenti attivati non mostri alcuna prova di separazione delle fasi o che la soluzione per infusione finale dei 2 compartimenti attivati non mostri alcuna presenza di particelle
- Dopo la rottura delle membrane non permanenti, il contenuto si deve usare immediatamente. Numeta G19E non deve essere conservato per un'infusione successiva. Non collegare eventuali sacche parzialmente utilizzate
- Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa a causa di possibili residui gassosi contenuti nella sacca principale
- E’ raccomandato l’utilizzo di un filtro da 1,2 micron per la somministrazione di Numeta G19E
| Vitamina B6 | 4,0 mg | |
| Acido Pantotenico | 15,0 mg | |
| Biotina | 60 µg | |
| Acido folico | 400 µg | |
| Vitamina B12 | 5,0 µg | |
| Vitamina C | 100 mg | |
| Vitamina A | 2300 IU | |
| Vitamina D | 400 IU | |
| Vitamina E | 7 IU | |
| Vitamina K | l 200 µg |
- Qualsiasi eventuale prodotto non utilizzato, rifiuti derivati e tutti i dispositivi usa e getta necessari devono essere smaltiti correttamente e non riutilizzati Periodo di validità dopo la miscelazione delle soluzioni: Usare il prodotto immediatamente dopo l'apertura delle membrane non permanenti tra i due o tre compartimenti. Gli studi di stabilità delle miscele sono stati condotti per 7 giorni a una temperatura compresa tra 2°C e 8°C, seguiti da 48 ore a 30°C.
Periodo di validità dopo l’integrazione (elettroliti, oligoelementi, vitamine, acqua):
Per specifiche miscele, i dati di stabilità in uso della formulazione di Numeta sono stati
dimostrati per 7 giorni a una temperatura compresa tra 2°C e 8°C, seguiti da 48 ore a 30°C.
Da un punto di vista microbiologico, il prodotto deve essere utilizzato immediatamente. Se
non utilizzato immediatamente, i tempi e le condizioni di conservazione all’utilizzo sono
responsabilità dell'utente e non devono essere superiori alle 24 ore, a temperature comprese
tra 2°C e 8°C, a meno che la ricostituzione/diluizione/supplementazione non sia avvenuta
in condizioni asettiche controllate e convalidate.
Non usare Numeta se la sacca è danneggiata. Questo è l'aspetto di una sacca danneggiata:
- le membrane di separazione non permanenti sono rotte
- uno dei compartimenti contiene una miscela delle soluzioni
- le soluzioni di amminoacidi e di glucosio non sono limpide, incolori o leggermente gialle e/o contengono particelle visibili
- l'emulsione di lipidi non è un liquido uniforme di color bianco latte.
I medicinali non devono essere gettati nell’acqua di scarico e nei rifiuti domestici. Chieda
al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere
l’ambiente.
Cosa contiene Numeta G19E
I principi attivi sono:
| n Principio Attivo | 2CB attivati (775 mL) | 3CB attivati (1000 mL) |
| e Compartimento Amminoacidi | ||
| g Alanina | 1,83 g | 1,83 g |
| Arginina | 1,92 g | 1,92 g |
| A Acido aspartico | 1,37 g | 1,37 g |
| Cisteina | 0,43 g | 0,43 g |
| Principio Attivo | 2CB attivati (775 mL) | o c 3CB attivati (1000 mL) |
| Acido glutammico | 2,29 g | 2,29 g |
| Glicina | 0,91 g | a 0,91 g |
| Istidina | 0,87 g | 0,87 g |
| Isoleucina | 1,53 g | m 1,53 g |
| Leucina | 2,29 g | 2,29 g |
| Lisina monoidrata (come lisina) | 2,82 g (2,51 g) | r a 2,82 g (2,51 g) |
| Metionina | 0,55 g | 0,55 g |
| Ornitina cloridrata (come ornitina) | F 0,73 g (0,57 g) | 0,73 g (0,57 g) |
| Fenilalanina | l 0,96 g | 0,96 g |
| Prolina | e 0,69 g | 0,69 g |
| Serina | 0,91 g | 0,91 g |
| Taurina | d 0,14 g | 0,14 g |
| Treonina | 0,85 g | 0,85 g |
| Triptofano | a 0,46 g | 0,46 g |
| Tirosina | 0,18 g | 0,18 g |
| n Valina | 1,74 g | 1,74 g |
| a Sodio Cloruro | 1,79 g | 1,79 g |
| i Potassio acetato | 3,14 g | 3,14 g |
| l Calcio cloruro biidrato | 0,56 g | 0,56 g |
| a Magnesio acetato tetraidrato | 0,55 g | 0,55 g |
| Sodio glicerofosfato idrato | 2,21 g | 2,21 g |
| t Compartimento Glucosio | ||
| I Glucosio monoidrato (come glucosio anidro) | 210,65 g (191,50 g) | 210,65 g (191,50 g) |
| a Compartimento Lipidi | ||
| i Olio di oliva purificato (circa 80%) + olio di soia purificato (circa 20%) | 28,1 g | |
La soluzione/emulsione ricostituita fornisce quanto segue:
| g Composizione | ||||
| 2CB attivati | 3CB attivati | |||
| A Per unità di volume (ml) Azoto (g) | 775 3,5 | 100 0,45 | 1000 3,5 | 100 0,35 |
| o Composizione | ||||
| 2CB attivati | c 3CB attivati | |||
| Per unità di volume (ml) Amminoacidi (g) Glucosio (g) Lipidi (g) Energia Calorie totali (kcal) Calorie non proteiche (kcal) Calorie da glucosio (kcal) Calorie lipidiche (kcal)a Calorie non proteiche/azoto (kcal/g N) Calorie lipidiche/calorie non proteiche (%) Calorie lipidiche/calorie totali (%) Elettroliti Sodio (mmol) Potassio (mmol) Magnesio (mmol) Calcio (mmol) Fosfato (mmol)b i Acetato (mmol) l Malato (mmol) Cloruro (mmol) | 775 23,0 192 0 858 766 766 0 220 NA NA 45,1 a 32,0 n 2,6 3,8 a 7,2 37,1 8,8 42,6 | 100 3,0 24,7 0 111 99 99 0 l 220 e N/A d N/A 5,8 4,1 0,33 0,50 0,93 4,8 1,1 5,5 | 1000 m 23,0 192 28,1 r a 1139 F 1047 766 281 301 27 25 45,8 32,0 2,6 3,8 9,4 37,1 8,8 42,6 | a 100 2,3 19,2 2,8 114 105 77 28 301 27 25 4,6 3,2 0,26 0,38 0,93 3,71 0,88 4,3 |
| a t pH (appross,) Osmolarità appross, (mOsm/L) | 5,5 1835 | 5,5 1835 | 5,5 1460 | 5,5 1460 |
Gli altri componenti sono:
per la regolazione del pH
-

- Paese di registrazione
- Forma farmaceuticaEmulsione per infusione endovenosa, 500 ML
- Codice ATCB05BA01
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a NUMETAForma farmaceutica: Soluzione per infusione, 500 MLPrincipio attivo: amino acidsProduttore: MONICO S.P.A.Prescrizione richiestaForma farmaceutica: Soluzione per infusione, 4 G/100 MLPrincipio attivo: amino acidsProduttore: INDUSTRIA FARMACEUTICA GALENICA SENESE S.R.L.Prescrizione richiestaForma farmaceutica: Soluzione per infusione, 500 MLPrincipio attivo: amino acidsPrescrizione richiesta
Medici online per NUMETA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di NUMETA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per NUMETA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.













