
Come usare POMBILITI
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Pombiliti 105 mg polvere per concentrato per soluzione per infusione
cipaglucosidasi alfa
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4. Contenuto di questo foglio
- 1. Cos’è Pombiliti e a cosa serve
- 2. Cosa deve sapere prima che le venga somministrato Pombiliti
- 3. Come è somministrato Pombiliti
- 4. Possibili effetti indesiderati
- 5. Come conservare Pombiliti
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Pombiliti e a cosa serve
Cos’è Pombiliti
Pombiliti è un tipo di “terapia enzimatica sostitutiva” utilizzata per il trattamento della malattia di
Pompe a esordio tardivo negli adulti. Contiene il principio attivo “cipaglucosidasi alfa”.
A cosa serve
Pombiliti viene sempre usato assieme a un altro farmaco chiamato miglustat 65 mg capsule rigide. È
Per qualsiasi dubbio sui medicinali, si rivolga al medico o al farmacista.
Come agisce Pombiliti
Le persone affette dalla malattia di Pompe hanno bassi livelli dell’enzima alfa-glucosidasi acida
(GAA). Questo enzima aiuta a controllare i livelli di glicogeno (un tipo di carboidrato) nel corpo.
Nella malattia di Pompe si accumulano elevate quantità di glicogeno nei muscoli del corpo. Questo
impedisce il corretto funzionamento dei muscoli, come i muscoli delle gambe che permettono di
camminare, quelli presenti sotto i polmoni che aiutano a respirare e il cuore.
Pombiliti penetra nelle cellule dei muscoli interessati dalla malattia di Pompe. Quando entra nelle
cellule, la cipaglucosidasi alfa agisce come l’enzima alfa-glucosidasi acida, aiutando a scomporre il
glicogeno e a controllarne i livelli.
2. Cosa deve sapere prima che le venga somministrato Pombiliti

Non deve prendere Pombiliti
- Se ha manifestato reazioni di ipersensibilità potenzialmente fatali a:
- cipaglucosidasi alfa
- miglustat
- uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6).
- Se ha dovuto interrompere una precedente infusione e non ha potuto riprenderla a causa di reazioni di ipersensibilità potenzialmente fatali. Avvertenze e precauzioniSi rivolga al medico, al farmacista o all’infermiere prima di usare Pombiliti. Consulti immediatamente il medico o l’infermierese manifesta, se ritiene di manifestare o se ha manifestato in passato una delle seguenti reazioni con un’altra terapia enzimatica sostitutiva:
- reazioni allergiche compresa anafilassi (reazione allergica grave) - per i sintomi delle reazioni pericolose per la vita, vedere il paragrafo 4 “Possibili effetti indesiderati”
- reazioni associate all’infusione durante la somministrazione del medicinale o nelle immediatamente successive - per i sintomi delle reazioni pericolose per la vita, vedere la sezione 4 sotto “Possibili effetti indesiderati”. Informi il medico se ha avuto in passato una malattia cardiaca o polmonare. Queste condizioni possono peggiorare durante o subito dopo l’infusione con Pombiliti. Informi immediatamente il medico o l’infermiere se sta manifestando respiro affannoso, tosse, battito del cuore accelerato o irregolare o qualsiasi altro effetto correlato a queste condizioni. Informi il medico anche in caso di gonfiore alle gambe o di gonfiore diffuso del corpo, eruzioni cutanee gravi o urine schiumose durante la minzione. Il medico deciderà se l’infusione di Pombiliti deve essere interrotta e le fornirà un trattamento medico adeguato. Il medico deciderà inoltre se potrà continuare a ricevere Pombiliti. Pretrattamento farmacologicoIl medico potrebbe somministrare altri medicinali prima di Pombiliti, tra cui:
- antistaminici e corticosteroidi per prevenire o ridurre le reazioni correlate all’infusione
- antipiretici per ridurre la febbre. Bambini e adolescentiQuesto medicinale non deve essere somministrato a pazienti di età inferiore ai 18 anni. Questo perché gli effetti di Pombiliti in associazione a miglustat in tale fascia d’età non sono noti. Altri medicinali e PombilitiInformi il medico o il farmacista se sta assumendo, ha recentemente assunto o assumerà qualsiasi altro medicinale. Questi includono i medicinali acquistabili senza prescrizione medica, tra cui quelli a base di erbe. Gravidanza e allattamentoSe è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte materno chieda immediatamente consiglio al medico o al farmacista prima di usare questo medicinale. Non esistono dati relativi all’uso di Pombiliti in associazione a miglustat durante la gravidanza.
- Non deve ricevere Pombiliti e/o miglustat 65 mg capsule rigide se è in gravidanza. Si assicuri di informare immediatamente il medico se è in gravidanza, sospetta di essere in gravidanza o sta pianificando una gravidanza. Potrebbero esserci rischi per il feto.
- Pombiliti in associazione a miglustat non deve essere somministrato a donne in allattamento. Si dovrà decidere se interrompere il trattamento o interrompere l’allattamento. Contraccezione e fertilitàLe pazienti di sesso femminile in età fertile devono utilizzare metodi contraccettivi affidabili durante l’uso di questi medicinali e per 4 settimane dopo l’interruzione di entrambi i medicinali. Guida di veicoli e utilizzo di macchinari
Potrebbe avvertire capogiri, sonnolenza oppure potrebbe avere la pressione sanguigna bassa
(ipotensione) dopo aver ricevuto Pombiliti o il pretrattamento farmacologico. Se ciò accade, non guidi
né usi strumenti o macchinari.
Pombiliti contiene sodio
Questo medicinale contiene 10,5 mg di sodio (componente principale del sale da cucina) per
flaconcino. Questo equivale allo 0,52% dell’assunzione massima giornaliera raccomandata con la
dieta di un adulto.
3. Come è somministrato Pombiliti
Pombiliti viene somministrato da un medico o da un infermiere mediante fleboclisi in una vena
(infusione endovenosa).
Informi il medico se desidera effettuare il trattamento a domicilio. Il medico deciderà, dopo una
valutazione, se lei può sottoporsi all’infusione a domicilio di Pombiliti in sicurezza. Se manifesta un
qualsiasi effetto indesiderato durante un’infusione di Pombiliti a domicilio, il personale incaricato può
interrompere l’infusione e avviare il trattamento medico adeguato.
Pombiliti deve essere usato insieme a miglustat. Usi soltanto le capsule di miglustat da 65 mg insieme
a cipaglucosidasi alfa. NONusi le capsule di miglustat da 100 mg (si tratta di un medicinale diverso).
dose raccomandata.
Quanto Pombiliti viene somministrato
La quantità di medicinale che le verrà somministrata si basa sul peso corporeo. La dose iniziale
raccomandata è di 20 mg per ogni chilogrammo di peso corporeo.
Quando e per quanto tempo viene somministrato Pombiliti
- Il trattamento con Pombiliti ha luogo una volta ogni due settimane. Le capsule di miglustat da 65 mg capsule rigide per informazioni su come assumere miglustat.
- L’infusione di cipaglucosidasi alfa deve iniziare 1 ora dopo l’assunzione di miglustat 65 mg capsule rigide.
- In caso di ritardo, l’inizio dell’infusione non deve aver luogo oltre 3 ore dopo l’assunzione di miglustat.
- L’infusione di cipaglucosidasi alfa ha una durata di circa 4 ore.
Figura 1. Tempistica di somministrazione della dose
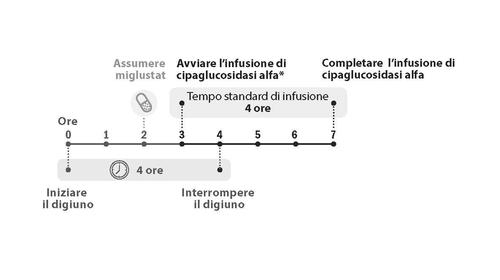
*
Passaggio da un’altra terapia enzimatica sostitutiva
Se attualmente è in trattamento con un’altra terapia enzimatica sostitutiva:
- il medico le indicherà quando interrompere l’altra terapia enzimatica sostitutiva prima di iniziare Pombiliti
- informi il medico quando ha completato l’ultima dose. Se le viene somministrato più Pombiliti di quanto necessarioSe ha difficoltà a respirare, se avverte una sensazione di gonfiore o di battito cardiaco accelerato, potrebbe aver ricevuto una quantità in eccesso di Pombiliti. Informi immediatamente il medico. Un’eccessiva velocità di infusione di Pombiliti potrebbe causare sintomi correlati a un accumulo di liquidi nel corpo, tra cui respiro corto, battito cardiaco accelerato o gonfiore diffuso del corpo. Se salta una dose di PombilitiSe ha saltato un’infusione, contatti il medico o l’infermiere appena possibile per fissare un nuovo appuntamento per ricevere la terapia con Pombiliti in associazione a miglustat 24 ore dopo l’ultima assunzione di miglustat. Se interrompe il trattamento con PombilitiParli con il medico se desidera interrompere il trattamento con Pombiliti. I sintomi della malattia potrebbero peggiorare se interrompe il trattamento.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Pombiliti viene usato con miglustat e gli effetti indesiderati possono verificarsi con entrambi i
medicinali. Gli effetti indesiderati sono stati osservati principalmente durante o poco dopo l’infusione
di Pombiliti (effetti correlati all’infusione). Informi immediatamente il medico se manifesta una
reazione correlata all’infusione o una reazione allergica. Alcune di queste reazioni possono diventare
gravi e potenzialmente fatali. Per prevenire tali reazioni, il medico può somministrare dei medicinali
prima dell’infusione.
Reazioni correlate all’infusione
La maggior parte delle reazioni correlate all’infusione è di entità lieve o moderata. I sintomi delle
reazioni correlate all’infusione possono includere difficoltà a respirare, gonfiore, febbre, brividi,
vertigini, arrossamento della pelle, prurito ed eruzione cutanea.
Reazioni allergiche
Le reazioni allergiche possono includere sintomi quali eruzione cutanea in qualsiasi parte del corpo,
occhi gonfi, prolungata difficoltà a respirare, tosse, gonfiore delle labbra, della lingua o della gola,
prurito della pelle e orticaria.
Molto comuni(possono interessare più di 1 persona su 10)
- mal di testa
Comuni(possono interessare fino a 1 persona su 10)
- grave reazione allergica potenzialmente fatale (reazione anafilattica)
- sensazione di vertigine
- tremore
- sonnolenza
- disturbi del gusto
- sensazione di intorpidimento, formicolio (parestesia)
- battito cardiaco rapido
- arrossamento della pelle
- pressione sanguigna bassa
- respiro affannoso
- tosse
- diarrea
- sensazione di malessere (nausea)
- mal di stomaco
- flatulenza
- gonfiore
- vomito
- orticaria
- prurito
- eruzione cutanea
- sudorazione eccessiva
- contrazioni muscolari dolorose
- dolori muscolari
- debolezza muscolare
- dolore alle articolazioni
- stanchezza
- febbre
- brividi
- sensazione di malessere al torace
- gonfiore nella zona del corpo dove è stato inserito l’ago
- dolore
- gonfiore delle mani, dei piedi, delle caviglie, delle gambe
- aumento della pressione sanguigna Non comuni(possono interessare fino a 1 persona su 100)
- reazione allergica
- impossibilità di tenere o mantenere l’equilibrio
- sensazione di bruciore
- emicrania
- sensazione di mancamento
- insolito pallore cutaneo
- asma
- respiro sibilante
- fastidio in bocca e in gola
- gonfiore in gola
- indigestione
- dolore o contrazioni dolorose dell’esofago
- dolore o fastidio in bocca
- gonfiore della lingua
- alterazione del colore della pelle
- gonfiore della pelle
- dolore nella zona tra le costole e l’anca
- affaticamento muscolare
- rigidità muscolare
- debolezza
- dolore alle guance, alle gengive, alle labbra, al mento
- dolore nella zona del corpo in cui è stato inserito l’ago
- sensazione di malessere generale
- dolore toracico
- tumefazione al viso
- variazioni della temperatura corporea
- graffi o danni alla pelle Segnalazione degli effetti indesideratiSe manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema nazionale di segnalazione riportato nell’allegato V. Segnalando gli effetti indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Pombiliti
Il medico, il farmacista o l’infermiere è responsabile della conservazione di questo medicinale e dello
smaltimento corretto dei flaconcini aperti. Le informazioni seguenti sono destinate esclusivamente agli
operatori sanitari.
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sul flaconcino e sulla scatola dopo
“Scad.”. La data di scadenza si riferisce alla data dell’ultimo giorno di quel mese.
Flaconcini non aperti: conservare in frigorifero (2 °C – 8 °C). Tenere il flaconcino nell’imballaggio
esterno per proteggere il medicinale dalla luce.
Dopo la diluizione, si raccomanda l’uso immediato. Tuttavia, è stato dimostrato che è possibile
conservare la sacca per infusione endovenosa con Pombiliti per 6 ore a 20 °C - 25°C e per 24 ore a
2 °C - 8 °C.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non usa più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Pombiliti
Il principio attivo è cipaglucosidasi alfa. Un flaconcino contiene 105 mg di cipaglucosidasi alfa. Dopo
la ricostituzione, la soluzione nel flaconcino contiene 15 mg di cipaglucosidasi alfa per mL. La
concentrazione finale di cipaglucosidasi alfa diluita nella sacca per infusione endovenosa varia da
0,5 mg/mL a 4 mg/mL.
Gli altri componenti sono:
- sodio citrato diidrato (E331)
- acido citrico monoidrato (E330)
- mannitolo (E421)
- polisorbato 80 (E433) Descrizione dell’aspetto di Pombiliti e contenuto della confezionePombiliti è una polvere di colore da bianco a lievemente giallognolo. Dopo la ricostituzione, appare come una soluzione da cristallina a opalescente, da incolore a lievemente gialla, priva di particelle estranee e praticamente priva di particolato sotto forma di particelle da bianche a traslucide. La soluzione ricostituita deve essere ulteriormente diluita in una sacca per infusione. Pombiliti è una polvere per concentrato per soluzione per infusione contenuta in un flaconcino. Confezioni da 1 flaconcino, 10 flaconcini o 25 flaconcini È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Amicus Therapeutics Europe Limited
Block 1, Blanchardstown Corporate Park
Ballycoolin Road
Blanchardstown, Dublino
D15 AKK1
Ireland
Tel: +353 (0) 1 588 0836
Fax: +353 (0) 1 588 6851
e-mail: [email protected]
Produttore
Manufacturing Packaging Farmaca (MPF) B.V.
Neptunus 12, Heerenveen, 8448CN, Paesi Bassi
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Amicus Therapeutics Europe Limited
Tél/Tel: (+32) 0800 89172
e-mail: [email protected]
Lietuva
Amicus Therapeutics Europe Limited
Tel: (+370) 8800 33167
El. paštas: [email protected]
България
Amicus Therapeutics Europe Limited
Teл.: (+359) 00800 111 3214
имейл: [email protected]
Luxembourg/Luxemburg
Amicus Therapeutics Europe Limited
Tél/Tel: (+352) 800 27003
e-mail: [email protected]
Česká republika
Amicus Therapeutics Europe Limited
Tel.: (+420) 800 142 207
e-mail: [email protected]
Magyarország
Amicus Therapeutics Europe Limited
Tel.: (+36) 06 800 21202
e-mail: [email protected]
Danmark
Amicus Therapeutics Europe Limited
Tlf.: (+45) 80 253 262
e-mail: [email protected]
Malta
Amicus Therapeutics Europe Limited
Tel: (+356) 800 62674
e-mail: [email protected]
Deutschland
Amicus Therapeutics GmbH
Tel: (+49) 0800 000 2038
E-mail: [email protected]
Nederland
Amicus Therapeutics BV
Tel: (+31) 20 235 8510 / (+31) 0800 022 8399
e-mail: [email protected]
Eesti
Amicus Therapeutics Europe Limited
Tel: (+372) 800 0111 911
e-post: [email protected]
Norge
Amicus Therapeutics Europe Limited
Tlf: (+47) 800 13837
e-post: [email protected]
Ελλάδα
Amicus Therapeutics Europe Limited
Τηλ: (+30) 00800 126 169
e-mail: [email protected]
Österreich
Amicus Therapeutics Europe Limited
Tel: (+43) 0800 909 639
E-Mail: [email protected]
España
Amicus Therapeutics S.L.U.
Tel: (+34) 900 941 616
e-mail: [email protected]
Polska
Amicus Therapeutics Europe Limited
Tel.: (+48) 0080 012 15475
e-mail: [email protected]
France
Amicus Therapeutics SAS
Tél: (+33) 0 800 906 788
e-mail: [email protected]
Portugal
Amicus Therapeutics Europe Limited
Tel: (+351) 800 812 531
e-mail: [email protected]
Hrvatska
Amicus Therapeutics Europe Limited
Tel: (+358) 0800 222 452
e-pošta: [email protected]
Ireland
Amicus Therapeutics Europe Limited
Tel: (+353) 1800 936 230
e-mail: [email protected]
România
Amicus Therapeutics Europe Limited
Tel.: (+40) 0808 034 288
e-mail: [email protected]
Slovenija
Amicus Therapeutics Europe Limited
Tel.: (+386) 0800 81794
e-pošta: [email protected]
Ísland
Amicus Therapeutics Europe Limited
Sími: (+354) 800 7634
Netfang: [email protected]
Slovenská republika
Amicus Therapeutics Europe Limited
Tel: (+421) 0800 002 437
e-mail: [email protected]
Italia
Amicus Therapeutics S.r.l.
Tel: (+39) 800 795 572
e-mail: [email protected]
Suomi/Finland
Amicus Therapeutics Europe Limited
Puh/Tel: (+358) 0800 917 780
sähköposti/e-mail: [email protected]
Κύπρος
Amicus Therapeutics Europe Limited
Τηλ: (+357) 800 97595
e-mail: [email protected]
Sverige
Amicus Therapeutics Europe Limited
Tfn: (+46) 020 795 493
e-post: [email protected]
Latvija
Amicus Therapeutics Europe Limited
Tel: (+371) 800 05391
e-pasts: [email protected]
United Kingdom (Northern Ireland)
Amicus Therapeutics, UK Limited
Tel: (+44) 08 0823 46864
e-mail: [email protected]
Altre fonti d'informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali: http://www.ema.europa.eu. Inoltre, sono riportati link ad altri siti web su malattie rare
e relativi trattamenti terapeutici.
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari.
Istruzioni per l’uso: ricostituzione, diluizione e somministrazione
Pombiliti deve essere ricostituito con acqua per preparazioni iniettabili, quindi diluito con una
soluzione iniettabile di sodio cloruro 9 mg/mL (0,9%) e infine somministrato mediante infusione
endovenosa. La ricostituzione e la diluizione devono essere eseguite in conformità alle norme di buona
pratica, soprattutto riguardo all’asepsi.
Poiché questo medicinale è una proteina, può verificarsi la formazione di particolato nella soluzione
ricostituita e in quella finale diluita nella sacca per infusione. Pertanto, per la somministrazione deve
essere usato un filtro in linea a basso legame proteico da 0,2 micron. È stato dimostrato che l’uso di un
filtro in linea da 0,2 micron rimuove le particelle visibili e non determina una perdita apparente di
proteina o di attività.
Stabilire il numero di flaconcini da ricostituire in base al regime posologico del paziente (mg/kg) e
rimuovere i flaconcini necessari dal frigorifero al fine di consentire loro di raggiungere la temperatura
ambiente (circa 30 minuti). Ogni flaconcino di Pombiliti è esclusivamente monouso.
Utilizzare una tecnica asettica.
Ricostituzione
Ricostituire ogni flaconcino da 105 mg di Pombiliti con 7,2 mL di acqua per preparazioni iniettabili
usando una siringa con un ago di diametro non superiore a 18 gauge. Aggiungere l’acqua per
preparazioni iniettabili lentamente, facendola scorrere lungo le pareti del flaconcino e non direttamente
sulla polvere liofilizzata. Inclinare e ruotare delicatamente ogni flaconcino. Non capovolgere, agitare o
scuotere il flaconcino. Il volume di estrazione appare come una soluzione da cristallina a opalescente,
da incolore a lievemente gialla, priva di particelle estranee e praticamente priva di particolato sotto
forma di particelle da bianche a traslucide. Ispezionare immediatamente i flaconcini ricostituiti per
verificare la presenza di particolato e alterazioni del colore. Non usare se all’esame immediato si
osservano particelle estranee diverse da quanto descritto sopra o se il colore della soluzione ricostituita
è alterato. Il pH della soluzione ricostituita è circa 6.0.
Dopo la ricostituzione, è consigliabile diluire tempestivamente i flaconcini (vedere di seguito).
Diluizione
Una volta ricostituita come indicato sopra, la soluzione ricostituita nel flaconcino contiene 15 mg di
cipaglucosidasi alfa per mL. Il volume ricostituito consente il prelievo preciso di 7,0 mL (pari a
105 mg) da ciascun flaconcino. Questo deve essere poi ulteriormente diluito come segue: usando una
siringa con ago di diametro non superiore a 18 gauge, prelevare lentamente la soluzione ricostituita dai
flaconcini, includendo la quantità inferiore a 7,0 mL del flaconcino parziale, fino a ottenere la dose del
paziente. La concentrazione finale raccomandata di cipaglucosidasi alfa nelle sacche per infusione
varia da 0,5 mg/mL a 4 mg/mL. Rimuovere l’aria presente all’interno della sacca per infusione.
Inoltre, prelevare dalla soluzione iniettabile di sodio cloruro 9 mg/mL (0,9%) che sarà sostituita dal
volume totale (mL) di cipaglucosidasi alfa ricostituita. Iniettare lentamente Pombiliti ricostituito
direttamente nella soluzione iniettabile di sodio cloruro 9 mg/mL (0,9%). Capovolgere o massaggiare
delicatamente la sacca per infusione per miscelare la soluzione diluita. Non scuotere né agitare
eccessivamente la sacca per infusione.
La soluzione finale per l’infusione deve essere somministrata appena possibile dopo la preparazione.
Il medicinale non utilizzato e i rifiuti derivati da questo medicinale devono essere smaltiti in
conformità alla normativa locale vigente.
Somministrazione
L’infusione di Pombiliti deve iniziare 1 ora dopo l’assunzione delle capsule di miglustat. In caso di
ritardo dell’infusione, l’inizio non deve avvenire oltre 3 ore dopo l’assunzione di miglustat.
Il regime posologico raccomandato di Pombiliti è di 20 mg/kg di peso corporeo, somministrati una
volta ogni 2 settimane mediante infusione endovenosa.
Le infusioni devono essere somministrate in modo incrementale. Si raccomanda di avviare l’infusione
a una velocità iniziale di 1 mg/kg/ora, in seguito gradualmente aumentarla di 2 mg/kg/ora circa ogni
30 minuti, se non vi sono segni di reazioni correlate all’infusione (IAR), fino a raggiungere un
massimo di 7 mg/ kg/ora.
- Paese di registrazione
- Forma farmaceuticaPolvere per concentrato per soluzione per infusione, 105 mg
- Codice ATCA16AB23
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a POMBILITIForma farmaceutica: Concentrato per soluzione per infusione, 500 UPrincipio attivo: laronidaseProduttore: SANOFI B.V.Prescrizione richiestaForma farmaceutica: Soluzione per infusione, 150 MGPrincipio attivo: cerliponase alfaProduttore: BIOMARIN INTERNATIONAL LIMITEDPrescrizione non richiestaForma farmaceutica: Polvere per concentrato per soluzione per infusione, 200 UPrincipio attivo: imigluceraseProduttore: SANOFI B.V.Prescrizione richiesta
Medici online per POMBILITI
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di POMBILITI — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per POMBILITI online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.











