
Come usare STEQEYMA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
STEQEYMA 130 mg concentrato per soluzione per infusione
ustekinumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
Questo foglio è stato scritto per le persone che prendono questo medicinale.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Steqeyma e a cosa serve
- 2. Cosa deve sapere prima di usare Steqeyma
- 3. Come usare Steqeyma
- 4. Possibili effetti indesiderati
- 5. Come conservare Steqeyma
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Steqeyma e a cosa serve
Cos’è Steqeyma
Steqeyma contiene il principio attivo “ustekinumab”, un anticorpo monoclonale. Gli anticorpi
monoclonali sono proteine che riconoscono e legano determinate proteine specifiche presenti
nell’organismo.
Steqeyma appartiene ad un gruppo di medicinali chiamati “immunosoppressori”. Questi medicinali
riducono in parte l’attività del sistema immunitario.
A cosa serve Steqeyma
Steqeyma è usato per trattare le seguenti malattie infiammatorie:
- malattia di Crohn da moderata a grave - negli adulti;
Malattia di Crohn
La malattia di Crohn è una malattia infiammatoria dell'intestino. Se ha la malattia di Crohn, sarà
trattato prima con altri farmaci. Se non risponde sufficientemente bene o é intollerante a questi
medicinali, le potrà essere somministrato Steqeyma per ridurre i segni e i sintomi della sua malattia.
2. Cosa deve sapere prima di usare Steqeyma
Non usi Steqeyma
- Se è allergico a ustekinumabo ad uno qualsiasi degli altri componenti di questo medicinale (elencati nel successivo paragrafo 6)
- Se è affetto da un’infezione attivache il suo medico ritiene importante.
Se non è sicuro che una delle condizioni sopra riportate si riferisca a lei, ne parli con il medico o il
farmacista, prima di usare Steqeyma.
Avvertenze e precauzioni
Si rivolga al medico o al farmacista prima di usare Steqeyma. Il medico controllerà il suo stato di
salute prima di ogni trattamento. Si assicuri di informare il medico, prima di ogni trattamento, in
merito alle malattie da cui è affetto. Inoltre, informi il medico anche se è stato a contatto di recente con
persone che avrebbero potuto avere la tubercolosi. Il medico la visiterà ed effettuerà degli esami per la
tubercolosi, prima di somministrarle Steqeyma. Se il medico ritiene che è a rischio tubercolosi è
possibile che le somministri dei medicinali per curare la tubercolosi.
Attenzione agli effetti indesiderati gravi
Steqeyma può causare gravi effetti indesiderati, incluse reazioni allergiche ed infezioni. Deve prestare
attenzione a determinati segni della malattia mentre assume Steqeyma. Vedere “Effetti indesiderati
gravi” al paragrafo 4 per una lista completa di questi effetti indesiderati.
Prima di usare Steqeyma contatti il medico
- Se ha mai avuto una reazione allergica a ustekinumab. Chieda al medico se non è sicuro.
- Se ha mai avuto un qualsiasi tipo di cancro- questo perché gli immunosoppressori come Steqeyma indeboliscono in parte il sistema immunitario. Questo può aumentare il rischio di cancro.
- Se è stato trattato per la psoriasi con altri medicinali biologici (un prodotto medicinaleproveniente da una fonte biologica e solitamente somministrato mediante iniezione)- il rischio di cancro può essere più elevato.
- Se ha o ha avuto una recente infezione o se ha delle aperture anomale sulla pelle (fistole).
- Se ha mai avuto una qualsiasi lesione nuova o modificata entro l’area della psoriasi o sulla pelle normale.
- Se sta assumendo un qualsiasi altro tipo di trattamento per la psoriasi e/o artritepsoriasica- come un altro immunosoppressore o la fototerapia (quando il corpo è trattato con un tipo di luce ultravioletta (UV)). Anche questi trattamenti possono ridurre in parte l’attività del sistema immunitario. L’uso contemporaneo di queste terapie con ustekinumab non è stato studiato. Tuttavia, è possibile che possa aumentare la possibilità di patologie correlate ad un indebolimento del sistema immunitario.
- Se sta usando o ha mai usato iniezioni per il trattamento delle allergie- non è noto se ustekinumab può avere un effetto su di esse.
- Se ha un’età uguale o maggiore ai 65 anni-può avere una maggiore probabilità di contrarre infezioni.
Se non è sicuro che una delle condizioni citate in precedenza possa riguardarla, ne parli con il medico
o il farmacista prima di sottoporsi a un trattamento con Steqeyma.
Durante il trattamento con ustekinumab alcuni pazienti hanno manifestato reazioni simili al lupus,
incluso lupus cutaneo o sindrome simile al lupus (sindrome simil-lupoide). Consulti immediatamente
il medico se manifesta un’eruzione cutanea rossa, in rilievo e squamosa, talvolta con un margine più
scuro, in aree della pelle esposte al sole o in presenza di dolore articolare.
Attacco cardiaco e ictus
In uno studio su pazienti affetti da psoriasi trattati con ustekinumab sono stati osservati attacco
cardiaco e ictus. Il medico controllerà regolarmente i fattori di rischio per le malattie cardiache e
l’ictus per assicurarsi che siano trattati in modo appropriato. Si rivolga immediatamente a un medico
se sviluppa dolore toracico, debolezza o una sensazione anomala su un lato del corpo, flaccidità del
volto, o anomalie del linguaggio o della vista.
Bambini e adolescenti
Steqeyma non è raccomandato per il trattamento di bambini di età inferiore ai 18 anni con malattia di
Crohn perché non è stato studiato in questa fascia di età.
Altri medicinali, vaccini e Steqeyma
Informi il medico o il farmacista:
- se sta assumendo, ha recentemente assunto oppure potrebbe assumere qualsiasi altro medicinale
- se recentemente si è fatto vaccinare o sta per essere vaccinato. Alcuni tipi di vaccini (vaccini vivi) non devono essere somministrati mentre sta usando Steqeyma.
- se ha ricevuto Steqeyma durante la gravidanza, informi il pediatra del/la suo/a bambino/a del trattamento con Steqeyma prima che il/la suo/a bambino/a riceva qualsiasi vaccino, inclusi vaccini vivi come il vaccino BCG (usato per la prevenzione della tubercolosi). Se ha ricevuto Steqeyma durante la gravidanza, i vaccini vivi non sono raccomandati per il/la suo/a bambino/a nei primi sei mesi dopo la nascita, a meno che il pediatra del/la suo/a bambino/a non raccomandi altrimenti.
Gravidanza e allattamento
- È preferibile evitare l’uso di Steqeyma in gravidanza. Non sono noti gli effetti di ustekinumab sulle donne in gravidanza. Se è in età fertile, è consigliabile evitare di iniziare una gravidanza; deve usare un adeguato metodo contraccettivo durante l’uso di Steqeyma e per almeno 15 settimane dopo la sospensione del trattamento con Steqeyma.
- Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza chieda consiglio al medico.
- Ustekinumab può raggiungere il nascituro attraverso la placenta. Se ha ricevuto Steqeyma durante la gravidanza, il/la suo/a bambino/a potrebbe avere un rischio maggiore di contrarre un’infezione.
- Se ha ricevuto Steqeyma durante la gravidanza, è importante che ne informi il pediatra e gli altri operatori sanitari prima che il/la suo/a bambino/a riceva qualsiasi vaccino. Se ha ricevuto Steqeyma durante la gravidanza, i vaccini vivi come il vaccino BCG (usato per la prevenzione della tubercolosi) non sono raccomandati per il/la suo/a bambino/a nei primi sei mesi dopo la nascita, a meno che il pediatra non raccomandi altrimenti.
- Ustekinumab può essere escreto nel latte materno in quantità molto ridotte. Se sta allattando con latte materno o se prevede di allattare chieda consiglio al medico. Lei e il medico deciderete se deve allattare o utilizzare Steqeyma. Non può fare entrambe le cose.
Guida di veicoli e utilizzo di macchinari
Steqeyma non altera o altera in modo trascurabile la capacità di guidare veicoli o di usare macchinari.
Steqeyma contiene sodio
Steqeyma contiene meno di 1 mmol di sodio (23 mg) per dose, cioè è essenzialmente "senza sodio".
Tuttavia, prima che Steqeyma venga somministrato, viene miscelato con una soluzione che contiene
sodio. Parli con il suo medico se sta seguendo una dieta a basso contenuto di sale.
3. Come usare Steqeyma
Steqeymaa è destinato per l’uso sotto la guida e supervisione di un medico con esperienza nella
diagnosi e nel trattamento della malattia di Crohn.
Steqeyma 130 mg concentrato per soluzione per infusione le sarà somministrato dal medico, attraverso
una flebo nella vena del braccio (infusione endovenosa) per almeno un'ora. Discuta con il medico
quando dovrà sottoporsi alle iniezioni e alle successive visite di controllo.
Quanto Steqeyma viene somministrato
Sarà il medico a decidere di quanto Steqeyma ha bisogno e per quanto tempo.
Adulti a partire dai 18 anni
- Il medico calcolerà la dose di infusione endovenosa raccomandata per lei in base al suo peso corporeo.
Il suo peso corporeo Dose
≤ 55 kg 260 mg
> 55 kg a ≤ 85 kg 390 mg
> 85 kg 520 mg
- Dopo la dose endovenosa iniziale assumerà la dose successiva di 90 mg Steqeyma con un’iniezione sotto la pelle (iniezione sottocutanea) 8 settimane dopo, e poi ogni 12 settimane.
Come viene somministrato Steqeyma
- La prima dose di Steqeyma per il trattamento della malattia di Crohn è somministrata dal medico mediante una flebo in vena fatta nel suo braccio (infusione endovenosa). Informi il medico nel caso in cui abbia eventuali domande sull’utilizzo di Steqeyma.
Se dimentica di usare Steqeyma
Se dimentica o manca l’appuntamento per la somministrazione della dose, contatti il medico per
fissare un nuovo appuntamento.
Se interrompe il trattamento con Steqeyma
Non è pericoloso interrompere l’impiego di Steqeyma. Tuttavia, se interrompe il trattamento i sintomi
possono ripresentarsi.
Nel caso in cui abbia ulteriori domande sull’uso di questo medicinale, chieda al medico o al
farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Effetti indesiderati gravi
Alcuni pazienti possono presentare gravi effetti indesiderati che possono necessitare di un trattamento
urgente.
Reazioni allergiche – queste possono necessitare di un trattamento urgente, quindi contatti
il medico o richieda assistenza medica di urgenza se nota uno dei seguenti segni.
- Reazioni allergiche gravi (“anafilassi”) sono rare in pazienti che assumono ustekinumab (interessano fino a 1 paziente su 1 000). I segni includono: o difficoltà a respirare o a deglutire o bassa pressione sanguigna, che può causare capogiri o sensazione di testa leggera o gonfiore della faccia, delle labbra, della bocca o della gola.
- I segni comuni di una reazione allergica includono eruzione cutanea ed orticaria (interessano fino a 1 paziente su 100).
Reazioni correlate all’infusione – Se è in trattamento per la malattia di Crohn, la prima
dose di Steqeyma viene somministrata attraverso una flebo (infusione endovenosa). Alcuni
pazienti hanno manifestato reazioni allergiche gravi durante l’infusione.
In rari casi sono state riportate reazioni polmonari allergiche e infiammazione polmonare
in pazienti che ricevono ustekinumab. Informi immediatamente il medico se sviluppa
sintomi come tosse, mancanza di respiro e febbre.
Se presenta una reazione allergica grave, il medico può decidere che lei non deve usare
Steqeyma di nuovo.
Infezioni – queste possono necessitare di un trattamento urgente, quindi contatti subito il
medico se nota uno dei seguenti segni.
- Le infezioni del naso e della gola e il raffreddore comune sono comuni (interessano fino a 1 paziente su 10).
- Le infezioni del torace sono non comuni (possono interessare fino a 1 paziente su 100)
- L’infiammazione del tessuto sottocutaneo (‘cellulite’) è non comune (interessa fino a 1 paziente su 100).
- Herpes zoster (un tipo di eruzione cutanea dolorosa con vesciche) è non comune (interessa fino a 1 paziente su 100).
Steqeyma può diminuire la capacità di combattere le infezioni. Alcune infezioni possono
diventare gravi e possono includere infezioni provocate da virus, funghi, batteri (incluso quello
della tubercolosi) o parassiti, comprese infezioni che si verificano principalmente nelle persone
con sistema immunitario indebolito (infezioni opportunistiche). In pazienti trattati con
ustekinumab sono state segnalate infezioni opportunistiche del cervello (encefalite, meningite),
dei polmoni e degli occhi.
Deve prestare attenzione ai segni di infezione mentre sta usando Steqeyma. Questi includono:
- febbre, sintomi simil influenzali, sudorazione notturna, perdita di peso
- sensazione di stanchezza o di fiato corto, tosse persistente
- caldo, pelle arrossata e dolente, o una eruzione cutanea dolorosa e con vesciche
- bruciore quando urina
- diarrea
- disturbo visivo o perdita della vista
- cefalea, rigidità del collo, sensibilità alla luce, nausea o confusione
Informi immediatamente il medico se nota uno qualsiasi di questi segni di infezione. Questi
possono essere segni di infezione come infezioni del torace, infezioni della cute, herpes zoster o
infezioni opportunistiche che possono avere complicanze gravi. Si rivolga al medico se ha un
qualsiasi tipo di infezione che persiste o continua a ripresentarsi. Il medico può decidere di
interrompere Steqeyma fino a quando l’infezione non si risolve. Inoltre informi il medico se ha
eventuali tagli o ferite aperte che possono infettarsi.
Desquamazione cutanea – aumento del rossore e desquamazione della cute su un’ampia
superficie del corpo possono essere sintomi di psoriasi eritrodermica o dermatite
esfoliativa, le quali sono gravi condizioni della pelle. Se nota uno di questi segni deve
informare immediatamente il suo medico.
Altri effetti indesiderati
Effetti indesiderati comuni(interessano fino a 1 paziente su 10)
- Diarrea
- Nausea
- Vomito
- Sensazione di stanchezza
- Sensazione di capogiro
- Mal di testa
- Prurito
- Dolore alla schiena, muscolare o articolare
- Mal di gola
- Arrossamento e dolore nel sito dell’iniezione
- Sinusite
Effetti indesiderati non comuni(interessano fino a 1 paziente su 100)
- Infezione dentali
- Infezione micotica vaginale
- Depressione
- Naso chiuso o che cola
- Sanguinamento, lividi, rigidità, gonfiore e prurito nel punto in cui viene eseguita l’iniezione
- Sentirsi debole
- Palpebra cadente e rilassamento muscolare ad un lato del viso (“paralisi facciale” o “paralisi di Bell”), che solitamente è temporanea
- Un cambiamento della psoriasi con rossore e nuove bolle cutanee piccole, gialle o bianche, talvolta accompagnate da febbre (psoriasi pustolosa)
- Desquamazione della pelle (esfoliazione della pelle)
- Acne
Effetti indesiderati rari(interessano fino a 1 paziente su 1 000)
- Rossore e desquamazione della cute su un’ampia superficie del corpo, che possono essere pruriginosi o dolorosi (dermatite esfoliativa). Sintomi simili alcune volte si sviluppano come una naturale evoluzione nella tipologia dei sintomi della psoriasi (psoriasi eritrodermica)
- Infiammazione dei piccoli vasi sanguigni, che può portare a un’eruzione cutanea con piccoli bozzi rossi o viola, febbre o dolore articolare (vasculite)
Effetti indesiderati molto rari (interessano fino a 1 paziente su 10 000)
- Formazione di vesciche cutanee con possibile arrossamento, prurito e dolore (pemfigoide bolloso).
- Lupus cutaneo o sindrome simile al lupus (eruzione cutanea rossa, in rilievo e squamosa su aree della pelle esposte al sole, talvolta in presenza di dolore articolare).
Segnalazione degli effetti indesiderati
Se si manifesta un qualsiasi effetti indesiderato, compresi quelli non elencati in questo foglio, si
rivolga al medico o al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione riportato nell’ Allegato V . Segnalando gli effetti indesiderati lei può
contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Steqeyma
- Steqeyma 130 mg concentrato per soluzione per infusione viene somministrato in ospedale o in clinica e i pazienti non hanno bisogno di maneggiarlo o conservarlo.
- Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
- Conservare in frigorifero (2 °C - 8 °C). Non congelare.
- Tenere il flaconcino nell’imballaggio esterno, per proteggere il medicinale dalla luce.
- Se necessario, i singoli flaconcini di Steqeyma possono anche essere conservati a temperatura ambiente fino a 30 °C, per un unico periodo di massimo 31 giorni, nell'imballaggio esterno al fine di proteggerli dalla luce. Registrare la data in cui il flaconcino viene rimosso per la prima volta dal frigorifero e la data in cui va eliminato nello spazio previsto sulla confezione esterna. La data in cui va eliminato non deve superare la data di scadenza originale stampata sulla confezione. Una volta che un flaconcino è stato conservato a temperatura ambiente (fino a 30 °C), non deve essere rimesso in frigorifero. Gettare il flaconcino se non utilizzato entro 31 giorni a temperatura ambiente o entro la data di scadenza originale, a seconda di quale è precedente.
- Non agitare i flaconcini di Steqeyma. Lo scuotimento energico prolungato può danneggiare il medicinale.
Non usi questo medicinale
- Dopo la data di scadenza che è riportata sull’etichetta e sull’astuccio dopo EXP o “Scad.”. La data
di scadenza si riferisce all’ultimo giorno del mese.
- Se il liquido presenta un colore alterato, è opaco o se si vedono particelle estranee che galleggiano (vedere il paragrafo 6 “Descrizione dell’aspetto di Steqeyma e contenuto della confezione”).
- Se sa o crede che il medicinale sia stato esposto a temperature estreme (ad esempio accidentalmente congelato o riscaldato).
- Se il prodotto è stato agitato energicamente.
- Se il sigillo è rotto.
Steqeyma è monouso. La soluzione diluita per infusione inutilizzata che resta nel flaconcino e nella
siringa deve essere eliminata in conformità alla normativa locale vigente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Steqeyma
- Il principio attivo è ustekinumab. Ogni flaconcino contiene 130 mg di ustekinumab in 26 mL.
- Gli eccipienti sono: EDTA sale disodico diidrato, L-istidina, L-istidina monoidrocloridrato monoidrato, L-metionina, polisorbato 80, saccarosio, acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Steqeyma e contenuto della confezione
Steqeyma è un concentrato per soluzione per infusione da limpido a leggermente opalescente, da
incolore a giallo pallido. È fornito in una confezione di cartone contenente 1 dose unica, in flaconcino
di vetro da 30 mL. Ogni flaconcino contiene 130 mg di ustekinumab in 26 mL di concentrato per
soluzione per infusione.
Titolare dell’autorizzazione all’immissione in commercio
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungheria
Produttore
Nuvisan France SARL
2400, Route des Colles
06410, Biot
Francia
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Celltrion Healthcare Belgium BVBA
Tél/Tel: + 32 1528 7418
[email protected]
Lietuva
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
България
Celltrion Healthcare Hungary Kft.
Teл.: + 36 1 231 0493
Luxembourg/Luxemburg
Celltrion Healthcare Belgium BVBA
Tél/Tel: + 32 1528 7418
[email protected]
Česká republika
Celltrion Healthcare Hungary Kft.
Tel: + 36 1 231 0493
Magyarország
Celltrion Healthcare Hungary Kft.
Tel.: + 36 1 231 0493
Danmark
Celltrion Healthcare Denmark ApS
Tlf.: +45 3535 2989
[email protected]
Malta
Mint Health Ltd
Tel: +356 2093 9800
Deutschland
Celltrion Healthcare Deutschland GmbH
Tel: +49 (0)30 346494150
[email protected]
Nederland
Celltrion Healthcare Netherlands B.V.
Tel: + 31 20 888 7300
[email protected]
Eesti
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
[email protected]
Norge
Celltrion Healthcare Norway AS
[email protected]
España
CELLTRION FARMACEUTICA (ESPAÑA)
S.L.
Tel: +34 919 94 23 90
[email protected]
Österreich
Astro-Pharma GmbH
Tel: +43 1 97 99 860
Ελλάδα
ΒΙΑΝΕΞ Α.Ε.
Τηλ: +30 210 8009111
Polska
Celltrion Healthcare Hungary Kft.
Tel.: + 36 1 231 0493
France
Celltrion Healthcare France SAS
Tél.: +33 (0)1 71 25 27 00
Portugal
CELLTRION PORTUGAL, UNIPESSOAL
LDA
Tel: +351 21 936 8542
[email protected]
Hrvatska
Oktal Pharma d.o.o.
Tel: +385 1 6595 777
România
Celltrion Healthcare Hungary Kft.
Tel: + 36 1 231 0493
Ireland
Celltrion Healthcare Ireland Limited
Tel: +353 1 223 4026
[email protected]
Slovenija
OPH Oktal Pharma d.o.o.
Tel.: +386 1 519 29 22
Ísland
Celltrion Healthcare Hungary Kft.
Sími: +36 1 231 0493
[email protected]
Slovenská republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Suomi/Finland
Celltrion Healthcare Finland Oy.
Puh/Tel: +358 29 170 7755
[email protected]
Κύπρος
C.A. Papaellinas Ltd
Τηλ: +357 22741741
Italia
Celltrion Healthcare Italy S.R.L.
Tel: +39 0247927040
[email protected]
Sverige
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
[email protected]
Latvija
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
per i medicinali: https://www.ema.europa.eu .
Le seguenti informazioni sono destinate esclusivamente agli operatori sanitari.
Tracciabilità
Al fine di migliorare la tracciabilità dei medicinali biologici, il nome e il numero di lotto del
medicinale somministrato devono essere chiaramente registrati.
Istruzioni per la diluizione.
Steqeyma concentrato per soluzione per infusione deve essere diluito, preparato e infuso da un
operatore sanitario con tecnica asettica.
- 1. Calcolare la dose e il numero di flaconcini di Steqeyma necessari in base al peso del paziente (vedi paragrafo 3, Tabella 1). Ogni flaconcino da 26 mL di Steqeyma contiene 130 mg di ustekinumab.
- 2. Estrarre ed eliminare un volume di soluzione di cloruro di sodio 9 mg/mL (0,9%) dalla sacca di infusione da 250 mL pari al volume di Steqeyma da aggiungere (eliminare 26 mL di cloruro di sodio per ogni flaconcino di Steqeyma necessario, per 2 flaconcini eliminare 52 mL, per 3 flaconcini eliminare 78 mL, per 4 flaconcini eliminare 104 mL).
- 3. Prelevare 26 mL di Steqeyma da ogni flaconcino necessario e aggiungerlo alla sacca di infusione da 250 mL. Il volume finale nella sacca di infusione deve essere di 250 mL. Mescolare delicatamente.
- 4. Controllare visivamente la soluzione diluita prima dell'infusione. Non utilizzare se si osservano visibili particelle opache, scolorimento o particelle estranee.
- 5. Infondere la soluzione diluita per un periodo di almeno un'ora. Una volta diluita, l’infusione deve essere completata entro quarantotto ore dalla diluizione nella sacca da infusione.
- 6. Utilizzare un solo set per infusione con filtro in linea sterile, non pirogenico, a basso legame con le proteine (dimensione dei pori 0,2 micrometri).
- 7. Ogni flaconcino è monouso e il medicinale non utilizzato deve essere smaltito in conformità alla normativa locale vigente.
Conservazione
Se necessario, la soluzione per infusione diluita può essere conservata a temperatura ambiente fino a
30 °C. L’infusione deve essere completata entro 48 ore dalla diluizione nella sacca da infusione. Non
congelare.
STEQEYMA 45 mg soluzione iniettabile in siringa preriempita
ustekinumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
Questo foglio è stato scritto per le persone che prendono questo medicinale. Se lei è il genitore o
la persona che si prende cura di un bambino a cui deve essere somministrato Steqeyma, legga
attentamente queste informazioni prima della somministrazione.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Steqeyma e a cosa serve
- 2. Cosa deve sapere prima di usare Steqeyma
- 3. Come usare Steqeyma
- 4. Possibili effetti indesiderati
- 5. Come conservare Steqeyma
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Steqeyma e a cosa serve
Cos’è Steqeyma
Steqeyma contiene il principio attivo “ustekinumab”, un anticorpo monoclonale. Gli anticorpi
monoclonali sono proteine che riconoscono e legano determinate proteine specifiche presenti
nell’organismo.
Steqeyma appartiene ad un gruppo di medicinali chiamati “immunosoppressori”. Questi medicinali
riducono in parte l’attività del sistema immunitario.
A cosa serve Steqeyma
Steqeyma è usato per trattare le seguenti malattie infiammatorie:
- psoriasi a placche - negli adulti e nei bambini a partire dai 6 anni
- artrite psoriasica - negli adulti
- malattia di Crohn da moderata a grave - negli adulti
Psoriasi a placche
La psoriasi a placche è una condizione della pelle che causa infiammazione della pelle e delle unghie.
Steqeyma ridurrà l’infiammazione e altri segni della malattia.
Steqeyma è usato negli adulti con psoriasi a placche da moderata a grave, che non possono usare
ciclosporina, metotrexato o la fototerapia, o nei quali questi trattamenti non funzionano.
Steqeyma è usato nei bambini e negli adolescenti a partire dai 6 anni con psoriasi a placche da
moderata a grave, che non possono tollerare la fototerapia o altre terapie sistemiche o quando questi
trattamenti non hanno funzionato.
Artrite psoriasica
L’artrite psoriasica è una malattia infiammatoria delle articolazioni, di solito accompagnata dalla
psoriasi. Se ha una artrite psoriasica attiva lei sarà prima trattato con altri medicinali. Se non dovesse
rispondere in maniera adeguata a questi medicinali, potrà prendere Steqeyma per:
- ridurre i segni ed i sintomi della malattia.
- migliorare la funzionalità fisica.
- rallentare il danno alle articolazioni.
Malattia di Crohn
La malattia di Crohn è una malattia infiammatoria dell'intestino. Se ha la malattia di Crohn sarà
trattato prima con altri farmaci. Se non risponde sufficientemente bene o è intollerante a questi
medicinali, le potrà essere somministrato Steqeyma per ridurre i segni e i sintomi della sua malattia.
2. Cosa deve sapere prima di usare Steqeyma
Non usi Steqeyma
- Se è allergico a ustekinumabo ad uno qualsiasi degli altri componenti di questo medicinale (elencati nel successivo paragrafo 6).
- Se è affetto da un’infezione attivache il suo medico ritiene importante.
Se non è sicuro che una delle condizioni sopra riportate si riferisca a lei, ne parli con il medico o il
farmacista, prima di usare Steqeyma.
Avvertenze e precauzioni
Si rivolga al medico o al farmacista prima di usare Steqeyma. Il medico controllerà il suo stato di
salute prima di ogni trattamento. Si assicuri di informare il medico, prima di ogni trattamento, in
merito alle malattie da cui è affetto. Inoltre, informi il medico anche se è stato a contatto di recente con
persone che avrebbero potuto avere la tubercolosi. Il medico la visiterà ed effettuerà degli esami per la
tubercolosi, prima di somministrarle Steqeyma. Se il medico ritiene che è a rischio tubercolosi è
possibile che le somministri dei medicinali per curare la tubercolosi.
Attenzione agli effetti indesiderati gravi
Steqeyma può causare gravi effetti indesiderati, incluse reazioni allergiche ed infezioni. Deve prestare
attenzione a determinati segni della malattia mentre assume Steqeyma. Vedere “Effetti indesiderati
gravi” al paragrafo 4 per una lista completa di questi effetti indesiderati.
Prima di usare Steqeyma contatti il medico
- Se ha mai avuto una reazione allergica a ustekinumab. Chieda al medico se non è sicuro.
- Se ha mai avuto un qualsiasi tipo di cancro- questo perché gli immunosoppressori come Steqeyma indeboliscono in parte il sistema immunitario. Questo può aumentare il rischio di cancro.
- Se è stato trattato per la psoriasi con altri medicinali biologici (un prodotto medicinaleproveniente da una fonte biologica e solitamente somministrato mediante iniezione)- il rischio di cancro può essere più elevato.
- Se ha o ha avuto una recente infezione.
- Se ha mai avuto una qualsiasi lesione nuova o modificataentro l’area della psoriasi o sulla pelle normale.
- Se sta assumendo un qualsiasi altro tipo di trattamento per la psoriasi e/o artritepsoriasica- come un altro immunosoppressore o la fototerapia (quando il corpo è trattato con un tipo di luce ultravioletta (UV)). Anche questi trattamenti possono ridurre in parte l’attività del sistema immunitario. L’uso contemporaneo di queste terapie con ustekinumab non è stato studiato. Tuttavia è possibile che possa aumentare la possibilità di patologie correlate ad un
indebolimento del sistema immunitario.
- Se sta usando o ha mai usato iniezioni per il trattamento delle allergie- non è noto se ustekinumab può avere un effetto su di esse.
- Se ha un’età uguale o maggiore ai 65 anni- può avere una maggiore probabilità di contrarre infezioni.
Se non è sicuro che una delle condizioni citate in precedenza possa riguardarla, ne parli con il medico
o il farmacista prima di sottoporsi a un trattamento con Steqeyma.
Durante il trattamento con ustekinumab alcuni pazienti hanno manifestato reazioni simili al lupus,
incluso lupus cutaneo o sindrome simile al lupus (sindrome simil-lupoide). Consulti immediatamente
il medico se manifesta un’eruzione cutanea rossa, in rilievo e squamosa, talvolta con un margine più
scuro, in aree della pelle esposte al sole o in presenza di dolore articolare.
Attacco cardiaco e ictus
In uno studio su pazienti affetti da psoriasi trattati con ustekinumab sono stati osservati attacco
cardiaco e ictus. Il medico controllerà regolarmente i fattori di rischio per le malattie cardiache e
l’ictus per assicurarsi che siano trattati in modo appropriato. Si rivolga immediatamente a un medico
se sviluppa dolore toracico, debolezza o una sensazione anomala su un lato del corpo, flaccidità del
volto, o anomalie del linguaggio o della vista.
Bambini e adolescenti
Steqeyma non è raccomandato per il trattamento di bambini con psoriasi di età inferiore ai 6 anni, o
per il trattamento di bambini di età inferiore ai 18 anni con artrite psoriasica o malattia di Crohn
perché non è stato studiato in questa fascia di età.
Altri medicinali, vaccini e Steqeyma
Informi il medico o il farmacista:
- se sta assumendo, ha recentemente assunto oppure potrebbe assumere qualsiasi altro medicinale
- se recentemente si è fatto vaccinare o sta per essere vaccinato. Alcuni tipi di vaccini (vaccini vivi) non devono essere somministrati mentre sta usando Steqeyma.
- se ha ricevuto Steqeyma durante la gravidanza, informi il pediatra del/la suo/a bambino/a del trattamento con Steqeyma prima che il/la suo/a bambino/a riceva qualsiasi vaccino, inclusi vaccini vivi come il vaccino BCG (usato per la prevenzione della tubercolosi). Se ha ricevuto Steqeyma durante la gravidanza, i vaccini vivi non sono raccomandati per il/la suo/a bambino/a nei primi sei mesi dopo la nascita, a meno che il pediatra del/la suo/a bambino/a non raccomandi altrimenti.
Gravidanza e allattamento
- È preferibile evitare l’uso di Steqeyma in gravidanza. Non sono noti gli effetti di ustekinumab sulle donne in gravidanza. Se è in età fertile, è consigliabile evitare di iniziare una gravidanza; deve usare un adeguato metodo contraccettivo durante l’uso di Steqeyma e per almeno 15 settimane dopo la sospensione del trattamento con Steqeyma. Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza chieda consiglio al medico.
- Ustekinumab può raggiungere il nascituro attraverso la placenta. Se ha ricevuto Steqeyma durante la gravidanza, il/la suo/a bambino/a potrebbe avere un rischio maggiore di contrarre un’infezione.
- Se ha ricevuto Steqeyma durante la gravidanza, è importante che ne informi il pediatra e gli altri operatori sanitari prima che il/la suo/a bambino/a riceva qualsiasi vaccino. Se ha ricevuto Steqeyma durante la gravidanza, i vaccini vivi come il vaccino BCG (usato per la prevenzione della tubercolosi) non sono raccomandati per il/la suo/a bambino/a nei primi sei mesi dopo la nascita, a meno che il pediatra non raccomandi altrimenti.
- Ustekinumab può essere escreto nel latte materno in quantità molto ridotte. Se sta allattando con latte materno o se prevede di allattare chieda consiglio al medico. Lei e il medico deciderete se deve allattare o utilizzare Steqeyma. Non può fare entrambe le cose.
Guida di veicoli e utilizzo di macchinari
Steqeyma non altera o altera in modo trascurabile la capacità di guidare veicoli o di usare macchinari.
3. Come usare Steqeyma
Steqeyma è destinato per l’uso sotto la guida e supervisione di un medico con esperienza nel
trattamento delle condizioni per cui è indicato Steqeyma.
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico. Se ha dubbi, consulti il
medico. Discuta con il medico quando dovrà sottoporsi alle iniezioni e alle successive visite di
controllo.
Quanto Steqeyma viene somministrato
Sarà il medico a decidere di quanto Steqeyma ha bisogno e per quanto tempo.
Adulti a partire dai 18 anni
Psoriasi e artrite psoriasica
- La dose iniziale raccomandata è 45 mg di Steqeyma. I pazienti con un peso maggiore di 100 chilogrammi (kg) possono iniziare con una dose di 90 mg invece di 45 mg.
- Dopo la dose iniziale assumerà la dose successiva 4 settimane dopo, e poi ogni 12 settimane. Le dosi successive sono solitamente le stesse della dose iniziale.
Malattia di Crohn
- Durante il trattamento, la prima dose di circa 6 mg/kg di Steqeyma le è somministrata dal medico mediante una flebo in vena fatta nel suo braccio (infusione endovenosa). Dopo la dose iniziale, riceverà la dose successiva di 90 mg di Steqeyma dopo 8 settimane, poi ogni 12 settimane con un’iniezione sotto la pelle (via sottocutanea).
- In alcuni pazienti, dopo la prima iniezione sottocute, la dose di 90 mg di Steqeyma può essere somministrata ogni 8 settimane. Il medico deciderà quando si dovrà ricevere la dose successiva.
Bambini e adolescenti a partire dai 6 anni
Psoriasi
Non esiste una formulazione di Steqeyma per i bambini con psoriasi a placche con peso inferiore a
60 kg; pertanto, devono essere utilizzati altri prodotti contenenti ustekinumab.
- Il medico calcolerà la dose giusta, incluso la quantità (volume) di Steqeyma che deve essere iniettata per garantire la somministrazione della dose corretta. La dose corretta dipenderà dal peso corporeo del bambino al momento della somministrazione di ogni dose.
- Se il peso corporeo è inferiore ai 60 kg, non è disponibile una formulazione di Steqeyma e devono essere utilizzati altri prodotti contenenti ustekinumab.
- Se il peso corporeo è compreso tra 60 kg e 100 kg, la dose raccomandata è di 45 mg di Steqeyma.
- Se il peso supera i 100 kg, la dose raccomandata è di 90 mg di Steqeyma.
- Dopo la dose iniziale, dovrà ricevere la dose successiva dopo 4 settimane, e successivamente ogni 12 settimane.
Come viene somministrato Steqeyma
- Steqeyma è somministrato mediante un’iniezione sottocute (“per via sottocutanea”). All’inizio del trattamento, il personale medico o infermieristico può iniettarle Steqeyma.
- Tuttavia, lei e il medico potete decidere se può iniettarsi Steqeyma da solo. In questo caso, le verrà insegnato come iniettarsi Steqeyma da solo.
- Per le istruzioni su come iniettare Steqeyma, vedere “Istruzioni per la somministrazione” alla
Informi il medico nel caso in cui abbia eventuali domande sull’iniezione da praticare da solo.
Se usa più Steqeyma di quanto deve
Se ha usato o ha ricevuto troppo Steqeyma, informi immediatamente il medico o il farmacista. Porti
sempre la confezione esterna del medicinale con sé, anche se è vuota.
Se dimentica di usare Steqeyma
Se dimentica una dose, contatti il medico o il farmacista. Non prenda una dose doppia per compensare
la dimenticanza della dose.
Se interrompe il trattamento con Steqeyma
Non è pericoloso interrompere l’impiego di Steqeyma. Tuttavia, se interrompe il trattamento i sintomi
possono ripresentarsi.
Nel caso in cui abbia ulteriori domande sull’uso di questo medicinale, chieda al medico o al
farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Effetti indesiderati gravi
Alcuni pazienti possono presentare gravi effetti indesiderati che possono necessitare di un trattamento
urgente.
Reazioni allergiche – queste possono necessitare di un trattamento urgente, quindi contatti
il medico o richieda assistenza medica di urgenza se nota uno dei seguenti segni.
- Reazioni allergiche gravi (“anafilassi”) sono rare in pazienti che assumono ustekinumab (interessano fino a 1 paziente su 1 000). I segni includono: o difficoltà a respirare o a deglutire o bassa pressione sanguigna, che può causare capogiri o sensazione di testa leggera o gonfiore della faccia, delle labbra, della bocca o della gola.
- I segni comuni di una reazione allergica includono eruzione cutanea ed orticaria (interessano fino a 1 paziente su 100).
In rari casi sono state riportate reazioni polmonari allergiche e infiammazione polmonare
in pazienti che ricevono ustekinumab. Informi immediatamente il medico se sviluppa
sintomi come tosse, mancanza di respiro e febbre.
Se presenta una reazione allergica grave, il medico può decidere che lei non deve usare
Steqeyma di nuovo.
Infezioni – queste possono necessitare di un trattamento urgente, quindi contatti subito il
medico se nota uno dei seguenti segni.
- Le infezioni del naso e della gola e il raffreddore comune sono comuni (interessano fino a 1 paziente su 10).
- Le infezioni del torace sono non comuni (possono interessare fino ad 1 paziente su 100)
- L’infiammazione del tessuto sottocutaneo (‘cellulite’) è non comune (interessa fino a 1 paziente su 100).
- Herpes zoster (un tipo di eruzione cutanea dolorosa con vesciche) è non comune (interessa fino a 1 paziente su 100).
Steqeyma può diminuire la capacità di combattere le infezioni. Alcune infezioni possono diventare
gravi e possono includere infezioni provocate da virus, funghi, batteri (inclusi quelli della tubercolosi)
o parassiti, comprese infezioni che si verificano principalmente nelle persone con sistema immunitario
indebolito (infezioni opportunistiche). In pazienti trattati con ustekinumab sono state segnalate
infezioni opportunistiche del cervello (encefalite, meningite), dei polmoni e degli occhi.
Deve prestare attenzione ai segni di infezione mentre sta usando Steqeyma. Questi includono:
- febbre, sintomi simil influenzali, sudorazione notturna, perdita di peso
- sensazione di stanchezza o di fiato corto, tosse persistente
- caldo, pelle arrossata e dolente, o una eruzione cutanea dolorosa e con vesciche
- bruciore quando urina
- diarrea
- disturbo visivo o perdita della vista
- cefalea, rigidità del collo, sensibilità alla luce, nausea o confusione
Informi immediatamente il medico se nota uno qualsiasi di questi segni di infezione. Questi possono
essere segni di infezioni come infezioni del torace, infezioni della cute, herpes zoster o infezioni
opportunistiche che possono avere complicanze gravi. Si rivolga al medico se ha un qualsiasi tipo di
infezione che persiste o continua a ripresentarsi. Il medico può decidere di interrompere Steqeyma
fino a quando l’infezione non si risolve. Inoltre informi il medico se ha eventuali tagli o ferite aperte
che possono infettarsi.
Desquamazione cutanea – aumento del rossore e desquamazione della cute su un’ampia
superficie del corpo possono essere sintomi di psoriasi eritrodermica o dermatite
esfoliativa, le quali sono gravi condizioni della pelle. Se nota uno di questi segni deve
informare immediatamente il suo medico.
Altri effetti indesiderati
Effetti indesiderati comuni(interessano fino a 1 paziente su 10)
- Diarrea
- Nausea
- Vomito
- Sensazione di stanchezza
- Sensazione di capogiro
- Mal di testa
- Prurito
- Dolore alla schiena, muscolare o articolare
- Mal di gola
- Arrossamento e dolore nel sito dell’iniezione
- Sinusite
Effetti indesiderati non comuni(interessano fino a 1 paziente su 100)
- Infezione dentali
- Infezione micotica vaginale
- Depressione
- Naso chiuso o che cola
- Sanguinamento, lividi, rigidità, gonfiore e prurito nel punto in cui viene eseguita l’iniezione
- Sentirsi debole
- Palpebra cadente e rilassamento muscolare ad un lato del viso (“paralisi facciale” o “paralisi di Bell”), che solitamente è temporanea
- Un cambiamento della psoriasi con rossore e nuove bolle cutanee piccole, gialle o bianche, talvolta accompagnate da febbre (psoriasi pustolosa)
- Desquamazione della pelle (esfoliazione della pelle)
- Acne
Effetti indesiderati rari(interessano fino a 1 paziente su 1 000)
- Rossore e desquamazione della cute su un’ampia superficie del corpo, che possono essere pruriginosi o dolorosi (dermatite esfoliativa). Sintomi simili alcune volte si sviluppano
come una naturale evoluzione nella tipologia dei sintomi della psoriasi (psoriasi
eritrodermica)
- Infiammazione dei piccoli vasi sanguigni, che può portare a un’eruzione cutanea con piccoli bozzi rossi o viola, febbre o dolore articolare (vasculite)
Effetti indesiderati molto rari(interessano fino a 1 paziente su 10 000)
- Formazione di vesciche cutanee con possibile arrossamento, prurito e dolore (pemfigoide bolloso).
- Lupus cutaneo o sindrome simile al lupus (eruzione cutanea rossa, in rilievo e squamosa su aree della pelle esposte al sole, talvolta in presenza di dolore articolare).
Segnalazione degli effetti indesiderati
Se si manifesta un qualsiasi effetti indesiderato, compresi quelli non elencati in questo foglio, si
rivolga al medico o al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione riportato nell’allegato V. Segnalando gli effetti indesiderati lei può
contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Steqeyma
- Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
- Conservare in frigorifero (2 °C - 8 °C). Non congelare.
- Tenere la siringa preriempita nell’imballaggio esterno, per proteggere il medicinale dalla luce.
- Se necessario, le singole siringhe preriempite di Steqeyma possono anche essere conservate a temperatura ambiente fino a 30 °C, per un unico periodo di massimo 31 giorni, nell'imballaggio esterno al fine di proteggerle dalla luce. Registrare la data in cui la siringa preriempita viene rimossa per la prima volta dal frigorifero e la data in cui va eliminata nello spazio previsto sulla confezione esterna. La data in cui va eliminata non deve superare la data di scadenza originale stampata sulla confezione. Una volta che una siringa è stata conservata a temperatura ambiente (fino a 30 °C), non deve essere rimessa in frigorifero. Gettare la siringa se non utilizzata entro 31 giorni a temperatura ambiente o entro la data di scadenza originale, a seconda di quale è precedente.
- Non agitare le siringhe preriempite di Steqeyma. Lo scuotimento energico prolungato può danneggiare il medicinale.
Non usi questo medicinale
- Dopo la data di scadenza che è riportata sull’etichetta e sull’astuccio dopo EXP o Scad. La data di scadenza si riferisce all’ultimo giorno del mese.
- Se il liquido presenta un colore alterato, è opaco o se si vedono particelle estranee che galleggiano (vedere il paragrafo 6 “Descrizione dell’aspetto di Steqeyma e contenuto della confezione”).
- Se sa o crede che il medicinale sia stato esposto a temperature estreme (ad esempio accidentalmente congelato o riscaldato).
- Se il prodotto è stato agitato energicamente. Steqeyma è monouso. Il prodotto inutilizzato che resta nella siringa deve essere eliminato.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Steqeyma
- Il principio attivo è ustekinumab. Ogni siringa preriempita contiene 45 mg di ustekinumab in 0,5 mL.
- Gli eccipienti sono: L-istidina, L-istidina monoidrocloridrato monoidrato, polisorbato 80, saccarosio, acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Steqeyma e contenuto della confezione
Steqeyma è una soluzione per iniezione da limpida a leggermente opalescente (aspetto simile a quello
della perla), da incolore a giallo pallido. La soluzione può contenere qualche piccola particella
traslucida o bianca di proteine. È fornito in una confezione di cartone contenente 1 dose unica, in
siringa preriempita di vetro da 1 mL. Ogni siringa preriempita contiene una dose di ustekinumab
45 mg in 0,5 mL di soluzione per iniezione.
Titolare dell’autorizzazione all’immissione in commercio
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungheria
Produttore
Nuvisan France SARL
2400, Route des Colles
06410, Biot
Francia
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Celltrion Healthcare Belgium BVBA
Tél/Tel: + 32 1528 7418
[email protected]
Lietuva
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
България
Celltrion Healthcare Hungary Kft.
Teл.: + 36 1 231 0493
Luxembourg/Luxemburg
Celltrion Healthcare Belgium BVBA
Tél/Tel: + 32 1528 7418
[email protected]
Česká republika
Celltrion Healthcare Hungary Kft.
Tel: + 36 1 231 0493
Magyarország
Celltrion Healthcare Hungary Kft.
Tel.: + 36 1 231 0493
Danmark
Celltrion Healthcare Denmark ApS
Tlf.: +45 3535 2989
[email protected]
Malta
Mint Health Ltd
Tel: +356 2093 9800
Deutschland
Celltrion Healthcare Deutschland GmbH
Tel: +49 (0)30 346494150
[email protected]
Nederland
Celltrion Healthcare Netherlands B.V.
Tel: + 31 20 888 7300
[email protected]
Eesti
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
[email protected]
Norge
Celltrion Healthcare Norway AS
[email protected]
España
CELLTRION FARMACEUTICA (ESPAÑA)
S.L.
Tel: +34 919 94 23 90
[email protected]
Österreich
Astro-Pharma GmbH
Tel: +43 1 97 99 860
Ελλάδα
ΒΙΑΝΕΞ Α.Ε.
Τηλ: +30 210 8009111
Polska
Celltrion Healthcare Hungary Kft.
Tel.: + 36 1 231 0493
France
Celltrion Healthcare France SAS
Tél.: +33 (0)1 71 25 27 00
Portugal
CELLTRION PORTUGAL, UNIPESSOAL
LDA
Tel: +351 21 936 8542
[email protected]
Hrvatska
Oktal Pharma d.o.o.
Tel: +385 1 6595 777
România
Celltrion Healthcare Hungary Kft.
Tel: + 36 1 231 0493
Ireland
Celltrion Healthcare Ireland Limited
Tel: +353 1 223 4026
[email protected]
Slovenija
OPH Oktal Pharma d.o.o.
Tel.: +386 1 519 29 22
Ísland
Celltrion Healthcare Hungary Kft.
Sími: +36 1 231 0493
[email protected]
Slovenská republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Italia
Celltrion Healthcare Italy S.R.L.
Tel: +39 0247927040
[email protected]
Suomi/Finland
Celltrion Healthcare Finland Oy.
Puh/Tel: +358 29 170 7755
[email protected]
Κύπρος
C.A. Papaellinas Ltd
Τηλ: +357 22741741
Sverige
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
[email protected]
Latvija
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
per i medicinali: https://www.ema.europa.eu .
Istruzioni per la somministrazione
All’inizio del trattamento, l’operatore sanitario la assisterà durante la prima iniezione. Tuttavia, lei e il
suo medico potete decidere se può iniettarsi Steqeyma da solo. In questo caso, le verrà insegnato come
iniettarsi Steqeyma. Informi il medico nel caso in cui abbia eventuali domande sul praticarsi
l’iniezione da solo.
Informazioni importanti
- Nonaprire l’astuccio sigillato fino a quando non si è pronti a usare la siringa preriempita.
- Nonrimuovere il cappuccio fino al momento di praticare l’iniezione.
- Nonmescolare Steqeyma con altri liquidi iniettabili.
- La siringa preriempita non può essere riutilizzata. Eliminare la siringa preriempita usata immediatamente dopo l’uso in un contenitore per lo smaltimento di oggetti appuntiti (vedere Passaggio 14. Smaltimento di Steqeyma).
Conservazione di Steqeyma
- Tenere la siringa preriempita fuori dalla vista e dalla portata dei bambini. Contiene parti piccole.
- Conservare la siringa preriempita in frigorifero tra 2 °C e 8 °C. Noncongelare.
- Conservare questo medicinale ben chiuso nell’astuccio per proteggerlo dalla luce.
- Se necessario, le singole siringhe preriempite di Steqeyma possono anche essere conservate a temperatura ambiente fino a 30 °C, per un unico periodo di massimo 31 giorni nell’imballaggio esterno per proteggerle dalla luce.
- Nonagitare le siringhe preriempite di Steqeyma. Lo scuotimento energico può danneggiare il medicinale.
- Nonusare il medicinale se è stato agitato energicamente.
- Nonusare la siringa preriempita se è caduta.
Prima dell’usoDopo l’uso
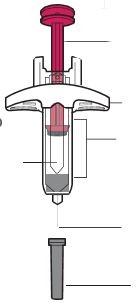
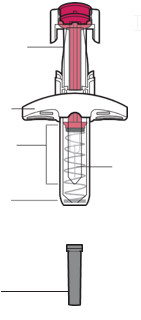
Stantuffo
Impugnatura
Finestrella di
controllo
MedicinaleAgo
Protezione
dell’ago
Ago
Cappuccio
Figura A
Preparazione all’iniezione
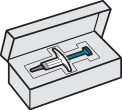
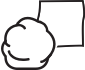


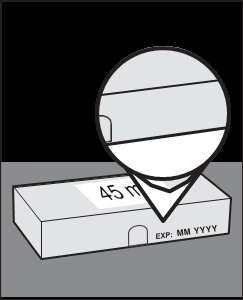
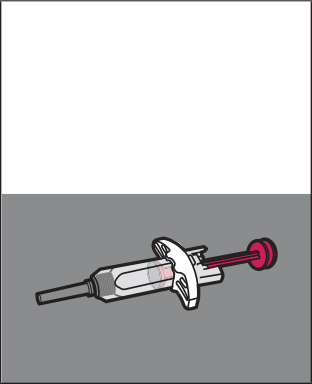
30
minuti
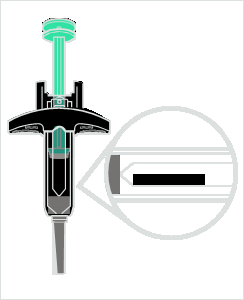



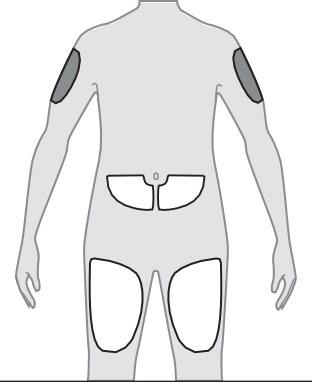
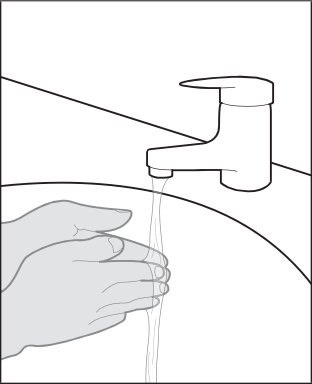
Somministrazione dell’iniezione
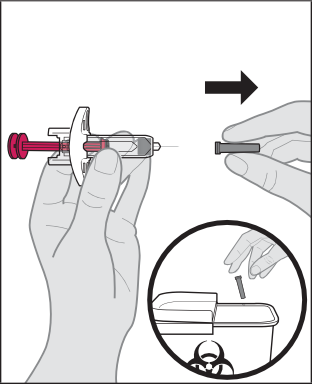
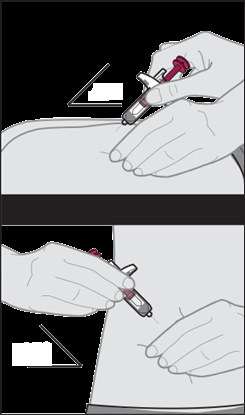
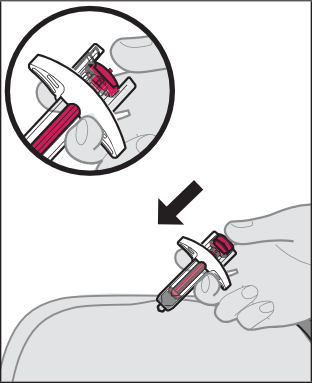

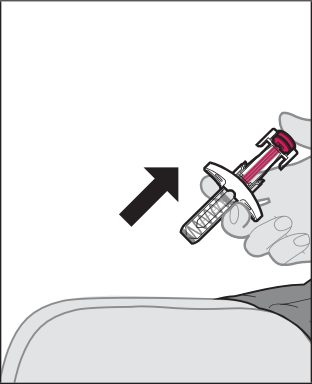
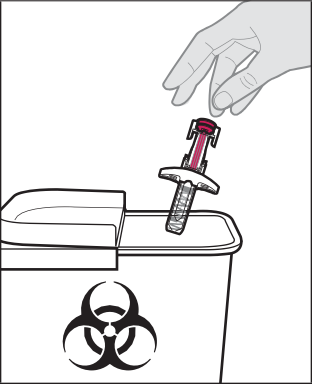
Dopo l’iniezione
STEQEYMA 90 mg soluzione per iniezione in siringa preriempita
ustekinumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
Questo foglio è stato scritto per le persone che prendono questo medicinale. Se lei è il genitore o
la persona che si prende cura di un bambino a cui deve essere somministrato Steqeyma, legga
attentamente queste informazioni prima della somministrazione.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Steqeyma e a cosa serve
- 2. Cosa deve sapere prima di usare Steqeyma
- 3. Come usare Steqeyma
- 4. Possibili effetti indesiderati
- 5. Come conservare Steqeyma
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Steqeyma e a cosa serve
Cos’è Steqeyma
Steqeyma contiene il principio attivo “ustekinumab”, un anticorpo monoclonale.
Gli anticorpi monoclonali sono proteine che riconoscono e legano determinate proteine specifiche
presenti nell’organismo.
Steqeyma appartiene ad un gruppo di medicinali chiamati “immunosoppressori”. Questi medicinali
riducono in parte l’attività del sistema immunitario.
A cosa serve Steqeyma
Steqeyma è usato per trattare le seguenti malattie infiammatorie:
- psoriasi a placche - negli adulti e nei bambini a partire dai 6 anni
- artrite psoriasica - negli adulti
- malattia di Crohn da moderata a grave - negli adulti
Psoriasi a placche
La psoriasi a placche è una condizione della pelle che causa infiammazione della pelle e delle unghie.
Steqeyma ridurrà l’infiammazione e altri segni della malattia.
Steqeyma è usato negli adulti con psoriasi a placche da moderata a grave, che non possono usare
ciclosporina, metotrexato o la fototerapia, o nei quali questi trattamenti non funzionano.
Steqeyma è usato nei bambini e negli adolescenti a partire dai 6 anni con psoriasi a placche da
moderata a grave, che non possono tollerare la fototerapia o altre terapie sistemiche o quando questi
trattamenti non hanno funzionato.
Artrite psoriasica
L’artrite psoriasica è una malattia infiammatoria delle articolazioni, di solito accompagnata dalla
psoriasi. Se ha una artrite psoriasica attiva lei sarà prima trattato con altri medicinali. Se non dovesse
rispondere in maniera adeguata a questi medicinali, potrà prendere Steqeyma per:
- ridurre i segni ed i sintomi della malattia
- migliorare la funzionalità fisica
- rallentare il danno alle articolazioni
Malattia di Crohn
La malattia di Crohn è una malattia infiammatoria dell'intestino. Se ha la malattia di Crohn sarà
trattato prima con altri farmaci. Se non risponde sufficientemente bene o è intollerante a questi
medicinali, le potrà essere somministrato Steqeyma per ridurre i segni e i sintomi della sua malattia.
2. Cosa deve sapere prima di usare Steqeyma
Non usi Steqeyma
- Se è allergico a ustekinumabo ad uno qualsiasi degli altri componenti di questo medicinale (elencati nel successivo paragrafo 6).
- Se è affetto da un’infezione attivache il suo medico ritiene importante.
Se non è sicuro che una delle condizioni sopra riportate si riferisca a lei, ne parli con il medico o il
farmacista, prima di usare Steqeyma.
Avvertenze e precauzioni
Si rivolga al medico o al farmacista prima di usare Steqeyma. Il medico controllerà il suo stato di
salute prima di ogni trattamento. Si assicuri di informare il medico, prima di ogni trattamento, in
merito alle malattie da cui è affetto. Inoltre, informi il medico anche se è stato a contatto di recente con
persone che avrebbero potuto avere la tubercolosi. Il medico la visiterà ed effettuerà degli esami per la
tubercolosi, prima di somministrarle Steqeyma. Se il medico ritiene che è a rischio tubercolosi è
possibile che le somministri dei medicinali per curare la tubercolosi.
Attenzione agli effetti indesiderati gravi
Steqeyma può causare gravi effetti indesiderati, incluse reazioni allergiche ed infezioni. Deve prestare
attenzione a determinati segni della malattia mentre assume Steqeyma. Vedere “Effetti indesiderati
gravi” al paragrafo 4 per una lista completa di questi effetti indesiderati.
Prima di usare Steqeyma contatti il medico
- Se ha mai avuto una reazione allergicaa ustekinumab. Chieda al medico se non è sicuro.
- Se ha mai avuto un qualsiasi tipo di cancro- questo perché gli immunosoppressori come Steqeyma indeboliscono in parte il sistema immunitario. Questo può aumentare il rischio di cancro.
- Se è stato trattato per la psoriasi con altri medicinali biologici (un prodotto medicinaleproveniente da una fonte biologica e solitamente somministrato mediante iniezione)- il rischio di cancro può essere più elevato.
- Se ha o ha avuto una recente infezione .
- Se ha mai avuto una qualsiasi lesione nuova o modificataentro l’area della psoriasi o sulla pelle normale.
- Se sta assumendo un qualsiasi altro tipo di trattamento per la psoriasi e/o artritepsoriasica- come un altro immunosoppressore o la fototerapia (quando il corpo è trattato con un tipo di luce ultravioletta (UV)). Anche questi trattamenti possono ridurre in parte l’attività del sistema immunitario. L’uso contemporaneo di queste terapie con ustekinumab non è stato
studiato. Tuttavia è possibile che possa aumentare la possibilità di patologie correlate ad un
indebolimento del sistema immunitario.
- Se sta usando o ha mai usato iniezioni per il trattamento delle allergie- non è noto se ustekinumab può avere un effetto su di esse.
- Se ha un’età uguale o maggiore ai 65 anni- può avere una maggiore probabilità di contrarre infezioni.
Se non è sicuro che una delle condizioni citate in precedenza possa riguardarla, ne parli con il medico
o il farmacista prima di sottoporsi a un trattamento con Steqeyma.
Durante il trattamento con ustekinumab alcuni pazienti hanno manifestato reazioni simili al lupus,
incluso lupus cutaneo o sindrome simile al lupus (sindrome simil-lupoide). Consulti immediatamente
il medico se manifesta un’eruzione cutanea rossa, in rilievo e squamosa, talvolta con un margine più
scuro, in aree della pelle esposte al sole o in presenza di dolore articolare.
Attacco cardiaco e ictus
In uno studio su pazienti affetti da psoriasi trattati con ustekinumab sono stati osservati attacco
cardiaco e ictus. Il medico controllerà regolarmente i fattori di rischio per le malattie cardiache e
l’ictus per assicurarsi che siano trattati in modo appropriato. Si rivolga immediatamente a un medico
se sviluppa dolore toracico, debolezza o una sensazione anomala su un lato del corpo, flaccidità del
volto, o anomalie del linguaggio o della vista.
Bambini e adolescenti
Steqeyma non è raccomandato per il trattamento di bambini con psoriasi di età inferiore ai 6 anni, o
per il trattamento di bambini di età inferiore ai 18 anni con artrite psoriasica o malattia di Crohn
perché non è stato studiato in questa fascia di età.
Altri medicinali, vaccini e Steqeyma
Informi il medico o il farmacista:
- se sta assumendo, ha recentemente assunto oppure potrebbe assumere qualsiasi altro medicinale
- se recentemente si è fatto vaccinare o sta per essere vaccinato. Alcuni tipi di vaccini (vaccini vivi) non devono essere somministrati mentre sta usando Steqeyma.
- se ha ricevuto Steqeyma durante la gravidanza, informi il pediatra del/la suo/a bambino/a del trattamento con Steqeyma prima che il/la suo/a bambino/a riceva qualsiasi vaccino, inclusi vaccini vivi come il vaccino BCG (usato per la prevenzione della tubercolosi). Se ha ricevuto Steqeyma durante la gravidanza, i vaccini vivi non sono raccomandati per il/la suo/a bambino/a nei primi sei mesi dopo la nascita, a meno che il pediatra del/la suo/a bambino/a non raccomandi altrimenti.
Gravidanza e allattamento
- È preferibile evitare l’uso di Steqeyma in gravidanza. Non sono noti gli effetti di ustekinumab sulle donne in gravidanza. Se è in età fertile, è consigliabile evitare di iniziare una gravidanza; deve usare un adeguato metodo contraccettivo durante l’uso di Steqeyma e per almeno 15 settimane dopo la sospensione del trattamento con Steqeyma.
- Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza chieda consiglio al medico.
- Ustekinumab può raggiungere il nascituro attraverso la placenta. Se ha ricevuto Steqeyma durante la gravidanza, il/la suo/a bambino/a potrebbe avere un rischio maggiore di contrarre un’infezione.
- Se ha ricevuto Steqeyma durante la gravidanza, è importante che ne informi il pediatra e gli altri operatori sanitari prima che il/la suo/a bambino/a riceva qualsiasi vaccino. Se ha ricevuto Steqeyma durante la gravidanza, i vaccini vivi come il vaccino BCG (usato per la prevenzione della tubercolosi) non sono raccomandati per il/la suo/a bambino/a nei primi sei mesi dopo la nascita, a meno che il pediatra non raccomandi altrimenti.
- Ustekinumab può essere escreto nel latte materno in quantità molto ridotte. Se sta allattando con latte materno o se prevede di allattare chieda consiglio al medico. Lei e il medico deciderete se deve allattare o utilizzare Steqeyma. Non può fare entrambe le cose.
Guida di veicoli e utilizzo di macchinari
Steqeyma non altera o altera in modo trascurabile la capacità di guidare veicoli o di usare macchinari.
3. Come usare Steqeyma
Steqeyma è destinato per l’uso sotto la guida e supervisione di un medico con esperienza nel
trattamento delle condizioni per cui è indicato Steqeyma.
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico. Se ha dubbi, consulti il
medico. Discuta con il medico quando dovrà sottoporsi alle iniezioni e alle successive visite di
controllo.
Quanto Steqeyma viene somministrato
Sarà il medico a decidere di quanto Steqeyma ha bisogno e per quanto tempo.
Adulti a partire dai 18 anni
Psoriasi e artrite psoriasica
- La dose iniziale raccomandata è 45 mg di Steqeyma. I pazienti con un peso maggiore di 100 chilogrammi (kg) possono iniziare con una dose di 90 mg invece di 45 mg.
- Dopo la dose iniziale assumerà la dose successiva 4 settimane dopo, e poi ogni 12 settimane. Le dosi successive sono solitamente le stesse della dose iniziale.
Malattia di Crohn
- Durante il trattamento, la prima dose di circa 6 mg/kg di Steqeyma le è somministrata dal medico mediante una flebo in vena fatta nel suo braccio (infusione endovenosa). Dopo la dose iniziale, riceverà la dose successiva di 90 mg di Steqeyma dopo 8 settimane, poi ogni 12 settimane con un’iniezione sotto la pelle (via sottocutanea).
- In alcuni pazienti, dopo la prima iniezione sottocute, la dose di 90 mg di Steqeyma può essere somministrata ogni 8 settimane. Il medico deciderà quando si dovrà ricevere la dose successiva.
Bambini e adolescenti a partire dai 6 anni
Psoriasi
Non esiste una formulazione di Steqeyma per i bambini con psoriasi a placche con peso inferiore a
60 kg, pertanto devono essere utilizzati altri prodotti contenenti ustekinumab.
- Il medico calcolerà la dose giusta, incluso la quantità (volume) di Steqeyma che deve essere iniettata per garantire la somministrazione della dose corretta. La dose corretta dipenderà dal peso corporeo del bambino al momento della somministrazione di ogni dose.
- Se il peso corporeo è inferiore ai 60 kg, non è disponibile una formulazione di Steqeyma e devono essere utilizzati altri prodotti a base di ustekinumab.
- Se il peso corporeo è compreso tra 60 kg e 100 kg, la dose raccomandata è di 45 mg di Steqeyma.
- Se il peso supera i 100 kg, la dose raccomandata è di 90 mg di Steqeyma.
- Dopo la dose iniziale, dovrà ricevere la dose successiva dopo 4 settimane, e successivamente ogni 12 settimane.
Come viene somministrato Steqeyma
Steqeyma è somministrato mediante un’iniezione sottocute (“per via sottocutanea”). All’inizio del
trattamento, il personale medico o infermieristico può iniettarle Steqeyma.
- Tuttavia, lei e il suo medico potete decidere se può iniettarsi Steqeyma da solo. In questo caso, le verrà insegnato come iniettarsi Steqeyma da solo.
- Per le istruzioni su come iniettare Steqeyma, vedere “Istruzioni per la somministrazione” alla
Informi il medico nel caso in cui abbia eventuali domande sull’iniezione da praticare da solo.
Se usa più Steqeyma di quanto deve
Se ha usato o ha ricevuto troppo Steqeyma, informi immediatamente il medico o il farmacista. Porti
sempre la confezione esterna del medicinale con sé, anche se è vuota.
Se dimentica di usare Steqeyma
Se dimentica una dose, contatti il medico o il farmacista. Non prenda una dose doppia per compensare
la dimenticanza della dose.
Se interrompe il trattamento con Steqeyma
Non è pericoloso interrompere l’impiego di Steqeyma. Tuttavia, se interrompe il trattamento i sintomi
possono ripresentarsi.
Nel caso in cui abbia ulteriori domande sull’uso di questo medicinale, chieda al medico o al
farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Effetti indesiderati gravi
Alcuni pazienti possono presentare gravi effetti indesiderati che possono necessitare di un trattamento
urgente.
Reazioni allergiche – queste possono necessitare di un trattamento urgente, quindi contatti
il medico o richieda assistenza medica di urgenza se nota uno dei seguenti segni.
- Reazioni allergiche gravi (“anafilassi”) sono rare in pazienti che assumono ustekinumab (interessano fino a 1 paziente su 1 000). I segni includono: o difficoltà a respirare o a deglutire o bassa pressione sanguigna, che può causare capogiri o sensazione di testa leggera o gonfiore della faccia, delle labbra, della bocca o della gola.
- I segni comuni di una reazione allergica includono eruzione cutanea ed orticaria (interessano fino a 1 paziente su 100).
In rari casi sono state riportate reazioni polmonari allergiche e infiammazione polmonare
in pazienti che ricevono ustekinumab. Informi immediatamente il medico se sviluppa
sintomi come tosse, mancanza di respiro e febbre.
Se presenta una reazione allergica grave, il medico può decidere che lei non deve usare
Steqeyma di nuovo.
Infezioni – queste possono necessitare di un trattamento urgente, quindi contatti subito il
medico se nota uno dei seguenti segni.
- Le infezioni del naso e della gola e il raffreddore comune sono comuni (interessano fino a 1 paziente su 10).
- Le infezioni del torace sono non comuni (possono interessare fino ad 1 paziente su 100)
- L’infiammazione del tessuto sottocutaneo (‘cellulite’) è non comune (interessa fino a 1 paziente su 100).
- Herpes zoster (un tipo di eruzione cutanea dolorosa con vesciche) è non comune (interessa fino a 1 paziente su 100).
Steqeyma può diminuire la capacità di combattere le infezioni. Alcune infezioni possono
diventare gravi e possono includere infezioni provocate da virus, funghi, batteri (incluso quello
della tubercolosi) o parassiti, comprese infezioni che si verificano principalmente nelle persone
con sistema immunitario indebolito (infezioni opportunistiche). In pazienti trattati con
ustekinumab sono state segnalate infezioni opportunistiche del cervello (encefalite, meningite),
dei polmoni e degli occhi.
Deve prestare attenzione ai segni di infezione mentre sta usando Steqeyma. Questi includono:
- febbre, sintomi simil influenzali, sudorazione notturna, perdita di peso
- sensazione di stanchezza o di fiato corto, tosse persistente
- caldo, pelle arrossata e dolente, o una eruzione cutanea dolorosa e con vesciche
- bruciore quando urina
- diarrea
- disturbo visivo o perdita della vista
- cefalea, rigidità del collo, sensibilità alla luce, nausea o confusione
Informi immediatamente il medico se nota uno qualsiasi di questi segni di infezione. Questi
possono essere segni di infezioni come infezioni del torace, infezioni della cute, herpes zoster o
infezioni opportunistiche che possono avere complicanze gravi. Si rivolga al medico se ha un
qualsiasi tipo di infezione che persiste o continua a ripresentarsi. Il medico può decidere di
interrompere Steqeyma fino a quando l’infezione non si risolve. Inoltre informi il medico se ha
eventuali tagli o ferite aperte che possono infettarsi.
Desquamazione cutanea – aumento del rossore e desquamazione della cute su un’ampia
superficie del corpo possono essere sintomi di psoriasi eritrodermica o dermatite
esfoliativa, le quali sono gravi condizioni della pelle. Se nota uno di questi segni deve
informare immediatamente il suo medico.
Altri effetti indesiderati
Effetti indesiderati comuni (interessano fino a 1 paziente su 10)
- Diarrea
- Nausea
- Vomito
- Sensazione di stanchezza
- Sensazione di capogiro
- Mal di testa
- Prurito
- Dolore alla schiena, muscolare o articolare
- Mal di gola
- Arrossamento e dolore nel sito dell’iniezione
- Sinusite
Effetti indesiderati non comuni(interessano fino a 1 paziente su 100)
- Infezione dentali
- Infezione micotica vaginale
- Depressione
- Naso chiuso o che cola
- Sanguinamento, lividi, rigidità, gonfiore e prurito nel punto in cui viene eseguita l’iniezione
- Sentirsi debole
- Palpebra cadente e rilassamento muscolare ad un lato del viso (“paralisi facciale” o “paralisi di Bell”), che solitamente è temporanea
- Un cambiamento della psoriasi con rossore e nuove bolle cutanee piccole, gialle o bianche, talvolta accompagnate da febbre (psoriasi pustolosa)
- Desquamazione della pelle (esfoliazione della pelle)
- Acne
Effetti indesiderati rari(interessano fino a 1 paziente su 1 000)
- Rossore e desquamazione della cute su un’ampia superficie del corpo, che possono essere pruriginosi o dolorosi (dermatite esfoliativa). Sintomi simili alcune volte si sviluppano come una naturale evoluzione nella tipologia dei sintomi della psoriasi (psoriasi eritrodermica)
- Infiammazione dei piccoli vasi sanguigni, che può portare a un’eruzione cutanea con piccoli bozzi rossi o viola, febbre o dolore articolare (vasculite)
Effetti indesiderati molto rari (interessano fino a 1 paziente su 10 000)
- Formazione di vesciche cutanee con possibile arrossamento, prurito e dolore (pemfigoide bolloso).
- Lupus cutaneo o sindrome simile al lupus (eruzione cutanea rossa, in rilievo e squamosa su aree della pelle esposte al sole, talvolta in presenza di dolore articolare).
Segnalazione degli effetti indesiderati
Se si manifesta un qualsiasi effetti indesiderato, compresi quelli non elencati in questo foglio, si
rivolga al medico o al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione riportato nell’Allegato V. Segnalando gli effetti indesiderati lei può
contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Steqeyma
- Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
- Conservare in frigorifero (2 °C - 8 °C). Non congelare.
- Tenere la siringa preriempita nell’imballaggio esterno, per proteggere il medicinale dalla luce.
- Se necessario, le singole siringhe preriempite di Steqeyma possono anche essere conservate a temperatura ambiente fino a 30 °C, per un unico periodo di massimo 31 giorni, nell'imballaggio esterno al fine di proteggerle dalla luce. Registrare la data in cui la siringa preriempita viene rimossa per la prima volta dal frigorifero e la data in cui va eliminata nello spazio previsto sulla confezione esterna. La data in cui va eliminata non deve superare la data di scadenza originale stampata sulla confezione. Una volta che una siringa è stata conservata a temperatura ambiente (fino a 30 °C), non deve essere rimessa in frigorifero. Gettare la siringa se non utilizzata entro 31 giorni a temperatura ambiente o entro la data di scadenza originale, a seconda di quale è precedente.
- Non agitare le siringhe preriempite di Steqeyma. Lo scuotimento energico prolungato può danneggiare il medicinale.
Non usi questo medicinale
- Dopo la data di scadenza che è riportata sull’etichetta e sull’astuccio dopo EXP o Scad. La data di scadenza si riferisce all’ultimo giorno del mese.
- Se il liquido presenta un colore alterato, è opaco o se si vedono particelle estranee che galleggiano (vedere il paragrafo 6 “Descrizione dell’aspetto di Steqeyma e contenuto della confezione”).
- Se sa o crede che il medicinale sia stato esposto a temperature estreme (ad esempio accidentalmente congelato o riscaldato).
- Se il prodotto è stato agitato energicamente. Steqeyma è monouso. Il prodotto inutilizzato che resta nella siringa deve essere eliminato.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Steqeyma
- Il principio attivo è ustekinumab. Ogni siringa preriempita contiene 90 mg di ustekinumab in 1 mL.
- Gli eccipienti sono: L-istidina, L-istidina monoidrocloridrato monoidrato, polisorbato 80, saccarosio, acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Steqeyma e contenuto della confezione
Steqeyma è una soluzione per iniezione da limpida a leggermente opalescente (aspetto simile a quello
della perla), da incolore a giallo pallido. La soluzione può contenere qualche piccola particella
traslucida o bianca di proteine. È fornito in una confezione di cartone contenente 1 dose unica, in
siringa preriempita di vetro da 1 mL. Ogni siringa preriempita contiene una dose di ustekinumab
90 mg in 1 mL di soluzione per iniezione.
Titolare dell’autorizzazione all’immissione in commercio
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungheria
Produttore
Nuvisan France SARL
2400, Route des Colles
06410, Biot
Francia
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 1528 7418
[email protected]
Lietuva
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
България
Celltrion Healthcare Hungary Kft.
Teл.: +36 1 231 0493
Luxembourg/Luxemburg
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 1528 7418
[email protected]
Česká republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Magyarország
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
Danmark
Celltrion Healthcare Denmark ApS
Tlf.: +45 3535 2989
[email protected]
Malta
Mint Health Ltd
Tel: +356 2093 9800
Deutschland
Celltrion Healthcare Deutschland GmbH
Tel: +49 (0)30 346494150
[email protected]
Nederland
Celltrion Healthcare Netherlands B.V.
Tel: +31 20 888 7300
[email protected]
Eesti
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
[email protected]
Norge
Celltrion Healthcare Norway AS
[email protected]
España
CELLTRION FARMACEUTICA (ESPAÑA)
S.L.
Tel: +34 919 94 23 90
[email protected]
Österreich
Astro-Pharma GmbH
Tel: +43 1 97 99 860
Ελλάδα
ΒΙΑΝΕΞ Α.Ε.
Τηλ: +30 210 8009111
Polska
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
France
Celltrion Healthcare France SAS
Tél: +33 (0)1 71 25 27 00
Portugal
CELLTRION PORTUGAL, UNIPESSOAL
LDA
Tel: +351 21 936 8542
[email protected]
Hrvatska
Oktal Pharma d.o.o.
Tel: +385 1 6595 777
România
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Ireland
Celltrion Healthcare Ireland Limited
Tel: +353 1 223 4026
[email protected]
Slovenija
OPH Oktal Pharma d.o.o.
Tel: +386 1 519 29 22
Ísland
Celltrion Healthcare Hungary Kft.
Sími: +36 1 231 0493
[email protected]
Slovenská republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Suomi/Finland
Celltrion Healthcare Finland Oy.
Puh/Tel: +358 29 170 7755
[email protected]
Κύπρος
C.A. Papaellinas Ltd
Τηλ: +357 22741741
Italia
Celltrion Healthcare Italy S.R.L.
Tel: +39 0247927040
[email protected]
Sverige
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
[email protected]
Latvija
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
per i medicinali: https://www.ema.europa.eu .
Istruzioni per la somministrazione
All’inizio del trattamento, l’operatore sanitario la assisterà durante la prima iniezione. Tuttavia, lei e il
suo medico potete decidere se può iniettarsi Steqeyma da solo. In questo caso, le verrà insegnato come
iniettarsi Steqeyma. Informi il medico nel caso in cui abbia eventuali domande sul praticarsi
l’iniezione da solo.
Informazioni importanti
- Nonaprire l’astuccio sigillato fino a quando non si è pronti a usare la siringa preriempita.
- Nonrimuovere il cappuccio fino al momento di praticare l’iniezione.
- Nonmescolare Steqeyma con altri liquidi iniettabili.
- La siringa preriempita non può essere riutilizzata. Eliminare la siringa preriempita usata immediatamente dopo l’uso in un contenitore per lo smaltimento di oggetti appuntiti (vedere Passaggio 14. Smaltimento di Steqeyma).
Conservazione di Steqeyma
- Tenere la siringa preriempita fuori dalla vista e dalla portata dei bambini. Contiene parti piccole.
- Conservare la siringa preriempita in frigorifero tra 2 °C e 8 °C. Noncongelare.
- Conservare questo medicinale ben chiuso nell’astuccio per proteggerlo dalla luce.
- Se necessario, le singole siringhe preriempite di Steqeyma possono anche essere conservate a temperatura ambiente fino a 30 °C, per un unico periodo di massimo 31 giorni nell’imballaggio esterno per proteggerle dalla luce.
- Nonagitare le siringhe preriempite di Steqeyma. Lo scuotimento energico può danneggiare il medicinale.
- Nonusare il medicinale se è stato agitato energicamente.
- Nonusare la siringa preriempita se è caduta.
Prima dell’usoDopo l’uso
Stantuffo
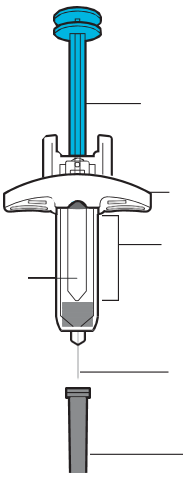
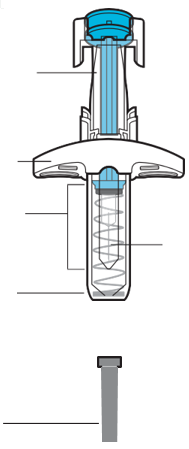
Impugnatura
Finestrella di
controllo
Ago
Protezione
dell’ago
Medicinale
Ago
Cappuccio
Figura A
Preparazione all’iniezione


Figura B
30
minuti

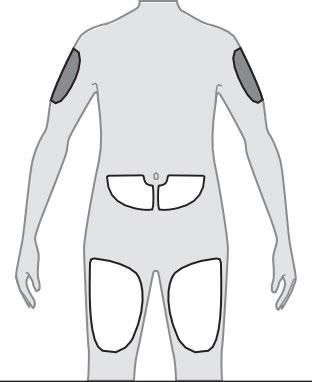
Somministrazione dell’iniezione
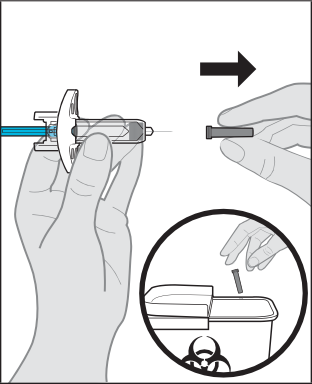
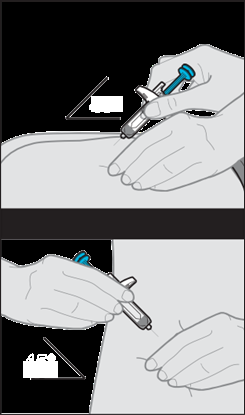
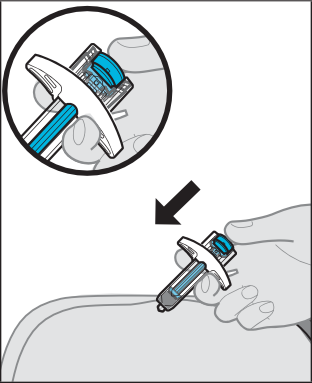
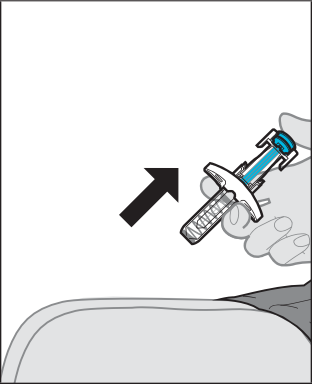
Dopo l’iniezione
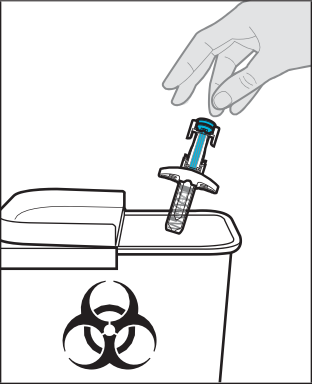
-


- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile in siringa pre-riempita, 45 mg
- Codice ATCL04AC05
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a STEQEYMAForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 45 mgPrincipio attivo: ustekinumabProduttore: ACCORD HEALTHCARE, S.L.U.Prescrizione richiestaForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 45 mgPrincipio attivo: ustekinumabProduttore: FORMYCON AGPrescrizione richiestaForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 45 mgPrincipio attivo: ustekinumabProduttore: ACCORD HEALTHCARE, S.L.U.Prescrizione richiesta
Medici online per STEQEYMA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di STEQEYMA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per STEQEYMA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.





