
Come usare TRIAXIS
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
TRIAXIS
Sospensione iniettabile in siringa pre-riempita
Vaccino antidifterico, antitetanico, antipertossico (componenti acellulari)
(adsorbito, contenuto antigenico ridotto)
Legga attentamente questo foglio prima che lei o il suo bambino siate vaccinati perché contiene
importanti informazioni per voi.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo vaccino è stato prescritto soltanto per lei o per il suo bambino. Non lo dia ad altri.
- Se lei o il suo bambino manifestate un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Cos’è Triaxis e a che cosa serve
- 2. Cosa deve sapere prima che Triaxis venga somministrato a lei o al suo bambino
- 3. Come e quando usare Triaxis
- 4. Possibili effetti indesiderati
- 5. Come conservare Triaxis
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Triaxis e a che cosa serve
Triaxis ( dTpa) è un vaccino. I vaccini vengono impiegati per proteggere contro le malattie infettive. Essi
agiscono inducendo le difese naturali del corpo a produrre una protezione contro i batteri che causano
determinate malattie.
Questo vaccino è usato per stimolare la protezione contro la difterite, il tetano e la pertosse (tosse convulsa)
nei bambini dai quattro anni, negli adolescenti e negli adulti, a seguito di un ciclo primario di vaccinazione
completo.
L’impiego di Triaxis durante la gravidanza consente il trasferimento della protezione al bambino all’interno
del grembo materno per proteggerlo dalla pertosse durante i primi mesi di vita.
Limitazioni nella protezione fornita
Triaxis eviterà l’insorgenza di queste malattie solo se esse sono causate dagli stessi batteri verso i quali il
vaccino agisce. Lei o il suo bambino potreste ancora contrarre malattie simili se esse sono causate da altri
batteri o virus.
Triaxis non contiene alcun batterio o virus vivi e non può causare nessuna malattia infettiva contro la quale
protegge.
Si ricordi che nessun vaccino può fornire una protezione completa, per tutta la vita in tutte le persone
vaccinate.
2. Cosa deve sapere prima che Triaxis venga somministrato a lei o al suo bambino
Per assicurarsi che Triaxis sia idoneo per lei o per il suo bambino, è importante che lei informi il medico o
l’infermiere se uno qualsiasi dei punti riportati di seguito interessa lei o il suo bambino. Se c’è qualcosa che
non comprende, chieda spiegazioni al medico o all’infermiere.
Non usi Triaxis se lei o il suo bambino:
- avete avuto una reazione allergica a:
- vaccini della difterite, del tetano, della pertosse,
- uno qualsiasi degli altri componenti (elencati nel Paragrafo 6),
- uno qualsiasi dei componenti residui derivanti dalla produzione (formaldeide, glutaraldeide) che possono essere presenti in tracce.
- avete avuto una reazione grave che interessa il cervello, entro una settimana dall’assunzione di una precedente dose di vaccino contro la tosse convulsa.
- avete una malattia febbrile grave in fase acuta . La vaccinazione dovrà essere rimandata finché lei o il suo bambino non sarete guariti. Una malattia di entità minore non accompagnata da febbre in genere non rappresenta un valido motivo per rimandare la vaccinazione. Il suo medico deciderà se somministrare Triaxis a lei o al suo bambino.
Avvertenze e precauzioni
Si rivolga al medico o all’infermiere prima della vaccinazione se lei o il suo bambino:
- avete ricevuto una dose di richiamo di un vaccino per la difterite e il tetano nelle ultime 4 settimane. In questo caso lei o il suo bambino non dovreste ricevere la vaccinazione con Triaxis e il medico deciderà sulla base delle raccomandazioni ufficiali quando lei o il suo bambino potete ricevere un’ulteriore iniezione.
- avete avuto una sindrome di Guillain-Barré (perdita temporanea di movimento e della sensibilità in una parte o in tutto il corpo) nelle 6 settimane successive alla somministrazione di una precedente dose di un vaccino contenente tossoide tetanico. Il medico deciderà se somministrare Triaxis a lei o al suo bambino.
- avete una malattia progressiva che interessa il cervello/i nervi, o convulsioni incontrollate. Il medico prima di tutto inizierà il trattamento e quando le condizioni si saranno stabilizzate procederà con la vaccinazione.
- avete un sistema immunitario impoverito o ridotto a causa di:
- medicinali (ad es. steroidi, chemioterapia o radioterapia)
- infezione da HIV o AIDS
- qualsiasi altra malattia.
Il vaccino può non risultare efficace quanto nei soggetti con un sistema immunitario sano. Se possibile, la
vaccinazione deve essere rimandata fino alla guarigione di queste malattie o al termine del trattamento.
- avete un qualunque disturbo del sangue a causa del quale facilmente presentate ecchimosi o sanguinamento per un lungo periodo di tempo in seguito a lievi tagli (per esempio una patologia del sangue come emofilia o trombocitopenia, o un trattamento con medicinali anticoagulanti).
Può verificarsi svenimento a seguito, o anche prima, di qualsiasi iniezione con ago. Pertanto, informi il
medico o l'infermiere se lei o il suo bambino siete svenuti dopo una precedente iniezione.
Informi il medico, il farmacista o l'infermiere prima di usare Triaxis se lei o il suo bambino avete avuto
reazioni allergiche al lattice. Le siringhe preriempite (1,5 mL) con il cappuccio morbido contengono un
derivato di lattice di gomma naturale che può causare una reazione allergica.
Altri medicinali o vaccini e Triaxis
Informi il medico, l’infermiere o il farmacista se lei o il suo bambino state assumendo, avete recentemente
assunto, o potreste assumere qualsiasi altro medicinale.
Poiché Triaxis non contiene batteri vivi, in genere può essere somministrato contemporaneamente ad altri
vaccini o immunoglobuline, ma in un sito di iniezione differente. Studi hanno dimostrato che Triaxis può
essere somministrato contemporaneamente ad uno qualsiasi dei seguenti vaccini: vaccino contro l’epatite B,
vaccino della poliomielite (iniettabile o orale), vaccino inattivato contro l’influenza e vaccino ricombinante
contro il papillomavirus umano, rispettivamente. Somministrazioni contemporanee di più di un vaccino
dovranno essere effettuate in arti differenti.
Se lei o il suo bambino state ricevendo un trattamento medico che interessa il sangue o il sistema
immunitario suo o di suo figlio (come farmaci che fluidificano il sangue, steroidi, chemioterapia), faccia
riferimento al paragrafo “Avvertenze e precauzioni”, sopra riportato.
Gravidanza, allattamento e fertilità
Se è in corso gravidanza o se sta allattando con latte materno, se sospetta o sta pianificando una gravidanza
informi il medico o l’infermiere. Il suo medico la aiuterà a decidere se lei deve ricevere Triaxis durante la
gravidanza.
Guida di veicoli e utilizzo di macchinari
Non sono stati effettuati studi sugli effetti di Triaxis sulla capacità di guidare veicoli o utilizzare macchinari.
Triaxis non ha o ha un effetto trascurabile sulla capacità di guidare veicoli e utilizzare macchinari.
3. Come usare Triaxis
Quando lei o il suo bambino riceverete il vaccino
Il medico determinerà se Triaxis è idoneo per lei o per il suo bambino, in base a:
- quali vaccini sono stati somministrati, in passato, a lei o al suo bambino
- quante dosi di vaccini simili sono state somministrate, in passato, a lei o al suo bambino
- quando è stata somministrata l’ultima dose di un vaccino simile a lei o al suo bambino
Il medico deciderà quanto tempo dovrete aspettare tra una vaccinazione e l’altra.
Se lei è in gravidanza, il suo medico la aiuterà a decidere se lei deve ricevere Triaxis durante la gravidanza.
Dosaggio e modo di somministrazione
Chi le somministrerà Triaxis?
Triaxis deve essere somministrato da un operatore sanitario che è stato istruito all’uso dei vaccini e in un
ospedale o ambulatorio attrezzati per intervenire nel caso si presenti, in seguito all’iniezione, una qualsiasi
reazione grave, rara di tipo allergico al vaccino.
Dosaggio
Tutte le fasce di età per le quali è indicato Triaxis riceveranno 1 iniezione (mezzo millilitro).
Nel caso in cui lei o il suo bambino abbiate subito un infortunio che richiede un'azione preventiva contro la
malattia del tetano, il medico può decidere di somministrare Triaxis con o senza le immunoglobuline
tetaniche.
Triaxis può essere usato per il richiamo della vaccinazione. Il medico le darà consigli sulla ripetizione della
vaccinazione.
Modo di somministrazione
Il medico o l’infermiere le somministrerà il vaccino mediante iniezione intramuscolare nella parte superiore
ed esterna del braccio (muscolo deltoide).
Il medico o l’infermiere nonle inietterà il vaccino all’interno di un vaso sanguigno, nel gluteo o sotto la
pelle. In caso di patologie della coagulazione del sangue, essi potranno decidere di effettuare l’iniezione sotto
la pelle, sebbene questo possa comportare ulteriori effetti locali indesiderati, inclusa la formazione di un
piccolo nodulo sotto la pelle.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico, al farmacista o all’infermiere.
4. Possibili effetti indesiderati
Come tutti i medicinali, Triaxis può causare effetti indesiderati, sebbene non tutte le persone li manifestino.
Reazioni allergiche gravi
Se qualcuno di questi sintomi dovesse manifestarsi dopo aver lasciato il luogo dove è stato
somministrato il vaccino a lei o al suo bambino, deve consultare un medico IMMEDIATAMENTE:
- difficoltà di respirazione,
- colorazione bluastra della lingua o delle labbra,
- eruzione cutanea,
- gonfiore del viso o della gola,
- bassa pressione sanguigna che causa capogiro o collasso.
Quando questi segni o sintomi si manifestano, essi si sviluppano di solito subito dopo la somministrazione
del vaccino e mentre lei o il suo bambino vi trovate ancora in ospedale o nell’ambulatorio medico.
Altri effetti indesiderati
I seguenti effetti indesiderati sono stati osservati durante gli studi clinici effettuati nei gruppi di età specifici.
Bambini da 4 a 6 anni di età
Molto comuni (possono interessare più di 1 soggetto su 10):
- diminuzione dell'appetito
- mal di testa
- diarrea
- stanchezza
- dolore
- arrossamento
- gonfiore nell'area in cui è stato iniettato il vaccino
Comuni (possono interessare fino a 1 soggetto su 10):
- nausea
- vomito
- eruzione cutanea
- dolori (in tutto il corpo) o debolezza muscolare
- dolore e gonfiore delle articolazioni
- febbre
- brividi
- patologie ai linfonodi ascellari
Adolescenti da 11 a 17 anni di età
Molto comuni (possono interessare più di 1 soggetto su 10):
- mal di testa
- diarrea
- nausea
- dolori (in tutto il corpo) o debolezza muscolare
- dolore o gonfiore delle articolazioni
- stanchezza/debolezza
- sensazione di malessere
- brividi
- dolore
- rossore e gonfiore nell'area in cui è stato iniettato il vaccino
Comuni (possono interessare fino a 1 soggetto su 10):
- vomito
- eruzione cutanea
- febbre
- patologie ai linfonodi ascellari
Adulti da 18 a 64 anni di età
Molto comuni (possono interessare più di 1 soggetto su 10):
- mal di testa
- diarrea
- dolore (in tutto il corpo) o debolezza muscolare
- stanchezza/debolezza
- sensazione di malessere
- dolore
- rossore e gonfiore nell'area in cui è stato iniettato il vaccino
Comuni (possono interessare fino a 1 soggetto su 10):
- nausea
- vomito
- eruzione cutanea
- dolore o gonfiore delle articolazioni
- febbre
- brividi
- patologie ai linfonodi ascellari
I seguenti ulteriori eventi avversi sono stati riportati nei differenti gruppi di età indicati, durante l’utilizzo
commerciale di Triaxis. La frequenza di questi eventi avversi non può essere determinata con precisione,
poiché si basa su segnalazioni volontarie in relazione al numero stimato di persone vaccinate.
- Reazioni allergiche/reazioni allergiche serie (lei può trovare la spiegazione di come riconoscere tali
reazioni all’inizio del Paragrafo 4), formicolio o intorpidimento, paralisi di parte del corpo o di tutto il
corpo (sindrome di Guillain-Barré), infiammazione dei nervi del braccio (neurite brachiale), perdita della
funzione del nervo che controlla i muscoli del viso (paralisi facciale), convulsioni, svenimento,
infiammazione del midollo spinale (mielite), infiammazione della componente muscolare del cuore
(miocardite), prurito, orticaria, infiammazione di un muscolo (miosite), gonfiore esteso all’arto
accompagnato da arrossamento, calore, sensibilità o dolore nell’area dove è stato somministrato il
vaccino, ecchimosi, ascesso, o una piccola massa nell’area dove è stato somministrato il vaccino.
Segnalazione degli effetti indesiderati
Se lei o il suo bambino manifestate un qualsiasi effetto indesiderato, compresi quelli non elencati in questo
foglio, si rivolga al medico, al farmacista o all’infermiere. Lei può inoltre segnalare gli effetti indesiderati
direttamente tramite il sistema nazionale di segnalazione riportato all’indirizzo:
https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse .
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza di
questo medicinale.
5. Come conservare Triaxis
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usare Triaxis dopo la data di scadenza indicata sull’etichetta dopo la dicitura “Scad.”. La data di
scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2°C - 8°C). Non congelare. Se congelato, il vaccino deve essere eliminato.
Conservare il vaccino nell’astuccio esterno per proteggerlo dalla luce.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come eliminare
i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6Contenuto della confezione e altre informazioni
Cosa contiene Triaxis
I principi attivi contenuti in ciascuna dose (0,5 ml) del vaccino sono:
Tossoide Difterico non meno di 2 Unità Internazionali (2 Lf)
Tossoide Tetanico non meno di 20 Unità Internazionali (5 Lf)
Antigeni della Pertosse:
Tossoide Pertossico 2,5 microgrammi
Emoagglutinina filamentosa 5 microgrammi
Pertactina 3 microgrammi
Fimbrie di Tipo 2 e 3 5 microgrammi
Adsorbiti su Alluminio Fosfato 1,5 mg (0,33 mg di Al )
Il fosfato di alluminio è incluso in questo vaccino come adiuvante. Gli adiuvanti sono sostanze incluse in
alcuni vaccini per accelerare, migliorare e/o prolungare gli effetti protettivi del vaccino.
Gli altri componenti sono: fenossietanolo, acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Triaxis e contenuto della confezione
Triaxis si presenta come una sospensione iniettabile in siringa pre-riempita da 0,5 ml:
- senza ago - confezione da 1 o 10
- con 1 o 2 aghi separati - confezione da 1 o 10
- con ago di sicurezza separato - confezione da 1 o 10.
È possibile che non tutte le confezioni siano commercializzate.
Il vaccino si presenta come una sospensione bianca torbida che può sedimentare durante la conservazione e
formare aggregati grumosi o sfaldati. Dopo averlo agitato bene, il vaccino si presenta come un liquido
uniformemente bianco. Se sono presenti aggregati, il prodotto può essere agitato nuovamente fino
all’ottenimento di una sospensione uniforme.
Titolare dell’autorizzazione all’immissione in commercio:
Sanofi Winthrop Industrie
82 Avenue Raspail
94250 Gentilly
Francia
Rappresentante per l’Italia
Sanofi S.r.l. - Viale L. Bodio, 37/B – 20158 Milano
Produttore responsabile del rilascio dei lotti:
Sanofi Winthrop Industrie
1541 avenue Marcel Mérieux
69280 Marcy l’Etoile
Francia
E/o
Sanofi Winthrop Industrie
Voie de l’Institut - Parc Industriel d’Incarville
B.P 101
27100 Val de Reuil
Francia
Questo medicinale è autorizzato negli Stati Membri dello Spazio Economico Europeo con le seguenti
denominazioni:
Austria, Germania Covaxis
Belgio, Danimarca, Finlandia, Francia, Grecia, Irlanda,
Italia, Lussemburgo, Olanda, Norvegia, Portogallo, Spagna,
Svezia.
Triaxis
Bulgaria, Cipro, Croazia, Repubblica Ceca, Estonia,
Ungheria, Lettonia, Lituania, Malta, Polonia, Romania,
Slovacchia, Slovenia, Regno Unito (Irlanda del Nord).
Adacel
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari.
In assenza di studi di compatibilità, Triaxis non deve essere miscelato con altri medicinali.
Preparazione per la somministrazioneLa siringa pre-riempita può essere fornita con un Luer Lock con il
cappuccio morbido (Figura A) o con il cappuccio rigido (Figura B). La siringa con la sospensione iniettabile
deve essere ispezionata visivamente prima della somministrazione. In caso si rilevasse la presenza di
particolato, di perdite, di attivazione prematura dello stantuffo o del sigillo della punta difettoso, gettare la
siringa preriempita. La siringa è destinata a un solo uso e non deve essere riutilizzata.
Istruzioni per l'uso della siringa pre-riempita Luer Lock:
Figura A: Siringa Luer Lock con cappuccio morbido
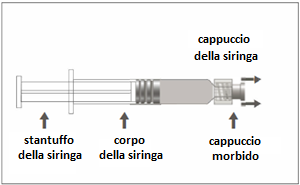
| t I a i Passaggio 1: Tenendo il cappuccio della z siringa in una mano (evitare di tenere lo stantuffo o il corpo della siringa), togliere il n cappuccio. e | 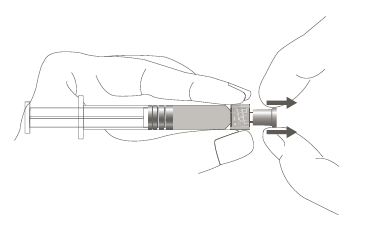 |
| Passaggio 2: Per collegare l'ago alla siringa, ruotare delicatamente l'ago in senso orario nella siringa finché non si avverte una leggera resistenza. | m a c o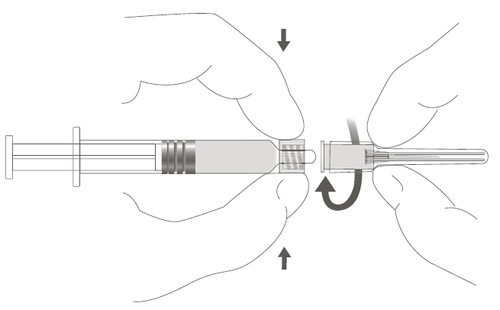 |
Figura B: Siringa Luer Lock con cappuccio rigido
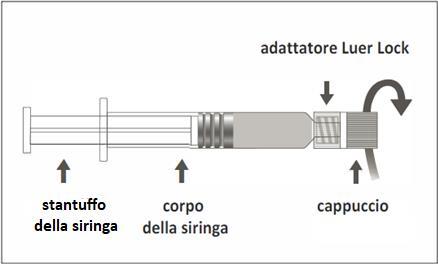
| a i l Passaggio 1: Tenendo l’adattatore Luer Lock a in una mano (evitare di tenere lo stantuffo o il corpo della siringa), togliere il cappuccio t ruotandolo. I | n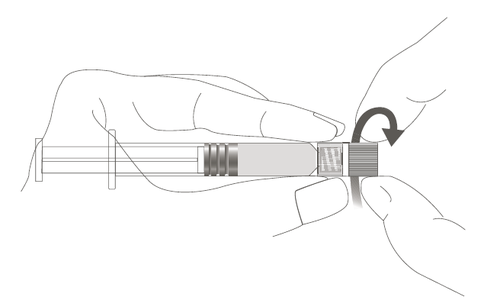 |
| a i z n Passaggio 2: Per collegare l'ago alla siringa, e ruotare delicatamente l'ago nell’adattatore Luer Lock della siringa finché non si avverte g una leggera resistenza. | 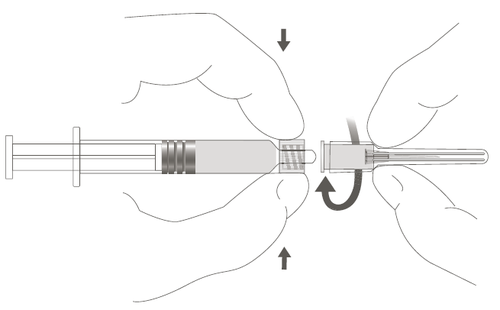 |
Istruzioni per l’uso dell’ago di sicurezza con siringa pre-riempita con Luer Lock:
Seguire i passaggi 1 e 2 sopra per preparare la siringa Luer Lock e l'ago per il posizionamento
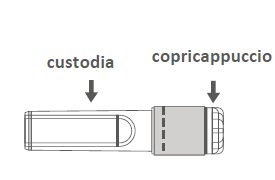
| Figura C: Ago di sicurezza (all'interno della custodia) | o Figura D: Componenti dell'ago di sicurezza (predisposti per l'uso) |
 | r m a c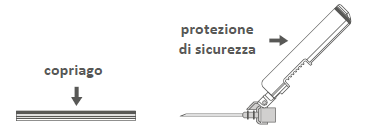 |
F Passaggio 3: Estrarre l'ago di sicurezza dalla custodia. L'ago è coperto dalla protezione di sicurezza e dal copriago. l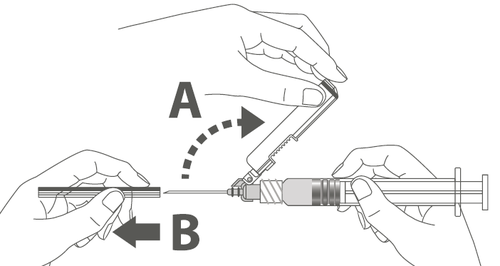 | |
| Passaggio 4: A: Allontanare la protezione di sicurezza dall'ago e dirigerlo verso il corpo della siringa secondo l'angolo mostrato. B: Estrarre il copriago. | n a d e |
| a i l Passaggio 5: Al termine dell'iniezione, bloccare a (attivare) la protezione di sicurezza utilizzando una delle tre (3) tecniche illustrate di attivazione t con una sola mano: superficie, pollice o dita. I Nota: l'attivazione è verificata da un "click" acustico e/o tattile. a | 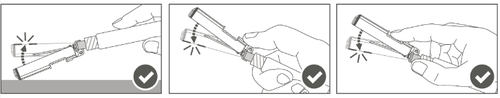 |
| i z n Passaggio 6: Ispezionare visivamente l'attivazione della protezione di sicurezza. La e protezione di sicurezza deve essere completamente bloccata (attivata) come g mostrato nell’Immagine C. A | 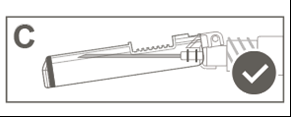 |
Il medicinale non utilizzato e i rifiuti derivati da tale medicinale devono essere smaltiti in conformità alla
normativa locale vigente.
Gli aghi non devono essere rincappucciati.
| L’Immagine D indica che la protezione di sicurezza NON è completamente bloccata (non attivata). | r m a c o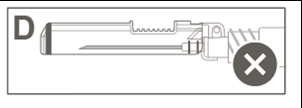 |
| a Attenzione: Non tentare di sbloccare (disattivare) il dispositivo di sicurezza forzando l'ago fuori dalla protezione di sicurezza. | |
-


- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile, 0,5 ML
- Codice ATCJ07AJ52
- Principio attivo
- Prescrizione richiestaNo
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a TRIAXISForma farmaceutica: Sospensione iniettabile, 0,5 MLPrincipio attivo: pertussis, purified antigen, combinations with toxoidsProduttore: GLAXOSMITHKLINE S.P.A.Prescrizione non richiestaForma farmaceutica: Sospensione iniettabile in siringa pre-riempita, 0,5 MLPrincipio attivo: pertussis, purified antigen, combinations with toxoidsProduttore: AJ VACCINES A/SPrescrizione non richiestaForma farmaceutica: Polvere e solvente per soluzione iniettabile, 0,5 MLPrincipio attivo: haemophilus influenzae B, combinations with toxoidsProduttore: SANOFI WINTHROP INDUSTRIEPrescrizione richiesta
Medici online per TRIAXIS
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di TRIAXIS — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per TRIAXIS online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.













