
Come usare CERVARIX
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra traduzioneContenuto del foglietto illustrativo
Cervarix sospensione iniettabile in flaconcino
Vaccino contro il Papillomavirus umano [Tipi 16, 18] (Ricombinante, adiuvato, adsorbito)
Legga attentamente questo foglio prima di usare questo vaccino perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia mai ad altre persone.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Che cos'è Cervarix e a cosa serve
- 2. Cosa deve sapere prima di usare Cervarix
- 3. Come usare Cervarix
- 4. Possibili effetti indesiderati
- 5. Come conservare Cervarix
- 6. Contenuto della confezione e altre informazioni
1. Che cos’è Cervarix e a cosa serve
Cervarix è un vaccino sviluppato per proteggere dalle malattie causate da infezione da Papillomavirus
umani (HPV) a partire dall’età di 9 anni.
Queste malattie comprendono:
- cancro cervicale (cancro della cervice, cioè della parte inferiore dell’utero) e cancro anale,
- lesioni pre-cancerose cervicali, vulvari, vaginali e lesioni anali (modifiche nei genitali o nelle cellule anali che comportano il rischio di evolvere in cancro).
I tipi di Papillomavirus umani (HPV) contenuti nel vaccino (tipi HPV 16 e 18) sono responsabili di
circa il 70% dei casi di cancro cervicale, il 90% dei casi di cancro anale e il 70% delle lesioni pre-
cancerose di vulva e vagina HPV-correlate. Anche altri tipi di HPV possono causare il cancro ano-
genitale. Cervarix non protegge contro tutti i tipi di HPV.
Quando una donna o un uomo vengono vaccinati con Cervarix, il sistema immunitario (il sistema
naturale di difesa del corpo) produce anticorpi contro i ceppi di HPV 16 e 18..
Cervarix non è infettivo e pertanto non può causare le malattie correlate all’infezione da HPV.
Cervarix non cura le malattie correlate all’infezione da HPV già presenti al momento della
vaccinazione.
Cervarix deve essere usato in accordo con le raccomandazioni ufficiali.
2. Cosa deve sapere prima di usare Cervarix
Non usi Cervarix:
- se è allergico ad uno qualsiasi dei principi attivi o a uno qualsiasi dei componenti di questo vaccino (elencati al paragrafo 6). I segni di una reazione allergica possono includere reazione cutanea pruriginosa, sensazione di respiro corto e gonfiore del viso o della lingua.
Avvertenze e precauzioni
Si rivolga al medico o al farmacista prima di ricevere Cervarix:
- se ha un problema di sanguinamento o presenta facilmente lividi;
- se ha una qualsiasi malattia che riduce la sua resistenza alle infezioni come l’infezione da HIV;
- se è affetto da un’infezione grave con temperatura elevata. Può essere necessario rinviare la vaccinazione a dopo la guarigione. Un’infezione lieve come un raffreddore non dovrebbe rappresentare un problema, ma ne parli prima con il medico.
Si può verificare svenimento (soprattutto negli adolescenti) in seguito a, o anche prima di, qualsiasi
iniezione con ago. Pertanto informi il medico o l’infermiere se lei o suo figlio siete svenuti in seguito
ad una precedente iniezione.
Come tutti i vaccini, Cervarix può non proteggere completamente tutte le persone che sono vaccinate.
Cervarix non protegge dalle malattie causate dall’infezione da HPV dei tipi 16 o 18 se le persone sono
già infettate dal Papillomavirus umano di tipo 16 o 18 al momento della vaccinazione.
Anche se la vaccinazione può proteggere contro il cancro della cervice uterina, essa non sostituisce il
regolare controllo della cervice uterina. La persona vaccinata deve continuare a seguire i consigli del
medico riguardo allo striscio vaginale/Pap test (test per controllare i cambiamenti delle cellule della
cervice causati dall’infezione da HPV) e sulle misure di prevenzione e di protezione.
Dato che Cervarix non protegge contro tutti i tipi di Papillomavirus umano, la persona vaccinata deve
continuare ad adottare le appropriate precauzioni contro l’esposizione al virus dell’HPV e contro le
malattie sessualmente trasmissibili.
Cervarix non protegge contro altre malattie non causate dal Papillomavirus umano.
Altri medicinali e Cervarix
Cervarix può essere somministrato con un altro vaccino di richiamo combinato contro difterite (d),
tetano (T) e pertosse [acellulare] (pa) con o senza virus della poliomielite inattivato (IPV), (vaccini
dTpa, dTpa-IPV), con un vaccino combinato contro l’epatite A e l’epatite B (Twinrix), con un
vaccino contro l'epatite B (Engerix B), o con un vaccino meningococcico sierogruppo A, C, W-135, Y
coniugato con tossoide tetanico (MenACWY-TT), in un sito di iniezione distinto (un'altra parte del
corpo, ad esempio l’altro braccio) durante la stessa visita.
Cervarix può non raggiungere un effetto ottimale se impiegato con altri medicinali che sopprimono il
sistema immunitario.
Negli studi clinici, i contraccettivi orali (ad esempio la pillola) non hanno ridotto la protezione ottenuta
con Cervarix.
Informi il medico se sta assumendo, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale, o se è stato vaccinato di recente con qualsiasi altro vaccino.
Gravidanza, allattamento e fertilità
Se è in corso una gravidanza, se la gravidanza si verifica durante il ciclo di vaccinazione o se sta
pianificando una gravidanza, si raccomanda di rimandare o interrompere la vaccinazione fino al
completamento della gravidanza.
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con latte
materno, chieda consiglio al medico prima di usare questo vaccino.
Guida di veicoli e utilizzo di macchinari
Cervarix non è in grado di influenzare la capacità di guidare o utilizzare macchinari. Tuttavia, non
guidi o non utilizzi macchinari se si sente poco bene.
Cervarix contiene cloruro di sodio
Questo medicinale contiene meno di 1mmol (23 mg) di sodio per dose, cioè essenzialmente “senza
sodio”.
3. Come usare Cervarix
Come viene somministrato il vaccino
Il medico o l’infermiere somministrerà Cervarix mediante iniezione intramuscolare nella parte
superiore del braccio.
Quante volte viene somministrato
Cervarix è indicato per l’uso dai 9 anni di età.
Il numero totale di iniezioni che riceverà dipende dalla sua età al momento della prima iniezione:
Se lei ha un’età compresa tra i 9 e i 14 anni
riceverà due iniezioni:
Prima iniezione: alla data stabilita
Seconda iniezione: tra i 5 e i 13 mesi dopo la prima iniezione
Se lei ha un’età pari o superiore a 15 anni
riceverà 3 iniezioni:
Prima iniezione: alla data stabilita
Seconda iniezione: 1 mese dopo la prima iniezione
Terza iniezione: 6 mesi dopo la prima iniezione
Se necessario, la schedula di vaccinazione può essere più flessibile. Parli con il medico per maggiori
informazioni.
Quando Cervarix viene somministrato come prima dose, si raccomanda che Cervarix (e non un altro
vaccino contro il virus HPV) venga somministrato per il ciclo completo di vaccinazione.
Cervarix non è raccomandato per l’uso sotto i 9 anni di età.
Il vaccino non deve mai essere somministrato in vena.
Se salta una dose
È importante che segua le istruzioni ricevute dal medico o dall’infermiere circa le visite per le
somministrazioni successive. Se dimentica di tornare per la somministrazione alla data fissata, chieda
consiglio al medico.
Se non termina il ciclo completo di vaccinazione (due o tre iniezioni in funzione dell’età al momento
della vaccinazione), può non ottenere la risposta e la protezione ottimali.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo vaccino può causare effetti indesiderati sebbene non tutte le persone li
manifestino.
Gli effetti indesiderati che si sono verificati durante gli studi clinici condotti con Cervarix sono i
seguenti:
♦ Molto comuni (più frequenti di 1 ogni 10 dosi di vaccino):
♦ dolore o fastidio al sito di iniezione
- arrossamento o gonfiore al sito di iniezione
- mal di testa ♦ dolore muscolare, dolore o debolezza muscolare (non causati da esercizio fisico) ♦ stanchezza
♦ Comuni (meno frequenti di 1 ogni 10 dosi di vaccino ma più frequenti di 1 ogni 100):
♦ sintomi gastrointestinali inclusi nausea, vomito, diarrea e dolore addominale
♦ prurito, arrossamento della pelle, orticaria
♦ dolore alle articolazioni
♦ febbre (temperatura uguale o superiore a 38°C)
♦ Non comuni (meno frequenti di 1 ogni 100 dosi di vaccino ma più frequenti di 1 ogni 1.000):
- infezioni del tratto respiratorio superiore (infezione del naso, della gola o della trachea)
- capogiri
- altre reazioni al sito di iniezione come indurimento, formicolio o intorpidimento.
Gli effetti indesiderati che sono stati riportati durante la commercializzazione di Cervarix includono:
- reazioni allergiche. Queste possono essere riconosciute tramite: eritema pruriginoso alle mani e ai piedi, gonfiore agli occhi e al viso, difficoltà a respirare o a deglutire, improvviso calo della pressione sanguigna e perdita di coscienza. Queste reazioni avvengono solitamente prima di lasciare lo studio medico. Tuttavia se suo figlio dovesse avere uno qualsiasi di questi sintomi contatti urgentemente un medico.
- gonfiore delle ghiandole del collo, delle ascelle o dell’inguine
- svenimento talvolta accompagnato da tremore o rigidità.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione riportato nell’allegato V*.
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza di
questo medicinale.
5. Come conservare Cervarix
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla confezione. La data di
scadenza si riferisce all’ultimo giorno del mese.
Conservare in frigorifero (2°C–8°C).
Non congelare.
Conservare nella confezione originale per proteggere il medicinale dalla luce.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Cervarix
- I principi attivi sono:
Proteina L1 del Papillomavirus umano di tipo 16 20 microgrammi
Proteina L1 del Papillomavirus umano di tipo 18 20 microgrammi
Papillomavirus umano = HPV
adiuvato con AS04 contenente:
- 3- O-desacyl-4’-monofosforyl lipide A (MPL) 50 microgrammi
adsorbito su alluminio idrossido, idrato (Al(OH) ) 0,5 milligrammi Al in totale
Proteina L1 nella forma di particelle non infettive simili al virus (VLPs) prodotte mediante
tecnologia del DNA ricombinante impiegando un sistema di espressione del Baculovirus che usa
cellule Hi-5 Rix 4446 derivate dall’insetto Trichoplusia ni.
- Gli altri componenti sono sodio cloruro (NaCl), sodio fosfato monobasico diidrato (NaH PO .2H O) e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Cervarix e contenuto della confezione
Sospensione iniettabile.
Cervarix è una sospensione bianca torbida.
Cervarix è disponibile in flaconcini da 1 dose (0,5 ml) in confezioni da 1, 10 e 100 pezzi.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart, Belgio
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
Belgique/België/Belgien
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
Lietuva
GlaxoSmithKline Biologicals SA
Tel: +370 80000334
България
GlaxoSmithKline Biologicals Тел. +359
80018205
Luxembourg/Luxemburg
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
Česká republika
GlaxoSmithKline s.r.o.
Tel: + 420 2 22 00 11 11
[email protected]
Magyarország
GlaxoSmithKline Biologicals SA
Tel.: +36 80088309
Danmark
GlaxoSmithKline Pharma A/S
Tlf: + 45 36 35 91 00
Malta
GlaxoSmithKline Biologicals SATel: +356
80065004
[email protected]
Deutschland
GlaxoSmithKline GmbH & Co. KG
Tel: + 49 (0)89 360448701
[email protected]
Nederland
GlaxoSmithKline BV
Tel: + 31 (0)33 2081100
Norge
GlaxoSmithKline AS
Tlf: + 47 22 70 20 00
Ελλάδα
GlaxoSmithKline Μονοπρόσωπη A.E.B.E
Tηλ: + 30 210 68 82 100
Eesti
GlaxoSmithKline Biologicals SATel: +372
8002640
Österreich
GlaxoSmithKline Pharma GmbH.
Tel: + 43 (0)1 97075 0
[email protected]
España
GlaxoSmithKline, S.A.
Tel: + 34 900 202 700
[email protected]
Polska
GSK Services Sp. z o.o.
Tel.: + 48 (22) 576 9000
France
Laboratoire GlaxoSmithKline
Tél: + 33 (0) 1 39 17 84 44
[email protected]
Hrvatska
GlaxoSmithKline Biologicals SA
Tel.: +385 800787089
Portugal
GlaxoSmithKline - Produtos Farmacêuticos, Lda.
Tel: + 351 21 412 95 00
[email protected]
România
GlaxoSmithKline Biologicals SATel: +40
800672524
Ireland
GlaxoSmithKline (Ireland) Ltd
Tel: + 353 (0)1 495 5000
Slovenija
GlaxoSmithKline Biologicals SATel: +386
80688869
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
GlaxoSmithKline Biologicals SATel: +421
800500589
Italia
GlaxoSmithKline S.p.A.
Tel: + 39 (0)45 7741 111
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Κύπρος
GlaxoSmithKline Biologicals SAΤηλ: +357
80070017
Sverige
GlaxoSmithKline AB
Tel: + 46 (0)8 638 93 00
[email protected]
Latvija
GlaxoSmithKline Biologicals SATel: +371
80205045
United Kingdom (Irlanda del Nord)
GlaxoSmithKline Biologicals SA
Tel: +44(0)800 221441
[email protected]
Altre fonti di informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia Europea
dei Medicinali: http://www.ema.europa.eu/.
-------------------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Cervarix deve essere somministrato il prima possibile dopo essere stato rimosso dal frigorifero.
Tuttavia, è stata dimostrata stabilità quando conservato fuori dal frigorifero fino a 3 giorni a
temperatura compresa tra 8°C e 25°C o fino ad 1 giorno a temperatura compresa tra 25°C e 37°C. Se
non utilizzato al termine di questo periodo il vaccino deve essere eliminato.
Durante la conservazione del flaconcino si può osservare un deposito bianco fine con un surnatante
chiaro incolore. Ciò non costituisce segno di deterioramento.
Il contenuto del flaconcino deve essere ispezionato visivamente sia prima che dopo l’agitazione per
verificare l’assenza di qualsiasi particella estranea e/o aspetto fisico anormale, prima di effettuare la
somministrazione.
In caso si riscontri una qualsiasi di tali condizioni, eliminare il vaccino.
Il vaccino deve essere agitato bene prima dell’uso.
Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
Cervarix sospensione iniettabile, flaconcino multidose
Vaccino contro il Papillomavirus umano [Tipi 16, 18] (Ricombinante, adiuvato, adsorbito)
Legga attentamente questo foglio prima di usare questo vaccino perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia mai ad altrie persone.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Che cos'è Cervarix e a cosa serve
- 2. Cosa deve sapere prima di usare Cervarix
- 3. Come usare Cervarix
- 4. Possibili effetti indesiderati
- 5. Come conservare Cervarix
- 6. Contenuto della confezione e altre informazioni
1. Che cos’è Cervarix e a cosa serve
Cervarix è un vaccino sviluppato per proteggere dalle malattie causate da infezione da Papillomavirus
umani (HPV) a partire dall’età di 9 anni.
Queste malattie comprendono:
- cancro cervicale (cancro della cervice, cioè della parte inferiore dell’utero) e cancro anale,
- lesioni pre-cancerose cervicali, vulvari, vaginali e lesioni anali (modifiche nei genitali o nelle cellule anali che comportano il rischio di evolvere in cancro).
I tipi di Papillomavirus umani (HPV) contenuti nel vaccino (tipi HPV 16 e 18) sono responsabili di
circa il 70% dei casi di cancro cervicale, il 90% dei casi di cancro anale e il 70% delle lesioni pre-
cancerose di vulva e vagina HPV-correlate. Anche altri tipi di HPV possono causare il cancro ano-
genitale. Cervarix non protegge contro tutti i tipi di HPV.
Quando una donna o un uomo vengono vaccinati con Cervarix, il sistema immunitario (il sistema
naturale di difesa del corpo) produce anticorpi contro i ceppi di HPV 16 e 18..
Cervarix non è infettivo e pertanto non può causare le malattie correlate all’infezione da HPV.
Cervarix non cura le malattie correlate all’infezione da HPV già presenti al momento della
vaccinazione.
Cervarix deve essere usato in accordo con le raccomandazioni ufficiali.
2. Cosa deve sapere prima di usare Cervarix
Non usi Cervarix:
- se è allergica ad uno qualsiasi dei principi attivi o a uno qualsiasi dei componenti di questo vaccino (elencati al paragrafo 6). I segni di una reazione allergica possono includere reazione cutanea pruriginosa, sensazione di respiro corto e gonfiore del viso o della lingua.
Avvertenze e precauzioni
Si rivolga al medico o al farmacista prima di ricevere Cervarix:
- se ha un problema di sanguinamento o presenta facilmente lividi;
- se ha una qualsiasi malattia che riduce la sua resistenza alle infezioni come l’infezione da HIV;
- se è affetta da un’ infezione grave con temperatura elevata. Può essere necessario rinviare la vaccinazione a dopo la guarigione. Un’infezione lieve come un raffreddore non dovrebbe rappresentare un problema, ma ne parli prima con il medico.
Si può verificare svenimento (soprattutto negli adolescenti) in seguito a, o anche prima di, qualsiasi
iniezione con ago. Pertanto informi il medico o l’infermiere se lei o suo figlio siete svenuti in seguito
ad una precedente iniezione.
Come tutti i vaccini, Cervarix può non proteggere completamente tutte le persone che sono vaccinate.
Cervarix non protegge dalle malattie causate dall’infezione da HPV dei tipi 16 o 18 se le persone sono
già infettate dal Papillomavirus umano di tipo 16 o 18 al momento della vaccinazione.
Anche se la vaccinazione può proteggere contro il cancro della cervice uterina, essa non sostituisce il
regolare controllo della cervice uterina. La persona vaccinata deve continuare a seguire i consigli del
medico sullo striscio vaginale/Pap test (test per controllare i cambiamenti delle cellule della cervice
causati dall’infezione da HPV) e sulle misure di prevenzione e di protezione.
Dato che Cervarix non protegge contro tutti i tipi di Papillomavirus umano, la persona vaccinata deve
continuare ad adottare le appropriate precauzioni contro l’esposizione al virus dell’HPV e contro le
malattie sessualmente trasmissibili.
Cervarix non protegge contro altre malattie non causate dal Papillomavirus umano.
Altri medicinali e Cervarix
Cervarix può essere somministrato con un altro vaccino di richiamo combinato contro difterite (d),
tetano (T) e pertosse [acellulare] (pa) con o senza virus della poliomielite inattivato (IPV), (vaccini
dTpa, dTpa-IPV), con un vaccino combinato contro epatite A ed epatite B (Twinrix), con un vaccino
contro epatite B (Engerix B), o con un vaccino meningococcico sierogruppo A, C, W-135, Y
coniugato con tossoide tetanico (MenACWY-TT), in un sito di iniezione distinto (un'altra parte del
corpo, ad esempio l’altro braccio) durante la stessa visita.
Cervarix può non raggiungere un effetto ottimale se impiegato con altri medicinali che sopprimono il
sistema immunitario.
Negli studi clinici, i contraccettivi orali (es. la pillola) non hanno ridotto la protezione ottenuta con
Cervarix.
Informi il medico se sta assumento, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale, o se è stato vaccinato di recente con qualsiasi altro vaccino.
Gravidanza, allattamento e fertilità
Se è in corso una gravidanza, se la gravidanza si verifica durante il ciclo di vaccinazione o se sta
pianificando una gravidanza, si raccomanda di rimandare o interrompere la vaccinazione fino al
completamento della gravidanza.
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con latte
materno, chieda consiglio al medico prima di usare questo vaccino.
Guida di veicoli e utilizzo di macchinari
Cervarix non è in grado di influenzare la capacità di guidare o utilizzare macchinari. Tuttavia, non
guidi o non utilizzi macchinari se si sente poco bene.
Cervarix contiene cloruro di sodio
Questo medicinale contiene meno di 1mmol (23 mg) di sodio per dose, cioè essenzialmente “senza
sodio”.
3. Come usare Cervarix
Come viene somministrato il vaccino
Il medico o l’infermiere somministrerà Cervarix mediante iniezione intramuscolare nella parte
superiore del braccio.
Quante volte viene somministrato
Cervarix è indicato per l’uso dai 9 anni di età.
Il numero totale di iniezioni che riceverà dipende dalla sua età al momento della prima iniezione:
Se lei ha un’età compresa tra i 9 e i 14 anni
riceverà 2 iniezioni:
Prima iniezione: alla data stabilita
Seconda iniezione: tra 5 e 13 mesi dopo la prima iniezione
Se lei ha 15 anni o più
riceverà 3 iniezioni:
Prima iniezione: alla data stabilita
Seconda iniezione: 1 mese dopo la prima iniezione
Terza iniezione: 6 mesi dopo la prima iniezione
Se necessario, la schedula di vaccinazione può essere più flessibile. Parli con il medico per maggiori
informazioni.
Quando Cervarix viene somministrato come prima dose, si raccomanda che Cervarix (e non un altro
vaccino contro il virus HPV) venga somministrato per il ciclo completo di vaccinazione.
Cervarix non è raccomandato per l’uso sotto i 9 anni di età.
Il vaccino non deve mai essere somministrato in vena.
Se salta una dose
È importante che segua le istruzioni ricevute dal medico o dall’infermiere circa le visite per le
somministrazioni successive. Se dimentica di tornare per la somministrazione alla data fissata, chieda
consiglio al medico.
Se non termina il ciclo completo di vaccinazione (due o tre iniezioni in funzione dell’età al momento
della vaccinazione), può non ottenere la risposta e la protezione ottimali.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo vaccino può causare effetti indesiderati sebbene non tutte le persone li
manifestino.
Gli effetti indesiderati che si sono verificati durante gli studi clinici condotti con Cervarix sono i
seguenti:
♦ Molto comuni (più frequenti di 1 ogni 10 dosi di vaccino):
♦ dolore o fastidio al sito di iniezione
- arrossamento o gonfiore al sito di iniezione
- mal di testa ♦ dolore muscolare, dolore o debolezza muscolare (non causati da esercizio fisico) ♦ stanchezza
♦ Comuni (meno frequenti di 1 ogni 10 dosi di vaccino ma più frequenti di 1 ogni 100):
♦ sintomi gastrointestinali inclusi nausea, vomito, diarrea e dolore addominale
♦ prurito, arrossamento della pelle, orticaria
♦ dolore alle articolazioni
♦ febbre (temperatura uguale o superiore a 38°C)
♦ Non comuni (meno frequenti di 1 ogni 100 dosi di vaccino ma più frequenti di 1 ogni 1.000):
- infezioni del tratto respiratorio superiore (infezione del naso, della gola o della trachea)
- capogiri
- altre reazioni al sito di iniezione come indurimento, formicolio o intorpidimento.
Gli effetti indesiderati che sono stati riportati durante la commercializzazione di Cervarix includono:
- reazioni allergiche. Queste possono essere riconosciute tramite: eritema pruriginoso alle mani e ai piedi, gonfiore agli occhi e al viso, difficoltà a respirare o a deglutire, improvviso calo della pressione sanguigna e perdita di coscienza. Queste reazioni avvengono solitamente prima di lasciare lo studio medico. Tuttavia se suo figlio dovesse avere uno qualsiasi di questi sintomi contatti urgentemente un medico.
- gonfiore delle ghiandole del collo, delle ascelle o dell’inguine
- svenimento talvolta accompagnato da tremore o rigidità.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione riportato nell’allegato V*.
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza di
questo medicinale.
5. Come conservare Cervarix
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla confezione. La data di
scadenza si riferisce all’ultimo giorno del mese.
Conservare in frigorifero (2°C–8°C).
Non congelare.
Conservare nella confezione originale per proteggere il medicinale dalla luce.
Si raccomanda l’utilizzo immediato dopo la prima apertura. Se non viene utilizzato immediatamente, il
vaccino deve essere conservato in frigorifero (2°C-8°C). Se non viene utilizzato entro 6 ore esso deve
essere scartato.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Cervarix
- I principi attivi sono:
Proteina L1 del Papillomavirus umano di tipo 16 20 microgrammi
Proteina L1 del Papillomavirus umano di tipo 18 20 microgrammi
Papillomavirus umano = HPV
adiuvato con AS04 contenente:
- 3- O-desacyl-4’- monofosforyl lipide A (MPL) 50 microgrammi
adsorbito su alluminio idrossido, idrato (Al(OH) ) 0,5 milligrammi Al in totale
Proteina L1 nella forma di particelle non infettive simili al virus (VLPs) prodotte mediante
tecnologia del DNA ricombinante impiegando un sistema di espressione del Baculovirus che usa
cellule Hi-5 Rix 4446 derivate dall’insetto Trichoplusia ni.
- Gli altri componenti sono sodio cloruro (NaCl), sodio fosfato monobasico diidrato (NaH PO .2H O) e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Cervarix e contenuto della confezione
Sospensione iniettabile.
Cervarix è una sospensione bianca torbida.
Cervarix è disponibile in flaconi da 2 dosi (1 ml) in confezioni da 1, 10 e 100 pezzi.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart, Belgio
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
Belgique/België/Belgien
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
Lietuva
GlaxoSmithKline Biologicals SATel: +370
80000334
България
GlaxoSmithKline Biologicals SAТел. +359
80018205
Luxembourg/Luxemburg
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
Česká republika
GlaxoSmithKline s.r.o.
Tel: + 420 2 22 00 11 11
[email protected]
Magyarország
GlaxoSmithKline Biologicals SATel.: +36
80088309
Danmark
GlaxoSmithKline Pharma A/S
Tlf: + 45 36 35 91 00
[email protected]
Malta
GlaxoSmithKline Biologicals SATel: +356
80065004
Deutschland
GlaxoSmithKline GmbH & Co. KG
Tel: + 49 (0)89 360448701
[email protected]
Nederland
GlaxoSmithKline BV
Tel: + 31 (0)33 2081100
Norge
GlaxoSmithKline AS
Tlf: + 47 22 70 20 00
Ελλάδα
GlaxoSmithKline Μονοπρόσωπη A.E.B.E
Tηλ: + 30 210 68 82 100
Eesti
GlaxoSmithKline Biologicals SA
Tel: +372 8002640
Österreich
GlaxoSmithKline Pharma GmbH.
Tel: + 43 (0)1 97075 0
[email protected]
España
GlaxoSmithKline, S.A.
Tel: + 34 900 202 700
[email protected]
Polska
GSK Services Sp. z o.o.
Tel.: + 48 (22) 576 9000
Portugal
GlaxoSmithKline - Produtos Farmacêuticos, Lda.
Tel: + 351 21 412 95 00
[email protected]
România
GlaxoSmithKline Biologicals SATel: +40
800672524
Ireland
GlaxoSmithKline (Ireland) Ltd
Tel: + 353 (0)1 495 5000
France
Laboratoire GlaxoSmithKline
Tél: + 33 (0) 1 39 17 84 44
[email protected]
Hrvatska
GlaxoSmithKline Biologicals SATel.: +385
800787089
Slovenija
GlaxoSmithKline Biologicals SATel: +386
80688869
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
GlaxoSmithKline Biologicals SATel: +421
800500589
Italia
GlaxoSmithKline S.p.A.
Tel: + 39 (0)45 7741 111
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Κύπρος
GlaxoSmithKline Biologicals SAΤηλ: +357
80070017
Sverige
GlaxoSmithKline AB
Tel: + 46 (0)8 638 93 00
[email protected]
Latvija
GlaxoSmithKline Biologicals SATel: +371
80205045
United Kingdom (Irlanda del Nord)
GlaxoSmithKline Biologicals SA
Tel: +44 (0)800 221 441
[email protected]
Altre fonti di informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’ Agenzia Europea
dei Medicinali: http://www.ema.europa.eu/.
-------------------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Cervarix deve essere somministrato il prima possibile dopo essere stato rimosso dal frigorifero.
Tuttavia, è stata dimostrata stabilità quando conservato fuori dal frigorifero fino a 3 giorni a
temperatura compresa tra 8°C e 25°C o fino ad 1 giorno a temperatura compresa tra 25°C e 37°C. Se
non utilizzato al termine di questo periodo il vaccino deve essere eliminato.
Durante la conservazione del flaconcino si può osservare un deposito bianco fine con un surnatante
chiaro incolore. Ciò non costituisce segno di deterioramento.
Il contenuto del flaconcino deve essere ispezionato visivamente sia prima che dopo l’agitazione per
verificare l’assenza di qualsiasi particella estranea e/o aspetto fisico anormale, prima di effettuare la
somministrazione.
In caso si riscontri una qualsiasi di tali condizioni, eliminare il vaccino.
Il vaccino deve essere agitato bene prima dell’uso.
Quando viene utilizzato il flaconcino multidose, ogni dose da 0,5 ml deve essere aspirata utilizzando
un ago e una siringa sterili; devono essere prese precauzioni in modo da evitare la contaminazione del
contenuto.
Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
Cervarix sospensione iniettabile in siringa preriempita
Vaccino contro il Papillomavirus umano [Tipi 16, 18] (Ricombinante, adiuvato, adsorbito)
Legga attentamente questo foglio prima di usare questo vaccino perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia mai ad altre persone.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Che cos'è Cervarix e a cosa serve
- 2. Cosa deve sapere prima di usare Cervarix
- 3. Come usare Cervarix
- 4. Possibili effetti indesiderati
- 5. Come conservare Cervarix
- 6. Contenuto della confezione e altre informazioni
1. Che cos’è Cervarix e a cosa serve
Cervarix è un vaccino sviluppato per proteggere dalle malattie causate da infezione da Papillomavirus
umani (HPV) a partire dall’età di 9 anni.
Queste malattie comprendono:
- cancro cervicale (cancro della cervice, cioè della parte inferiore dell’utero) e cancro anale,
- lesioni pre-cancerose cervicali, vulvari, vaginali e lesioni anali (modifiche nei genitali o nelle cellule anali che comportano il rischio di evolvere in cancro).
I tipi di Papillomavirus umani (HPV) contenuti nel vaccino (tipi HPV 16 e 18) sono responsabili di
circa il 70% dei casi di cancro cervicale, il 90% dei casi di cancro anale e il 70% delle lesioni pre-
cancerose di vulva e vagina HPV-correlate. Anche altri tipi di HPV possono causare il cancro ano-
genitale. Cervarix non protegge contro tutti i tipi di HPV.
Quando una donna o un uomo vengono vaccinati con Cervarix, il sistema immunitario (il sistema
naturale di difesa del corpo) produce anticorpi contro i ceppi di HPV 16 e 18.
Cervarix non è infettivo e pertanto non può causare le malattie correlate all’infezione da HPV.
Cervarix non cura le malattie correlate all’infezione da HPV già presenti al momento della
vaccinazione.
Cervarix deve essere usato in accordo con le raccomandazioni ufficiali.
2. Cosa deve sapere prima di usare Cervarix
Non usi Cervarix:
- se è allergica ad uno qualsiasi dei principi attivi o a uno qualsiasi dei componenti di questo vaccino (elencati al paragrafo 6). I segni di una reazione allergica possono includere reazione cutanea pruriginosa, sensazione di respiro corto e gonfiore del viso o della lingua.
Avvertenze e precauzioni
Si rivolga al medico o al farmacista prima di ricevere Cervarix:
- se ha un problema di sanguinamento o presenta facilmente lividi;
- se ha una qualsiasi malattia che riduce la sua resistenza alle infezioni come l’infezione da HIV;
- se è affetto da un’ infezione grave con temperatura elevata. Può essere necessario rinviare la vaccinazione a dopo la guarigione. Un’ infezione lieve come un raffreddore non dovrebbe rappresentare un problema, ma ne parli prima con il medico.
Si può verificare svenimento (soprattutto negli adolescenti) in seguito a, o anche prima di, qualsiasi
iniezione con ago. Pertanto informi il medico o l’infermiere se lei o suo figlio siete svenuti in seguito
ad una precedente iniezione.
Come tutti i vaccini, Cervarix può non proteggere completamente tutte le persone che sono vaccinate.
Cervarix non protegge dalle malattie causate dall’infezione da HPV dei tipi 16 o 18 se le persone sono
già infettate dal Papillomavirus umano di tipo 16 o 18 al momento della vaccinazione.
Anche se la vaccinazione può proteggere contro il cancro della cervice uterina, essa non sostituisce il
regolare controllo della cervice uterina. La persona vaccinata deve continuare a seguire i consigli del
medico sullo striscio vaginale/Pap test (test per controllare i cambiamenti delle cellule della cervice
causati dall’infezione da HPV) e sulle misure di prevenzione e di protezione.
Dato che Cervarix non protegge contro tutti i tipi di Papillomavirus umano, la persona vaccinata deve
continuare ad adottare le appropriate precauzioni contro l’esposizione al virus dell’HPV e contro le
malattie sessualmente trasmissibili.
Cervarix non protegge contro altre malattie non causate dal Papillomavirus umano.
Altri medicinali e Cervarix
Cervarix può essere somministrato con un altro vaccino di richiamo combinato contro difterite (d),
tetano (T) e pertosse [acellulare] (pa) con o senza virus della poliomielite inattivato (IPV), (vaccini
dTpa, dTpa-IPV), con un vaccino combinato contro epatite A ed epatite B (Twinrix) , con un vaccino
contro epatite B (Engerix B o con un vaccino meningococcico sierogruppo A, C, W-135, Y coniugato
con tossoide tetanico (MenACWY-TT), in un sito di iniezione distinto (un'altra parte del corpo, ad
esempio l’altro braccio) durante la stessa visita.
Cervarix può non raggiungere un effetto ottimale se impiegato con altri medicinali che sopprimono il
sistema immunitario.
Negli studi clinici, i contraccettivi orali (ad esempio la pillola) non hanno ridotto la protezione ottenuta
con Cervarix.
Informi il medico se sta assumendo, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale, o se è stato vaccinato di recente con qualsiasi altro vaccino.
Gravidanza, allattamento e fertilità
Se è in corso una gravidanza, se la gravidanza si verifica durante il ciclo di vaccinazione o se sta
pianificando una gravidanza, si raccomanda di rimandare o interrompere la vaccinazione fino al
completamento della gravidanza.
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con latte
materno, chieda consiglio al medico prima di usare questo vaccino.
Guida di veicoli e utilizzo di macchinari
Cervarix non è in grado di influenzare la capacità di guidare o utilizzare macchinari. Tuttavia, non
guidi o non utilizzi macchinari se si sente poco bene.
Cervarix contiene cloruro di sodio
Questo medicinale contiene meno di 1mmol (23 mg) di sodio per dose, cioè essenzialmente “senza
sodio”.
3. Come usare Cervarix
Come viene somministrato il vaccino
Il medico o l’infermiere somministrerà Cervarix mediante iniezione intramuscolare nella parte
superiore del braccio.
Quante volte viene somministrato
Cervarix è indicato per l’uso dai 9 anni di età.
Il numero totale di iniezioni che riceverà dipende dalla sua età al momento della prima iniezione:
Se lei ha un’età compresa tra i 9 e i 14 anni
riceverà 2 iniezioni:
Prima iniezione: alla data stabilita
Seconda iniezione: tra i 5 e i 13 mesi dopo la prima iniezione
Se lei ha 15 anni o più
riceverà 3 iniezioni:
Prima iniezione: alla data stabilita
Seconda iniezione: 1 mese dopo la prima iniezione
Terza iniezione: 6 mesi dopo la prima iniezione
Se necessario, la schedula di vaccinazione può essere più flessibile. Parli con il medico per maggiori
informazioni.
Quando Cervarix viene somministrato come prima dose, si raccomanda che Cervarix (e non un altro
vaccino contro il virus HPV) venga somministrato per il ciclo completo di vaccinazione.
Cervarix non è raccomandato per l’uso sotto i 9 anni di età.
Il vaccino non deve mai essere somministrato in vena.
Se salta una dose
È importante che segua le istruzioni ricevute dal medico o dall’infermiere circa le visite per le
somministrazioni successive. Se dimentica di tornare per la somministrazione alla data fissata, chieda
consiglio al medico.
Se non termina il ciclo completo di vaccinazione (due o tre iniezioni in funzione dell’età al momento
della vaccinazione), può non ottenere la risposta e la protezione ottimali.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo vaccino può causare effetti indesiderati sebbene non tutte le persone li
manifestino.
Gli effetti indesiderati che si sono verificati durante gli studi clinici condotti con Cervarix sono i
seguenti:
♦ Molto comuni (più frequenti di 1 ogni 10 dosi di vaccino): dolore o fastidio al sito di iniezione,
arrossamento o gonfiore al sito di iniezione, mal di testa, dolore muscolare, dolore o debolezza
muscolare (non causati da esercizio fisico), stanchezza.
♦ Comuni (meno frequenti di 1 ogni 10 dosi di vaccino ma più frequenti di 1 ogni 100): sintomi
gastrointestinali inclusi nausea, vomito, diarrea e dolore addominale, prurito, arrossamento della
pelle, orticaria, dolore alle articolazioni, febbre (temperatura uguale o superiore a 38°C).
- Non comuni (meno frequenti di 1 ogni 100 dosi di vaccino ma più frequenti di 1 ogni 1.000): infezioni del tratto respiratorio superiore (infezione del naso, della gola o della trachea), capogiri, altre reazioni al sito di iniezione come indurimento, formicolio o intorpidimento.
Gli effetti indesiderati che sono stati riportati durante la commercializzazione di Cervarix includono:
- reazioni allergiche. Queste possono essere riconosciute tramite: eritema pruriginoso alle mani e ai piedi, gonfiore agli occhi e al viso, difficoltà a respirare o a deglutire, improvviso calo della pressione sanguigna e perdita di coscienza. Queste reazioni avvengono solitamente prima di lasciare lo studio medico. Tuttavia se suo figlio dovesse avere uno qualsiasi di questi sintomi contatti urgentemente un medico.
- gonfiore delle ghiandole del collo, delle ascelle o dell’inguine
- svenimento talvolta accompagnato da tremore o rigidità.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione riportato nell’allegato V.*.
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza di
questo medicinale.
5. Come conservare Cervarix
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla confezione. La data di
scadenza si riferisce all’ultimo giorno del mese.
Conservare in frigorifero (2°C–8°C).
Non congelare.
Conservare nella confezione originale per proteggere il medicinale dalla luce.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Cervarix
- I principi attivi sono:
Proteina L1 del Papillomavirus umano di tipo 16 20 microgrammi
Proteina L1 del Papillomavirus umano di tipo 18 20 microgrammi
Papillomavirus umano = HPV
adiuvato con AS04 contenente:
- 3- O-desacyl-4’-monofosforyl lipide A (MPL) 50 microgrammi
adsorbito su alluminio idrossido, idrato (Al(OH) ) 0,5 milligrammi Al in
totale
Proteina L1 nella forma di particelle non infettive simili al virus (VLPs) prodotte mediante
tecnologia del DNA ricombinante impiegando un sistema di espressione del Baculovirus che usa
cellule Hi-5 Rix 4446 derivate dall’insetto Trichoplusia ni.
- Gli altri componenti sono sodio cloruro (NaCl), sodio fosfato monobasico diidrato (NaH PO .2H O) e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Cervarix e contenuto della confezione
Sospensione iniettabile in siringa preriempita.
Cervarix è una sospensione bianca torbida.
Cervarix è disponibile in siringhe preriempite da 1 dose con o senza aghi separati in confezioni da 1 e
- 10.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart, Belgio
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
Belgique/België/Belgien
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
Lietuva
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
България
GlaxoSmithKline Biologicals SA
Тел. +359 80018205
Luxembourg/Luxemburg
GlaxoSmithKline Pharmaceuticals SA./NV
Tél/Tel: + 32 10 85 52 00
Česká republika
GlaxoSmithKline s.r.o.
Tel: + 420 2 22 00 11 11
[email protected]
Magyarország
GlaxoSmithKline Biologicals SA
Tel.: +36 80088309
Danmark
GlaxoSmithKline Pharma A/S
Tlf: + 45 36 35 91 00
[email protected]
Malta
GlaxoSmithKline Biologicals SA
Tel: +356 80065004
Deutschland
GlaxoSmithKline GmbH & Co. KG
Tel: + 49 (0)89 360448701
Nederland
GlaxoSmithKline BV
Tel: + 31 (0)33 2081100
[email protected]
Eesti
GlaxoSmithKline Biologicals SA
Tel: +372 8002640
Norge
GlaxoSmithKline AS
Tlf: + 47 22 70 20 00
Ελλάδα
GlaxoSmithKline Μονοπρόσωπη A.E.B.E
Tηλ: + 30 210 68 82 100
Österreich
GlaxoSmithKline Pharma GmbH.
Tel: + 43 (0)1 97075 0
[email protected]
España
GlaxoSmithKline, S.A.
Tel: + 34 900 202 700
[email protected]
Polska
GSK Services Sp. z o.o.
Tel.: + 48 (22) 576 9000
Portugal
GlaxoSmithKline - Produtos Farmacêuticos, Lda.
Tel: + 351 21 412 95 00
[email protected]
România
GlaxoSmithKline Biologicals SA
Tel: +40 800672524
Ireland
GlaxoSmithKline (Ireland) Ltd
Tel: + 353 (0)1 495 5000
France
Laboratoire GlaxoSmithKline
Tél: + 33 (0) 1 39 17 84 44
[email protected]
Hrvatska
GlaxoSmithKline Biologicals SA
Tel.: +385 800787089
Slovenija
GlaxoSmithKline Biologicals SA
Tel: +386 80688869
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
GlaxoSmithKline Biologicals SA
Tel.: +421 800500589
Italia
GlaxoSmithKline S.p.A.
Tel:+ 39 (0)45 7741 111
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Κύπρος
GlaxoSmithKline Biologicals SA
Τηλ: +357 80070017
Sverige
GlaxoSmithKline AB
Tel: + 46 (0)8 638 93 00
[email protected]
Latvija
GlaxoSmithKline Biologicals SA
Tel: +371 80205045
United Kingdom (Irlanda del Nord)
GlaxoSmithKline Biologicals SA
Tel: +44 (0)800 221441
[email protected]
Altre fonti di informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia Europea
dei Medicinali: http://www.ema.europa.eu/.
-------------------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Cervarix deve essere somministrato il prima possibile dopo essere stato rimosso dal frigorifero.
Tuttavia, è stata dimostrata stabilità quando conservato fuori dal frigorifero fino a 3 giorni a
temperatura compresa tra 8°C e 25°C o fino ad 1 giorno a temperatura compresa tra 25°C e 37°C. Se
non utilizzato al termine di questo periodo il vaccino deve essere eliminato.
Durante la conservazione della siringa si può osservare un deposito bianco fine con un surnatante
chiaro incolore. Ciò non costituisce segno di deterioramento.
Il contenuto della siringa deve essere ispezionato visivamente sia prima che dopo l’agitazione per
verificare l’assenza di qualsiasi particella estranea e/o aspetto fisico anormale, prima di effettuare la
somministrazione.
In caso si riscontri una qualsiasi di tali condizioni, eliminare il vaccino.
Il vaccino deve essere agitato bene prima dell’uso.
Istruzioni per la siringa pre-riempita
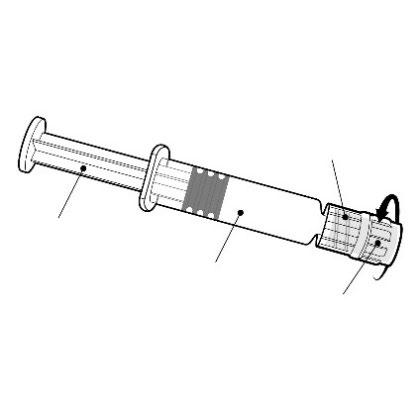
Adattatore Luer Lock
Tenere la siringa per il corpo, non per lo
stantuffo.
Svitare il tappo della siringa ruotando in senso
antiorario.
Stantuff
Corpo
Cappuccio
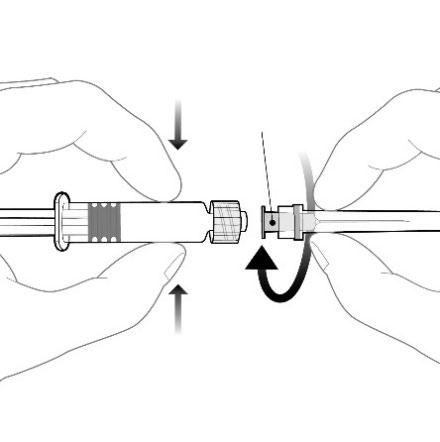
Mozzo dell’ago
Per attaccare l’ago alla siringa, collegare
delicatamente il mozzo dell’ago all’Adattatore
Luer Lock e ruotare un quarto di giro in senso
orario fino a quando se ne avverte il blocco.
Non estrarre lo stantuffo della siringa dal corpo.
Se ciò accade, non somministrare il vaccino.
Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
-

- Paese di registrazione
- Forma farmaceuticaSospensione iniettabile, 20MCG/20MCG
- Codice ATCJ07BM02
- Principio attivo
- Prescrizione richiestaNo
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a CERVARIXForma farmaceutica: Polvere e solvente per soluzione iniettabile, 0.5 mlPrincipio attivo: respiratory syncytial virus vaccinesProduttore: PFIZER EUROPE MA EEIGPrescrizione richiestaForma farmaceutica: Sospensione iniettabile in siringa pre-riempita, 720 U. + 20 MCGPrincipio attivo: combinationsProduttore: GLAXOSMITHKLINE BIOLOGICALS S.A.Prescrizione non richiestaForma farmaceutica: Polvere e sospensione per sospensione iniettabile, 0,5 mlPrincipio attivo: respiratory syncytial virus vaccinesProduttore: GLAXOSMITHKLINE BIOLOGICALS S.A.Prescrizione non richiesta
Medici online per CERVARIX
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di CERVARIX — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per CERVARIX online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.








