
Come usare NIMENRIX
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Nimenrix polvere e solvente per soluzione iniettabile in siringa preriempita
Vaccino coniugato meningococcico gruppi A, C, W-135 e Y
Legga attentamente questo foglio prima di ricevere questo vaccino perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto per lei o il suo bambino. Non lo dia ad altre persone.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4. Questo foglio è stato scritto supponendo che la persona da vaccinare possa leggerlo, ma poiché il vaccino può essere somministrato ad adulti e bambini è possibile che lei lo debba leggere per il bambino.
Contenuto di questo foglio:
- 1. Cos’è Nimenrix e a cosa serve
- 2. Cosa deve sapere prima di ricevere Nimenrix
- 3. Come usare Nimenrix
- 4. Possibili effetti indesiderati
- 5. Come conservare Nimenrix
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Nimenrix e a cosa serve
Cos’è Nimenrix e a cosa serve
Nimenrix è un vaccino che aiuta a proteggere contro le infezioni causate da batteri (germi) chiamati
“ Neisseria meningitidis” tipi A, C, W-135 e Y.
I batteri “ Neisseria meningitidis” tipi A, C, W-135 e Y possono causare malattie gravi quali:
- Meningite - una infezione del tessuto che riveste il cervello e il midollo spinale
- Setticemia - una infezione del sangue. Queste infezioni si trasmettono facilmente da persona a persona e se non trattate possono causare la morte. Nimenrix può essere somministrato agli adulti, adolescenti, bambini e nella prima infanzia a partire da età superiore alle 6 settimane.
Come agisce Nimenrix
Nimenrix aiuta il corpo a produrre la protezione (anticorpi) contro i batteri. Questi anticorpi aiutano a
proteggersi contro la malattia.
Nimenrix proteggerà solo contro le infezioni causate dai batteri “ Neisseria meningitidis”tipi A, C, W-
135 e Y.
2. Cosa deve sapere prima di ricevere Nimenrix
Nimenrix non deve essere somministrato se:
- se è allergico ai principi attivi o ad uno qualsiasi degli altri componenti di questo vaccino (elencati al paragrafo 6). Segni di una reazione allergica possono includere eritema cutaneo pruriginoso, mancanza di respiro e gonfiore del viso o della lingua. Consulti immediatamente il medico se nota unaqualsiasi di queste reazioni.Se non è sicuro, chieda al medico o all’infermiere prima che venga somministrato Nimenrix.
Avvertenze e precauzioni
Consulti il medico o l’infermiere prima di ricevere questo vaccino se:
- ha una infezione con febbre elevata (sopra i 38 °C). Se questa condizione si applica al suo caso, la vaccinazione non le verrà fatta fino a quando non si sentirà meglio. Una infezione minore come un raffreddore non è un problema. Tuttavia parli prima con il medico o l’infermiere.
- Se lei ha problemi di sanguinamento o se è soggetto facilmente alla formazione di lividi.
Se quanto sopra la riguarda (o non ne è sicuro), parli con il medico o l’infermiere prima che le venga
somministrato Nimenrix.
Nimenrix può non proteggere completamente tutte le persone vaccinate. Se ha un sistema immunitario
debole (ad esempio a causa di infezione HIV o di medicinali che influenzano il sistema immunitario)
potrebbe non ottenere il massimo beneficio da Nimenrix.
Si può verificare svenimento (soprattutto negli adolescenti) in seguito a, o anche prima di, qualsiasi
iniezione con ago. Pertanto informi il medico o l’infermiere se lei o il bambino siete svenuti con una
iniezione precedente.
Altri medicinali e Nimenrix
Informi il medico o l’infermiere se sta assumendo o ha recentemente assunto qualsiasi altro
medicinale, inclusi altri vaccini e medicinali senza prescrizione medica.
Nimenrix può non agire al meglio se sta assumendo medicinali che riducono l’efficacia del sistema
immunitario.
Nella prima infanzia, Nimenrix può essere somministrato contemporaneamente con vaccini per difterite
- tetano - pertosse acellulare (DTaP), compresi vaccini DTaP combinati con epatite B, poliovirus inattivato o Haemophilus influenzaetipo b (HBV, IPV o Hib), come il vaccino DTaP-HBV-IPV/Hib, e con il vaccino pneumococcico coniugato 10-valente.
A partire dal primo anno di vita, Nimenrix può essere somministrato contemporaneamente ad uno
qualsiasi dei seguenti vaccini: vaccini per epatite A (HAV) ed epatite B (HBV), vaccini per morbillo –
parotite – rosolia (MPR), vaccini per morbillo – parotite – rosolia – varicella (MPRV), vaccino
pneumococcico coniugato 10-valente o vaccini non adiuvati per l’influenza stagionale.
Nel secondo anno di vita, Nimnerix può anche essere somministrato contemporaneamente con vaccini
combinati per difterite – tetano – pertosse acellulare (DTaP), compresi vaccini DTaP combinati con
epatite B, poliovirus inattivato o Haemophilus influenzaetipo b (HBV, IPV o Hib), come il vaccino
DTaP-HBV-IPV/Hib, e con il vaccino pneumococcico coniugato 13-valente.
Nelle persone di età compresa tra 9 e 25 anni, Nimenrix può essere somministrato in concomitanza
con il vaccino bivalente [Tipo 16 e 18] contro il Papilloma Virus Umano e un vaccino combinato
contro difterite (a ridotto contenuto di antigeni), tetano e pertosse acellulare (dTap).
Quando possibile, Nimenrix e un vaccino contenente tossoide tetanico TT, quale il vaccino DTaP-
HBV-IPV/Hib, devono essere co-somministrati oppure Nimenrix deve essere somministrato almeno
un mese prima del vaccino contenente TT.
Un sito di iniezione differente sarà utilizzato per ogni vaccino.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con
latte materno chieda consiglio al medico prima di ricevere Nimenrix.
Guida di veicoli e utilizzo di macchinari
E’ improbabile che Nimenrix interferisca con la capacità di guidare veicoli o utilizzare macchinari.
Tuttavia non guidi o non usi macchinari se non si sente bene.
Nimenrix contiene Sodio
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per dose, cioè essenzialmente “senza
sodio”.
3. Come usare Nimenrix
Nimenrix verrà somministrato da un medico o da un infermiere.
Nimenrix è sempre iniettato in un muscolo, solitamente nella parte superiore del braccio o della coscia.
Immunizzazione primaria
Prima infanzia con età compresa tra 6 settimane e meno di 6 mesi
Due iniezioni somministrate a 2 mesi di distanza, ad esempio a 2 e 4 mesi di età (la prima iniezione
può essere somministrata dall’età di 6 settimane).
Prima infanzia dai 6 mesi di età, bambini, adolescenti e adulti
Una iniezione.
Dosi di richiamo
Prima infanzia con età compresa tra 6 settimane e meno di 12 mesi:
Una dose di richiamo a 12 mesi di età ad almeno 2 mesi di distanza dall’ultima dose di Nimenrix.
Soggetti di età pari o superiore a 12 mesi precedentemente vaccinati:
Informi il medico se ha ricevuto una precedente iniezione con un altro vaccino meningococcico
differente da Nimenrix.
Il medico la informerà se e quando necessita di un’altra dose di Nimenrix, specialmente se lei o il
bambino:
- avete ricevuto la prima dose a 6-14 mesi di età e potreste essere particolarmente a rischio di infezione dovuta a Neisseria meningitidistipi W-135 e Y
- avete ricevuto la dose approssimativamente più di un anno fa e potreste correre un rischio di infezione causata da Neisseria meningitidistipo A
- avete ricevuto la prima dose a un’età compresa tra 12 e 23 mesi e potreste correre un rischio particolare di infezione causata da Neisseria meningitidistipi A, C, W-135 e Y
Verrà informato quando lei o il bambino dovrete sottoporvi all’iniezione successiva. Se lei o il
bambino saltate un’iniezione, è importante prendere un altro appuntamento.
Si assicuri che lei o il bambino terminiate tutto il ciclo di vaccinazione.
Se ha qualsiasi dubbio sull’uso di questo medicinale si rivolga al medico o al farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino. I seguenti effetti indesiderati possono verificarsi con questo medicinale:
Molto comune (si può verificare in più di 1 caso ogni 10 dosi di vaccino):
- febbre
- stanchezza (affaticamento)
- mal di testa
- sensazione di sonnolenza
- perdita di appetito
- sensazione di irritabilità
- gonfiore, dolore e rossore al sito di iniezione
Comune (si può verificare fino a 1 caso ogni 10 dosi di vaccino):
- lividi (ematoma) al sito di iniezione
- problemi di stomaco e digestione quali diarrea, vomito e nausea.
- eruzione cutanea (prima infanzia).
Non comune (si può verificare fino a 1 caso ogni 100 dosi di vaccino):
- eritema cutaneo
- orticaria
- prurito
- pianto
- sensazioni di stordimento
- dolori muscolari
- dolore alle braccia o alle gambe
- stato di malessere generale
- difficoltà a dormire
- diminuzione delle sensazioni o sensibilità, particolarmente nella pelle
- reazioni al sito di iniezione quali prurito, una sensazione di calore o intorpidimento o nodulo duro
- reazione allergica
Raro (si può verificare fino a 1 caso ogni 1.000 dosi di vaccino):
- attacchi (crisi convulsive) associati a temperatura elevata
Non nota:la frequenza non può essere stabilita sulla base dei dati disponibili
- gonfiore e rossore al sito di iniezione; ciò può interessare una vasta area dell’arto sede della vaccinazione
- ingrossamento dei linfonodi
- grave reazione allergica
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti
indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Nimenrix
- Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
- Non usi questo medicinale dopo la data di scadenza che è riportata sulla confezione. La data di scadenza si riferisce all’ultimo giorno di quel mese.
- Conservare in frigorifero (2 °C - 8 °C)
- Conservare nella confezione originale per proteggere il medicinale dalla luce
- Non congelare
- Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Nimenrix
- I principi attivi sono:
- Dopo la ricostituzione, 1 dose (0,5 mL) contiene: Neisseria meningitidispolisaccaride del gruppo A 5 microgrammi Neisseria meningitidispolisaccaride del gruppo C 5 microgrammi Neisseria meningitidispolisaccaride del gruppo W-135 5 microgrammi Neisseria meningitidispolisaccaride del gruppo Y 5 microgrammi
coniugato alla proteina vettore del tossoide tetanico 44 microgrammi
- Gli altri componenti sono:
- Nella polvere: saccarosio e trometamolo
- Nel solvente: sodio cloruro (vedere paragrafo 2 “Nimenrix contiene sodio”) e acqua per preparazioni iniettabili
Descrizione dell’aspetto di Nimenrix e contenuto della confezione
Nimenrix è una polvere e un solvente per soluzione iniettabile.
Nimenrix viene fornito come polvere bianca, anche compattata, in un flaconcino di vetro monodose e
un solvente limpido e incolore in una siringa preriempita.
Questi devono essere miscelati insieme prima dell’uso. Il vaccino miscelato apparirà come una
soluzione limpida incolore.
Nimenrix è disponibile in confezioni da 1 o 10 unità con o senza aghi.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Titolare dell’autorizzazione all’immissione in
commercio:
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Belgio
Produttore responsabile del rilascio dei lotti:
Pfizer Manufacturing Belgium N.V.
Rijksweg 12
2870 Puurs-Sint-Amands
Belgio
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Luxembourg/Luxemburg
Pfizer S.A./N.V.
Tél/Tel: + 32 (0)2 554 62 11
Lietuva
Pfizer Luxembourg SARL filialas Lietuvoje
Tel. + 370 52 51 4000
България
Пфайзер Люксембург САРЛ, Клон
България
Teл: +359 2 970 4333
Magyarország
Pfizer Kft
Tel: +36 1 488 3700
Česká Republika
Pfizer, spol. s r.o.
Tel: +420 283 004 111
Malta
Vivian Corporation Ltd.
Tel: + 35621 344610
Danmark
Pfizer ApS
Tlf: + 45 44 201 100
Nederland
Pfizer BV
Tel: +31 (0)800 63 34 636
Deutschland
Pfizer Pharma GmbH
Tel: + 49 (0)30 550055-51000
Norge
Pfizer AS
Tlf: +47 67 526 100
Eesti
Pfizer Luxembourg SARL Eesti filiaal
Tel: +372 666 7500
Österreich
Pfizer Corporation Austria Ges.m.b.H
Tel: + 43 (0)1 521 15-0
Ελλάδα
Pfizer Ελλάς A.E.
Τηλ.: +30 210 6785 800
Polska
Pfizer Polska Sp. z o.o.
Tel.: +48 22 335 61 00
España
Pfizer, S.L.
Télf: +34914909900
Portugal
Laboratórios Pfizer, Lda.
Tel: +351 21 423 5500
France
Pfizer
Tél +33 1 58 07 34 40
România
Pfizer Romania S.R.L
Tel: +40 (0) 21 207 28 00
Hrvatska
Pfizer Croatia d.o.o.
Tel: + 385 1 3908 777
Slovenija
Pfizer Luxembourg SARL
Pfizer, podružnica za svetovanje s področja
farmacevtske dejavnosti, Ljubljana
Tel.: + 386 (0) 1 52 11 400
Ireland
Pfizer Healthcare Ireland
Tel: 1800 633 363 (toll free)
+44 (0)1304 616161
Slovenská republika
Pfizer Luxembourg SARL,
organizačná zložka
Tel: + 421 2 3355 5500
Suomi/Finland
Pfizer Oy
Puh/Tel: +358 (0)9 430 040
Ísland
Icepharma hf
Simi: + 354 540 8000
Italia
Pfizer S.r.l.
Tel: +39 06 33 18 21
Sverige
Pfizer AB
Tel: +46 (0)8 550 520 00
Kύπρος
Pfizer Ελλάς Α.Ε. (Cyprus Branch)
Tηλ: +357 22 817690
United Kingdom (Northern Ireland)
Pfizer Limited
Tel: +44 (0) 1304 616161
Latvija
Pfizer Luxembourg SARL filiāle Latvijā
Tel.: + 371 670 35 775
Altre fonti di informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
per i medicinali, https://www.ema.europa.eu .
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Il vaccino è solo per uso intramuscolare. Non somministrare per via intravascolare, intradermica o
sottocutanea.
Se Nimenrix viene co-somministrato con altri vaccini, devono essere utilizzati diversi siti di iniezione.
Nimenrix non deve essere miscelato con altri vaccini.
Istruzioni per la ricostituzione del vaccino con il solvente presentato in siringa preriempita:
Nimenrix deve essere ricostituito aggiungendo l’intero contenuto della siringa preriempita di solvente
al flaconcino contenente la polvere.
Per inserire l’ago nella siringa, fare riferimento alle figure. Tuttavia, la siringa fornita con Nimenrix
potrebbe essere leggermente diversa (senza vite filettata) rispetto alla siringa descritta nella figura. In
questo caso, l’ago deve essere inserito senza avvitamento.
- 1. Tenendo il corpodella siringa in una mano (evitare di tenere lo stantuffo della siringa), svitare il tappo della siringa ruotandolo in senso antiorario.
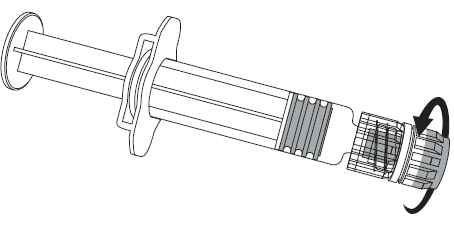
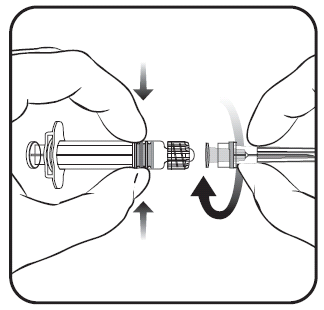
- 2. Per inserire l’ago nella siringa, ruotare l’ago in senso orario nella siringa fino a che si blocca (vedere figura).
- 3. Rimuovere la protezione dell’ago, operazione che in qualche caso può risultare un po’ difficoltosa.

- 4. Aggiungere il solvente alla polvere. Dopo l’aggiunta del solvente alla polvere, la miscela deve essere ben agitata affinché la polvere sia completamente disciolta nel solvente.
Il vaccino ricostituito è una soluzione limpida incolore.
Prima della somministrazione il vaccino ricostituito deve essere ispezionato visivamente per accertare
l’assenza di particelle estranee e/o variazioni dell’aspetto fisico. Nel caso si verificasse uno dei due
fenomeni, scartare il vaccino.
Dopo la ricostituzione il vaccino deve essere usato subito.
Un nuovo ago deve essere usato per somministrare il vaccino.
Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
Nimenrix polvere e solvente per soluzione iniettabile in flaconcini
Vaccino coniugato meningococcico gruppi A, C, W-135 e Y
Legga attentamente questo foglio prima di ricevere questo vaccino perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto per lei o il suo bambino. Non lo dia ad altre persone.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o al farmacista. Vedere paragrafo 4. Questo foglietto è stato scritto supponendo che la persona cui il vaccino è destinata lo legga, ma il vaccino può essere somministrato ad adulti e bambini cosicché può darsi il caso che lei lo stia leggendo per il suo bambino.
Contenuto di questo foglio
- 1. Cos’è Nimenrix e a cosa serve
- 2. Cosa deve sapere prima di ricevere Nimenrix
- 3. Come usare Nimenrix
- 4. Possibili effetti indesiderati
- 5. Come conservare Nimenrix
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Nimenrix e a cosa serve
Cos’è Nimenrix e a cosa serve
Nimenrix è un vaccino che aiuta a proteggere contro le infezioni causate da batteri (germi) chiamati
“ Neisseria Meningitidis” tipi A, C, W-135 e Y.
I batteri “ Neisseria Meningitidis” tipi A, C, W-135 e Y possono causare malattie gravi quali:
- Meningite - una infezione del tessuto che riveste il cervello e il midollo spinale
- Setticemia - una infezione del sangue. Queste infezioni si trasmettono facilmente da persona a persona e se non trattate possono causare morte. Nimenrix può essere somministrato agli adulti, adolescenti, bambini e nella prima infanzia a partire da età superiore alle 6 settimane.
Come agisce Nimenrix
Nimenrix aiuta il corpo a produrre la protezione (anticorpi) contro i batteri. Questi anticorpi aiutano a
proteggerti contro la malattia.
Nimenrix proteggerà solo contro le infezioni causate dai batteri “ Neisseria Meningitidis”tipi A, C, W-
135 e Y.
2. Cosa deve sapere prima di ricevere Nimenrix
Nimenrix non deve essere somministrato se:
- se è allergico ai principi attivi o ad uno qualsiasi degli altri componenti di questo vaccino (elencati al paragrafo 6). Segni di una reazione allergica possono includere eritema cutaneo pruriginoso, mancanza di respiro e gonfiore del viso o della lingua. Consulti immediatamente il suo medico se nota unaqualsiasi di queste reazioni.Se non è sicuro, chieda al medico o all’infermiere prima che venga somministrato Nimenrix.
Avvertenze e precauzioni
Consulti il medico o l’infermiere prima di ricevere questo vaccino se:
- ha una infezione con una temperatura elevata (sopra i 38 °C). Se questa condizione si applica al suo caso, la vaccinazione non le verrà fatta fino a quando non si sentirà meglio. Una infezione minore come un raffreddore non dovrebbe essere un problema. Tuttavia parli prima con il medico o l’infermiere.
- Se lei ha problemi di sanguinamento o se lei è soggetto facilmente alla formazione di lividi.
Se quanto sopra la riguarda (o non ne è sicuro), parli con il medico o l’infermiere prima che le venga
somministrato Nimenrix.
Nimenrix può non proteggere completamente tutte le persone vaccinate. Se ha un sistema immunitario
debole (ad esempio a causa di infezione HIV o di medicinali che influenzano il sistema immunitario)
potrebbe non ottenere il massimo beneficio da Nimenrix.
Si può verificare svenimento (soprattutto negli adolescenti) in seguito a, o anche prima di qualsiasi
iniezione con ago. Pertanto informi il medico o l’infermiere se lei o il suo bambino siete svenuti con
una iniezione precedente.
Altri medicinali e Nimenrix
Informi il medico o l’infermiere se sta assumendo o ha recentemente assunto qualsiasi altro
medicinale, inclusi altri vaccini e medicinali senza prescrizione medica.
Nimenrix può non agire al meglio se sta assumendo medicinali che riducono l’efficacia del sistema
immunitario.
Nella prima infanzia, Nimenrix può essere somministrato contemporaneamente con vaccini per difterite
- tetano - pertosse acellulare (DTaP), compresi vaccini DTaP combinati con epatite B, poliovirus inattivato o Haemophilus influenzaetipo b (HBV, IPV o Hib), come il vaccino DTaP-HBV-IPV/Hib, e con il vaccino pneumococcico coniugato 10-valente.
A partire dal primo anno di vita, Nimenrix può essere somministrato contemporaneamente ad uno
qualsiasi dei seguenti vaccini: vaccini per epatite A (HAV) ed epatite B (HBV), vaccini per morbillo –
parotite – rosolia (MPR), vaccini per morbillo – parotite – rosolia – varicella (MPRV), vaccino
pneumococcico coniugato 10-valente o vaccini non adiuvati per l’influenza stagionale.
Nel secondo anno di vita, Nimenrix può anche essere somministrato contemporaneamente con vaccini
combinati per difterite – tetano – pertosse acellulare (DTaP), compresi vaccini DTaP combinati con
epatite B, poliovirus inattivato o Haemophilus influenzaetipo b (HBV, IPV o Hib), come il vaccino
DTaP-HBV-IPV/Hib, e con il vaccino pneumococcico coniugato 13-valente.
Nelle persone di età compresa tra 9 e 25 anni, Nimenrix può essere somministrato in concomitanza
con il vaccino contro il Papilloma Virus Umano [Tipo 16 e 18] e un vaccino combinato contro difterite
(a ridotto contenuto di antigeni), tetano e pertosse acellulare (dTap).
Quando possibile, Nimenrix e un vaccino contenente TT, quale il vaccino DTaP-HBV-IPV/Hib,
devono essere co-somministrati oppure Nimenrix deve essere somministrato almeno un mese prima
del vaccino contenente TT.
Un sito di iniezione differente sarà utilizzato per ogni vaccino.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con
latte materno chieda consiglio al medico prima di ricevere Nimenrix.
Guida di veicoli e utilizzo di macchinari
E’ improbabile che Nimenrix interferisca con la capacità di guidare veicoli o utilizzare macchinari.
Tuttavia non guidi o non usi macchinari se non si sente bene.
Nimenrix contiene Sodio
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per dose, cioè essenzialmente “senza
sodio”.
3. Come usare Nimenrix
Nimenrix verrà somministrato da un medico o da un infermiere.
Nimenrix viene sempre iniettato in un muscolo, solitamente nella parte superiore del braccio o della
coscia.
Immunizzazione primaria
Prima infanzia con età compresa tra 6 settimane e meno di 6 mesi
Due iniezioni somministrate a 2 mesi di distanza, ad esempio a 2 e 4 mesi di età (la prima iniezione
può essere somministrata dall’età di 6 settimane).
Prima infanzia dai 6 mesi di età, bambini, adolescenti e adulti
Una iniezione.
Dosi di richiamo
Prima infanzia con età compresa tra 6 settimane e meno di 12 mesi:
Una dose di richiamo a 12 mesi di età ad almeno 2 mesi di distanza dall’ultima dose di Nimenrix.
Soggetti di età pari o superiore a 12 mesi precedentemente vaccinati:
Informi il medico se ha ricevuto una precedente iniezione con un altro vaccino meningococcico
differente da Nimenrix. Il medico la informerà se e quando necessita di un’altra dose di Nimenrix,
specialmente se lei il bambino:
- avete ricevuto la prima dose a 6-14 mesi di età e potreste essere particolarmente a rischio di infezione dovuta a Neisseria meningitidistipi W-135 e Y
- avete ricevuto la dose approssimativamente più di un anno fa e potreste correre un rischio di infezione causata da Neisseria meningitidistipo A
- avete ricevuto la prima dose a un’età compresa tra 12 e 23 mesi e potreste correre un rischio particolare di infezione causata da Neisseria meningitidistipi A, C, W-135 e Y
Verrà informato quando lei o il bambino dovrete sottoporvi all’iniezione successiva. Se lei o il
bambino saltate un’iniezione, è importante prendere un altro appuntamento.
Si assicuri che lei o il bambino terminiate tutto il ciclo di vaccinazione.
Se ha qualsiasi dubbio sull’uso di questo medicinale si rivolga al medico o al farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino. I seguenti effetti indesiderati possono verificarsi con questo medicinale:
Molto comune (si può verificare in più di 1 caso ogni 10 dosi di vaccino):
- febbre
- stanchezza (affaticamento)
- mal di testa
- sensazione di sonnolenza
- perdita di appetito
- sensazione di irritabilità
- gonfiore, dolore e rossore al sito di iniezione
Comune (si può verificare fino a 1 caso ogni 10 dosi di vaccino):
- lividi (ematoma) al sito di iniezione
- problemi di stomaco e digestione quali diarrea, vomito e nausea
- eruzione cutanea (prima infanzia).
Non comune (si può verificare fino a 1 caso ogni 100 dosi di vaccino):
- eritema cutaneo
- orticaria
- prurito
- pianto
- sensazioni di stordimento
- dolori muscolari
- dolore alle braccia o alle gambe
- stato di malessere generale
- difficoltà a dormire
- diminuzione delle sensazioni o sensibilità, particolarmente nella pelle
- reazioni al sito di iniezione quali prurito, una sensazione di calore o intorpidimento o nodulo duro
- reazione allergica
Raro (si può verificare fino a 1 caso ogni 1.000 dosi di vaccino):
- attacchi (crisi convulsive) associati a temperatura elevata
Non nota:la frequenza non può essere stabilita sulla base dei dati disponibili:
- gonfiore e rossore al sito di iniezione; ciò può interessare una vasta area dell’arto sede della vaccinazione
- ingrossamento dei linfonodi
- grave reazione allergica
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti
indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Nimenrix
- Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
- Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola. La data di scadenza si riferisce all’ultimo giorno di quel mese.
- Conservare in frigorifero (2 °C - 8 °C)
- Conservare nella confezione originale per proteggere dalla luce
- Non congelare
- Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Nimenrix
- I principi attivi sono:
- Dopo la ricostituzione, 1 dose (0,5 mL) contiene: Neisseria meningitidispolisaccaride1 del gruppo A 5 microgrammi Neisseria meningitidispolisaccaride1 del gruppo C 5 microgrammi Neisseria meningitidispolisaccaride1 del gruppo W-135 5 microgrammi Neisseria meningitidispolisaccaride1 del gruppo Y 5 microgrammi coniugato alla proteina vettore del tossoide tetanico 44 microgrammi
- Gli altri componenti sono:
- Nella polvere: saccarosio e trometamolo
- Nel solvente: sodio cloruro (vedere paragrafo 2 “Nimenrix contiene sodio”) e acqua per preparazioni iniettabili
Descrizione dell’aspetto di Nimenrix e contenuto della confezione
Nimenrix è una polvere e un solvente per soluzione iniettabile.
Nimenrix viene fornito come polvere bianca, anche compattata, in un flaconcino di vetro monodose e
un solvente chiaro ed incolore in un flaconcino.
Questi devono essere miscelati insieme prima dell’uso. Il vaccino miscelato apparirà come una
soluzione chiara incolore.
Nimenrix è disponibile in confezioni da 50.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Titolare dell’autorizzazione all’immissione in
commercio:
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Belgio
Produttore responsabile del rilascio dei lotti:
Pfizer Manufacturing Belgium N.V.
Rijksweg 12
2870 Puurs-Sint-Amands
Belgio
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Luxembourg/Luxemburg
Pfizer S.A./N.V.
Tél/Tel: + 32 (0)2 554 62 11
Lietuva
Pfizer Luxembourg SARL filialas Lietuvoje
Tel. + 370 52 51 4000
България
Пфайзер Люксембург САРЛ, Клон
България
Teл: +359 2 970 4333
Magyarország
Pfizer Kft
Tel: +36 1 488 3700
Česká Republika
Pfizer, spol. s r.o.
Tel: +420 283 004 111
Malta
Vivian Corporation Ltd.
Tel: + 35621 344610
Danmark
Pfizer ApS
Tlf: + 45 44 201 100
Nederland
Pfizer BV
Tel: +31 (0)800 63 34 636
Deutschland
Pfizer Pharma GmbH
Tel: + 49 (0)30 550055-51000
Norge
Pfizer AS
Tlf: +47 67 526 100
Eesti
Pfizer Luxembourg SARL Eesti filiaal
Tel: +372 666 7500
Österreich
Pfizer Corporation Austria Ges.m.b.H
Tel: + 43 (0)1 521 15-0
Ελλάδα
Pfizer Ελλάς A.E.
Τηλ.: +30 210 6785 800
Polska
Pfizer Polska Sp. z o.o.
Tel.: +48 22 335 61 00
España
Pfizer, S.L.
Télf: +34914909900
Portugal
Laboratórios Pfizer, Lda.
Tel: +351 21 423 5500
France
Pfizer
Tél +33 1 58 07 34 40
România
Pfizer Romania S.R.L
Tel: +40 (0) 21 207 28 00
Hrvatska
Pfizer Croatia d.o.o.
Tel: + 385 1 3908 777
Slovenija
Pfizer Luxembourg SARL
Pfizer, podružnica za svetovanje s področja
farmacevtske dejavnosti, Ljubljana
Tel.: + 386 (0) 1 52 11 400
Ireland
Pfizer Healthcare Ireland
Tel: 1800 633 363 (toll free)
+44 (0)1304 616161
Slovenská republika
Pfizer Luxembourg SARL,
organizačná zložka
Tel: + 421 2 3355 5500
Suomi/Finland
Pfizer Oy
Puh/Tel: +358 (0)9 430 040
Ísland
Icepharma hf
Simi: + 354 540 8000
Italia
Pfizer S.r.l.
Tel: +39 06 33 18 21
Sverige
Pfizer AB
Tel: +46 (0)8 550 520 00
Kύπρος
Pfizer Ελλάς Α.Ε. (Cyprus Branch)
Tηλ: +357 22 817690
United Kingdom (Northern Ireland)
Pfizer Limited
Tel: +44 (0) 1304 616161
Latvija
Pfizer Luxembourg SARL filiāle Latvijā
Tel.: + 371 670 35 775
Altre fonti di informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
per i medicinali, https://www.ema.europa.eu .
-----------------------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Il vaccino è solo per uso intramuscolare. Non somministrare per via intravascolare, intradermica o
sottocutanea.
Se Nimenrix viene co-somministrato con altri vaccini, devono essere utilizzati diversi siti di iniezione.
Nimenrix non deve essere miscelato con altri vaccini.
Istruzioni per la ricostituzione del vaccino con il solvente presentato in flaconcini:
Nimenrix deve essere ricostituito aggiungendo l’intero contenuto del flaconcino di solvente al
flaconcino contenente la polvere.
- 1. Prelevare l’intero contenuto del flaconcino di solvente e aggiungere il solvente al flaconcino di polvere.
- 2. La miscela deve essere ben agitata affinchéla polvere sia completamente disciolta nel solvente.
Il vaccino ricostituito è una soluzione chiara incolore.
Prima della somministrazione il vaccino ricostituito deve essere ispezionato visivamente per accertare
l’assenza di particelle estranee e/o variazioni dell’aspetto fisico. Nel caso si verificasse uno dei due
fenomeni, scartare il vaccino.
Dopo la ricostituzione il vaccino deve essere usato subito.
Un nuovo ago deve essere usato per somministrare il vaccino.
Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
-

- Paese di registrazione
- Forma farmaceuticaPolvere e solvente per soluzione iniettabile, 5 MCG/5MCG/5MCG/5MCG
- Codice ATCJ07AH08
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a NIMENRIXForma farmaceutica: Soluzione iniettabile, 0,5 MLProduttore: SANOFI WINTHROP INDUSTRIEPrescrizione richiestaForma farmaceutica: Polvere e soluzione per soluzione iniettabileProduttore: GLAXOSMITHKLINE VACCINES S.R.L.Prescrizione non richiestaForma farmaceutica: Sospensione iniettabile in siringa pre-riempita, 0,5MLPrincipio attivo: meningococcus B, multicomponent vaccineProduttore: GLAXOSMITHKLINE VACCINES S.R.L.Prescrizione non richiesta
Medici online per NIMENRIX
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di NIMENRIX — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per NIMENRIX online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.








