
Come usare AMVUTTRA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Amvuttra 25 mg soluzione iniettabile in siringa preriempita
vutrisiran
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Amvuttra e a cosa serve
- 2. Cosa deve sapere prima di usare Amvuttra
- 3. Come usare Amvuttra
- 4. Possibili effetti indesiderati
- 5. Come conservare Amvuttra
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Amvuttra e a cosa serve
Il principio attivo contenuto in Amvuttra è vutrisiran.
A cosa serve Amvuttra
Amvuttra è un medicinale usato per il trattamento di una malattia chiamata “amiloidosi ATTR”, una
malattia che può trasmettersi da una generazione all’altra e può essere causata anche
dall’invecchiamento. L’amiloidosi ATTR è causata da problemi con una proteina presente
nell’organismo, che prende il nome di “transtiretina” (TTR). Si tratta di una proteina prodotta
principalmente nel fegato e che trasporta vitamina A e altre sostanze nel corpo.
Nelle persone affette da questa malattia, piccole fibre della proteina TTR si aggregano formando
depositi, che prendono il nome di “amiloide”. L’amiloide può accumularsi intorno o all’interno dei
nervi, nel cuore e in altre sedi del corpo, impedendo loro di funzionare come dovrebbero. Ciò provoca
i sintomi che caratterizzano la malattia.
Come agisce Amvuttra
Amvuttra agisce riducendo la quantità della proteina TTR prodotta dal fegato, in modo che vi sia una
quantità minore di proteina TTR nel sangue in grado di formare l’amiloide. Ciò può contribuire a
ridurre gli effetti di questa malattia.
Amvuttra viene usato solo negli adulti.
2. Cosa deve sapere prima di usare Amvuttra
Non usi Amvuttra
- se in passato ha manifestato una reazione allergica grave a vutrisiran o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6).
Se non è sicuro, si rivolga al medico, al farmacista o all’infermiere prima di usare questo medicinale.
Avvertenze e precauzioni
Livelli bassi di vitamina A nel sangue e integratori vitaminici
Amvuttra riduce la quantità di vitamina A nel sangue.
Il medico le chiederà di assumere un’integrazione giornaliera di vitamina A. Si attenga alla dose di
vitamina A raccomandata dal medico.
I segni di carenza di vitamina A possono includere: problemi con la vista soprattutto la notte, occhi
secchi, visione offuscata o appannata.
- Se nota cambiamenti nella vista o altri problemi agli occhi durante l’uso di Amvuttra, si rivolga al medico. Se necessario, il medico potrà indirizzarla ad un oculista per un controllo.
Livelli troppo alti e troppo bassi di vitamina A possono nuocere allo sviluppo del feto. Pertanto, le
donne in età fertile devono escludere lo stato di gravidanza prima di iniziare il trattamento con
Amvuttra e utilizzare metodi contraccettivi efficaci (vedere il paragrafo “Gravidanza, allattamento e
contraccezione” di seguito).
- I livelli di vitamina A possono rimanere bassi per oltre 12 mesi dopo l’ultima dose di Amvuttra.
- Informi il medico se sta pianificando una gravidanza. Il medico le dirà di interrompere l’assunzione di Amvuttra e l’integrazione di vitamina A. Il medico si assicurerà inoltre che i suoi livelli di vitamina A siano tornati alla normalità prima di tentare il concepimento.
- Informi il medico se inizia una gravidanza non pianificata. Il medico le dirà di interrompere l’assunzione di Amvuttra. Durante i primi 3 mesi di gravidanza, il medico potrebbe dirle di interrompere l’integrazione di vitamina A. Durante gli ultimi 6 mesi di gravidanza, il medico potrebbe dirle di riprendere l’integrazione di vitamina A se i livelli di vitamina A non sono ancora tornati alla normalità, a causa di un aumento del rischio di carenza di vitamina A negli ultimi 3 mesi di gravidanza.
Bambini e adolescenti
Amvuttra non è raccomandato nei bambini e negli adolescenti di età inferiore a 18 anni.
Altri medicinali e Amvuttra
Informi il medico, il farmacista o l’infermiere se sta assumendo, ha recentemente assunto o potrebbe
assumere qualsiasi altro medicinale.
Gravidanza, allattamento e contraccezione
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico o al farmacista prima di prendere questo medicinale.
Gravidanza
Non deve assumere Amvuttra se è in gravidanza.
Donne in età fertile
Amvuttra ridurrà il livello di vitamina A nel sangue e la vitamina A è importante per il normale
sviluppo del feto (vedere sopra “Avvertenze e precauzioni”).
- Se è una donna in età fertile, deve utilizzare un metodo contraccettivo efficace durante il trattamento con Amvuttra.
- Parli con il medico o l’infermiere dei metodi di contraccezione appropriati.
- Prima di iniziare il trattamento con Amvuttra deve essere escluso lo stato di gravidanza.
- Informi il medico se sta pianificando una gravidanza o se è in stato di gravidanza non pianificata. Il medico le dirà di interrompere l’assunzione di Amvuttra.
Allattamento
Non è noto se vutrisiran sia escreto nel latte materno. Il medico considererà i potenziali benefici del
trattamento per lei rispetto ai rischi dell’allattamento per il neonato.
Guida di veicoli e utilizzo di macchinari
È improbabile che Amvuttra alteri la capacità di guidare veicoli e di usare macchinari. Il medico le
dirà se la sua condizione le consente di guidare veicoli e utilizzare macchinari in modo sicuro.
Amvuttra contiene sodio
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per mL, cioè essenzialmente ‘senza
sodio’.
3. Come usare Amvuttra
Amvuttra può essere autosomministrato oppure somministrato da una persona che le presta assistenza
o da un operatore sanitario.
Il medico o l’operatore sanitario mostrerà a lei e/o alla persona che le presta assistenza come preparare
e iniettare una dose di Amvuttra, prima che lei possa eseguirla da solo.
Per le istruzioni su come usare Amvuttra, legga le “Istruzioni per l’uso” alla fine di questo foglio.
In che quantità deve usare Amvuttra
La dose raccomandata è di 25 mg una volta ogni 3 mesi.
Dove viene somministrata l’iniezione
Amvuttra viene somministrato mediante iniezione sotto la pelle (“iniezione sottocutanea”) nell’area
della pancia (addome), nella parte superiore del braccio (se l’iniezione viene effettuata da qualcun altro)
o nella coscia.
Per quanto tempo usare Amvuttra
Il medico le dirà per quanto tempo dovrà usare Amvuttra. Non interrompa il trattamento con Amvuttra
a meno che non le venga indicato dal medico.
Se usa più Amvuttra di quanto deve
Nell’improbabile eventualità che lei usi una quantità eccessiva (un sovradosaggio), si rivolga al
medico o al farmacista, anche se non ha alcun sintomo. Il medico la sottoporrà a un controllo per
l’eventuale sviluppo di effetti indesiderati.
Se dimentica di usare Amvuttra
Se viene saltata una dose, somministri Amvuttra appena possibile. Poi riprenda la somministrazione
ogni 3 mesi, a partire dalla dose più recente somministrata.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico, al farmacista o
all’infermiere.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Informi il medico, il farmacista o l’infermiere se nota uno qualsiasi dei seguenti effetti indesiderati:
Comuni: possono interessare fino a 1 persona su 10
- arrossamento, dolore, prurito, lividi o calore nella parte del corpo in cui è stata somministrata l’iniezione
- esami del sangue che mostrano un aumento degli enzimi del fegato chiamati fosfatasi alcalina e alanina aminotransferasi
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti
indesiderati può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Amvuttra
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sull’etichetta, sul coperchio del
vassoio e sulla scatola dopo “Scad.”. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Non conservare a temperatura superiore a 30°C.
Non congelare.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Amvuttra
- Il principio attivo è vutrisiran. Ogni siringa preriempita contiene vutrisiran sodico equivalente a 25 mg di vutrisiran in 0,5 mL di soluzione.
- Gli altri componenti sono: sodio diidrogeno fosfato diidrato, disodio fosfato diidrato, cloruro di sodio e acqua per preparazioni iniettabili. Per aggiustare il pH possono essere utilizzati sodio idrossido e acido fosforico (vedere “Amvuttra contiene sodio” al paragrafo 2).
Descrizione dell’aspetto di Amvuttra e contenuto della confezione
Questo medicinale è una soluzione iniettabile (iniettabile) limpida, da incolore a gialla. Ogni
confezione contiene una siringa preriempita monodose.
Titolare dell’autorizzazione all’immissione in commercio e produttore
Alnylam Netherlands B.V.
Antonio Vivaldistraat 150
1083 HP Amsterdam
Paesi Bassi
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Alnylam Netherlands B.V.
Tél/Tel: 0800 81 443 (+32 234 208 71)
[email protected]
Luxembourg/Luxemburg
Alnylam Netherlands B.V.
Tél/Tel: 80085235 (+352 203 014 48)
[email protected]
България
Genesis Pharma Bulgaria EOOD
Teл.: +359 2 969 3227
[email protected]
Lietuva
Medison Pharma Lithuania UAB
Tel: +370 37 213824
[email protected]
Česká republika
Medison Pharma s.r.o.
Tel: +420 221 343 336
mailto: [email protected]
Magyarország
Medison Pharma Hungary Kft
Tel.: +36 1 293 0955
[email protected]
Danmark
Alnylam Sweden AB
Tlf.: 433 105 15 (+45 787 453 01)
[email protected]
Malta
Genesis Pharma (Cyprus) Ltd
Tel: +357 22765715
[email protected]
Deutschland
Alnylam Germany GmbH
Tel: 0800 2569526 (+49 89 20190112)
[email protected]
Nederland
Alnylam Netherlands B.V.
Tel: 0800 282 0025 (+31 20 369 7861)
[email protected]
Eesti
Medison Pharma Estonia OÜ
Tel: +372 679 5085
[email protected]
Norge
Alnylam Sweden AB
Tlf: 800 544 00 (+472 1405 657)
[email protected]
Ελλάδα
ΓΕΝΕΣΙΣ ΦΑΡΜΑ Α.Ε
Τηλ: +30 210 87 71 500
[email protected]
Österreich
Alnylam Austria GmbH
Tel: 0800 070 339 (+43 720 778 072)
[email protected]
España
Alnylam Pharmaceuticals Spain SL
Polska
Medison Pharma Sp. z o.o.
Tel: 900810212 (+34 910603753)
[email protected]
Tel.: +48 22 152 49 42
[email protected]
France
Alnylam France SAS
Tél: 0805 542 656 (+33 187650921)
[email protected]
Portugal
Alnylam Portugal
Tel: 707201512 (+351 21 269 8539)
[email protected]
Hrvatska
Genesis Pharma Adriatic d.o.o
Tel: +385 1 5530 011
[email protected]
România
Genesis Biopharma Romania SRL
Tel: +40 21 403 4074
[email protected]
Ireland
Alnylam Netherlands B.V.
Tel: 1800 924260 (+353 818 882213)
[email protected]
Slovenija
Genesis Biopharma SL d.o.o
Tel: +386 1 292 70 90
[email protected]
Ísland
Alnylam Netherlands B.V.
Sími: +31 20 369 7861
[email protected]
Slovenská republika
Medison Pharma s.r.o.
Tel: +421 2 201 109 65
[email protected]
Italia
Alnylam Italy S.r.l.
Tel: 800 90 25 37 (+39 02 89 73 22 91)
[email protected]
Suomi/Finland
Alnylam Sweden AB
Puh/Tel: 0800 417 452 (+358 942 727 020)
[email protected]
Κύπρος
Genesis Pharma (Cyprus) Ltd
Τηλ: +357 22765715
[email protected]
Sverige
Alnylam Sweden AB
Tel: 020109162 (+46 842002641)
[email protected]
Latvija
Medison Pharma Latvia SIA
Tel: +371 67 717 847
[email protected]
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, https://www.ema.europa.eu .
------------------------------------------------------------------------------------------------------------------------
S RUZ N PER L’US
Amvuttra 25 mg soluzione iniettabile in siringa preriempita
vutrisiran
Siringa preriempita monodose con dispositivo di protezione dell’ago
Legga queste istruzioni prima di usare la siringa preriempita.
Informazioni sulla siringa preriempita
La siringa preriempita (denominata “siringa”) è monouso e deve essere gettata dopo l’uso.
Via e modo di somministrazione
Ogni confezione contiene una siringa monouso di Amvuttra. Ogni siringa di Amvuttra contiene 25 mg
di vutrisiran da iniettare sotto la pelle (iniezione sottocutanea) una volta ogni 3 mesi.
Il medico o l’operatore sanitario mostrerà a lei e/o alla persona che le presta assistenza come preparare
e iniettare una dose di Amvuttra, prima che lei possa praticare l’iniezione da solo. Se necessario, si
rivolga all’operatore sanitario o al medico per ulteriori istruzioni e assistenza.
Conservi queste istruzioni fino al termine dell’utilizzo della siringa.
Come conservare Amvuttra
Nonconservare a temperatura superiore a 30ºC.
Noncongelare.
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Avvertenze importanti
Nonusare se la confezione è danneggiata o presenta segni di manomissione.
Nonusare la siringa se è caduta su una superficie dura.
Nontoccare lo stantuffo fino al momento di praticare l’iniezione.
Nonrimuovere il cappuccio dell’ago fino al momento dell’iniezione.
Nonrimettere mai il cappuccio sulla siringa.
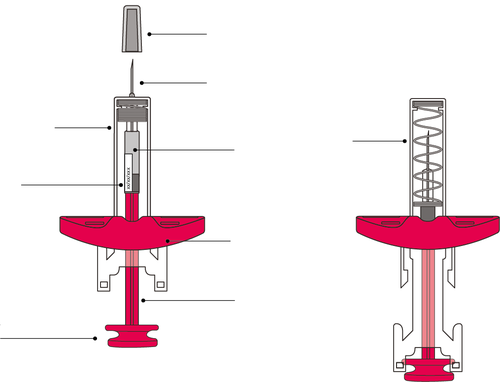
Aspetto della siringa prima e dopo l’uso:
Prima dell’usoDopo l’uso
Fase 1: Raccolta dei materiali

Raccogliere i seguenti materiali (non forniti) e
collocarli su una superficie piana pulita:
- Fazzolettino imbevuto di alcol
- Garza o batuffolo di cotone
- Cerotto adesivo
- Contenitore per materiali taglienti
Fase 2: Preparazione della siringa
Se conservata in frigorifero, lasciare che la
siringa raggiunga la temperatura ambiente per
almeno 30 minuti prima dell’uso.
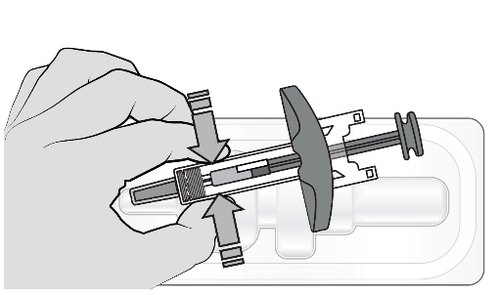
Nonriscaldare la siringa in altro modo,
ad esempio con forno a microonde, acqua
calda o vicino ad altre fonti di calore.
Rimuovere la siringa dalla confezione afferrando
il corpo della siringa.
Nontoccare lo stantuffo fino al momento
di praticare l’iniezione.
Nonusare la siringa se è caduta su una
superficie dura.
Nonrimuovere il cappuccio dell’ago fino
al momento dell’iniezione.
Fase 3: Ispezione della siringa
Controllare quanto segue:
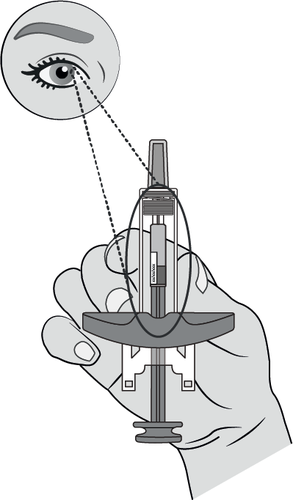
✓ La siringa non deve presentare danni,
come segni di rottura o perdite.
✓ Il cappuccio dell’ago deve essere intatto
e attaccato alla siringa.
✓ La soluzione medicinale contenuta nella
siringa deve essere limpida, da incolore a
gialla.
✓ Sull’etichetta della siringa deve essere
riportato “Amvuttra 25 mg”.
✓ La data di scadenza sull’etichetta della
siringa.
È normale vedere delle bolle d’aria all’interno
della siringa.
Nonusare la siringa se si osservano
problemi durante l’ispezione della siringa
e della soluzione medicinale.
Nonusare dopo la data di scadenza.
Nonusare se la soluzione contiene
particolato o se appare torbida o presenta
alterazione del colore.
Rivolgersi all’operatore sanitario se si
osservano problemi.
Fase 4: Scelta della sede di iniezione
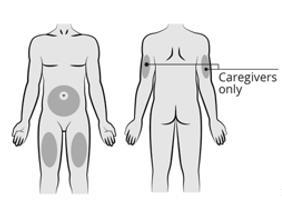
Scegliere una sede di iniezione tra le seguenti
aree:
- Addome, eccetto per l’area di 5 cm intorno all’ombelico.
- Parte anteriore delle cosce.
- Se l’iniezione è praticata da qualcun altro, può essere scelto anche il retro della parte superiore del braccio.
Noneseguire l’iniezione in aree della
pelle che presentano dolorabilità,
arrossamento, gonfiore, lividi o
indurimento o entro 5 cm dall’ombelico.
Fase : Preparazione per l’iniezione
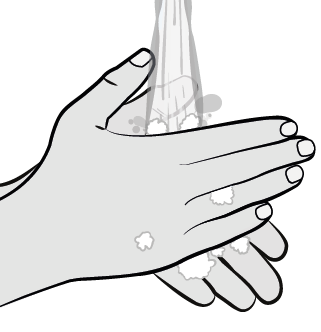
Lavarsi le mani con acqua e sapone e asciugarle
accuratamente con un asciugamano pulito.
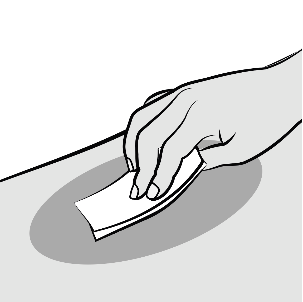
Pulire la sede scelta per l’iniezione con un
fazzolettino imbevuto di alcol.
Lasciare asciugare la pelle all’aria prima di
eseguire l’iniezione. Evitare di toccare o di
soffiare sulla sede di iniezione dopo averla pulita.
Fase 6: Rimozione del cappuccio dell’ago
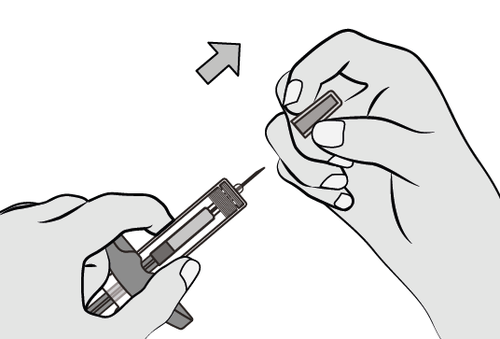
Afferrare il corpo della siringa con una mano.
Con l’altra mano estrarre il cappuccio dell’ago
tirandolo e gettarlo immediatamente.
È normale vedere una goccia di liquido sulla
punta dell’ago.
Nontoccare l’ago né lasciare che entri in
contatto con superfici.
Nonrimettere il cappuccio sulla siringa.
Nontirare lo stantuffo.
Nonusare la siringa se è caduta su una
superficie dura.
Fase 7: nserimento dell’ago
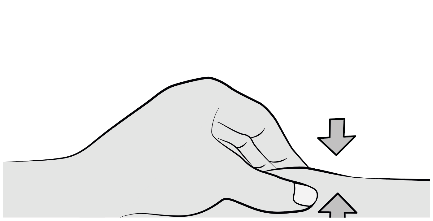
Con la mano libera, pizzicare delicatamente la
pelle pulita intorno alla sede di iniezione, al fine
di creare una protuberanza per eseguire
l’iniezione.
Inserire completamente l’ago nella pelle pizzicata
con un angolo di 45-90 gradi.
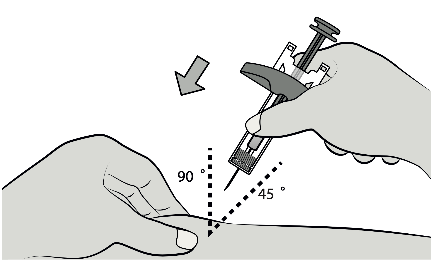
Fase 8: Iniezione del medicinale
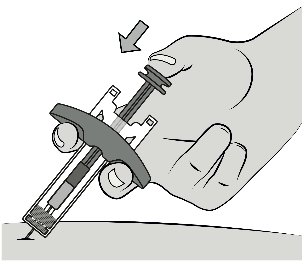
Utilizzando l’appoggio per il pollice, premere lo
stantuffo afferrando contemporaneamente la
flangia per le dita.
Premere lo stantuffo completamente, fino al
termine della corsa, per iniettare tutta la soluzione
medicinale.
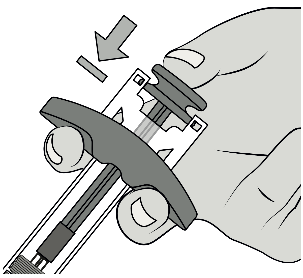
Lo stantuffo deve essere premuto
completamenteper somministrare la
dose.
Fase 9: Rilascio dello stantuffo
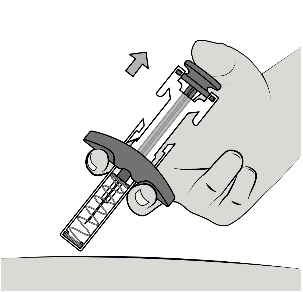
Rilasciare lo stantuffo per consentire al
dispositivo di protezione di coprire l’ago.
Rimuovere la siringa dalla pelle.
Nonbloccare il movimento dello
stantuffo.
Nontirare verso il basso il dispositivo di
protezione dell’ago. Il dispositivo di
protezione copre automaticamente l’ago.
Fase 10: Controllo della sede di iniezione
Potrebbe essere presente una piccola quantità di
sangue o liquido nella sede di iniezione.
In questo caso, esercitare pressione sulla sede di
iniezione con una garza o un batuffolo di cotone
fino ad arrestare l’eventuale sanguinamento.
Evitare di strofinare la sede di iniezione.
Fase 11: Smaltimento della siringa
Gettare immediatamentela siringa usata in un
contenitore per materiali taglienti.
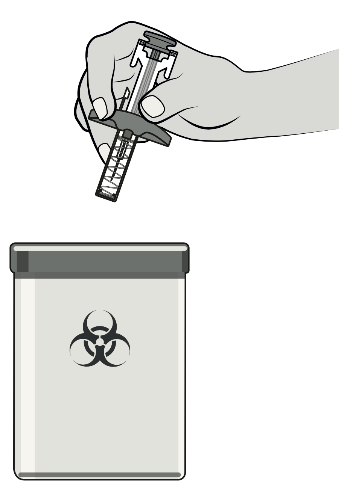
Utilizzare esclusivamente un
contenitore per materiali taglientiper
smaltire le siringhe.
-

- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile in siringa pre-riempita, 25 mg
- Codice ATCN07XX18
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a AMVUTTRAForma farmaceutica: Compressa, 10 mgPrincipio attivo: amifampridineProduttore: ACCORD HEALTHCARE, S.L.U.Prescrizione richiestaForma farmaceutica: Compressa, 10 mgPrincipio attivo: amifampridineProduttore: SERB S.A.Prescrizione richiestaForma farmaceutica: Film orodispersibile, 50 MGPrincipio attivo: riluzoleProduttore: ZAMBON S.P.A.Prescrizione richiesta
Medici online per AMVUTTRA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di AMVUTTRA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per AMVUTTRA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.













