
Come usare KESIMPTA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Kesimpta 20 mg soluzione iniettabile in siringa preriempita
ofatumumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Kesimpta e a cosa serve
- 2. Cosa deve sapere prima di usare Kesimpta
- 3. Come usare Kesimpta
- 4. Possibili effetti indesiderati
- 5. Come conservare Kesimpta
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Kesimpta e a cosa serve
Cos’è Kesimpta
Kesimpta contiene il principio attivo ofatumumab. Ofatumumab appartiene ad un gruppo di medicinali
denominati anticorpi monoclonali.
Per cosa è usato Kesimpta
Kesimpta è usato per trattare adulti affetti da forme recidivanti di sclerosi multipla (SMR).
Come funziona Kesimpta
Kesimpta funziona legandosi a un bersaglio chiamato CD20 presente sulla superficie delle cellule B.
Le cellule B sono un tipo di cellule bianche del sangue (globuli bianchi) che fanno parte del sistema
immunitario (le difese dell’organismo). Nella sclerosi multipla, il sistema immunitario attacca lo strato
protettivo presente intorno alle cellule nervose. Le cellule B sono coinvolte in questo processo.
Kesimpta colpisce e rimuove le cellule B e quindi riduce la possibilità di avere una ricaduta, allevia i
sintomi e rallenta la progressione della malattia.
2. Cosa deve sapere prima di usare Kesimpta
Non usi Kesimpta
- se è allergico a ofatumumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6)
- se le è stato comunicato che ha gravi problemi al sistema immunitario
- se soffre di una grave infezione
- se ha un cancro.
Avvertenze e precauzioni
Si rivolga al rivolga al medico prima di usare Kesimpta
- Kesimpta può provocare la riattivazione del virus dell’epatite B. Il medico la sottoporrà ad un esame del sangue per controllare se è a rischio di avere un’infezione da epatite B. Se questo mostra che ha avuto l’epatite B o è un portatore del virus dell’epatite B, il medico le chiederà di rivolgersi ad uno specialista.
- Prima di iniziare il trattamento con Kesimpta, il medico può controllare il suo sistema immunitario.
- Se ha un’infezione, il medico può decidere che non le può essere dato Kesimpta o può ritardare il trattamento con Kesimpta fino a quando l’infezione non si sarà risolta.
- Il medico controllerà se ha bisogno di vaccinazioni prima di iniziare il trattamento con Kesimpta. Se ha bisogno di un tipo di vaccino chiamato vaccino vivo o vivo-attenuato, questo deve essere somministrato almeno 4 settimane prima di iniziare il trattamento con Kesimpta. Altri tipi di vaccini devono essere somministrati almeno 2 settimane prima di iniziare il trattamento con Kesimpta.
Mentre usa Kesimpta
Si rivolga al medico:
- se ha una reazione generale correlata all’iniezione o una reazione locale al sito di iniezione. Questi sono gli effetti indesiderati più comuni del trattamento con Kesimpta e sono descritti al paragrafo 4. Di solito si verificano nelle 24 ore dopo che Kesimpta è iniettato, in particolare dopo la prima iniezione. La prima iniezione deve avvenire sotto la guida di un operatore sanitario
- se ha un’infezione. È possibile che contragga un’infezione più facilmente oppure un’infezione che ha già in corso può peggiorare. Questo avviene perché le cellule immunitarie che sono bersaglio di Kesimpta aiutano anche a combattere l’infezione. Le infezioni possono essere gravi e talvolta anche mettere in pericolo di vita
- se prevede di sottoporsi a vaccinazioni. Il medico le comunicherà se la vaccinazione necessaria per lei sarà con un vaccino vivo, un vaccino vivo-attenuato o un altro tipo di vaccino. Durante il trattamento con Kesimpta non le devono essere somministrati vaccini vivi o attenuati in quanto ciò può provocare un’infezione. Altri tipi di vaccini potrebbero risultare meno efficaci se somministrati durante il trattamento con Kesimpta.
Si rivolga al medico immediatamente se si manifesta uno dei seguenti sintomi durante il trattamento
con Kesimpta, perché possono essere segni di una condizione grave:
- se ha eruzione cutanea, orticaria, difficoltà a respirare, gonfiore del viso, delle palpebre, delle labbra, della bocca, della lingua o della gola, costrizione al torace o sensazione di svenimento. Questi potrebbero essere segni o sintomi di una reazione allergica.
- se pensa che la sclerosi multipla stia peggiorando (ad es. debolezza o cambiamenti della visione) o se nota sintomi nuovi o insoliti. Questi effetti possono indicare una rara malattia al cervello causata da un’infezione virale chiamata leucoencefalopatia multifocale progressiva (PML).
Bambini e adolescenti
Non somministrare questo medicinale a bambini e adolescenti di età inferiore a 18 anni in quanto
Kesimpta non è ancora stato studiato in questo gruppo di età.
Altri medicinali e Kesimpta
Informi il medico o il farmacista se sta assumendo, ha recentemente assunto o potrebbe assumere
qualsiasi altro medicinale.
In particolare, informi il medico o il farmacista:
- se sta assumendo, ha recentemente assunto o potrebbe assumere farmaci che influenzano il sistema immunitario perché questi possono avere un effetto additivo sul sistema immunitario
- se prevede di sottoporsi a vaccinazioni (vedere sopra "Avvertenze e precauzioni")
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico prima di prendere questo medicinale.
Gravidanza
Deve evitare di iniziare una gravidanza mentre usa Kesimpta e per 6 mesi dopo che ha smesso di
usarlo.
Se vi è la possibilità che possa iniziare una gravidanza deve usare misure contraccettive efficaci
durante il trattamento con Kesimpta e per 6 mesi dopo l’interruzione. Parli con il medico riguardo alle
opzioni disponibili.
Se inizia una gravidanza o pensa di essere in gravidanza durante il trattamento o entro 6 mesi dopo
l’ultima dose, informi immediatamente il medico. Il medico discuterà con lei dei potenziali rischi di
Kesimpta in gravidanza. Questo perché Kesimpta può ridurre il numero di cellule immunitarie (cellule
B) sia nella madre che nel nascituro. Il medico deve segnalare la gravidanza a Novartis. Anche lei può
segnalare la gravidanza contattando il rappresentante locale di Novartis (vedere paragrafo 6), oltre a
contattare il medico.
Allattamento
Kesimpta può passare nel latte materno. Si rivolga al medico per sapere i benefici e i rischi prima di
allattare il suo bambino durante l’utilizzo di Kesimpta.
Vaccinazione di neonati
Chieda consiglio al medico o al farmacista prima di vaccinare il suo neonato se ha usato Kesimpta
durante la gravidanza (vedere "Avvertenze e precauzioni" sopra).
Guida di veicoli e utilizzo di macchinari
È improbabile che Kesimpta influenzi la capacità di guidare veicoli e di utilizzare macchinari.
Kesimpta contiene sodio
Il medicinale contiene meno di 1 mmol (23 mg) di sodio per dose, cioè essenzialmente ‘senza sodio’.
3. Come usare Kesimpta
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico. Se ha dubbi consulti il
medico o il farmacista.
Kesimpta è somministrato tramite iniezione sottocutanea (iniezione sotto la pelle).
La prima iniezione deve avvenire sotto la guida di un operatore sanitario.
Le siringhe preriempite di Kesimpta sono solo monouso.
Per le istruzioni dettagliate su come iniettare Kesimpta, vedere le "Istruzioni per l’uso di Kesimpta
siringa preriempita" alla fine di questo foglio.
‘Codice QR da includere’ + www.kesimpta.eu
È possibile utilizzare Kesimpta in qualsiasi momento della giornata (mattina, pomeriggio o sera).
Quanto Kesimpta usare e quanto spesso usarlo
Non superare la dose prescritta dal medico.
- Il dosaggio iniziale è di 20 mg di Kesimpta somministrato al primo giorno del trattamento (Settimana 0) e poi alle settimane 1 e 2 (Settimana 1 e Settimana 2). Dopo queste 3 prime iniezioni, non è prevista un’iniezione alla settimana successiva (Settimana 3).
- A partire dalla Settimana 4 e poi ogni mese, la dose raccomandata è di 20 mg di Kesimpta.
Quanto tempo utilizzare Kesimpta
Continui ad utilizzare Kesimpta ogni mese per tutto il tempo indicato dal medico.
Il medico controllerà regolarmente la sua condizione per determinare se il trattamento sta avendo
l’effetto desiderato.
Se ha domande su quanto tempo utilizzare Kesimpta, parli con il medico, il farmacista o l’infermiere.
Se usa più Kesimpta di quanto deve
Se viene iniettato troppo Kesimpta, contatti immediatamente il medico.
Se dimentica di usare Kesimpta
Per ottenere il pieno beneficio di Kesimpta, è importante che si somministri ogni iniezione
puntualmente.
Se ha dimenticato un’iniezione di Kesimpta, se la autosomministri il più presto possibile. Non aspetti
la dose successiva pianificata. Gli intervalli per le iniezioni successive devono quindi essere calcolati
dal giorno in cui si somministra questa iniezione e non in base al programma originale (vedere anche
"Quanto Kesimpta usare e quanto spesso usarlo").
Se interrompe il trattamento con Kesimpta
Non smetta di usare Kesimpta e non modifichi la dose senza parlarne con il medico.
Alcuni effetti indesiderati possono essere correlati ad un basso livello di cellule B nel sangue. Dopo
aver interrotto il trattamento con Kesimpta il livello di cellule B nel sangue aumenterà gradualmente
fino alla normalità. Questo può richiedere diversi mesi. Durante questo periodo alcuni effetti
indesiderati descritti in questo foglio possono ancora verificarsi.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico o al farmacista.
| Tempo | Dose |
| Settimana 0 (primo giorno di trattamento) | m 20 mg |
| Settimana 1 | 20 mg |
| Settimana 2 | r 20 mg |
| Settimana 3 | Nessuna iniezione |
| Settimana 4 | a 20 mg |
| Ogni mese successivo | 20 mg |
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Gli effetti indesiderati di Kesimpta sono elencati di seguito. Se uno qualsiasi di questi effetti
indesiderati diventa grave, informi il medico, il farmacista o l’infermiere.
Molto comune(può interessare più di 1 persona su 10)
- infezione delle vie respiratorie superiori, con sintomi come mal di gola e naso che cola
- reazioni correlate all’iniezione, come febbre, mal di testa, dolore muscolare, brividi e stanchezza
- queste reazioni di solito si verificano nelle 24 ore successiva all’iniezione di Kesimpta, in particolare dopo la prima iniezione
- infezioni delle vie urinarie
- reazioni nel sito di iniezione, come rossore, dolore, prurito e gonfiore nel sito di iniezione
Comune(può interessare fino a 1 persona su 10)
- diminuzione del livello ematico di una proteina chiamata immunoglobulina M, che aiuta a proteggere contro le infezioni
- herpes orale
- nausea, vomito (sono stati segnalati in associazione alle reazioni correlate all'iniezione)
Non nota(la frequenza non può essere definita sulla base dei dati disponibili)
- reazioni allergiche con sintomi quali eruzione cutanea, orticaria, difficoltà a respirare, gonfiore del viso, delle palpebre, delle labbra, della bocca, della lingua o della gola, costrizione al torace o sensazione di svenimento
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema
nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti indesiderati può contribuire
a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Kesimpta
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola e sull’etichetta dopo
Scad. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare la siringa preriempita (le siringhe preriempite) nella confezione originale per proteggere il
medicinale dalla luce. Conservare in frigorifero (2 C – 8 C). Non congelare.
Se necessario, Kesimpta può essere lasciato fuori dal frigorifero per un solo periodo fino a 7 giorni a
temperatura ambiente (non superiore a 30°C). Se non è usato durante questo periodo, Kesimpta può
quindi essere rimesso in frigorifero per un massimo di 7 giorni.
Non usi questo medicinale se nota che la soluzione contiene particelle visibili o è torbida.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Kesimpta
- Il principio attivo è ofatumumab. Ogni siringa preriempita contiene 20 mg di ofatumumab.
- Gli altri componenti sono L-arginina, sodio acetato triidrato, cloruro di sodio, polisorbato 80, disodio edetato diidrato, acido cloridrico (per aggiustamento del pH), acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Kesimpta e contenuto della confezione
La soluzione iniettabile di Kesimpta si presenta da limpida a leggermente opalescente, da incolore a
leggermente gialla-brunastra.
Kesimpta è disponibile in confezioni unitarie contenenti 1 siringa preriempita e in confezioni multiple
composte da 3 scatole, ciascuna contenente 1 siringa preriempita.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlanda
Produttore
Novartis Pharma GmbH
Roonstrasse 25
90429 Norimberga
Germania
Novartis Farmacéutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcellona
Spagna
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Norimberga
Germania
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Lietuva
SIA Novartis Baltics Lietuvos filialas
Tel: +370 5 269 16 50
България
Novartis Bulgaria EOOD
Тел.: +359 2 489 98 28
Luxembourg/Luxemburg
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Česká republika
Novartis s.r.o.
Tel: +420 225 775 111
Magyarország
Novartis Hungária Kft.
Tel.: +36 1 457 65 00
Danmark
Novartis Healthcare A/S
Tlf: +45 39 16 84 00
Malta
Novartis Pharma Services Inc.
Tel: +356 2122 2872
Deutschland
Novartis Pharma GmbH
Tel: +49 911 273 0
Nederland
Novartis Pharma B.V.
Tel: +31 88 04 52 111
Eesti
SIA Novartis Baltics Eesti filiaal
Tel: +372 66 30 810
Norge
Novartis Norge AS
Tlf: +47 23 05 20 00
Ελλάδα
Novartis (Hellas) A.E.B.E.
Τηλ: +30 210 281 17 12
Österreich
Novartis Pharma GmbH
Tel: +43 1 86 6570
España
Novartis Farmacéutica, S.A.
Tel: +34 93 306 42 00
Polska
Novartis Poland Sp. z o.o.
Tel.: +48 22 375 4888
France
Novartis Pharma S.A.S.
Tél: +33 1 55 47 66 00
Portugal
Novartis Farma - Produtos Farmacêuticos, S.A.
Tel: +351 21 000 8600
Hrvatska
Novartis Hrvatska d.o.o.
Tel. +385 1 6274 220
România
Novartis Pharma Services Romania SRL
Tel: +40 21 31299 01
Ireland
Novartis Ireland Limited
Tel: +353 1 260 12 55
Slovenija
Novartis Pharma Services Inc.
Tel: +386 1 300 75 50
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
Novartis Slovakia s.r.o.
Tel: +421 2 5542 5439
Italia
Novartis Farma S.p.A.
Tel: +39 02 96 54 1
Suomi/Finland
Novartis Finland Oy
Puh/Tel: +358 (0)10 6133 200
Κύπρος
Novartis Pharma Services Inc.
Τηλ: +357 22 690 690
Sverige
Novartis Sverige AB
Tel: +46 8 732 32 00
Latvija
SIA Novartis Baltics
Tel: +371 67 887 070
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, https://www.ema.europa.eu
Istruzioni per l’uso della siringa preriempita di Kesimpta
Prima dell’iniezione di Kesimpta è importante comprendere e seguire queste istruzioni per l’uso. Se ha
dubbi, si rivolga al medico, al farmacista o all’infermiere prima di utilizzare Kesimpta per la prima
volta.
Si ricordi di:
- non utilizzarela siringa preriempita di Kesimpta se il sigillo sulla scatola esterna o il sigillo del blister sono danneggiati. Tenere la siringa preriempita di Kesimpta nella scatola sigillata fino a quando non si è pronti per l’uso
- non agitarela siringa preriempita di Kesimpta
- la siringa preriempita ha un dispositivo di protezione dell’ago che copre automaticamente l’ago dopo l’iniezione del medicinale. Il dispositivo di protezione è progettato per contribuire a tutelare da ferite accidentali da puntura di ago chiunque maneggi la siringa preriempita dopo l’iniezione
- non rimuovere il cappuccio protettivo dell’ago finché non si è pronti per l’iniezione
- fare attenzione a non toccare le alette di sicurezza della siringa prima dell’uso. Toccandole, il dispositivo di protezione dell’ago potrebbe coprire l’ago precocemente.
- Non utilizzare se la siringa preriempita è caduta su una superficie dura o è caduta dopo aver rimosso il cappuccio dell'ago.
- Eliminare la siringa preriempita di Kesimpta immediatamente dopo l’uso. Non riutilizzare lasiringa preriempita di Kesimpta. Vedere “Come smaltire la siringa preriempita di Kesimpta dopo l’utilizzo” alla fine di queste Istruzioni per l’uso.
Come conservare Kesimpta
- Conservare la confezione della siringa preriempita di Kesimpta in frigorifero a una temperatura compresa fra 2 °C e 8 °C.
- Tenere la siringa preriempita di Kesimpta nella confezione originale fino all’utilizzo per proteggerla dalla luce.
- Non congelarela siringa preriempita di Kesimpta.
Tenere Kesimpta fuori dalla vista e dalla portata dei bambini.
Componenti della siringa preriempita di Kesimpta (vedere Figura A):
Figura A
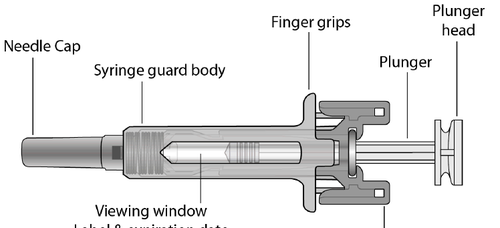
Cosa necessita per l’iniezione
Inclusa nella scatola:
- una nuova siringa preriempita di Kesimpta
Non inclusi nella scatola ( vedere Figura B):
- 1 tampone imbevuto di alcool
- 1 batuffolo di cotone o garza
- contenitore per lo smaltimento di materiale tagliente
Vedere “Come smaltire la siringa preriempita di Kesimpta
dopo l’utilizzo” alla fine di queste Istruzioni per l’uso.
Figura B

Preparazione della siringa preriempita di Kesimpta
Passaggio 1. Trovare un piano di lavoro pulito e ben illuminato.
Passaggio 2. Estrarre dal frigorifero la confezione contenente la siringa preriempita di Kesimpta e
lasciarla chiusaper circa 15-30 minuti sul piano di lavoro in modo che raggiunga la temperatura
ambiente.
Passaggio 3. Lavarsi accuratamente le mani con sapone e acqua.
Passaggio 4. Rimuovere la siringa preriempita dalla scatola ed estrarla dal blister impugnando il corpo
della siringa.
Passaggio 5. Guardare attraverso la finestra di osservazione presente sulla siringa preriempita. Il
liquido all’interno deve essere da limpido a leggermente opalescente. Potrebbero essere visibili delle
bolle d’aria di piccole dimensioni, questo è normale. Non usarela siringa preriempita se il liquido
contiene particelle facilmente visibili o è torbido.
Passaggio 6. Non usarese la siringa è danneggiata. Restituisca la siringa preriempita e la confezione
che la conteneva al farmacista.
Passaggio 7. Non usarela siringa preriempita se è
superata la data di scadenza ( vedere Figura C).
Restituisca al farmacista la siringa preriempita scaduta e
la sua confezione.
Figura C
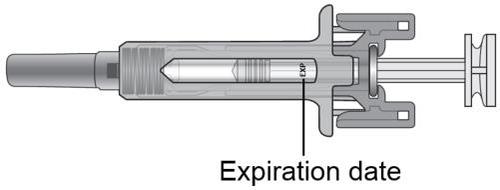
Scegliere e pulire la sede di iniezione
- Le aree del corpo che può utilizzare per l’iniezione di Kesimpta comprendono:
- la parte anteriore delle cosce ( vedere Figura D)
- l’area del basso stomaco (addome), escludendo un’area di 5 centimetri intorno all’ombelico ( vedere Figura D)
- la parte superiore esterna delle braccia, se l’iniezione è effettuata da chi la assiste o da un operatore sanitario ( vedere FiguraE). Figura D
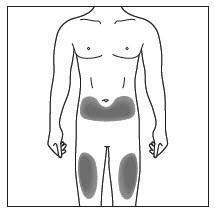
Figura E
(solo per chi la assiste o operatori
sanitari)
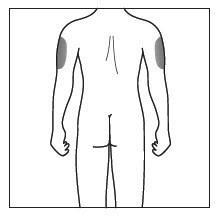
- Scegliere una sede differente ogni volta che si pratica l’iniezione di Kesimpta.
- Non praticare l’iniezionein aree dove la cute è sensibile, presenta lividi, è arrossata, desquamata o indurita. Evitare le aree dove sono presenti cicatrici, smagliature o infezioni.
Passaggio 8. Con un movimento circolare, pulire la sede di iniezione con un tampone imbevuto di
alcol. Lasciare che si asciughi prima di praticare l’iniezione. Non toccare nuovamente l’area pulita
prima di procedere all’iniezione.
Come praticare l’iniezione
Passaggio 9. Rimuovere con attenzione il cappuccio
protettivo copriago dalla siringa preriempita ( vedere
Figura F). Gettare via il cappuccio copriago. È possibile
che una goccia di liquido fuoriesca dalla punta dell’ago.
Questo è normale.
Figura F
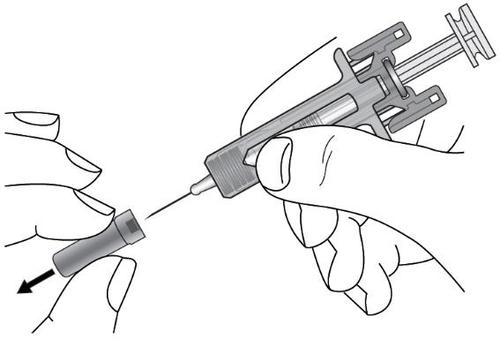
Passaggio 10. Pizzicare delicatamente con una mano la
pelle della sede di iniezione. Con l’altra mano inserire
l’ago nella pelle come illustrato ( vedere Figura G).
Spingere l’ago in profondità per assicurare che tutto il
medicinale sia somministrato.
Figura G
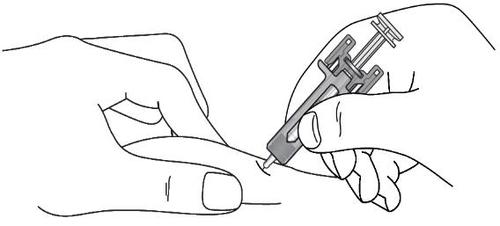
Passaggio 11. Tenere la siringa come illustrato ( vedere
Figura H). Premere lentamente lo stantuffo fino in
fondo in modo che la testa dello stantuffo sia
completamente tra le alette di protezione della siringa.
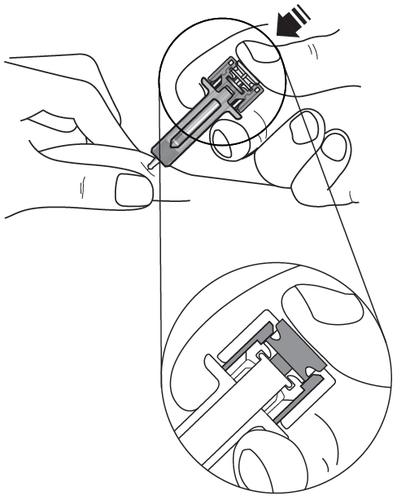
Passaggio 12. Continuare a mantenere premuto lo
stantuffo per 5 secondi, mantenendo la siringa in
posizione.
Figura H
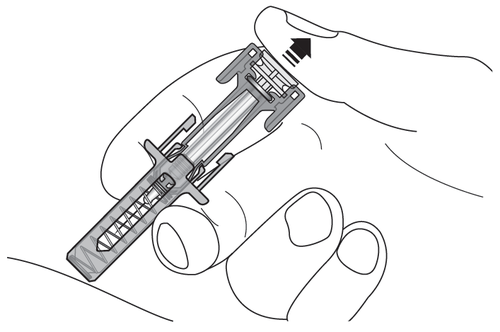
Passaggio 13. Rilasciare lentamentelo stantuffo per
consentire alla protezione della siringa di coprire l’ago
esposto ( vedere Figura I), quindi rimuovere la siringa
dalla sede di iniezione.
Passaggio 14. Potrebbe verificarsi un leggero
sanguinamento nella sede dell’iniezione. In tal caso può
premere un batuffolo di cotone o una garza sulla sede
dell’iniezione e tenerlo per 10 secondi. Non strofinare la
sede di iniezione. Se necessario, è possibile coprire la
sede dell’iniezione con un piccolo cerotto, se il
sanguinamento continua.
Figura I
Come smaltire la siringa preriempita di Kesimpta dopo l’utilizzo
Passaggio 15. Smaltire la siringa preriempita utilizzata
riponendola in un contenitore per materiale tagliente
(contenitore richiudibile, resistente alle forature o
similare) ( vedere Figura J).
- Non smaltirela siringa preriempita dopo l’utilizzo Figura J
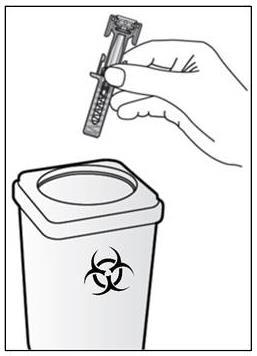
nel contenitore dei rifiuti domestici.
- Le siringhe usate non devono mai essere riutilizzate.
Tenere il contenitore per materiale tagliente fuori
dalla vista e dalla portata dei bambini.
Kesimpta 20 mg soluzione iniettabile in penna preriempita
ofatumumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Kesimpta e a cosa serve
- 2. Cosa deve sapere prima di usare Kesimpta
- 3. Come usare Kesimpta
- 4. Possibili effetti indesiderati
- 5. Come conservare Kesimpta
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Kesimpta e a cosa serve
Cos’è Kesimpta
Kesimpta contiene il principio attivo ofatumumab. Ofatumumab appartiene ad un gruppo di medicinali
denominati anticorpi monoclonali.
Per cosa è usato Kesimpta
Kesimpta è usato per trattare adulti affetti da forme recidivanti di sclerosi multipla (SMR).
Come funziona Kesimpta
Kesimpta funziona legandosi a un bersaglio chiamato CD20 presente sulla superficie delle cellule B.
Le cellule B sono un tipo di cellule bianche del sangue (globuli bianchi) che fanno parte del sistema
immunitario (le difese dell’organismo). Nella sclerosi multipla, il sistema immunitario attacca lo strato
protettivo presente intorno alle cellule nervose. Le cellule B sono coinvolte in questo processo
Kesimpta colpisce e rimuove le cellule B e quindi riduce la possibilità di avere una ricaduta, allevia i
sintomi e rallenta la progressione della malattia.
2. Cosa deve sapere prima di usare Kesimpta
Non usi Kesimpta
- se è allergico a ofatumumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6)
- se le è stato comunicato che ha gravi problemi al sistema immunitario
- se soffre di una grave infezione
- se ha un cancro.
Avvertenze e precauzioni
Si rivolga al rivolga al medico prima di Kesimpta
- Kesimpta può provocare la riattivazione del virus dell’epatite B. Il medico la sottoporrà ad un esame del sangue per controllare se è a rischio di avere un’infezione da epatite B. Se questo mostra che ha avuto l’epatite B o è un portatore del virus dell’epatite B, il medico le chiederà di rivolgersi ad uno specialista.
- Prima di iniziare il trattamento con Kesimpta, il medico può controllare il suo sistema immunitario.
- Se ha un’infezione, il medico può decidere che non le può essere dato Kesimpta o può ritardare il trattamento con Kesimpta fino a quando l’infezione non si sarà risolta.
- Il medico controllerà se lei ha bisogno di vaccinazioni prima di iniziare il trattamento con Kesimpta. Se ha bisogno di un tipo di vaccino chiamato vaccino vivo o vivo-attenuato, questo deve essere somministrato almeno 4 settimane prima di iniziare il trattamento con Kesimpta. Altri tipi di vaccini devono essere somministrati almeno 2 settimane prima di iniziare il trattamento Kesimpta.
Mentre usa Kesimpta
Si rivolga al medico:
- se ha una reazione generale correlata all’iniezione o una reazione locale al sito di iniezione. Questi sono gli effetti indesiderati più comuni del trattamento con Kesimpta e sono descritti al paragrafo 4. Di solito si verificano nelle 24 ore dopo che Kesimpta è iniettato, in particolare dopo la prima iniezione. La prima iniezione deve avvenire sotto la guida di un operatore sanitario
- se ha un’infezione. È possibile che contragga un’infezione più facilmente oppure un’infezione che ha già in corso può peggiorare. Questo avviene perché le cellule immunitarie che sono bersaglio di Kesimpta aiutano anche a combattere l’infezione. Le infezioni possono essere gravi e talvolta anche mettere in pericolo di vita
- se prevede di sottoporsi a vaccinazioni. Il medico le comunicherà se la vaccinazione necessaria per lei sarà con un vaccino vivo, un vaccino vivo-attenuato o un altro tipo di vaccino. Durante il trattamento con Kesimpta non le devono essere somministrati vaccini vivi o attenuati in quanto ciò può provocare un’infezione. Altri tipi di vaccini potrebbero risultare meno efficaci se somministrati durante il trattamento con Kesimpta.
Si rivolga al medico immediatamente se si manifesta uno dei seguenti sintomi durante il trattamento
con Kesimpta, perché possono essere segni di una condizione grave:
- se ha eruzione cutanea, orticaria, difficoltà a respirare, gonfiore del viso, delle palpebre, delle labbra, della bocca, della lingua o della gola, costrizione al torace o sensazione di svenimento. Questi potrebbero essere segni o sintomi di una reazione allergica.
- se pensa che la sclerosi multipla stia peggiorando (ad es. debolezza o cambiamenti della visione) o se nota sintomi nuovi o insoliti. Questi effetti possono indicare una rara malattia al cervello causata da un’infezione virale chiamata leucoencefalopatia multifocale progressiva (PML).
Bambini e adolescenti
Non somministrare questo medicinale a bambini e adolescenti di età inferiore a 18 anni in quanto
Kesimpta non è ancora stato studiato in questo gruppo di età.
Altri medicinali e Kesimpta
Informi il medico o il farmacista se sta assumendo, ha recentemente assunto o potrebbe assumere
qualsiasi altro medicinale.
In particolare, informi il medico o il farmacista:
- se sta assumendo, ha recentemente assunto o potrebbe assumere farmaci che influenzano il sistema immunitario perché questi possono avere un effetto additivo sul sistema immunitario
- se prevede di sottoporsi a vaccinazioni (vedere sopra "Avvertenze e precauzioni")
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico prima di prendere questo medicinale.
Gravidanza
Deve evitare di iniziare una gravidanza mentre usa Kesimpta e per 6 mesi dopo che ha smesso di
usarlo.
Se vi è la possibilità che possa iniziare una gravidanza deve usare misure contraccettive efficaci
durante il trattamento con Kesimpta e per 6 mesi dopo l’interruzione. Parli con il medico riguardo alle
opzioni disponibili.
Se inizia una gravidanza o pensa di essere in gravidanza durante il trattamento o entro 6 mesi dopo
l’ultima dose, informi immediatamente il medico. Il medico discuterà con lei dei potenziali rischi di
Kesimpta in gravidanza. Questo perché Kesimpta può ridurre il numero di cellule immunitarie (cellule
B) sia nella madre che nel nascituro. Il medico deve segnalare la gravidanza a Novartis. Anche lei può
segnalare la gravidanza contattando il rappresentante locale di Novartis (vedere paragrafo 6), oltre a
contattare il medico.
Allattamento
Kesimpta può passare nel latte materno. Si rivolga al medico per sapere i benefici e i rischi prima di
allattare il suo bambino durante l’utilizzo di Kesimpta.
Vaccinazione di neonati
Chieda consiglio al medico o al farmacista prima di vaccinare il suo neonato se ha usato Kesimpta
durante la gravidanza (vedere "Avvertenze e precauzioni" sopra).
Guida di veicoli e utilizzo di macchinari
È improbabile che Kesimpta influenzi la sua capacità di guidare e di utilizzare le macchinari.
Kesimpta contiene sodio
Il medicinale contiene meno di 1 mmol (23 mg) di sodio per dose, cioè essenzialmente ‘senza sodio’.
3. Come usare Kesimpta
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico o del farmacista. Se ha
dubbi consulti il medico o il farmacista.
Kesimpta è somministrato tramite iniezione sottocutanea (iniezione sotto la pelle).
La prima iniezione deve avvenire sotto la guida di un operatore sanitario.
Le penne preriempite Kesimpta sono solo monouso.
Per le istruzioni dettagliate su come iniettare Kesimpta, vedere le "Istruzioni per l’uso di Kesimpta
penna Sensoready” alla fine di questo foglio.
‘Codice QR da includere’ + www.kesimpta.eu
È possibile utilizzare Kesimpta in qualsiasi momento della giornata (mattina, pomeriggio o sera).
Quanto Kesimpta usare e quanto spesso usarlo
Non superare la dose prescritta dal medico.
- Il dosaggio iniziale è di 20 mg di Kesimpta somministrato al primo giorno del trattamento (Settimana 0) e poi alle settimane 1 e 2 (Settimana 1 e Settimana 2). Dopo queste 3 prime iniezioni, non è prevista un’iniezione alla settimana successiva (Settimana 3).
- A partire dalla Settimana 4 e poi ogni mese, la dose raccomandata è di 20 mg di Kesimpta.
Quanto tempo utilizzare Kesimpta
Continui ad utilizzare Kesimpta ogni mese per tutto il tempo indicato dal medico.
Il medico controllerà regolarmente la sua condizione per determinare se il trattamento sta avendo
l’effetto desiderato.
Se ha domande su quanto tempo utilizzare Kesimpta, parli con il medico, il farmacista o l’infermiere.
Se usa più Kesimpta di quanto deve
Se viene iniettato troppo Kesimpta, contatti immediatamente il medico.
Se dimentica di usare Kesimpta
Per ottenere il pieno beneficio di Kesimpta, è importante che si somministri ogni iniezione
puntualmente.
Se ha dimenticato un’iniezione di Kesimpta, se la autosomministri il più presto possibile. Non aspetti
la dose successiva pianificata. Gli intervalli per le iniezioni successive devono quindi essere calcolati
dal giorno in cui si somministra questa iniezione e non in base al programma originale (vedere anche
"Quanto Kesimpta usare e quanto spesso usarlo").
Se interrompe il trattamento con Kesimpta
Non smetta di usare Kesimpta e non modifichi la dose senza parlarne con il medico.
Alcuni effetti indesiderati possono essere correlati ad un basso livello di cellule B nel sangue. Dopo
aver interrotto il trattamento con Kesimpta il livello di cellule B nel sangue aumenterà gradualmente
fino alla normalità. Questo può richiedere diversi mesi. Durante questo periodo alcuni effetti
indesiderati descritti in questo foglio possono ancora verificarsi.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico o al farmacista.
| Tempo | m Dose |
| Settimana 0 (primo giorno di trattamento) | 20 mg |
| Settimana 1 | 20 mg |
| Settimana 2 | r 20 mg |
| Settimana 3 | a Nessuna iniezione |
| Settimana 4 | 20 mg |
| Ogni mese successivo | F 20 mg |
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino.
Gli effetti indesiderati di Kesimpta sono elencati di seguito. Se uno qualsiasi di questi effetti
indesiderati diventa grave, informi il medico, il farmacista o l’infermiere.
Molto comune(può interessare più di 1 persona su 10)
- infezione delle vie respiratorie superiori, con sintomi come mal di gola e naso che cola
- reazioni correlate all’iniezione, come febbre, mal di testa, dolore muscolare, brividi e stanchezza
- queste reazioni di solito si verificano nelle 24 ore successive all’iniezione di Kesimpta, in particolare dopo la prima iniezione
- infezioni delle vie urinarie
- reazioni nel sito di iniezione, come rossore, dolore, prurito e gonfiore nel sito di iniezione
Comune (può interessare fino a 1 persona su 10)
- diminuzione del livello ematico di una proteina chiamata immunoglobulina M, che aiuta a proteggere contro le infezioni
- herpes orale
- nausea, vomito (sono stati segnalati in associazione alle reazioni correlate all'iniezione)
Non nota(la frequenza non può essere definita sulla base dei dati disponibili)
- reazioni allergiche con sintomi quali eruzione cutanea, orticaria, difficoltà a respirare, gonfiore del viso, delle palpebre, delle labbra, della bocca, della lingua o della gola, costrizione al torace o sensazione di svenimento
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o, al farmacista. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema
nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti indesiderati può contribuire
a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Kesimpta
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola e sull’etichetta dopo
Scad. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare la penna preriempita (le penne preriempite) nella confezione originale per proteggere il
medicinale dalla luce. Conservare in frigorifero (2 C – 8 C). Non congelare.
Se necessario, Kesimpta può essere lasciato fuori dal frigorifero per un solo periodo fino a 7 giorni a
temperatura ambiente (non superiore a 30°C). Se non è usato durante questo periodo, Kesimpta può
quindi essere rimesso in frigorifero per un massimo di 7 giorni.
Non usi questo medicinale se nota che la soluzione contiene particelle visibili o è torbida.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene Kesimpta
- Il principio attivo è ofatumumab. Ogni penna preriempita contiene 20 mg di ofatumumab.
- Gli altri componenti sono L-arginina, sodio acetato triidrato, cloruro di sodio, polisorbato 80, disodio edetato diidrato, acido cloridrico (per aggiustamento del pH), acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Kesimpta e contenuto della confezione
La soluzione iniettabile di Kesimpta si presenta da limpida a leggermente opalescente, da incolore a
leggermente gialla-brunastra.
Kesimpta è disponibile in confezioni unitarie contenenti 1 penna preriempita Sensoready e in
confezioni multiple composte da 3 scatole, ciascuna contenente 1°penna preriempita Sensoready.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlanda
Produttore
Novartis Pharma GmbH
Roonstrasse 25
90429 Norimberga
Germania
Novartis Farmacéutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcellona
Spagna
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Norimberga
Germania
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Lietuva
SIA Novartis Baltics Lietuvos filialas
Tel: +370 5 269 16 50
България
Novartis Bulgaria EOOD
Тел.: +359 2 489 98 28
Luxembourg/Luxemburg
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Česká republika
Novartis s.r.o.
Tel: +420 225 775 111
Magyarország
Novartis Hungária Kft.
Tel.: +36 1 457 65 00
Danmark
Novartis Healthcare A/S
Tlf: +45 39 16 84 00
Malta
Novartis Pharma Services Inc.
Tel: +356 2122 2872
Deutschland
Novartis Pharma GmbH
Tel: +49 911 273 0
Nederland
Novartis Pharma B.V.
Tel: +31 88 04 52 111
Eesti
SIA Novartis Baltics Eesti filiaal
Tel: +372 66 30 810
Norge
Novartis Norge AS
Tlf: +47 23 05 20 00
Ελλάδα
Novartis (Hellas) A.E.B.E.
Τηλ: +30 210 281 17 12
Österreich
Novartis Pharma GmbH
Tel: +43 1 86 6570
España
Novartis Farmacéutica, S.A.
Tel: +34 93 306 42 00
Polska
Novartis Poland Sp. z o.o.
Tel.: +48 22 375 4888
France
Novartis Pharma S.A.S.
Tél: +33 1 55 47 66 00
Portugal
Novartis Farma - Produtos Farmacêuticos, S.A.
Tel: +351 21 000 8600
Hrvatska
Novartis Hrvatska d.o.o.
Tel. +385 1 6274 220
România
Novartis Pharma Services Romania SRL
Tel: +40 21 31299 01
Ireland
Novartis Ireland Limited
Tel: +353 1 260 12 55
Slovenija
Novartis Pharma Services Inc.
Tel: +386 1 300 75 50
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
Novartis Slovakia s.r.o.
Tel: +421 2 5542 5439
Italia
Novartis Farma S.p.A.
Tel: +39 02 96 54 1
Suomi/Finland
Novartis Finland Oy
Puh/Tel: +358 (0)10 6133 200
Κύπρος
Novartis Pharma Services Inc.
Τηλ: +357 22 690 690
Sverige
Novartis Sverige AB
Tel: +46 8 732 32 00
Latvija
SIA Novartis Baltics
Tel: +371 67 887 070
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, https://www.ema.europa.eu
Istruzioni per l’uso della penna Sensoready di Kesimpta
Prima dell’iniezione di Kesimpta è importante comprendere e seguire queste istruzioni per l'uso. Se ha
dubbi, si rivolga al medico, al farmacista o all’infermiere prima di utilizzare Kesimpta per la prima
volta.
Si ricordi di:
- non utilizzarela penna se il sigillo sulla scatola esterna o il sigillo del blister sono danneggiati. Tenere la penna nella scatola esterna sigillata fino a quando non si è pronti per l’uso
- non agitarela penna
- selascia cadere la penna, non la usise sembra danneggiata o se l’ha fatta cadere senza il cappuccio
- eliminare la penna immediatamente dopo l’uso. Non riutilizzare la penna. Vedere “Come smaltire la penna Sensoready di Kesimpta dopo l’utilizzo” alla fine di queste Istruzioni per l’uso.
Come conservare Kesimpta
- Conservare la penna confezionata in frigorifero a una temperatura compresa fra 2 °C e 8 °C.
- Tenere la penna nella confezione originale fino all’utilizzo per proteggerla dalla luce.
- Non congelarela penna.
Tenere Kesimpta fuori dalla vista e dalla portata dei bambini.
Componenti della penna Sensoready di Kesimpta (vedere figura A):
Figura A
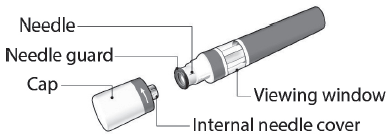
La penna Sensoready di Kesimpta è mostrata con il cappuccio rimosso. Nonrimuovere il cappuccio
fino a quando non è pronto per l’iniezione.
Cosa necessita per l’iniezione:
Incluso nella confezione:
- una nuova penna Sensoready di Kesimpta ( vedere Figura B) Figura B
Non incluso nella confezione ( vedere Figura C):
- 1 tampone imbevuto di alcool
- 1 batuffolo di cotone o garza
- contenitore per lo smaltimento di materiali taglienti Figura C

Vedere “Come smaltire la Penna Sensoready di
Kesimpta dopo l’utilizzo” alla fine di queste
Istruzioni per l’uso.
Prima dell’iniezione
Estrarre dal frigorifero la penna da 15 a 30 minuti prima dell’iniezionein modo che raggiunga la
temperatura ambiente.
Passaggio 1. Importanti controlli di sicurezza
prima dell’iniezione (vedere Figura D)
- Guardare attraverso la finestra di osservazione. Il liquido deve essere limpido o leggermente opalescente. Non usarese il liquido contiene particelle facilmente visibili o è torbido Potrebbe vedere delle piccole bolle d’aria, questo è normale.
- Fare attenzione alla data di scadenza (EXP)sulla penna. Non usarela penna dopo la data di scadenza. Figura D
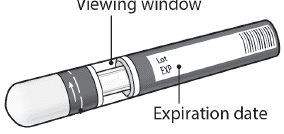
Contattare il farmacista o l’operatore sanitario se la
penna non soddisfa uno qualsiasi di questi requisiti.
Passaggio 2. Scelta della sede di iniezioneFigura E
- La sede raccomandata è la parte anteriore delle cosce. Si può anche usare il basso addome, escludendo un’area di 5 centimetri intorno all’ombelico ( vedere Figura E).
- Scegliere una sede differente per ogni nuova iniezione di Kesimpta.
- Non iniettarein aree dove la pelle è sensibile, sono presenti lividi, è arrossata, desquamata o indurita. Evitare le aree dove sono presenti cicatrici o smagliature o sedi di infezione.
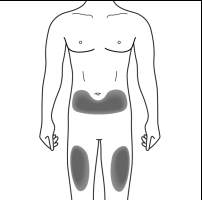
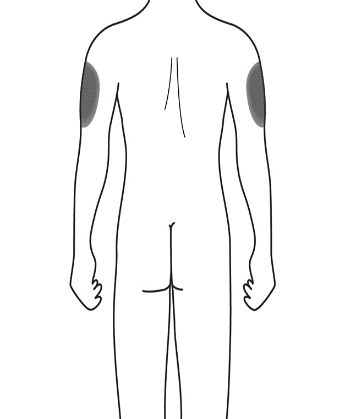
- Se l’iniezione le viene somministrata da una persona che l’assisteo da un operatoresanitario, può essere effettuata anche nella parte superiore esterna delle braccia ( vedereFigura F). Figura F(solo per chi la assiste o operatori sanitari)
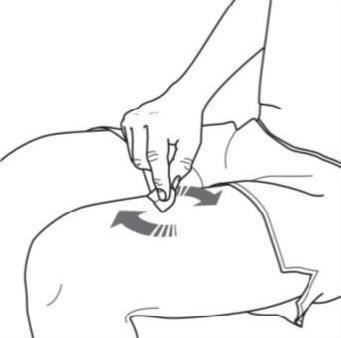
Passaggio 3. Pulizia della sede di iniezione
- Lavarsi le mani con acqua e sapone.
- Con un movimento circolare, pulire la sede di iniezione con un tampone imbevuto di alcol. Lasciare asciugare prima di effettuare l’iniezione ( vedere Figura G).
- Non toccare di nuovo l’area pulita prima di effettuare l’iniezione. Figura G
La sua iniezione
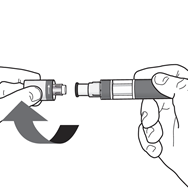
Passaggio 4. Rimozione del cappuccio:
- Rimuovere il cappuccio solo quando si è pronti per l’uso della penna.
- Svitare il cappuccio nella direzione delle frecce ( vedere Figura H).
- Una volta che è stato rimosso, gettare il cappuccio. Non tentare di rimettere ilcappuccio.
- Usare la penna entro 5 minuti dalla rimozione del cappuccio. È possibile che una goccia di liquido fuoriesca dalla punta dell’ago. Questo è normale. Figura H
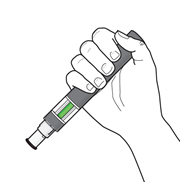
Passaggio 5. Posizione della penna:Figura I
- Tenere la penna a 90 gradi rispetto alla sede di iniezione pulita ( vedere Figura I).
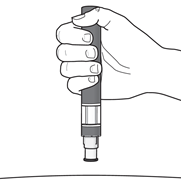
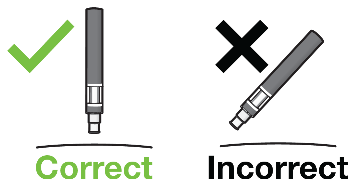
Importante:durante l’iniezionesentirà 2 click sonori.
- Il primo clickindica che l’iniezione è iniziata.
- Il secondo clickindica che l’iniezione è quasi completata. Continuare a tenere saldamente la penna contro la pelle fino a quando un indicatore verderiempierà la finestra e si fermerà.
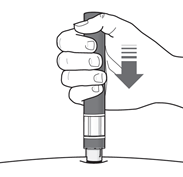
Passaggio 6. Iniziare l’iniezione
- Premere con fermezza la penna contro la pelle per iniziare l’iniezione ( vedere Figura J).
- Il primo clickindica che l’iniezione è iniziata.
- Continuare a mantenerela penna con fermezza contro la pelle.
- L’ indicatore verdemostra lo stato di avanzamento dell’iniezione. Figura J
Passaggio 7. Completare l’iniezioneFigura K
- Attendere il suono del secondo click. Questo indica che l’iniezione è quasicompletata.
- Controllare che l’ indicatore verdeabbia riempito la finestra e si sia fermato ( vedereFigura K).
- A questo punto è possibile rimuovere la penna ( vedere Figura L).
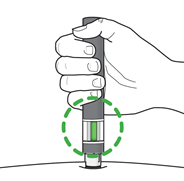
Figura L
Dopo la sua iniezione:
- Se l’indicatore verde non riempie la finestra, questo significa che non è stata somministrata la dose completa. Contattare il medico o il farmacista se l’indicatore verde non è visibile.
- Vi può essere una piccola quantità di sangue nel sito di iniezione. È possibile premere un batuffolo di cotone o garza sul sito di iniezione e tenerlo per 10 secondi. Non strofinare il sito di iniezione. È possibile coprire il sito di iniezione con un cerotto adesivo piccolo, se il sanguinamento continua.
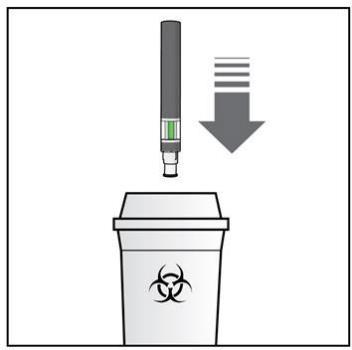
Come smaltire la penna Sensoready di Kesimpta dopo l’utilizzo
Passaggio 8. Smaltire la penna Sensoready di
Kesimpta
- Smaltire la penna utilizzata riponendola in un contenitore per materiale tagliente (es. un contenitore richiudibile, resistente alle forature o similari) ( vedere Figura M).
- Non tentare mai di riutilizzare la penna.
Tenere il contenitore per materiale tagliente fuori
dalla vista e dalla portata dei bambini
Figura M
-

- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile, 20 MG
- Codice ATCL04AG12
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a KESIMPTAForma farmaceutica: Polvere per soluzione per infusione endovenosa, 120 MGPrincipio attivo: belimumabProduttore: GLAXOSMITHKLINE (IRELAND) LIMITEDPrescrizione richiestaForma farmaceutica: Concentrato per soluzione per infusione, 150 mgPrincipio attivo: ublituximabProduttore: NEURAXPHARM PHARMACEUTICALS, S.LPrescrizione richiestaForma farmaceutica: Polvere per soluzione per infusione endovenosa, 300 MGPrincipio attivo: vedolizumabProduttore: TAKEDA PHARMA A/SPrescrizione richiesta
Medici online per KESIMPTA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di KESIMPTA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per KESIMPTA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.





