
Come usare MIRCERA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
MIRCERA
30 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
40 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
50 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
60 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
75 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
100 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
120 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
150 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
200 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
250 microgrammi/0,3 mL soluzione iniettabile in siringa preriempita
360 microgrammi/0,6 mL soluzione iniettabile in siringa preriempita
metossipolietilenglicole-epoetina beta
Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Cos’è MIRCERA e a cosa serve
- 2. Cosa deve sapere prima di usare MIRCERA
- 3. Come usare MIRCERA
- 4. Possibili effetti indesiderati
- 5. Come conservare MIRCERA
- 6. Contenuto della confezione e altre informazioni
1. Cos' è MIRCERA e a cosa serve
Questo medicinale le è stato prescritto perché soffre di anemia causata da malattia renale cronica e
associata a sintomi tipici quali stanchezza, debolezza e affanno. Questo significa che il sangue
contiene una quantità insufficiente di globuli rossi e il livello dell'emoglobina è troppo basso (i tessuti
del corpo potrebbero non ricevere ossigeno a sufficienza).
MIRCERA è indicato per trattare solo l'anemia sintomatica causata dalla malattia renale cronica in
pazienti adulti e pediatrici (di età compresa tra i 3 mesi ed inferiore ai 18 anni) in trattamento con la
terapia di mantenimento con ESA, agenti stimolanti dell'eritropoiesi, dopo che il loro livello di
emoglobina è stato stabilizzato con il precedente ESA. MIRCERA è un medicinale prodotto con la
tecnologia genica. Analogamente all'ormone naturale eritropoietina, MIRCERA aumenta il numero di
globuli rossi e il livello dell'emoglobina nel sangue.
2. Cosa deve sapere prima di usare MIRCERA
Non usi MIRCERA
- se è allergico a metossipolietilenglicole-epoetina beta o ad uno qualsiasi degli eccipienti di questo medicinale (elencati al paragrafo 6)
- se soffre di pressione sanguigna alta che non può essere controllata
Avvertenze e precauzioni
La sicurezza e l’efficacia della terapia con MIRCERA non sono state stabilite in altre indicazioni,
compreso il trattamento dell’anemia nei pazienti affetti da tumore.
La sicurezza e l'efficacia della terapia con MIRCERA nei pazienti pediatrici sono state stabilite solo in
pazienti il cui livello di emoglobina è stato precedentemente stabilizzato dal trattamento con un ESA.
Prima del trattamento con MIRCERA
- In alcuni pazienti trattati con agenti stimolanti l’eritropoiesi (ESA), incluso MIRCERA, è stata osservata una malattia chiamata aplasia eritroide pura (PRCA, interruzione o riduzione della produzione di globuli rossi) dovuta agli anticorpi antieritropoietina.
- Se il medico sospetta o conferma la presenza di questi anticorpi nel sangue, lei non deve essere trattato con MIRCERA.
- Se è un paziente con epatite C in trattamento con interferone e ribavirina deve parlare con il medico poiché l’associazione degli ESA con interferone e ribavirina può determinare una perdita di efficacia e, in rari casi, lo sviluppo di una condizione chiamata aplasia eritroide pura (PRCA), una grave forma di anemia. Gli ESA non sono approvati per il trattamento dell’anemia associata a epatite C.
- Se è un paziente con malattia renale cronica ed anemia, in trattamento con un ESA, ed è anche affetto da tumore deve essere informato che gli ESA potrebbero avere un impatto negativo sulle sue condizioni di salute. Deve discutere con il medico le alternative per il trattamento dell’anemia.
- Non è noto se MIRCERA abbia un effetto diverso sui pazienti affetti da emoglobinopatie (disturbi associati a emoglobina anormale), emorragie passate o attuali, convulsioni o conta piastrinica elevata. In caso di presenza di una di queste patologie, il medico gliene parlerà e il trattamento dovrà essere somministrato con cautela.
- Gli individui sani non devono usare MIRCERA. L'uso di questo medicinale può portare a livelli di emoglobina eccessivamente elevati e causare problemi al cuore o ai vasi sanguigni, con effetti potenzialmente letali.
Durante il trattamento con MIRCERA
- se è affetto da insufficienza renale cronica, e in particolare se non risponde in modo adeguato a MIRCERA, il medico controllerà la dose di MIRCERA perché se non risponde al trattamento, l’aumento ripetuto della dose di MIRCERA può aumentare il rischio di problemi al cuore o ai vasi sanguigni e potrebbe aumentare il rischio di infarto miocardico, ictus e morte.
- Il medico potrebbe iniziare il trattamento con MIRCERA se il livello dell’emoglobina è uguale o inferiore a 10 g/dL (6,21 mmol/L). Dopo l’inizio della terapia, il medico cercherà di mantenere il livello di emoglobina tra 10 e 12 g/dL (7,45 mmol/L).
- Prima e durante il trattamento con MIRCERA, il medico controllerà la quantità di ferro nel sangue. Qualora dovesse risultare troppo bassa, il medico potrebbe somministrarle un integratore aggiuntivo di ferro.
- Prima e durante il trattamento con MIRCERA, il medico controllerà la pressione sanguigna. Se questa dovesse risultare troppo alta e non potesse essere controllata con medicinali appropriati o con una dieta specifica, il medico interromperà il trattamento con MIRCERA o ridurrà la dose.
- Il medico controllerà che i livelli di emoglobina non superino un certo limite, poiché un’emoglobina elevata potrebbe metterla a rischio di avere un problema al cuore o ai vasi sanguigni, e potrebbe aumentare il rischio di trombosi, compresi casi di embolia polmonare, di infarto del miocardio, ictus e morte.
- Se avverte stanchezza, debolezza o affanno, si rivolga al medico perché queste sensazioni potrebbero significare che il trattamento con MIRCERA non è efficace. Il medico controllerà che non siano presenti altre cause di anemia e potrebbe richiedere analisi del sangue o esami del midollo osseo. Qualora abbia sviluppato PRCA, il trattamento con MIRCERA verrà interrotto. Non riceverà altri ESA e il medico provvederà a trattarla per questa condizione.
Bambini e adolescenti
MIRCERA può essere utilizzato per il trattamento di bambini e adolescenti, di età compresa tra i 3
mesi ed inferiore ai 18 anni, con anemia associata a malattie renali croniche. Tali pazienti devono
essere stabilizzati con la terapia di mantenimento a base di ESA prima di passare a MIRCERA e
possono o meno ricevere la dialisi.
Informi il medico, il farmacista o l'infermiere prima di prendere il medicinale se lei, o suo figlio ha
meno di 18 anni di età.
Faccia particolare attenzione con altri prodotti che stimolano la produzione di globuli rossi:
MIRCERA appartiene ad un gruppo di prodotti che stimolano la produzione di globuli rossi come la
proteina umana eritropoietina. Il medico dovrà sempre registrare lo specifico prodotto che sta
utilizzando.
In associazione al trattamento con epoetina sono state riferite gravi reazioni cutanee, comprese la
sindrome di Stevens-Johnson (SJS) e la necrolisi epidermica tossica (TEN).
SJS/TEN possono manifestarsi inizialmente come macchie rossastre a forma di bersaglio o chiazze
circolari che spesso si associano a vesciche centrali sul tronco. Possono essere presenti anche ulcere
nella zona della bocca, della gola, del naso, dei genitali e degli occhi (occhi arrossati e gonfi). Queste
eruzioni cutanee gravi sono spesso precedute da febbre e/o sintomi simil-influenzali. Le eruzioni
possono progredire in diffusa desquamazione della pelle e complicanze potenzialmente letali.
Se dovesse manifestare un’eruzione cutanea grave o un altro di questi sintomi cutanei, smetta di
prendere Mircera e contatti immediatamente il medico o si rechi subito al pronto soccorso.
Altri medicinali e MIRCERA
Informi il medico o il farmacista se sta assumendo, ha recentemente assunto o intende assumere
qualsiasi altro medicinale.
Non sono stati condotti studi sulle interazioni farmacologiche. Non vi è evidenza che MIRCERA
interagisca con altri medicinali.
MIRCERA con cibo e bevande
Cibo e bevande non hanno effetti su MIRCERA.
Gravidanza, allattamento e fertilità
Chieda consiglio al medico o al farmacista prima di prendere qualsiasi medicinale.
MIRCERA non è stato studiato nelle donne in stato di gravidanza o che allattano.
Informi il medico in caso di gravidanza sospetta o confermata o se intende iniziare una gravidanza. Il
medico valuterà il trattamento migliore da somministrarle durante la gravidanza.
Informi il medico se sta allattando o se intende farlo. Il medico le comunicherà l'eventuale necessità di
interrompere l'allattamento o il trattamento.
MIRCERA non ha dimostrato compromissione della fertilità negli animali. Il rischio potenziale per
l’uomo non è noto.
Guida di veicoli e utilizzo di macchinari
MIRCERA non influisce sulla capacità di guidare veicoli e utilizzare macchinari.
Informazioni importanti su alcuni eccipienti di MIRCERA
Questo medicinale contiene meno di 1 mmol di sodio (23 mg) per mL, cioè essenzialmente ‘senza
sodio’.
3. Come usare MIRCERA
Usi sempre questo medicinale seguendo esattamente le istruzioni del medico. Se ha dubbi consulti il
medico o il farmacista.
Il medico userà la più bassa dose efficace per controllare i sintomi dell'anemia.
Se non risponde adeguatamente a MIRCERA, il medico controllerà la dose che riceve e la informerà
qualora dovesse modificarla.
Il trattamento con MIRCERA deve essere iniziato sotto la supervisione di un operatore sanitario.
Le iniezioni successive possono essere somministrate da un operatore sanitario oppure, dopo un
opportuno addestramento, lei, in quanto adulto, può iniettarsi MIRCERA da solo (autoiniettarsi).
I bambini e gli adolescenti di età inferiore ai 18 anni non devono auto-iniettarsi MIRCERA, la
somministrazione deve essere eseguita da un operatore sanitario o da un adulto opportunamente
siringa preriempita per autoiniezione oppure per iniezione ad un altro individuo).
MIRCERA può essere iniettato sotto la cute nell'addome, nel braccio o nella coscia, oppure in vena. Il
medico deciderà cosa è meglio per lei.
Il medico eseguirà analisi del sangue periodiche per controllare la risposta dell'anemia al trattamento
mediante la misurazione del livello di emoglobina.
- Se lei è un adulto non attualmente in trattamento con un ESASe non è in dialisi, la dose iniziale raccomandata di MIRCERA è 1,2 microgrammi per ogni chilogrammo di peso corporeo da somministrare per via sottocutanea una volta ogni mese come singola iniezione.In alternativa, il medico può decidere di somministrare una dose iniziale di MIRCERA di 0,6 microgrammi per ogni chilogrammo di peso corporeo. La dose deve essere somministrata una volta ogni due settimane come singola iniezione endovenosa o sottocutanea. Una volta corretta l'anemia, il medico potrebbe cambiare il dosaggio a una somministrazione al mese. Se è in dialisi, la dose iniziale raccomandata è 0,6 microgrammi per ogni chilogrammo di peso corporeo. La dose deve essere somministrata una volta ogni due settimane come singola iniezione endovenosa o sottocutanea. Una volta corretta l'anemia, il medico potrebbe cambiare il dosaggio a una
Il medico può aumentare o ridurre la dose oppure interrompere temporaneamente il trattamento per
regolare il livello di emoglobina in modo appropriato. I cambiamenti di dose non saranno apportati più
di una volta al mese.
- Se è attualmente in trattamento con un altro ESAIl medico potrebbe sostituire il medicinale attuale con MIRCERA. Il medico deciderà di trattarla con MIRCERA somministrato in un'unica iniezione una volta al mese. Il medico calcolerà la dose iniziale di MIRCERA in base all'ultima dose del precedente medicinale. La prima dose di MIRCERA sarà somministrata nel giorno dell'iniezione previsto per il medicinale precedente.
Il medico può aumentare o ridurre la dose oppure interrompere temporaneamente il trattamento per
regolare il livello di emoglobina in modo appropriato. I cambiamenti di dose non saranno apportati più
di una volta al mese.
Se usa più MIRCERA di quanto deve
Se ha usato una dose eccessiva di MIRCERA, si rivolga al medico o al farmacista perché potrebbe
essere necessario eseguire delle analisi del sangue e interrompere il trattamento.
Se dimentica di usare MIRCERA
Se salta una dose di MIRCERA, somministri la dose dimenticata non appena possibile e chieda al
medico quando utilizzare le dosi successive.
Se interrompe il trattamento con MIRCERA
Il trattamento con MIRCERA è in genere a lungo termine. Tuttavia, può essere interrotto su consiglio
del medico in qualsiasi momento.
Se ha qualsiasi dubbio sull'uso di questo medicinale, si rivolga al medico o al farmacista.
4. Possibili effetti indesiderati
Come tutti i medicinali, Mircera può causare effetti indesiderati sebbene non tutte le persone li
manifestino.
Di seguito è elencata la frequenza dei possibili effetti indesiderati:
Un effetto indesiderato comune (può verificarsi fino a 1 paziente su 10) è l’ipertensione (pressione del
sangue alta).
Effetti indesiderati non comuni (possono verificarsi fino a 1 paziente su 100) sono:
- mal di testa
- trombosi in sito dell'accesso vascolare (coaguli di sangue nell'accesso della dialisi)
- trombocitopenia
- trombosi.
Effetti indesiderati rari (possono verificarsi fino a 1 paziente su 1000) sono:
- encefalopatia ipertensiva (pressione sanguigna molto alta che può causare mal di testa, soprattutto improvviso, lancinante, simile all’emicrania, confusione, disturbi del linguaggio, attacchi o convulsioni)
- embolia polmonare
- eruzione maculo-papulare (reazione con arrossamento della pelle che può includere pustole o foruncoli)
- vampate di calore
- ipersensibilità (reazione allergica che può causare insolito affanno o difficoltà nel respirare gonfiore della lingua, del volto o della gola oppure del sito di iniezione, capogiro, svenimento o collasso). Se manifesta questi sintomi, si rivolga immediatamente al medico per ricevere un trattamento.
Durante gli studi clinici i pazienti hanno mostrato una leggera diminuzione del numero di piastrine nel
sangue. Successivamente alla commercializzazione ci sono state segnalazioni di conta piastrinica al di
sotto del range di normalità (trombocitopenia).
In associazione al trattamento con epoetina sono state riferite reazioni di ipersensibilità, compresi casi
di reazione anafilattica ed eruzioni cutanee gravi, tra cui sindrome di Stevens-Johnson (SJS) e necrolisi
epidermica tossica. Queste possono manifestarsi come macule rossastre a forma di bersaglio o chiazze
circolari spesso associate a vesciche centrali sul tronco, desquamazione della pelle, ulcere nella zona
della bocca, della gola, del naso, dei genitali e degli occhi, e possono essere precedute da febbre e
sintomi simil-influenzali. Se dovesse manifestare questi sintomi, smetta di prendere Mircera e contatti
immediatamente il medico o si rechi subito al pronto soccorso; vedere anche il paragrafo 2.
Come con altri ESA, successivamente alla commercializzazione sono stati riportati casi di trombosi,
compresi casi di embolia polmonare.
È stata osservata in alcuni pazienti trattati con ESA, compreso MIRCERA. una condizione chiamata
aplasia eritroide pura (PRCA, interruzione o riduzione della produzione di globuli rossi) a causa di
anticorpi anti-eritropoietina.
Segnalazione degli effetti indesiderati
Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si
rivolga al medico o al farmacista.
Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema nazionale di
segnalazione riportato nell’ Allegato V . Segnalando gli effetti indesiderati lei può contribuire a fornire
maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare MIRCERA
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla confezione e sull'etichetta
della siringa preriempita dopo 'Scad./EXP'. La data di scadenza si riferisce all'ultimo giorno del mese.
Conservare in frigorifero (2 ° C-8 ° C). Non congelare.
Tenere la siringa preriempita nell’imballaggio esterno per proteggerla dalla luce.
È possibile togliere la siringa preriempita di MIRCERA dal frigorifero e conservarla a temperatura
ambiente non superiore ai 30 ° C per un unico periodo di un mese. Durante il periodo di tempo in cui
MIRCERA è conservato a temperatura ambiente non superiore ai 30°C non è necessario rimettere
MIRCERA in frigorifero prima dell’uso. Una volta tolto il medicinale dal frigorifero, il medicinale
deve essere utilizzato entro questo periodo di un mese.
Solo soluzioni limpide, da incolore a leggermente giallastre e prive di particelle visibili devono essere
iniettate.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici.
Chieda al farmacista come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere
l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene MIRCERA
- Il principio attivo è metossipolietilenglicole-epoetina beta. Una siringa preriempita contiene 30, 40, 50, 60, 75, 100, 120, 150, 200 o 250 microgrammi in 0,3 mL e 360 microgrammi in 0,6 mL.
- Gli eccipienti sono sodio fosfato monobasico monoidrato, sodio solfato, mannitolo (E421), metionina, polossamero 188 e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di MIRCERA e contenuto della confezione
MIRCERA è una soluzione iniettabile in siringa preriempita.
La soluzione è limpida, da incolore a leggermente giallastra e priva di particelle visibili.
MIRCERA è in una siringa preriempita con tappo dello stantuffo laminato e cappuccio della punta con
un ago 27G1/2. Ciascuna siringa preriempita contiene 0,3 mL o 0,6 mL di soluzione. Le siringhe
preriempite non sono progettate per la somministrazione di dosi parziali. MIRCERA è disponibile, per
tutti i dosaggi, in confezioni da 1; è inoltre disponibile in confezioni da 3 siringhe preriempite per i
dosaggi 30, 50 e 75 microgrammi/0,3 mL. È possibile che non tutte le confezioni siano
commercializzate.
Titolare dell'autorizzazione all'immissione in commercio
Roche Registration GmbH
Emil-Barell-Strasse 1
79639 Grenzach-Wyhlen
Germania
Produttore
Roche Pharma AG
Emil-Barell-Strasse 1
79639 Grenzach-Wyhlen
Germania
Per ulteriori informazioni su MIRCERA, contatti il rappresentante locale del titolare
dell'autorizzazione all'immissione in commercio:
België/Belgique/Belgien
N.V. Roche S.A.
Tél/Tel: +32 (0) 2 525 82 11
Lietuva
UAB “Roche Lietuva”
Tel: +370 5 2546799
България
Рош България ЕООД
Тел: +359 2 2 474 5444
Luxembourg/Luxemburg
(Voir/siehe Belgique/Belgien)
Česká republika
Roche s. r. o.
Tel: +420 - 2 20382111
Magyarország
Roche (Magyarország) Kft.
Tel: +36 - 1 279 4500
Danmark
Roche Pharmaceuticals A/S
Tlf: +45 - 36 39 99 99
Malta
(See Ireland)
Deutschland
Roche Pharma AG
Tel: +49 (0) 7624 140
Nederland
Roche Nederland B.V.
Tel: +31 (0) 348 438050
Eesti
Roche Eesti OÜ
Tel: + 372 - 6 177 380
Norge
Roche Norge AS
Tlf: +47 - 22 78 90 00
Ελλάδα
Roche (Hellas) A.E.
Τηλ: +30 210 61 66 100
Österreich
Roche Austria GmbH
Tel: +43 (0) 1 27739
España
Roche Farma S.A.
Tel: +34 - 91 324 81 00
Polska
Roche Polska Sp.z o.o.
Tel: +48 - 22 345 18 88
France
Roche
Tél: +33 (0) 1 47 61 40 00
Portugal
Roche Farmacêutica Química, Lda
Tel: +351 - 21 425 70 00
Hrvatska
Roche d.o.o.
Tel: +385 1 4722 333
România
Roche România S.R.L.
Tel: +40 21 206 47 01
Ireland
Roche Products (Ireland) Ltd.
Tel: +353 (0) 1 469 0700
Slovenija
Roche farmacevtska družba d.o.o.
Tel: +386 - 1 360 26 00
Ísland
Roche Pharmaceuticals A/S
c/o Icepharma hf
Sími: +354 540 8000
Slovenská republika
Roche Slovensko, s.r.o.
Tel: +421 - 2 52638201
Italia
Roche S.p.A.
Tel: +39 - 039 2471
Suomi/Finland
Roche Oy
Puh/Tel: +358 (0) 10 554 500
Kύπρος
Γ.Α.Σταμάτης & Σια Λτδ.
Τηλ: +357 - 22 76 62 76
Sverige
Roche AB
Tel: +46 (0) 8 726 1200
Latvija
Roche Latvija SIA
Tel: +371 – 6 7039831
United Kingdom (Northern Ireland)
Roche Products (Ireland) Ltd.
Tel: +44 (0) 1707 366000
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia Europea
dei Medicinali (EMA) http://www.ema.europa.eu
Siringa preriempita di MIRCERA
Istruzioni per l'uso
Le istruzioni riportate di seguito illustrano l'uso della siringa preriempita di MIRCERA per
l'autoiniezione o per eseguire un’iniezione ad un altro individuo.
È importante leggere e seguire attentamente queste istruzioni per poter usare la siringa
preriempita in modo corretto e sicuro.
Nontentare di somministrare un'iniezione finché non si è sicuri di aver compreso come usare
la siringa preriempita, in caso di dubbio contattare l’operatore sanitario. Bambini ed
adolescenti di età inferiore ai 18 anni non devonoautoiniettarsi MIRCERA, la
somministrazione deve esser effettuata da un operatore sanitario o da un adulto
opportunamente addestrato.
Seguire sempre tutte le indicazioni riportate in queste Istruzioni per l'uso in quanto possono
differire dalla vostra esperienza. Queste istruzioni aiuteranno a prevenire trattamenti errati o
rischi, come lesioni da puntura da ago o un'attivazione precoce del dispositivo di sicurezza
dell'ago, o problemi relativi al fissaggio dell'ago .
INFORMAZIONI IMPORTANTI
- Usare la siringa preriempita di MIRCERA soltanto dietro prescrizione del medicinale.
- Leggere le informazioni riportate sulla confezione e assicurarsi che la dose sia quella prescritta dal medico.
- Nonusare MIRCERA se la siringa, l’ago, la confezione o il vassoio di plastica che la contiene appaiono danneggiati.
- L’ago è fragile, maneggiarlo con cura.
- Non toccarele protezioni di attivazione (vedere Figura A) in quanto ciò può danneggiare la siringa e renderla inutilizzabile.
- Nonusare la siringa se il contenuto è torbido, opaco o presenta delle particelle.
- Non tentare mai di smontare la siringa.
- Non tirare o maneggiare mai la siringa tenendola per lo stantuffo.
- Nonrimuovere la protezione dell'ago finché non si è pronti a somministrare l'iniezione.
- Noningerire il medicinale contenuto nella siringa.
- Nonsomministrare l'iniezione attraverso gli indumenti.
- Nonriutilizzare o risterilizzare la siringa o l’ago.
- Le siringhe preriempite non sono progettate per la somministrazione di dosi parziali.
- Tenere siringa, ago e relativi accessori fuori dalla portata dei bambini
CONSERVAZIONE
Tenere la siringa preriempita, l’ago e il contenitore a prova di perforazione/per oggetti
appuntiti fuori dalla portata dei bambini.
Conservare la siringa e l’ago nella confezione originale fino al momento dell’utilizzo.
Conservare sempre la siringa e l’ago in frigorifero a una temperatura di 2 - 8°C.
Noncongelare il medicinale e proteggere il medicinale e l’ago dalla luce. Tenere la siringa e
l’ago all'asciutto.
MATERIALI CONTENUTI NELLA CONFEZIONE (Figura A):
- Una siringa preriempita di MIRCERA
- Un ago per iniezioni separato
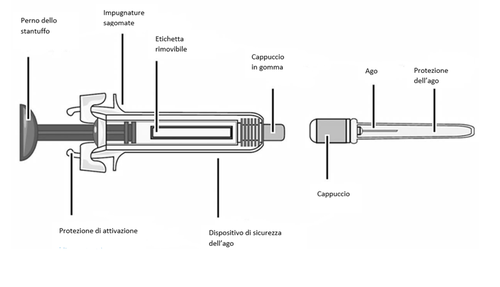
Figura A
MATERIALI NON CONTENUTI NELLA CONFEZIONE (Figura B):
Contenitore a prova di
perforazione o contenitore
per oggetti appuntiti per lo
smaltimento sicuro dell'ago
e della siringa usati
Tamponi imbevuti d'alcool per Batuffolo o garza di cotone
la pulizia del sito di iniezione sterile
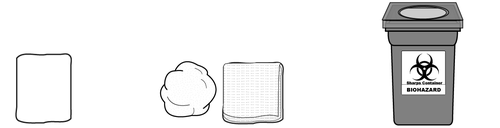
Figura B
Disporre tutti i materiali necessari per un'iniezione su una superficie piana, pulita e ben
illuminata, ad esempio su un tavolo.
COME SOMMINISTRARE L'INIEZIONE
Fase 1. Lasciare che la siringa raggiunga la temperatura ambiente
Togliere accuratamente dal
frigorifero la confezione contenente
la siringa preriempita di MIRCERA.
Tenere la siringa e l’ago nella
confezione per proteggerla dalla luce
e attendere almeno 30 minuti che
raggiunga la temperatura ambiente
(Figura C).
- Non attendere che il medicinale raggiunga la temperatura ambiente potrebbe determinare un'iniezione fastidiosa e difficoltà a premere lo stantuffo.
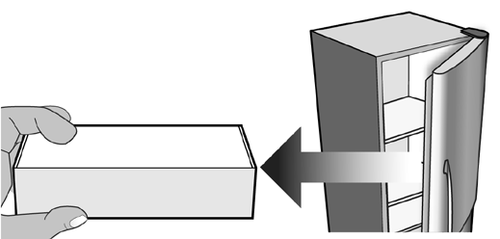
Figura C
- Nonriscaldare la siringa in nessun altro modo.
Aprire la confezione ed estrarre il
vassoio di plastica della siringa
preriempita di MIRCERA dalla
confezione senza aprire la pellicola
protettiva (Figura D).
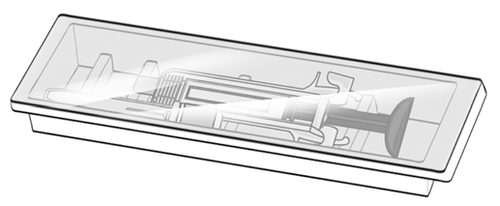
Figura D
Fase 2. Pulirsi le mani
Disinfettarsi bene le mani con acqua
tiepida e sapone o con un
igienizzante (Figura E).
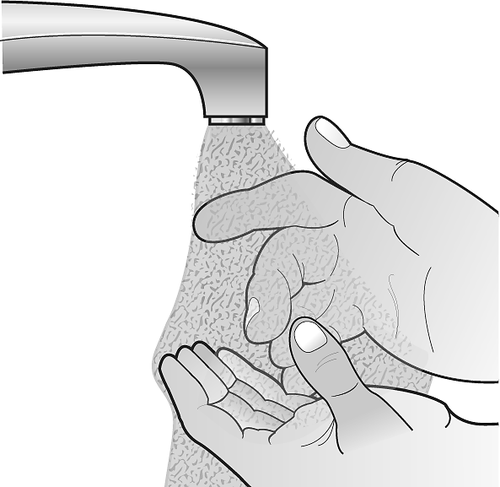
Figura E
Fase 3. Estrarre la siringa preriempita dal vassoio e ispezionarla visivamente
Aprire la pellicola protettiva del
vassoio di plastica ed estrarre l'ago
confezionato e la siringa, tenendo la
siringa per la parte centrale senza
toccare le protezioni di attivazione
(Figura F).
Tenere la siringa solo per il corpo
centrale perché qualsiasi contatto
con le protezioni di attivazione
potrebbe causare il rilascio
prematuro del dispositivo di
sicurezza.
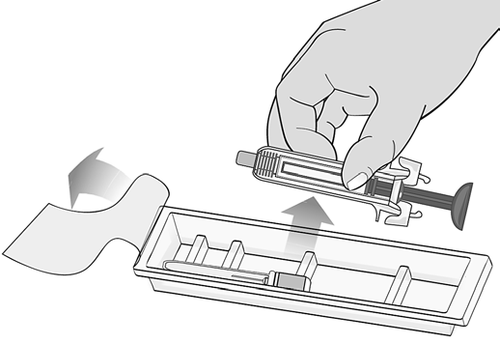
Figura F
Esaminare la siringa per possibili
danni e controllare la data di
scadenza riportata sulla siringa e
sulla confezione. Questo è
importante per garantire l'uso sicuro
della siringa e del medicinale (Figura
G).
Nonusare la siringa se:
- La si è fatta cadere accidentalmente.
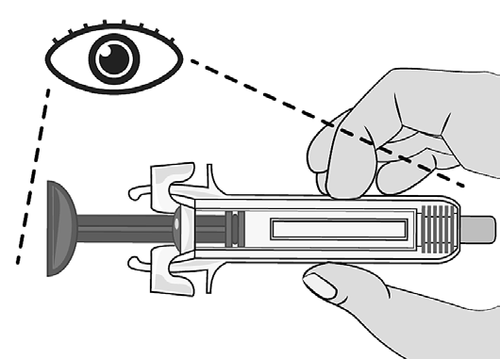
- Qualsiasi parte della siringa appare danneggiata. Figura G
- Il contenuto è torbido, opaco o presenta delle particelle.
- Se il colore della soluzione non è in un intervallo tra incolore a leggermente giallastro.
- È stata superata la data di scadenza.
Fase 4. Fissare l'ago alla siringa
Afferrare saldamente la siringa per il corpo
centrale, tenere il cappuccio di gomma,
quindi togliere il cappuccio di gomma dalla
siringa (piegare e tirare) (Figura H).
- Una volta rimosso, riporre immediatamente il cappuccio in gomma nel contenitore a prova di perforazione/nel contenitore per oggetti appuntiti.
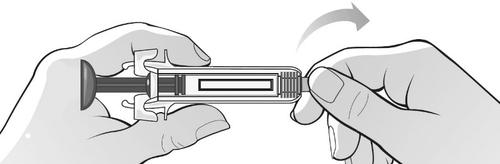
Figura H
- Nontoccare le protezioni di attivazione del dispositivo di sicurezza.
- Nonpremere lo stantuffo.
- Nontirare lo stantuffo.
Afferrare saldamente l'ago
confezionato con entrambe le mani
ed esaminare l’ago se presenta danni.
Rompere il sigillo con un movimento
rotatorio e togliere il cappuccio
dell'ago (Figura I).
Gettare immediatamente il
cappuccio dell’ago nel contenitore
per oggetti appuntiti/a prova di
perforazione. Nonrimuovere la
protezione dell'ago.
Non usare l’ago se:
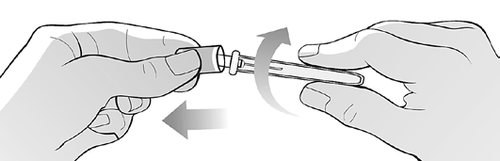
Figura I
- Hai fatto cadere accidentalmente
l’ago
- Qualsiasi parte dell’ago sembra essere danneggiata.
Fissare l'ago alla siringa premendolo
saldamente sulla siringa stessa e
ruotarlo leggermente (Figura J).
Fase 5. Rimuovere la protezione dell'ago e prepararsi all'iniezione
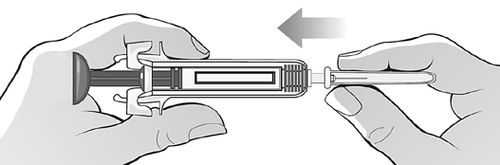
Figura J
Tenere saldamente la siringa al
centro del corpo con una mano e
rimuovere la protezione dell'ago
tirandola in senso orizzontale con
l'altra mano. Gettare la protezione
dell'ago nel contenitore a prova di
perforazione o nel contenitore per
oggetti appuntiti (Figura K).
- Una volta rimossa la protezioneo dell’ago nontoccare l'ago né lasciare che entri in contatto con qualsiasi superficie onde evitare che si contamini e onde evitare di procurarsi lesioni o dolore.
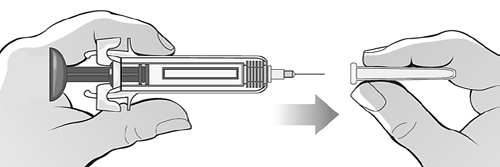
Figura K
- Potrebbe essere visibile una goccia di liquido all'estremità dell'ago. È normale.
- Non riposizionare mai la protezione dell'ago dopo averla tolta.
Per eliminare le bolle d'aria dalla
siringa preriempita, tenere la siringa
con l'ago rivolto verso l'alto.
Picchiettare delicatamente sulla
siringa per far spostare eventuali
bolle d'aria verso l'alto (Figure L e
M).
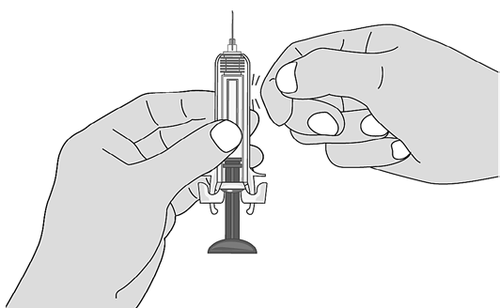
Premere lentamente lo stantuffo
Figura L
verso l'alto per eliminare tutta l’aria,
come mostrato dall'operatore
sanitario. (Figura M).
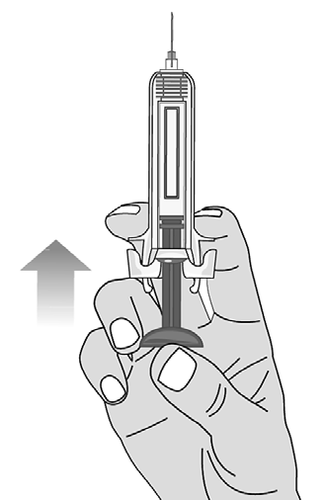
Fase 6. Somministrare l'iniezione
Figura M
Esistono due diversi modi (vie) per iniettare MIRCERA. Seguire le istruzioni dell'operatore
sanitario su come iniettare MIRCERA.
VIA SOTTOCUTANEA:
Se le è stato consigliato di iniettare MIRCERA sotto pelle, somministrare la dose come
descritto di seguito.
Scegliere una delle sedi di iniezione
raccomandate illustrate nella figura.
È possibile iniettare MIRCERA nella
parte superiore del braccio, nella
coscia o nell'addome, ma non
nell'area intorno all'ombelico (Figura
N).
La parte posteriore del braccio non è
un sito consigliato per
l'autoiniezione.
Utilizzare questo sito di iniezione
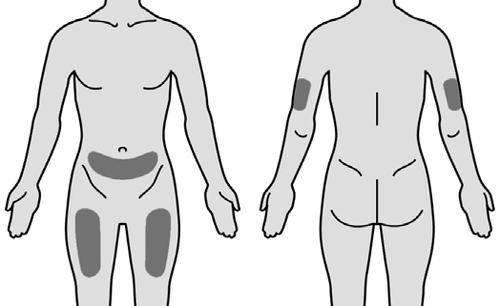
Figura Nsolo se si inietta ad un altro
individuo.
Quando si seleziona un sito di
iniezione:
- Si deve utilizzare una sede di iniezione diversa ogni volta che si somministra un'iniezione,
almeno a tre centimetri di
distanza dall'area utilizzata per
l'iniezione precedente.
- Noniniettare in aree che potrebbero essere irritate da una cintura o una fascia.
- Noniniettare in nei, cicatrici, lividi o aree in cui la pelle è sensibile al dolore, arrossata, indurita o non integra.
Pulire l'area della sede di iniezione
prescelta utilizzando un tampone
imbevuto di alcool per ridurre il
rischio di infezione; seguire
attentamente le istruzioni relative al
tampone imbevuto di alcool (Figura
O).
- Lasciare asciugare la pelle per circa 10 secondi.
- Non toccare l'area pulita prima dell'iniezione e nonsventolare o soffiare sull'area pulita.
- Eliminare subito il tampone imbevuto di alcool.
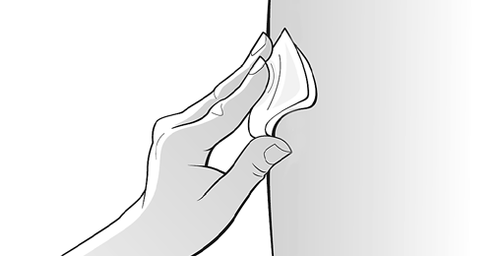
Figura O
Adottare una postura comoda prima
di eseguire un’iniezione di
MIRCERA.
Per essere sicuri di inserire
correttamente l'ago sotto la cute,
usare la mano libera per creare una
piega della pelle nella sede di
iniezione pulita. Formare una piega
della pelle è importante per garantire
che l'iniezione venga praticata sotto
la pelle (nel tessuto adiposo) ma non
più in profondità (nel muscolo).
L'iniezione nel muscolo potrebbe
risultare fastidiosa (Figura P).
Inserire completamente l'ago nella
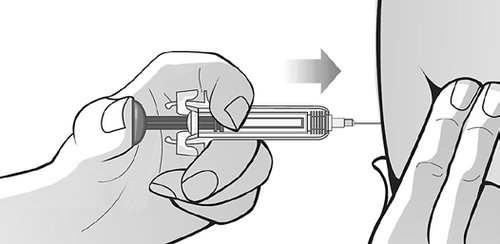
Figura P
pelle, ad angolo di 90° con un
movimento rapido e deciso. Tenere
la siringa in posizione e lasciare la
piega della pelle.
Nonspostare l’ago mentre è inserito
nella pelle.
Una volta che l’ago è completamente
inserito nella pelle, premere
lentamente lo stantuffo con il pollice,
tenendo la siringa con l'indice e il
medio contro le impugnature
sagomate, fino a quando sarà stato
iniettato tutto il medicinale.
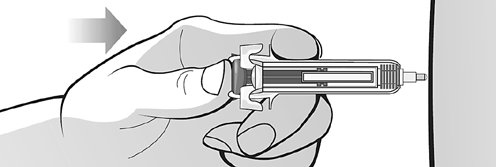
Figura Q
L'asta dello stantuffo dovrebbe essere
completamente spinta verso il basso
(depressa) e si dovrebbe sentire un
clic che indica l'attivazione della
protezione dell’ago (Figura Q).
Nonrilasciare lo stantuffo prima
della fine dell'iniezione o prima che
sia stato premuto completamente.
Estrarre l'ago dalla pelle SENZA
rilasciare lo stantuffo (Figura R).
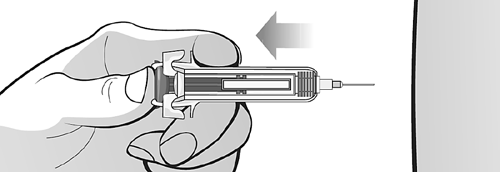
Rilasciare lo stantuffo in modo che il
copriago protegga l'ago (Figura S).
Figura R
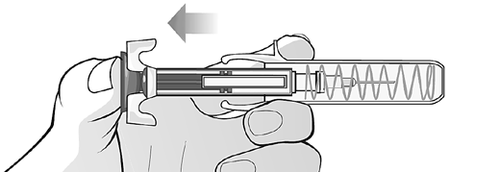
Figura S
Ora è possibile rimuovere l'etichetta
rimovibile, se necessario (Figura T).
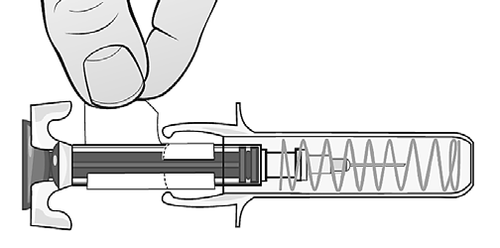
Dopo l’iniezione:
Figura T
- Premere per alcuni secondi sulla sede di iniezione con un batuffolo di cotone o una garza sterili.
- Eliminare subito il batuffolo di cotone o la garza dopol’uso.
- Nonsfregare la sede di iniezione con tessuti o mani sporche.
- Se necessario, è possibile proteggere la sede di iniezione applicandovi un cerotto.
Smaltimento della siringa:
- Nontentare di riapplicare la protezione dell’ago sull’ago stesso.
- Non riutilizzare o risterilizzare la siringa e/o l’ago.
- Nongettare la siringa utilizzata con l’ago nei rifiuti domestici.
- Gettare le siringhe utilizzate in un contenitore per oggetti appuntiti/a prova di perforazione in accordo alla normativa vigente.
- Smaltire l’intero contenitore per oggetti appuntiti / contenitore a prova di perforazione.
VIA ENDOVENOSA:
Se l'operatore sanitario le ha raccomandato di iniettare MIRCERA in una vena, seguire la
procedura descritta di seguito.
Dopo la preparazione della siringa descritta nelle fasi da 1 a 5:
Pulire l'accesso venoso per l’emodialisi con un tampone imbevuto di alcool seguendo le
istruzioni del fornitore o del fabbricante. Eliminare subito il tampone imbevuto di alcool
dopo l’uso.
Inserire l'ago della siringa preriempita nell'accesso
venoso pulito(Figura U).
Nontoccare il sito di iniezione dell’accesso
venoso.
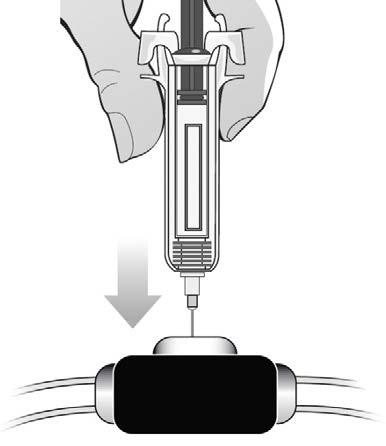
Premere lo stantuffo con il pollice, tenendo la
siringa con l'indice e il medio contro le
impugnature sagomate, fino a quando sarà stato
iniettato tutto il medicinale (Figura V).
Estrarre la siringa preriempita dall'accesso venoso
SENZArilasciare lo stantuffo.
Una volta rimossa, rilasciare lo stantuffo in modo
che il copriago protegga l'ago.
Ora è possibile rimuovere l'etichetta rimovibile, se
Figura U
necessario (Vedere Figura T).
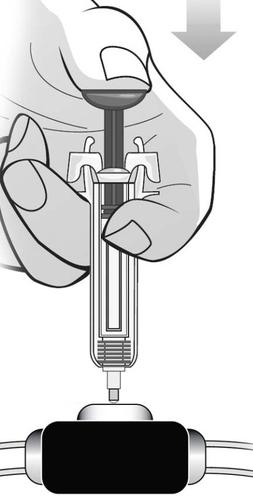
Figura V
Fase 7. Smaltire la siringa utilizzata con l’ago
- Nontentare di riapplicare la protezione dell’ago sull’ago stesso.
- Non riutilizzare o risterilizzare la siringa e/o l’ago.
- Nongettare la siringa utilizzata con l’ago nei rifiuti domestici.
- Gettare le siringhe utilizzate in un contenitore per oggetti appuntiti/a prova di perforazione in accordo alla normativa vigente.
- Smaltire l’intero contenitore per oggetti appuntiti / contenitore a prova di perforazione.
-

- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile, 50 MCG
- Codice ATCB03XA03
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a MIRCERAForma farmaceutica: Soluzione iniettabile, 1.000 UI/0,5 MLPrincipio attivo: erythropoietinProduttore: MEDICE ARZNEIMITTEL PUETTER GMBH & CO.KGPrescrizione richiestaForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 10 MCGPrincipio attivo: darbepoetin alfaProduttore: AMGEN EUROPE B.V.Prescrizione richiestaForma farmaceutica: Soluzione iniettabile, 1.000 UI/0,5 MLPrincipio attivo: erythropoietinProduttore: SANDOZ GMBHPrescrizione richiesta
Medici online per MIRCERA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di MIRCERA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per MIRCERA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.














