
Come usare CLUVIAT
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Cluviat 250 UI
Polvere e solvente per soluzione per iniezione/per infusione.
Concentrato di Fattore XIII plasmatico umano della coagulazione
perché contiene importanti informazioni per Lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto per Lei solamente. Non lo dia ad altre persone anche se i loro sintomi sono uguali ai Suoi, perché può essere pericoloso.
- Se nota la comparsa di effetti indesiderati o di qualsiasi effetto indesiderato non elencato in
Contenuto di questo foglio:
- 1. Che cos’è Cluviat e a che cosa serve
- 2. Cosa deve sapere prima di usare Cluviat
- 3. Come usare Cluviat
- 4. Possibili effetti indesiderati
- 5. Come conservare Cluviat
- 6. Contenuto della confezione e altre informazioni
1. Che cos’è Cluviat e a che cosa serve
Che cos’èCluviat?
Cluviat si presenta sotto forma di polvere bianca e solvente. La soluzione preparata deve essere
somministrata tramite iniezione in vena.
Cluviat è un prodotto costituito dal fattore XIII (FXIII) della coagulazione ottenuto da plasma
umano (la parte liquida del sangue) e svolge importanti funzioni nell’emostasi (arresto delle
emorragie).
A cosa serve Cluviat?
Cluviat viene usato nei pazienti adulti e pediatrici
- per il trattamento preventivo del deficit congenito del fattore XIII;
- per il trattamento perioperatorio delle emorragie chirurgiche con deficit congenito del fattore XIII.
2. Cosa deve sapere prima di usare Cluviat
I paragrafi che seguono contengono informazioni che il medico deve tenere presenti prima di
somministrare Cluviat.
Non prenda Cluviat:
- se è allergico ai principi attivi o a uno qualsiasi degli eccipienti di questo medicinale (vedere elenco al paragrafo 6). Informi il medico se è allergico a qualunque farmaco o alimento.
Avvertenze e precauzioni d’impiego
- se in passato ha manifestato reazioni allergiche al FXIII della coagulazione. Deve assumere antistaminici e corticosteroidi a scopo profilattico, se consigliato dal medico.
- in caso di reazioni allergiche o di tipo anafilattico (reazione allergica grave che provoca difficoltà respiratorie gravi o vertigini). La somministrazione di Cluviat deve esseresospesa immediatamente (ad es., interrompere l’infusione).In caso di shock, si devonoadottare le misure cliniche standard per il trattamento dello shock.
- se è stato colpito da trombosi recente (formazione di coaguli di sangue). Occorre cautela a causa dell’effetto stabilizzante la fibrina del FXIII.
- la formazione di inibitori (anticorpi neutralizzanti) è una complicazione nota del trattamento e significa che quest’ultimo non ha più effetto. Se l’emorragia non si arresta con l’assunzione di Cluviat, informi il medico immediatamente. Lei deve restare sotto stretto controllo medico per lo sviluppo di inibitori.
Il medico valuterà attentamente i benefici del trattamento con Cluviat rispetto al rischio di queste
complicazioni.
Sicurezza virale
Quando i medicinali sono preparati da sangue o plasma umano, vengono messe in atto alcune
misure per prevenire la trasmissione di agenti infettivi ai pazienti. Queste misure comprendono:
- attenta selezione dei donatori di sangue e di plasma in modo da assicurare che i donatori potenzialmente infetti vengano esclusi,
- controllo di ogni singola donazione e dei pool di plasma per evidenziare l'eventuale presenza di virus/infezioni,
- inclusione di passaggi, nel processo di lavorazione del sangue o del plasma, che possano inattivare o rimuovere i virus.
Nonostante queste misure, in caso di somministrazione di medicinali ottenuti dal sangue o dal
plasma umano, non è possibile escludere completamente la possibilità di trasmissione di infezioni.
Ciò vale anche per virus sconosciuti oppure emergenti o per altri tipi di infezioni.
Le misure adottate sono ritenute efficaci per i virus dotati di involucro come il virus
dell'immunodeficienza umana (HIV), il virus dell’epatite B e il virus dell’epatite C, nonché per i
virus senza involucro dell’epatite A e il parvovirus B19.
E’ fortemente raccomandato che, ogni volta che Le viene somministrato Cluviat, il medico registri
il nome e il numero di lotto del prodotto (riportato sulla confezione).
Il medico potrà raccomandare la vaccinazione contro l’epatite A e B se Lei assume
regolarmente/ripetutamente medicinali ottenuti dal plasma umano.
Assunzione di Cluviat con altri medicinali
- Informi il medico o il farmacista se sta assumendo, ha assunto di recente o potrebbe assumere qualsiasi altro medicinale.
- Non sono note interazioni del concentrato di fattore XIII plasmatico umano della coagulazione con altri medicinali.
- Cluviat non deve essere miscelato con altri medicinali, diluenti o solventi, ad eccezione di quelli elencati nel paragrafo 6 e deve essere somministrato tramite una linea di infusione separata.
Gravidanza, allattamento e fertilità
- Se è incinta, sospetta uno stato di gravidanza, desidera pianificare una maternità o sta allattando, chieda consiglio al medico o al farmacista prima di assumere questo medicinale.
- I dati limitati disponibili sull’uso clinico di Cluviat in gravidanza non hanno evidenziato effetti negativi sull’andamento della gravidanza e sullo sviluppo perinatale o postnatale. L’assunzione di Cluviat può quindi essere presa in considerazione durante la gravidanza, se necessario.
- Non vi sono dati sull’escrezione di Cluviat nel latte materno. Tuttavia, date le sue importanti dimensioni molecolari, l’escrezione nel latte materno è improbabile e, vista la sua natura proteica, l’assorbimento di molecole integre da parte del bambino è altrettanto improbabile. Cluviat può pertanto essere usato nelle donne che allattano.
- Non sono disponibili dati sulla fertilità.
Guida di veicoli e utilizzo di macchinari
Non sono stati effettuati studi sulla capacità di guidare veicoli e sull’uso di macchinari.
Cluviat contiene sodio
Tenga presente che Cluviat contiene sodio. Questo è importante se Lei segue una dieta a
contenuto controllato di sodio. Cluviat contiene da 124,4 a 195,4 mg (da 5,41 a 8,50 mmol) di
sodio per ogni dose (40 UI/kg di peso corporeo – 70 kg in media), se si assume la dose
raccomandata (2800 UI = 44,8 ml).
3. Come usare Cluviat
- Cluviat viene normalmente somministrato dal medico.
- Cluviat è destinato esclusivamente all’uso tramite iniezione in vena.
Dosaggio
Il medico calcolerà la dose corretta e deciderà la frequenza di somministrazione di Cluviat
tenendo conto degli effetti positivi del trattamento.
Per ulteriori informazioni, vedere il paragrafo “Le informazioni seguenti sono destinate
esclusivamente ai medici o agli operatori sanitari”.
Sovradosaggio
Non sono stati segnalati e non si prevedono casi di sovradosaggio in quanto il medicinale viene
somministrato da operatori sanitari.
4. Possibili effetti indesiderati
Come tutti i farmaci, questo medicinale può causare effetti indesiderati, sebbene non tutte le
persone li manifestino.
I seguenti effetti indesiderati sono stati osservati raramente(riguardano più di 1 su 10000
pazienti e meno di 1 su 1000 pazienti):
- Reazioni allergiche, come orticaria sistemica (rigonfiamenti pruriginosi della cute), eruzioni cutanee, abbassamento della pressione sanguigna (accompagnato da possibile senso di debolezza o vertigini) e difficoltà respiratorie.
- Aumento della temperatura.
I seguenti effetti indesiderati sono stati osservati molto raramente(riguardano meno di 1 su
10000 pazienti):
- Sviluppo di inibitori del FXIII.
In caso di reazioniallergiche, occorre sospendere immediatamente la somministrazione di
Cluviat e istituire un’idonea terapia. Si devono adottare le misure cliniche standard per il
trattamento dello shock.
Effetti indesiderati nei bambini e negli adolescenti
Nei bambini sono previsti gli stessi effetti indesiderati osservati negli adulti.
Segnalazione di effetti indesiderati
Se compaiono effetti indesiderati, informi il medico, l'infermiere o il farmacista, anche in caso di
indesiderati direttamente attraverso il sistema nazionale di segnalazione dell’Agenzia Italiana del
Farmaco, Sito web: http://www.agenziafarmaco.gov.it/content/come-segnalare-una-sospetta-
reazione-avversa.
Segnalando gli effetti indesiderati, Lei contribuirà a fornire ulteriori informazioni in merito alla
sicurezza di questo medicinale.
5. Come conservare Cluviat
- Conservare in frigorifero (+2°C - +8°C).
- Non congelare.
- Conservare il flaconcino nella confezione esterna, al fine di proteggerlo dalla luce.
- Cluviat non contiene conservanti. Il prodotto deve essere utilizzato immediatamente dopo la ricostituzione. Qualora non venga somministrato immediatamente, il tempo di conservazione non deve superare le 4 ore a temperatura ambiente. Non raffreddare o congelare la soluzione ricostituita.
- Tenere il medicinale fuori dalla vista e dalla portata dei bambini.
- Non utilizzare il medicinale dopo la data di scadenza indicata sull’etichetta e sulla scatola.
6. Contenuto della confezione e altre informazioni
Che cosa contiene Cluviat
Il principio attivo è:
Concentrato di Fattore XIII plasmatico umano della Coagulazione contenente 250 UI per
flaconcino.
Gli eccipienti sono:
Albumina umana, glucosio monoidrato, cloruro di sodio, idrossido di sodio (in piccole quantità
per l’aggiustamento del pH)
Solvente:Acqua per Preparazioni Iniettabili
Come si presenta Cluviat econtenuto della confezione
Cluviat si presenta sotto forma di polvere bianca e viene fornito con un solvente (Acqua per
Preparazioni Iniettabili).
La soluzione preparata deve essere incolore, da limpida a leggermente opalescente. Osservata in
controluce, non deve apparire torbida o contenere residui (depositi/particelle).
Presentazione
Una confezione da 250 UI contenente:
- 1 flaconcino con la polvere
- 1 flaconcino con 4 ml di acqua per preparazioni iniettabili
- 1 dispositivo di trasferimento filtro 20/20 (Mix2Vial)
- Set di somministrazione (scatola interna):
- 1 siringa monouso da 5 ml
- 1 set per iniezione in vena
- 2 tamponi imbevuti di alcool
- 1 cerotto non sterile
Titolare dell’Autorizzazione all'Immissione in Commercio e Produttore
CSL Behring GmbH
Emil-von-Behring-Strasse 76
35041 Marburg
Germania
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Posologia e modo di somministrazione
Posologia
1 ml equivale a circa 62,5 UI e 100 UI equivalgono a 1,6 ml, rispettivamente.
Importante:
La quantità da somministrare e la frequenza di somministrazione devono essere sempre finalizzate
all’efficacia clinica in ogni singolo caso.
Dosaggio
Il regime di dosaggio deve essere personalizzato sulla base del peso corporeo, dei valori di
laboratorio e delle condizioni cliniche del paziente.
Schema di Dosaggio per la Profilassi di Routine
Dose iniziale
- 40 Unità Internazionali (UI) per kg di peso corporeo.
- La velocità d’iniezione non deve superare i 4 ml al minuto.
Dosaggio successivo
- Il dosaggio deve essere scelto in base al più recente livello minimo di attività del FXIII, con somministrazione ogni 28 giorni (4 settimane) per mantenere un livello minimo di attività del FXIII di circa il 5 - 20%.
- Modifiche del dosaggio raccomandato di ±5 UI/kg devono essere valutate sulla base dei livelli minimi di attività del FXIII (come indicato nella Tabella 1) e delle condizioni cliniche del paziente.
- Le modifiche del dosaggio devono essere effettuate sulla base di uno specifico test sensibile, usato per determinare i livelli di FXIII. Un esempio di modifica del dosaggio tramite il test standard di attività Berichrom viene presentato qui di seguito nella Tabella 1.
Tabella 1: Modifica del Dosaggio con il Test di Attività Berichrom®
| n Livello Minimo di Attività del Fattore XIII (%) | Modifica del Dosaggio |
| e Un livello minimo <5% | Aumento di 5 unità/kg |
| Livello minimo dal 5% al 20% | Nessuna modifica |
| g Due livelli minimi >20% | Diminuzione di 5 unità/kg |
| Un livello minimo >25% | Diminuzione di 5 unità/kg |
L’attività espressa in unità viene determinata mediante il test di attività Berichrom , secondo
l’attuale Standard Internazionale per il Fattore XIII della Coagulazione del Sangue, Plasma.
Quindi, un’unità equivale in questo caso a un’Unità Internazionale.
Profilassi Preoperatoria
Dopo l’ultima dose profilattica di routine del paziente, qualora sia previsto un intervento
chirurgico:
- Tra 21 e 28 giorni dopo - somministrare al paziente l’intera dose profilattica subito prima dell’intervento, mentre la successiva dose profilattica deve essere somministrata dopo 28 giorni.
- Tra 8 e 21 giorni dopo - può essere somministrata una dose aggiuntiva (intera o parziale) prima dell’intervento. La dose deve essere stabilita in base ai livelli di attività del FXIII e alle condizioni cliniche del paziente e deve essere modificata secondo l’emivita di Cluviat.
- Entro 7 giorni dall’ultima dose - un’altra dose potrebbe non essere necessaria.
Le modifiche del dosaggio possono differire rispetto a queste raccomandazioni e devono essere
personalizzate sulla base dei livelli di attività del FXIII e delle condizioni cliniche del paziente.
Tutti i pazienti devono essere tenuti sotto stretto controllo durante e dopo un intervento
chirurgico.
Si raccomanda pertanto di monitorare l’aumento dell’attività del FXIII con un test specifico. In
caso di interventi chirurgici importanti e di emorragie gravi, l’obiettivo è quello di ottenere valori
prossimi alla normalità (soggetti sani: 70% - 140%).
Popolazione pediatrica
La posologia e il modo di somministrazione nei bambini e negli adolescenti si basano sul peso
corporeo e, quindi, generalmente sulle stesse linee guida adottate per gli adulti. La dose e/o la
frequenza di somministrazione per ogni paziente devono sempre tener conto dell’efficacia clinica
e dei livelli di attività del FXIII.
Popolazione anziana
La posologia e il modo di somministrazione nei soggetti anziani (> 65 anni) non sono stati
documentati da studi clinici.
Modo di somministrazione
Istruzioni generali
- La soluzione deve essere limpida o lievemente opalescente. Dopo la filtrazione/prelievo (vedere qui di seguito), il prodotto ricostituito deve essere controllato visivamente per evidenziare la presenza di particelle e di alterazioni di colore prima della somministrazione.
- Non usare soluzioni visibilmente torbide oppure soluzioni che contengono ancora flocculi o particelle.
- La ricostituzione e il prelievo devono essere effettuati in condizioni asettiche.
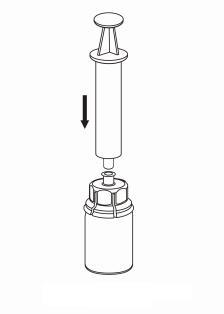
Ricostituzione
Portare il solvente a temperatura ambiente. Assicurarsi di togliere la capsula rimovibile del
prodotto e del solvente e che i tappi siano trattati con una soluzione asettica e lasciati asciugare
prima di aprire la confezione di Mix2Vial.
1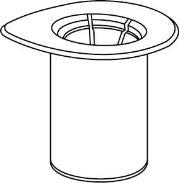 | m
| |||||||
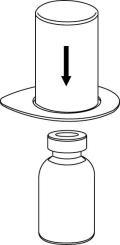 | 2 | a F
| ||||||
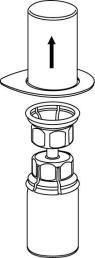 | 3 | d
| ||||||
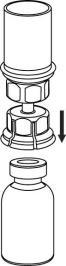 | 4 | t a l i | a
| |||||
n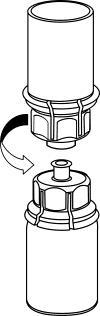 | I a i z 5 |
| ||||||
g e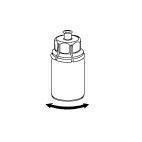 | 6 |
| ||||||
 | 7 | o
|
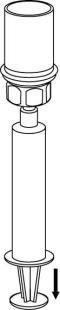
Prelievo e somministrazione
 | 8 | F
| |
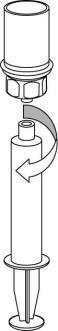 | 9 | l i |
|
Occorre prestare attenzione a non far entrare sangue nella siringa riempita con il prodotto, perché
vi è il rischio che il sangue si coaguli nella siringa e che, quindi, vengano somministrati al
paziente dei coaguli di fibrina.
La soluzione ricostituita deve essere somministrata per via endovenosaattraverso una linea di
iniezione/infusione separata (fornita con il prodotto) mediante lenta iniezione ad una velocità non
superiore ai 4 ml al minuto.
Ogni eventuale medicinale inutilizzato o materiale di scarto deve essere smaltito in conformità
con le disposizioni locali.
Cluviat 1250 UI
Polvere e solvente per soluzione per iniezione/per infusione.
Concentrato di Fattore XIII plasmatico umano della coagulazione
perché contiene importanti informazioni per Lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o al farmacista.
- Questo medicinale è stato prescritto per Lei solamente. Non lo dia ad altre persone anche se i loro sintomi sono uguali ai Suoi, perché può essere pericoloso.
- Se nota la comparsa di effetti indesiderati o di qualsiasi effetto indesiderato non elencato in
Contenuto di questo foglio:
- 1. Che cos’è Cluviat e a che cosa serve
- 2. Cosa deve sapere prima di usare Cluviat
- 3. Come usare Cluviat
- 4. Possibili effetti indesiderati
- 5. Come conservare Cluviat
- 6. Contenuto della confezione e altre informazioni
1. Che cos’è Cluviat e a che cosa serve
Che cos’èCluviat?
Cluviat si presenta sotto forma di polvere bianca e solvente. La soluzione preparata deve essere
somministrata tramite iniezione in vena.
Cluviat è un prodotto costituito dal fattore XIII (FXIII) della coagulazione ottenuto da plasma
umano (la parte liquida del sangue) e svolge importanti funzioni nell’emostasi (arresto delle
emorragie).
A cosa serve Cluviat?
Cluviat viene usato nei pazienti adulti e pediatrici
- per il trattamento preventivo del deficit congenito del fattore XIII;
- per il trattamento perioperatorio delle emorragie chirurgiche con deficit congenito del fattore XIII.
2. Cosa deve sapere prima di usare Cluviat
I paragrafi che seguono contengono informazioni che il medico deve tenere presenti prima di
somministrare Cluviat.
Non prenda Cluviat:
- se è allergico ai principi attivi o a uno qualsiasi degli eccipienti di questo medicinale (vedere elenco al paragrafo 6). Informi il medico se è allergico a qualunque farmaco o alimento.
Avvertenze e precauzioni d’impiego
- se in passato ha manifestato reazioni allergiche al FXIII della coagulazione. Deve assumere antistaminici e corticosteroidi a scopo profilattico, se consigliato dal medico.
- in caso di reazioni allergiche o di tipo anafilattico (reazione allergica grave che provoca difficoltà respiratorie gravi o vertigini). La somministrazione di Cluviat deve esseresospesa immediatamente (ad es., interrompere l’infusione).In caso di shock, si devonoadottare le misure cliniche standard per il trattamento dello shock.
- se è stato colpito da trombosi recente (formazione di coaguli di sangue). Occorre cautela a causa dell’effetto stabilizzante la fibrina del FXIII.
- la formazione di inibitori (anticorpi neutralizzanti) è una complicazione nota del trattamento e significa che quest’ultimo non ha più effetto. Se l’emorragia non si arresta con l’assunzione di Cluviat, informi il medico immediatamente. Lei deve restare sotto stretto controllo medico per lo sviluppo di inibitori.
Il medico valuterà attentamente i benefici del trattamento con Cluviat rispetto al rischio di queste
complicazioni.
Sicurezza virale
Quando i medicinali sono preparati da sangue o plasma umano, vengono messe in atto alcune
misure per prevenire la trasmissione di agenti infettivi ai pazienti. Queste misure comprendono:
- attenta selezione dei donatori di sangue e di plasma in modo da assicurare che i donatori potenzialmente infetti vengano esclusi,
- controllo di ogni singola donazione e dei pool di plasma per evidenziare l'eventuale presenza di virus/infezioni,
- inclusione di passaggi, nel processo di lavorazione del sangue o del plasma, che possano inattivare o rimuovere i virus.
Nonostante queste misure, in caso di somministrazione di medicinali ottenuti dal sangue o dal
plasma umano, non è possibile escludere completamente la possibilità di trasmissione di infezioni.
Ciò vale anche per virus sconosciuti oppure emergenti o per altri tipi di infezioni.
Le misure adottate sono ritenute efficaci per i virus dotati di involucro come il virus
dell'immunodeficienza umana (HIV), il virus dell’epatite B e il virus dell’epatite C, nonché per i
virus senza involucro dell’epatite A e il parvovirus B19.
E’ fortemente raccomandato che, ogni volta che Le viene somministrato Cluviat, il medico registri
il nome e il numero di lotto del prodotto (riportato sulla confezione).
Il medico potrà raccomandare la vaccinazione contro l’epatite A e B se Lei assume
regolarmente/ripetutamente medicinali ottenuti dal plasma umano.
Assunzione di Cluviat con altri medicinali
- Informi il medico o il farmacista se sta assumendo, ha assunto di recente o potrebbe assumere qualsiasi altro medicinale.
- Non sono note interazioni del concentrato di fattore XIII plasmatico umano della coagulazione con altri medicinali.
- Cluviat non deve essere miscelato con altri medicinali, diluenti o solventi, ad eccezione di quelli elencati nel paragrafo 6 e deve essere somministrato tramite una linea di infusione separata.
Gravidanza, allattamento e fertilità
- Se è incinta, sospetta uno stato di gravidanza, desidera pianificare una maternità o sta allattando, chieda consiglio al medico o al farmacista prima di assumere questo medicinale.
- I dati limitati disponibili sull’uso clinico di Cluviat in gravidanza non hanno evidenziato effetti negativi sull’andamento della gravidanza e sullo sviluppo perinatale o postnatale. L’assunzione di Cluviat può quindi essere presa in considerazione durante la gravidanza, se necessario.
- Non vi sono dati sull’escrezione di Cluviat nel latte materno. Tuttavia, date le sue importanti dimensioni molecolari, l’escrezione nel latte materno è improbabile e, vista la sua natura proteica, l’assorbimento di molecole integre da parte del bambino è altrettanto improbabile. Cluviat può pertanto essere usato nelle donne che allattano.
- Non sono disponibili dati sulla fertilità.
Guida di veicoli e utilizzo di macchinari
Non sono stati effettuati studi sulla capacità di guidare veicoli e sull’uso di macchinari.
Cluviat contiene sodio
Tenga presente che Cluviat contiene sodio. Questo è importante se Lei segue una dieta a
contenuto controllato di sodio. Cluviat contiene da 124,4 a 195,4 mg (da 5,41 a 8,50 mmol) di
sodio per ogni dose (40 UI/kg di peso corporeo –70 kg in media), se si assume la dose
raccomandata (2800 UI = 44,8 ml).
3. Come usare Cluviat
- Cluviat viene normalmente somministrato dal medico.
- Cluviat è destinato esclusivamente all’uso tramite iniezione in vena.
Dosaggio
Il medico calcolerà la dose corretta e deciderà la frequenza di somministrazione di Cluviat
tenendo conto degli effetti positivi del trattamento.
Per ulteriori informazioni, vedere il paragrafo “Le informazioni seguenti sono destinate
esclusivamente ai medici o agli operatori sanitari”.
Sovradosaggio
Non sono stati segnalati e non si prevedono casi di sovradosaggio in quanto il medicinale viene
somministrato da operatori sanitari.
4. Possibili effetti indesiderati
Come tutti i farmaci, questo medicinale può causare effetti indesiderati, sebbene non tutte le
persone li manifestino.
I seguenti effetti indesiderati sono stati osservati raramente(riguardano più di 1 su 10000
pazienti e meno di 1 su 1000 pazienti):
- Reazioni allergiche, come orticaria sistemica (rigonfiamenti pruriginosi della cute), eruzioni cutanee, abbassamento della pressione sanguigna (accompagnato da possibile senso di debolezza o vertigini) e difficoltà respiratorie.
- Aumento della temperatura.
I seguenti effetti indesiderati sono stati osservati molto raramente(riguardano meno di 1 su
10000 pazienti):
- Sviluppo di inibitori del FXIII.
In caso di reazioniallergiche, occorre sospendere immediatamente la somministrazione di
Cluviat e istituire un’idonea terapia. Si devono adottare le misure cliniche standard per il
trattamento dello shock.
Effetti indesiderati nei bambini e negli adolescenti
Nei bambini sono previsti gli stessi effetti indesiderati osservati negli adulti.
Segnalazione di effetti indesiderati
Se compaiono effetti indesiderati, informi il medico, l'infermiere o il farmacista, anche in caso di
indesiderati direttamente attraverso il sistema nazionale di segnalazione dell’Agenzia Italiana del
Farmaco, Sito web:http://www.agenziafarmaco.gov.it/content/come-segnalare-una-sospetta-
reazione-avversa.
Segnalando gli effetti indesiderati, Lei contribuirà a fornire ulteriori informazioni in merito alla
sicurezza di questo medicinale.
5. Come conservare Cluviat
- Conservare in frigorifero (+2°C - +8°C).
- Non congelare.
- Conservare il flaconcino nella confezione esterna, al fine di proteggerlo dalla luce.
- Cluviat non contiene conservanti. Il prodotto deve essere utilizzato immediatamente dopo la ricostituzione. Qualora non venga somministrato immediatamente, il tempo di conservazione non deve superare le 4 ore a temperatura ambiente. Non raffreddare o congelare la soluzione ricostituita.
- Tenere il medicinale fuori dalla vista e dalla portata dei bambini.
- Non utilizzare il medicinale dopo la data di scadenza indicata sull’etichetta e sulla scatola.
6. Contenuto della confezione e altre informazioni
Che cosa contiene Cluviat
Il principio attivo è:
Concentrato di Fattore XIII plasmatico umano della Coagulazione contenente 1250 UI per
flaconcino.
Gli eccipienti sono:
Albumina umana, glucosio monoidrato, cloruro di sodio, idrossido di sodio (in piccole quantità
per l’aggiustamento del pH)
Solvente:Acqua per Preparazioni Iniettabili
Come si presenta Cluviat econtenuto della confezione
Cluviat si presenta sotto forma di polvere bianca e viene fornito con un solvente (Acqua per
Preparazioni Iniettabili).
La soluzione preparata deve essere incolore, da limpida a leggermente opalescente. Osservata in
controluce, non deve apparire torbida o contenere residui (depositi/particelle).
Presentazione
Una confezione da 1250 UI contenente:
- 1 flaconcino con la polvere
- 1 flaconcino con 20 ml di acqua per preparazioni iniettabili
- 1 dispositivo di trasferimento filtro 20/20 (Mix2Vial)
- Set di somministrazione (scatola interna):
- 1 siringa monouso da 20 ml
- 1 set per iniezione in vena
- 2 tamponi imbevuti di alcool
- 1 cerotto non sterile
Titolare dell’Autorizzazione all'Immissione in Commercio e Produttore
CSL Behring GmbH
Emil-von-Behring-Strasse 76
35041 Marburg
Germania
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Posologia e modo di somministrazione
Posologia
1 ml equivale a circa 62,5 UI e 100 UI equivalgono a 1,6 ml, rispettivamente.
Importante:
La quantità da somministrare e la frequenza di somministrazione devono essere sempre finalizzate
all’efficacia clinica in ogni singolo caso.
Dosaggio
Il regime di dosaggio deve essere personalizzato sulla base del peso corporeo, dei valori di
laboratorio e delle condizioni cliniche del paziente.
Schema di Dosaggio per la Profilassi di Routine
Dose iniziale
- 40 Unità Internazionali (UI) per kg di peso corporeo.
- La velocità d’iniezione non deve superare i 4 ml al minuto.
Dosaggio successivo
- Il dosaggio deve essere scelto in base al più recente livello minimo di attività del FXIII, con somministrazione ogni 28 giorni (4 settimane) per mantenere un livello minimo di attività del FXIII di circa il 5 - 20%.
- Modifiche del dosaggio raccomandato di ±5 UI/kg devono essere valutate sulla base dei livelli minimi di attività del FXIII (come indicato nella Tabella 1) e delle condizioni cliniche del paziente.
- Le modifiche del dosaggio devono essere effettuate sulla base di uno specifico test sensibile, usato per determinare i livelli di FXIII. Un esempio di modifica del dosaggio tramite il test standard di attività Berichrom viene presentato qui di seguito nella Tabella 1.
Tabella 1: Modifica del Dosaggio con il Test di Attività Berichrom®
| i z Livello Minimo di Attività del Fattore XIII (%) | Modifica del Dosaggio |
| Un livello minimo <5% | Aumento di 5 unità/kg |
| n Livello minimo dal 5% al 20% | Nessuna modifica |
| Due livelli minimi >20% | Diminuzione di 5 unità/kg |
| e Un livello minimo >25% | Diminuzione di 5 unità/kg |
L’attività espressa in unità viene determinata mediante il test di attività Berichrom , secondo
l’attuale Standard Internazionale per il Fattore XIII della Coagulazione del Sangue, Plasma.
Quindi, un’unità equivale in questo caso a un’Unità Internazionale.
Profilassi Preoperatoria
Dopo l’ultima dose profilattica di routine del paziente, qualora sia previsto un intervento
chirurgico:
- Tra 21 e 28 giorni dopo - somministrare al paziente l’intera dose profilattica subito prima dell’intervento, mentre la successiva dose profilattica deve essere somministrata dopo 28 giorni.
- Tra 8 e 21 giorni dopo - può essere somministrata una dose aggiuntiva (intera o parziale) prima dell’intervento. La dose deve essere stabilita in base ai livelli di attività del FXIII e alle condizioni cliniche del paziente e deve essere modificata secondo l’emivita di Cluviat.
- Entro 7 giorni dall’ultima dose - un’altra dose potrebbe non essere necessaria.
Le modifiche del dosaggio possono differire rispetto a queste raccomandazioni e devono essere
personalizzate sulla base dei livelli di attività del FXIII e delle condizioni cliniche del paziente.
Tutti i pazienti devono essere tenuti sotto stretto controllo durante e dopo un intervento
chirurgico.
Si raccomanda pertanto di monitorare l’aumento dell’attività del FXIII con un test specifico. In
caso di interventi chirurgici importanti e di emorragie gravi, l’obiettivo è quello di ottenere valori
prossimi alla normalità (soggetti sani: 70% - 140%).
Popolazione pediatrica
La posologia e il modo di somministrazione nei bambini e negli adolescenti si basano sul peso
corporeo e, quindi, generalmente sulle stesse linee guida adottate per gli adulti. La dose e/o la
frequenza di somministrazione per ogni paziente devono sempre tener conto dell’efficacia clinica
e dei livelli di attività del FXIII.
Popolazione anziana
La posologia e il modo di somministrazione nei soggetti anziani (> 65 anni) non sono stati
documentati da studi clinici.
Modo di somministrazione
Istruzioni generali
- La soluzione deve essere limpida o lievemente opalescente. Dopo la filtrazione/prelievo (vedere qui di seguito), il prodotto ricostituito deve essere controllato visivamente per evidenziare la presenza di particelle e di alterazioni di colore prima della somministrazione.
- Non usare soluzioni visibilmente torbide oppure soluzioni che contengono ancora flocculi o particelle.
- La ricostituzione e il prelievo devono essere effettuati in condizioni asettiche.
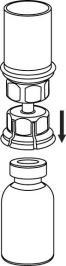
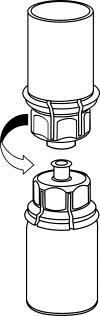
Ricostituzione
Portare il solvente a temperatura ambiente. Assicurarsi di togliere la capsula rimovibile del
prodotto e del solvente e che i tappi siano trattati con una soluzione asettica e lasciati asciugare
prima di aprire la confezione di Mix2Vial.
1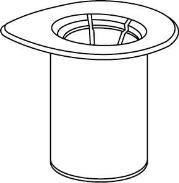 | a
| |||||||
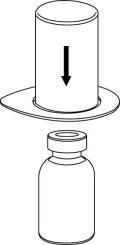 | 2 | r
| ||||||
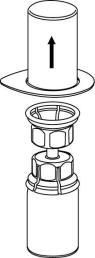 | 3 | l e
| ||||||
 | 4 | a l i | n
| |||||
 | I a i z 5 | t |
| |||||
e n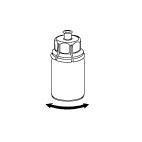 | 6 |
| ||||||
 | 7 | o
|
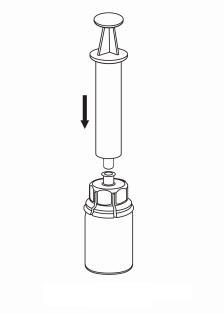
Prelievo e somministrazione
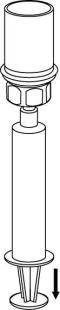 | 8 | F
| |
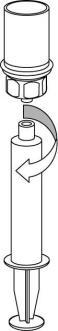 | 9 | l i |
|
Occorre prestare attenzione a non far entrare sangue nella siringa riempita con il prodotto, perché
vi è il rischio che il sangue si coaguli nella siringa e che, quindi, vengano somministrati al
paziente dei coaguli di fibrina.
La soluzione ricostituita deve essere somministrata per via endovenosa attraversouna linea
di iniezione/infusione separata (fornita con il prodotto) mediante lenta iniezione ad una velocità
non superiore ai 4 ml al minuto.
Ogni eventuale medicinale inutilizzato o materiale di scarto deve essere smaltito in conformità
con le disposizioni locali.
- Paese di registrazione
- Forma farmaceuticaPolvere e solvente per soluzione iniettabile/ per infusione, 250 U.I
- Codice ATCB02BD07
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a CLUVIATForma farmaceutica: Polvere e solvente per soluzione iniettabile, 250 UIPrincipio attivo: coagulation factor VIIIProduttore: TAKEDA MANUFACTURING AUSTRIA AGPrescrizione richiestaForma farmaceutica: Polvere e solvente per soluzione iniettabile, 250 UIPrincipio attivo: coagulation factor VIIIProduttore: BAXALTA INNOVATIONS GMBHPrescrizione richiestaForma farmaceutica: Polvere e solvente per soluzione iniettabile, 1000 UIPrincipio attivo: coagulation factor VIIIProduttore: CSL BEHRING GMBHPrescrizione richiesta
Medici online per CLUVIAT
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di CLUVIAT — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per CLUVIAT online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.












