
Come usare CRYSVITA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
CRYSVITA 10 mg soluzione iniettabile, 20 mg soluzione iniettabile, 30 mg soluzione iniettabile
burosumab
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è CRYSVITA e a cosa serve
- 2. Cosa deve sapere prima di usare CRYSVITA
- 3. Come usare CRYSVITA
- 4. Possibili effetti indesiderati
- 5. Come conservare CRYSVITA
- 6. Contenuto della confezione e altre informazioni
1. Cos’è CRYSVITA e a cosa serve
Cos’è CRYSVITA
CRYSVITA contiene il principio attivo burosumab, un tipo di medicinale noto come anticorpo
monoclonale umano.
A cosa serve CRYSVITA
CRYSVITA è usato per il trattamento dell’ipofosfatemia X-linked (XLH). È impiegato nei bambini e
negli adolescenti di età compresa tra 1 e 17 anni, e negli adulti.
CRYSVITA è usato per il trattamento dell’osteomalacia oncogenica, ossia indotta da tumore (TIO),
nei casi in cui non è possibile asportare con successo o individuare il tumore che causa questa
condizione, nei bambini e negli adolescenti di età compresa tra 1 e 17 anni e negli adulti.
Cos’è l’ipofosfatemia X-linked (XLH)
L’ipofosfatemia X-linked (XLH) è una malattia genetica.
- Le persone affette da XLH hanno livelli più elevati di un ormone chiamato fattore di crescita dei fibroblasti 23 (FGF23).
- L’FGF23 riduce la quantità di fosfato nel sangue.
- Il basso livello di fosfato può provocare:
- un indurimento delle ossa non adeguato e, in bambini e adolescenti, una crescita delle ossa non adeguata
- dolore e rigidità nelle ossa e nelle articolazioni.
Cos’è l’osteomalacia oncogenica (TIO)
- Le persone affette da TIO hanno livelli più elevati di un ormone chiamato FGF23, prodotto da alcuni tipi di tumore.
- L’FGF23 riduce la quantità di fosfato nel sangue.
- Il basso livello di fosfato può provocare rammollimento delle ossa, debolezza muscolare, stanchezza, dolore alle ossa e fratture.
Come agisce CRYSVITA
CRYSVITA si lega all’FGF23 nel sangue, impedendo l'azione di questo ormone, e aumenta la
quantità di fosfato nel sangue, in modo da consentire il raggiungimento di livelli normali.
2. Cosa deve sapere prima di usare CRYSVITA
Non usi CRYSVITA
- se è allergico a burosumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6)
- se sta assumendo integratori di fosfato o alcuni integratori di vitamina D (che contengono la cosiddetta vitamina D attiva, ad es. calcitriolo)
- se ha già un alto livello di fosfato nel sangue (“iperfosfatemia”)
- se ha una malattia renale grave o insufficienza renale.
Reazioni allergiche
Smetta di prendere CRYSVITA e contatti il medico immediatamente se compare uno dei seguenti
effetti indesiderati, perché potrebbe essere segno di una reazione allergica:
- eruzione cutanea e prurito in tutto il corpo
- gonfiore intenso di palpebre, bocca o labbra (angioedema)
- fiato corto
- battito cardiaco rapido
- sudorazione.
Se rientra in uno dei casi sopra elencati, non prenda CRYSVITA. Se ha dubbi si rivolga al medico
prima di usare CRYSVITA.
Avvertenze e precauzioni
Reazioni cutanee
Possono comparire reazioni cutanee nel sito in cui viene praticata l'iniezione; vedere paragrafo 4 per
ulteriori informazioni. Se queste reazioni sono intense, informi il medico.
Analisi e controlli
Il medico controllerà i livelli di fosfato e di calcio nel sangue e nelle urine e potrà eseguire inoltre
un'ecografia renale durante il trattamento, al fine di ridurre il rischio di iperfosfatemia (eccesso di
fosfato nel sangue) e mineralizzazione ectopica (accumulo di calcio in tessuti come i reni). Anche il
livello sierico di ormone paratiroideo sarà controllato di tanto in tanto.
Bambini di età inferiore a 1 anno
CRYSVITA non deve essere somministrato a bambini di età inferiore a 1 anno, perché la sicurezza e
gli effetti del medicinale non sono stati studiati in questa fascia d’età.
Altri medicinali e CRYSVITA
Informi il medico se sta assumendo, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale.
Non prenda CRYSVITA e informi il medico se sta assumendo:
- integratori di fosfato
- determinati integratori di vitamina D (che contengono la cosiddetta vitamina D attiva, ad es. calcitriolo). Esistono alcuni integratori di vitamina D che lei può continuare o iniziare a usare; il medico le indicherà quali sono.
Consulti il medico prima di prendere CRYSVITA:
- se sta assumendo medicinali che agiscono allo stesso modo del calcio nell'organismo (“calciomimetici”). Se usati insieme, possono ridurre il livello di calcio nel sangue
- se è affetto da TIO e sta per ricevere un trattamento per il tumore sottostante (radioterapia o asportazione chirurgica). In questo caso, il trattamento con CRYSVITA sarà iniziato solo dopo il trattamento del tumore sottostante e se i livelli di fosfato sierico sono bassi.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico o al farmacista prima di prendere questo medicinale, perché non
sono noti gli effetti di CRYSVITA sul bambino.
CRYSVITA non è raccomandato durante la gravidanza.
Se è in età fertile, deve usare un metodo contraccettivo efficace (controllo delle nascite) durante il
trattamento con CRYSVITA. Ne parli con il medico.
Non è noto se il CRYSVITA passi nel latte materno e il rischio per i neonati o i lattanti non può essere
escluso. Ne parli con il medico.
Guida di veicoli e utilizzo di biciclette e macchinari
È possibile che CRYSVITA causi capogiro e influisca sulla capacità di andare in bicicletta, utilizzare
strumenti o macchinari o guidare veicoli. Se ritiene di avere questo sintomo, non vada in bicicletta,
non utilizzi strumenti o macchinari, non guidi veicoli e informi il medico.
CRYSVITA contiene sorbitolo
Questo medicinale contiene 45,91 mg di sorbitolo per flaconcino equivalente a 45,91 mg/mL.
3. Come usare CRYSVITA
CRYSVITA deve essere somministrato mediante iniezione sotto la pelle (uso sottocutaneo) nella
parte superiore del braccio, nell’addome, nei glutei o nella coscia. Questo medicinale sarà
somministrato a lei o al suo bambino da un operatore sanitario. In alternativa, il medico può
raccomandare che sia lei a eseguire l’iniezione per sé o per il suo bambino. Un operatore sanitario le
mostrerà come fare. La prima auto-iniezione dopo l’inizio del trattamento o dopo una modifica della
dose deve essere eseguita in presenza di un operatore sanitario. Una sezione di “Istruzioni per l’Uso”
attenzione quando esegue l’iniezione di CRYSVITA per sé o per il suo bambino.
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico, dell’infermiere o del
farmacista. Se ha dubbi consulti il medico, l’infermiere o il farmacista.
Quantità di CRYSVITA necessaria
La dose si basa sul peso corporeo. Il medico stabilirà la dose giusta per lei.
Dose per XLH e TIO
La dose di CRYSVITA dovrà essere iniettata:
- ogni due settimane nei bambini e negli adolescenti di età compresa tra 1 e 17 anni
- ogni quattro settimane negli adulti.
Il medico eseguirà controlli per assicurarsi che lei riceva la dose giusta e potrà modificare la dose o la
frequenza di somministrazione se necessario.
Dose massima per pazienti affetti da XLH
La dose massima che riceverà per il trattamento dell’XLH è 90 mg.
Dose massima per pazienti affetti da TIO
La dose massima che riceverà per il trattamento del TIO
- per i bambini di età compresa tra 1 e 12 anni è 90 mg
- per gli adolescenti di età compresa tra 13 e 17 anni e per gli adulti è 180 mg.
Pazienti affetti da TIO
Se è affetto da TIO e necessita di un trattamento per il tumore sottostante (radioterapia o asportazione
chirurgica), il medico interromperà il trattamento con CRYSVITA. Una volta completato il
trattamento del tumore, il medico eseguirà i controlli dei livelli di fosfato sierico e riprenderà il
trattamento con CRYSVITA se tali livelli sono bassi.
Se ha ricevuto più CRYSVITA di quanto deve
Se ritiene che le sia stata somministrata una quantità eccessiva di CRYSVITA, informi
immediatamente il medico.
Se salta una dose di CRYSVITA
Se viene saltata una dose, consulti immediatamente il medico. La dose saltata deve essere
somministrata non appena possibile e il medico riorganizzerà le dosi future di conseguenza.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le
persone li manifestino.
Effetti indesiderati nei bambini e negli adolescenti affetti da XLH
Molto comune (può interessare più di 1 bambino e adolescente su 10)
- Ascesso (infezione) del dente
- Tosse
- Mal di testa
- Capogiro
- Vomito
- Nausea
- Diarrea
- Stitichezza
- Carie dentaria
- Eruzione cutanea
- Dolore ai muscoli (mialgia) e alle mani e ai piedi
- Reazioni nel sito in cui è stata praticata l’iniezione, che possono comprendere: o arrossamento o eruzione cutanea o dolore o prurito o gonfiore o sanguinamento o lividi
Queste reazioni nel sito di iniezione sono di solito lievi e si verificano entro un giorno
dall’iniezione; in genere migliorano in circa 1-3 giorni.
- Febbre
- Basso livello di vitamina D nel sangue
Non nota (la frequenza non può essere definita sulla base dei dati disponibili)
- Aumento del fosfato nel sangue
Effetti indesiderati nei bambini e negli adolescenti affetti da TIO
Non sono noti gli effetti indesiderati nei bambini e negli adolescenti poiché non sono stati effettuati
studi clinici.
Effetti indesiderati negli adulti affetti da XLH e TIO
Molto comune (può interessare più di 1 adulto su 10)
- Ascesso (infezione) del dente
- Mal di testa
- Capogiro
- Sindrome delle gambe senza riposo (desiderio irresistibile di muovere le gambe per far cessare dolore, fastidio o sensazioni strane alle gambe soprattutto prima di dormire o durante la notte)
- Stitichezza
- Dolore alla schiena
- Spasmo muscolare
- Reazioni nel punto in cui è stata eseguita l’iniezione, che possono comprendere dolore o gonfiore
- Bassi livelli di vitamina D nel sangue
Comune (può interessare fino a 1 adulto su 10)
- Eruzione cutanea
- Aumento del fosfato nel sangue
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema
nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti indesiderati può contribuire
a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare CRYSVITA
Conservi CRYSVITA fuori dalla vista e dalla portata dei bambini.
Non usi CRYSVITA dopo la data di scadenza che è riportata sulla scatola e sull’etichetta dopo
“Scad.”. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2 ° C – 8 ° C). Non congelare.
Tenere il flaconcino nell’imballaggio esterno per proteggere il medicinale dalla luce.
Non usi CRYSVITA se contiene particelle visibili.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Questo aiuterà a proteggere
l’ambiente.
per le istruzioni sullo smaltimento dei medicinali inutilizzati e dei materiali forniti.
Per qualsiasi domanda su come eliminare i medicinali che non utilizza più, si rivolga all’operatore
sanitario o al farmacista.
6. Contenuto della confezione e altre informazioni
Cosa contiene CRYSVITA
- Il principio attivo è burosumab. Ogni flaconcino contiene 10, 20 o 30 mg di burosumab.
- Gli altri componenti sono L-istidina, D-sorbitolo (E 420), polisorbato 80, L-metionina, acido cloridrico 10%, e acqua per preparazioni iniettabili. (Vedere “CRYSVITA contiene sorbitolo” al paragrafo 2 per ulteriori informazioni).
Descrizione dell’aspetto di CRYSVITA e contenuto della confezione
CRYSVITA è fornito in soluzione iniettabile da limpida a leggermente opalescente, da incolore a
marroncino-giallastro, in un flaconcino di vetro. Ogni confezione contiene 1 flaconcino.
Titolare dell’autorizzazione all’immissione in commercio
Kyowa Kirin Holdings B.V.
Bloemlaan 2
2132NP Hoofddorp
Paesi Bassi
[email protected]
Produttore
allphamed PHARBIL Arzneimittel GmbH
Hildebrandstr. 10-12
37081 Göttingen
Germania
Kyowa Kirin Holdings B.V.
Bloemlaan 2
2132NP Hoofddorp
Paesi Bassi
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, http://www.ema.europa.eu/ . Inoltre, sono riportati link ad altri siti web su malattie
rare e relativi trattamenti terapeutici.
ISTRUZIONI PER L’USO
Legga attentamente queste Istruzioni per l’Uso prima di utilizzare CRYSVITA:
- Esegua l’iniezione per sé o per il suo bambino solo se il suo medico le ha detto di farlo.
- L’iniezione deve essere eseguita solo dopo che avrà ricevuto adeguate istruzioni sulla tecnica di iniezione. La prima auto-iniezione dopo l’inizio del trattamento o dopo una modifica della dose deve essere eseguita in presenza di un operatore sanitario.
- Usi questo medicinale seguendo sempre esattamente le istruzioni del medico, del farmacista o dell’infermiere (operatore sanitario). Se ha dubbi si rivolga all’operatore sanitario.
- Il medico le prescriverà la dose corretta, misurata in milligrammi (mg). CRYSVITA è disponibile in flaconcini di tre diversi dosaggi: 10 mg, 20 mg e 30 mg. Ogni flaconcino è solo monouso. Usi sempre un nuovo flaconcino di CRYSVITA per ogni iniezione, consulti la Fase 5 per sapere come smaltire i flaconcini utilizzati e gli altri materiali forniti.
- L’operatore sanitario le dirà la quantità di CRYSVITA da somministrare per sé o per il suo bambino. È possibile che per ottenere la dose corretta per sé o per il suo bambino sia necessario più di un flaconcino.
- Se l’operatore sanitario le dice che è necessaria più di un’iniezione per somministrare la dose richiesta, per ogni iniezione deve ripetere le Fasi da 2 a 5 illustrate qui di seguito. Usi materiali nuovi e scelga una zona diversa del corpo per ogni iniezione.
- Usi solo la siringa e gli aghi forniti o prescritti dall’operatore sanitario per effettuare l’iniezione. o Usi sempre l’ago grande per aspirare il liquido e ricordi di sostituirlo con l’ago piccolo quando deve iniettarlo. o L’uso della siringa o dell’ago sbagliati può causare un errore nella dose o rendere l’iniezione più dolorosa.
- Quando CRYSVITA viene somministrato a un bambino piccolo, può essere utile la presenza di un’altra persona per fornire assistenza.
- Non usi CRYSVITA in caso di allergia a uno qualsiasi dei componenti di questo medicinale. Interrompa l’uso di CRYSVITA se ha una reazione allergica durante o dopo l’iniezione e contatti immediatamente l’operatore sanitario. Per maggiori informazioni, consulti il
Fase 1. Raccogliere e ispezionare i materiali forniti
Estragga dal frigorifero i flaconcini di CRYSVITA necessari.
Controlli il dosaggio sull’etichetta di ogni flaconcino.
Verifichi di avere il numero corretto di flaconcini corrispondente alla dose in milligrammi (mg), come
consigliato dall’operatore sanitario.
Se ha dubbi consulti l’operatore sanitario.
Lasci che i flaconcini si riscaldino a temperatura ambiente per 30 minuti. Non riscaldi i flaconcini in
altro modo, ad esempio con acqua calda o in un forno a microonde. Non esponga i flaconcini alla luce
diretta del sole.
Controlli la data di scadenza (indicata dopo Scad.) sull’etichetta del flaconcino.
Ispezioni il liquido contenuto nel flaconcino, senza agitare.
Non usi il flaconcino se:
- è stata superata la data di scadenza
- il colore è alterato, se è torbido o contiene particelle. Il liquido di CRYSVITA deve essere da limpido a leggermente opalescente, da incolore a marroncino-giallastro.
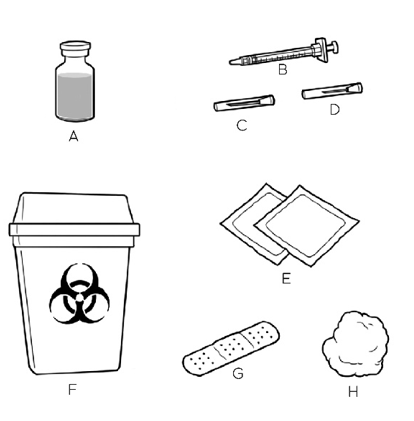
Posizioni tutti i materiali necessari su una superficie
piana e pulita. Per ogni iniezione saranno necessari:
- A. Flaconcino di CRYSVITA per l’iniezione
- B. Una siringa con stantuffo
- C. Un ago da siringa grande per prelevare CRYSVITA
- D. Un ago da siringa piccolo per iniettare CRYSVITA
- E. Fazzolettini imbevuti di alcol
- F. Contenitore per oggetti taglienti
- G. Cerotto (se richiesto)
- H. Garza o batuffolo di cotone Se non ha questi materiali, contatti l’operatore sanitario.
L’operatore sanitario le spiegherà l’uso dei diversi aghi.
L’ ago grandeserve per prelevare CRYSVITA dal flaconcino.
L’ ago piccoloserve per iniettare CRYSVITA.
Se ha dubbi consulti l’operatore sanitario prima dell’uso.
Non utilizzi materiali con pezzi mancanti o che risultano danneggiati in qualche modo.
Non rimuova il cappuccio da un ago fino a quando non è pronto a utilizzarlo.
Si lavi le mani accuratamente con acqua e sapone prima di passare alla Fase 2.
Fase 2. Prelevare CRYSVITA e preparare l’iniezione
Tolga la capsula di chiusura che sigilla il flaconcino in modo da esporre il tappo di gomma.
Pulisca il tappo di gomma con un fazzolettino imbevuto di alcol e lo lasci asciugare. Non tocchi il
tappo di gomma dopo averlo pulito.
Scelga l’ago grandee lo estragga dalla confezione
sterile, ma senza rimuovere il cappuccio che lo
copre.
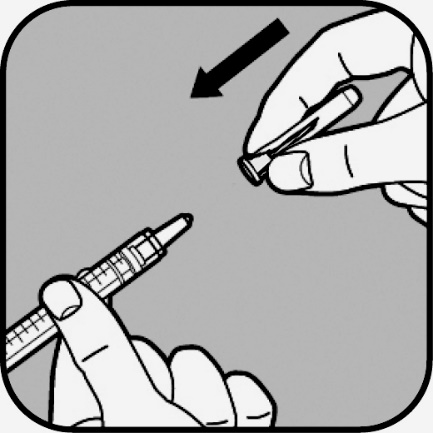
Per applicarlo alla siringa, tenga l’ago grandeper il
cappuccio protettivo con una mano e il corpo della
siringa con l’altra.
In base ai materiali che le sono stati forniti
- dovrà spingere l’ago sulla siringa ruotandolo in senso orario per stringerlo bene;
- oppurespingere l’ago verso il basso fino a quando non è saldamente applicato. Non tocchi l’ago o l’estremità della siringa a cui è applicato.
Una volta che l’ago è saldamente applicato, impugni il corpo della siringa tenendo l’ago rivolto verso
l’alto.
Rimuova il cappuccio dall’ago tirandolo.
Non getti via il cappuccio dell’ago.
Dopo avere tolto il cappuccio, l’ago non deve essere toccato né venire a contatto con altre superfici.
Non usi la siringa se la fa cadere dopo avere tolto il cappuccio o se l’ago appare danneggiato.
L’operatore sanitario le dirà la quantità di liquido da
iniettare, che sarà di norma 1 mL per ogni iniezione.
L’operatore sanitario le mostrerà quale tacca di
misura utilizzare se deve iniettare meno di 1 mL.
Usi sempre la tacca corrispondente alla sua dose. Se
ha dubbi consulti l’operatore sanitario prima
dell’uso.
Tiri indietro lo stantuffo della siringa fino a quando
l’estremità è allineata alla tacca corrispondente alla
sua dose. In questo modo, la siringa si riempie
d’aria.
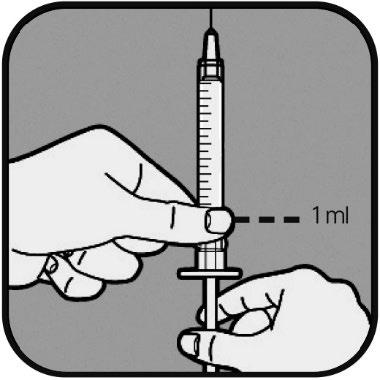
Posizioni il flaconcino su una superficie piana.
Lentamente, inserisca l’ago grande nel flaconcino
attraverso il tappo di gomma.
Eviti che la punta dell’ago venga a contatto con il
liquido nel flaconcino.
Se la punta dell’ago viene a contatto con il liquido,
ritragga lentamente l’ago fino a quando non tocca
più il liquido.
Spinga lentamente lo stantuffo nella siringa.
In questo modo l’aria viene immessa dalla siringa
nel flaconcino.
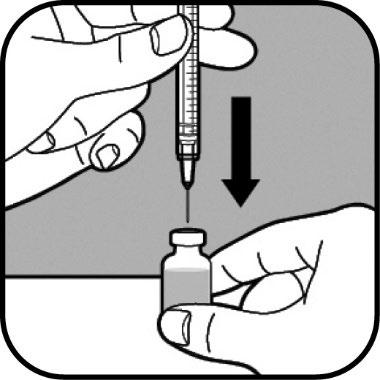
Capovolga il flaconcino mantenendo l’ago al suo
interno.
Si assicuri che la punta dell’ago sia sul fondo del
liquido.
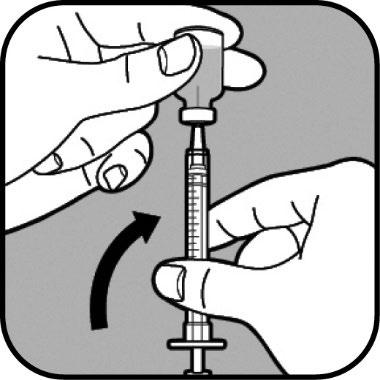
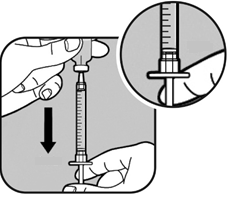
Lentamente, tiri indietro lo stantuffo per riempire la
siringa fino a quando l’estremità dello stantuffo è
allineata alla tacca corrispondente alla sua dose.
Tenga sempre la punta dell’ago nel liquido.
Controlli la presenza di bolle d’aria nel liquido
contenuto nella siringa.
Se nota delle bolle,
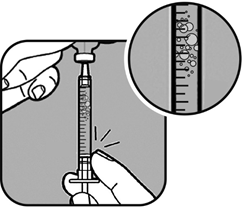
- tenga la siringa verticalmente con l’ago sempre all’interno del flaconcino,
- con il dito picchietti delicatamente il corpo della siringa per spostare le bolle d’aria,
- quando le bolle d’aria si trovano in alto, spinga lentamente lo stantuffo per espellerle.
Controlli nuovamente la dose rispetto alle tacche
sulla siringa.
Se necessario, prelevi ancora un po’ di liquido per
arrivare alla tacca corrispondente alla sua dose.
Ricontrolli l’eventuale presenza di bolle e ripeta la
procedura, se necessario.
Quando non ci sono più bolle nella siringa, estragga la siringa con l’ago dal flaconcino tirando verso il
basso.
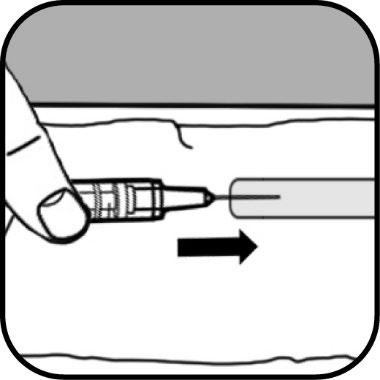
Rimuova l’ago grande dalla siringa.
- Per farlo, prenda il cappuccio dell’ago grande e lo posizioni su una superficie piana.
- Con una mano, infili l’ago grande nel cappuccio facendolo scorrere fino a coprirlo senza usare l’altra mano per evitare lesioni. Poi con l’altra mano fissi il cappuccio facendolo scattare in posizione.
- A seconda dei materiali di cui dispone, dovrà: o ruotare in senso antiorario l’ago grande con il cappuccio applicato per estrarlo dalla siringa
o oppure estrarre direttamente dalla siringa
l’ago grande con il cappuccio applicato e
metterlo nel contenitore per oggetti
taglienti.
Scelga l’ago piccoloe lo estragga dalla confezione sterile, ma senza rimuovere il cappuccio che lo
copre.
Per applicarlo alla siringa, tenga l’ago piccoloper il cappuccio protettivo con una mano e il corpo
della siringa con l’altra mano.
In base ai materiali che le sono stati forniti
- dovrà spingere l’ago sulla siringa ruotandolo in senso orario fino a quando non è saldo
- oppurespingere l’ago verso il basso fino a quando non è saldamente applicato. Non tocchi l’ago o l’estremità della siringa a cui è applicato.
Fase 3. Preparare il sito di iniezione
L’iniezione deve essere praticata nello strato di
grasso appena sotto la pelle. Dovrà scegliere un sito
di iniezione. Se esegue l’auto-iniezione le zone
adatte sono:
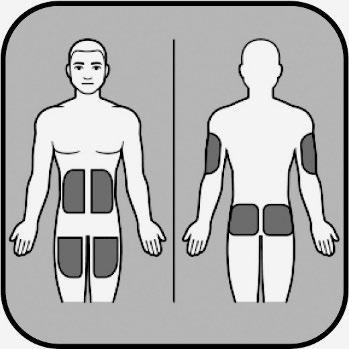
- addome e parte superiore delle cosce
Se effettua l’iniezione a qualcun altro, le zone adatte
sono:
- addome, parte superiore delle cosce, zona esterna della parte superiore delle braccia, glutei
Non iniettare:
- in una zona che presenta infiammazione, rossore o lividi o dove la pelle presenta lesioni
- in una zona in cui vi sono smagliature o cicatrici (incluse ustioni)
- direttamente in un neo, o nella zona intorno a un neo
Se effettua più di un’iniezione, scelga un sito diverso per ogni iniezione. Disinfetti ogni sito di
iniezione con un nuovo batuffolo imbevuto di alcol e lasci asciugare la pelle.
CRYSVITA deve essere iniettato nella pelle asciutta e pulita.
Fase 4. Iniettare CRYSVITA
Rimuova il cappuccio dell’ago piccolo tirandolo.
Stringa saldamente la pelle tra il pollice e le dita,
creando una zona di circa 5 cm di grandezza.
Tenga la siringa tra il pollice e l’indice della mano
dominante.
L’ago deve essere inserito nella pelle a un angolo di
45° o di 90°.
L’operatore sanitario le mostrerà quale angolo
utilizzare.
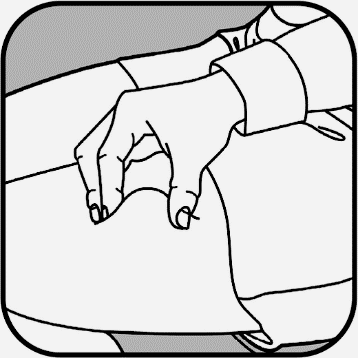
Usi un movimento rapido, come per lanciare una freccetta, per inserire l’ago nella pelle che tiene tra
le dita.
Non spinga lo stantuffo quando inserisce l’ago.
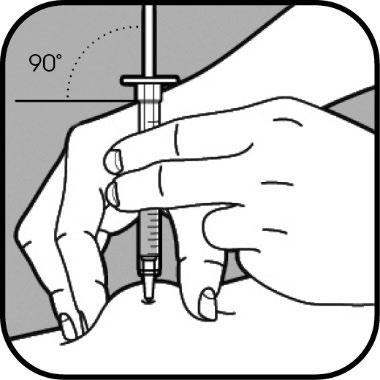
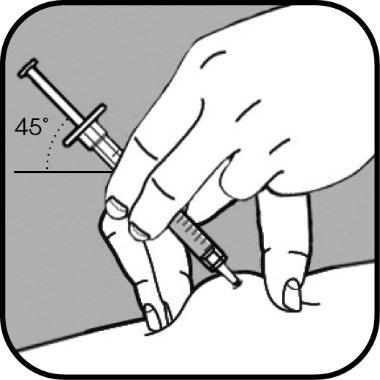
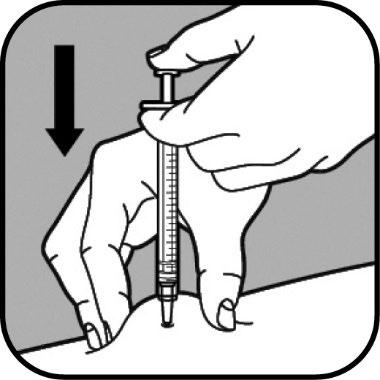
Quando l’ago è inserito non lo muova.
Continui a tenere la pelle tra le dita.
Spinga lentamente lo stantuffo nella siringa, per un
massimo di 30 secondi, fino svuotare la siringa.
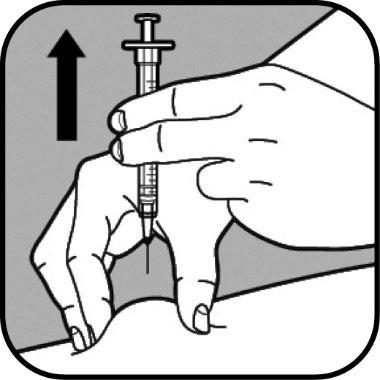
Dopo avere somministrato la dose completa,
concluda l’iniezione estraendo delicatamente la
siringa.
Lasci andare la pelle tra le dita.
Prema un batuffolo di cotone o una garza sul sito di
iniezione per alcuni secondi per interrompere il
sanguinamento. Applichi un cerotto se necessario.
Non massaggi il sito di iniezione.
Per evitare lesioni, non rimetta il cappuccio sull’ago
piccolo. Getti l’ago privo di cappuccio nel
contenitore per lo smaltimento di oggetti taglienti.
Fase 5. Dopo ogni iniezione
Getti gli aghi usati, i relativi cappucci e le siringhe nel contenitore per lo smaltimento di oggetti
taglienti; i flaconcini devono essere smaltiti in conformità alla normativa locale vigente.
Non getti aghi o siringhe nei rifiuti domestici.
Non conservi i flaconcini con il medicinale residuo per uso futuro e non li dia ad altre persone.
Quando il contenitore per oggetti taglienti è quasi pieno, segua le linee guida locali per richiedere un
altro contenitore e per smaltirlo correttamente.
Promemoria:se effettua più di un’iniezione, ripeta le Fasi da 2 a 5 per ogni iniezione.
Usi nuovi materiali per ogni iniezione.
Annoti la data dell’iniezione e tutte le zone in cui ha praticato l’iniezione, in modo da usare un sito
diverso per l’iniezione successiva.
Un video che mostra come preparare ed effettuare l’iniezione è disponibile al link seguente:
www.myinject.eu .
CRYSVITA 10 mg soluzione iniettabile in siringa preriempita, 20 mg soluzione iniettabile in siringa preriempita, 30 mg soluzione iniettabile in siringa preriempita
burosumab
Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è CRYSVITA e a cosa serve
- 2. Cosa deve sapere prima di usare CRYSVITA
- 3. Come usare CRYSVITA
- 4. Possibili effetti indesiderati
- 5. Come conservare CRYSVITA
- 6. Contenuto della confezione e altre informazioni
1. Cos’è CRYSVITA e a cosa serve
Cos’è CRYSVITA
CRYSVITA contiene il principio attivo burosumab, un tipo di medicinale noto come anticorpo
monoclonale umano.
A cosa serve CRYSVITA
CRYSVITA è usato per il trattamento dell’ipofosfatemia X-linked (XLH). È impiegato nei bambini e
negli adolescenti di età compresa tra 1 e 17 anni, e negli adulti.
CRYSVITA è usato per il trattamento dell’osteomalacia oncogenica, ossia indotta da tumore (TIO),
nei casi in cui non è possibile asportare con successo o individuare il tumore che causa questa
condizione, nei bambini e negli adolescenti di età compresa tra 1 e 17 anni e negli adulti.
Cos’è l’ipofosfatemia X-linked (XLH)
L’ipofosfatemia X-linked (XLH) è una malattia genetica.
- Le persone affette da XLH hanno livelli più elevati di un ormone chiamato fattore di crescita dei fibroblasti 23 (FGF23).
- L’FGF23 riduce la quantità di fosfato nel sangue.
- Il basso livello di fosfato può provocare:
- un indurimento delle ossa non adeguato e, in bambini e adolescenti, una crescita delle ossa non adeguata
- dolore e rigidità nelle ossa e nelle articolazioni.
Cos’è l’osteomalacia oncogenica (TIO)
- Le persone affette da TIO hanno livelli più elevati di un ormone chiamato FGF23, prodotto da alcuni tipi di tumore.
- L’FGF23 riduce la quantità di fosfato nel sangue.
- Il basso livello di fosfato può provocare rammollimento delle ossa, debolezza muscolare, stanchezza, dolore alle ossa e fratture.
Come agisce CRYSVITA
CRYSVITA si lega all’FGF23 nel sangue, impedendo l'azione di questo ormone, e aumenta la
quantità di fosfato nel sangue, in modo da consentire il raggiungimento di livelli normali.
2. Cosa deve sapere prima di usare CRYSVITA
Non usi CRYSVITA
- se è allergico a burosumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6)
- se sta assumendo integratori di fosfato o alcuni integratori di vitamina D (che contengono la cosiddetta vitamina D attiva, ad es. calcitriolo)
- se ha già un alto livello di fosfato nel sangue (“iperfosfatemia”)
- se ha una malattia renale grave o insufficienza renale.
Reazioni allergiche
Smetta di prendere CRYSVITA e contatti il medico immediatamente se compare uno dei seguenti
effetti indesiderati, perché potrebbe essere segno di una reazione allergica:
- eruzione cutanea e prurito in tutto il corpo
- gonfiore intenso di palpebre, bocca o labbra (angioedema)
- fiato corto
- battito cardiaco rapido
- sudorazione.
Se rientra in uno dei casi sopra elencati, non prenda CRYSVITA. Se ha dubbi si rivolga al medico
prima di usare CRYSVITA.
Avvertenze e precauzioni
Reazioni cutanee
Possono comparire reazioni cutanee nel sito in cui viene praticata l'iniezione; vedere paragrafo 4 per
ulteriori informazioni. Se queste reazioni sono intense, informi il medico.
Analisi e controlli
Il medico controllerà i livelli di fosfato e di calcio nel sangue e nelle urine e potrà eseguire inoltre
un'ecografia renale durante il trattamento, al fine di ridurre il rischio di iperfosfatemia (eccesso di
fosfato nel sangue) e mineralizzazione ectopica (accumulo di calcio in tessuti come i reni). Anche il
livello sierico di ormone paratiroideo sarà controllato di tanto in tanto.
Bambini di età inferiore a 1 anno
CRYSVITA non deve essere somministrato a bambini di età inferiore a 1 anno, perché la sicurezza e
gli effetti del medicinale non sono stati studiati in questa fascia d’età.
Altri medicinali e CRYSVITA
Informi il medico se sta assumendo, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale.
Non prenda CRYSVITA e informi il medico se sta assumendo:
- integratori di fosfato
- determinati integratori di vitamina D (che contengono la cosiddetta vitamina D attiva, ad es. calcitriolo). Esistono alcuni integratori di vitamina D che lei può continuare o iniziare a usare; il medico le indicherà quali sono.
Consulti il medico prima di prendere CRYSVITA:
- se sta assumendo medicinali che agiscono allo stesso modo del calcio nell'organismo (“calciomimetici”). Se usati insieme, possono ridurre il livello di calcio nel sangue
- se è affetto da TIO e sta per ricevere un trattamento per il tumore sottostante (radioterapia o asportazione chirurgica). In questo caso, il trattamento con CRYSVITA sarà iniziato solo dopo il trattamento del tumore sottostante e se i livelli di fosfato sierico sono bassi.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico o al farmacista prima di prendere questo medicinale, perché non
sono noti gli effetti di CRYSVITA sul bambino.
CRYSVITA non è raccomandato durante la gravidanza.
Se è in età fertile, deve usare un metodo contraccettivo efficace (controllo delle nascite) durante il
trattamento con CRYSVITA. Ne parli con il medico.
Non è noto se il CRYSVITA passi nel latte materno e il rischio per i neonati o i lattanti non può essere
escluso. Ne parli con il medico.
Guida di veicoli e utilizzo di biciclette e macchinari
È possibile che CRYSVITA causi capogiro e influisca sulla capacità di andare in bicicletta, utilizzare
strumenti o macchinari o guidare veicoli. Se ritiene di avere questo sintomo, non vada in bicicletta,
non utilizzi strumenti o macchinari, non guidi veicoli e informi il medico.
CRYSVITA contiene sorbitolo
CRYSVITA 10 mg soluzione iniettabile in siringa preriempita: questo medicinale contiene 15,30 mg
di sorbitolo per siringa preriempita.
CRYSVITA 20 mg soluzione iniettabile in siringa preriempita: questo medicinale contiene 30,61 mg
di sorbitolo per siringa preriempita.
CRYSVITA 30 mg soluzione iniettabile in siringa preriempita: questo medicinale contiene 45,91 mg
di sorbitolo per siringa preriempita.
3. Come usare CRYSVITA
CRYSVITA deve essere somministrato mediante iniezione sotto la pelle (uso sottocutaneo) nella
parte superiore del braccio, nell’addome, nei glutei o nella coscia. Questo medicinale può esserle
somministrato da un operatore sanitario o, in alternativa, il medico può raccomandare che sia lei o una
persona che la assiste a eseguire l’iniezione di CRYSVITA. Se le viene suggerito di eseguire
autonomamente l’iniezione, un operatore sanitario le fornirà istruzioni per mostrare a lei o alla
persona che la assiste il modo corretto di usare CRYSVITA prima della prima auto-iniezione.
La prima auto-iniezione dopo l’inizio del trattamento o dopo una modifica della dose deve essere
eseguita in presenza di un operatore sanitario. Una sezione di “Istruzioni per l’Uso” dettagliate per
istruzioni con attenzione quando esegue l’iniezione di CRYSVITA per sé o per il suo bambino.
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico, dell’infermiere o del
farmacista. Se ha dubbi consulti il medico, l’infermiere o il farmacista.
Quantità di CRYSVITA necessaria
La dose si basa sul peso corporeo. Il medico stabilirà la dose giusta per lei.
Dose per XLH e TIO
La dose di CRYSVITA dovrà essere iniettata:
- ogni due settimane nei bambini e negli adolescenti di età compresa tra 1 e 17 anni
- ogni quattro settimane negli adulti.
Il medico eseguirà controlli per assicurarsi che lei riceva la dose giusta e potrà modificare la dose o la
frequenza di somministrazione se necessario.
Dose massima per pazienti affetti da XLH
La dose massima che riceverà per il trattamento dell’XLH è 90 mg.
Dose massima per pazienti affetti da TIO
La dose massima che riceverà per il trattamento del TIO
- per i bambini di età compresa tra 1 e 12 anni è 90 mg
- per gli adolescenti di età compresa tra 13 e 17 anni e per gli adulti è 180 mg.
Pazienti affetti da TIO
Se è affetto da TIO e necessita di un trattamento per il tumore sottostante (radioterapia o asportazione
chirurgica), il medico interromperà il trattamento con CRYSVITA. Una volta completato il
trattamento del tumore, il medico eseguirà i controlli dei livelli di fosfato sierico e riprenderà il
trattamento con CRYSVITA se tali livelli sono bassi.
Se ha ricevuto più CRYSVITA di quanto deve
Se ritiene che le sia stata somministrata una quantità eccessiva di CRYSVITA, informi
immediatamente il medico.
Se salta una dose di CRYSVITA
Se viene saltata una dose, consulti immediatamente il medico. La dose saltata deve essere
somministrata non appena possibile e il medico riorganizzerà le dosi future di conseguenza.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le
persone li manifestino.
Effetti indesiderati nei bambini e negli adolescenti affetti da XLH
Molto comune (può interessare più di 1 bambino e adolescente su 10)
- Ascesso (infezione) del dente
- Tosse
- Mal di testa
- Capogiro
- Vomito
- Nausea
- Diarrea
- Stitichezza
- Carie dentaria
- Eruzione cutanea
- Dolore ai muscoli (mialgia) e alle mani e ai piedi
- Reazioni nel sito in cui è stata praticata l’iniezione, che possono comprendere: o arrossamento o eruzione cutanea o dolore o prurito o gonfiore o sanguinamento o lividi Queste reazioni nel sito di iniezione sono di solito lievi e si verificano entro un giorno dall’iniezione; in genere migliorano in circa 1-3 giorni.
- Febbre
- Basso livello di vitamina D nel sangue
Non nota (la frequenza non può essere definita sulla base dei dati disponibili)
- Aumento del fosfato nel sangue
Effetti indesiderati nei bambini e negli adolescenti affetti da TIO
Non sono noti gli effetti indesiderati nei bambini e negli adolescenti poiché non sono stati effettuati
studi clinici.
Effetti indesiderati negli adulti affetti da XLH e TIO
Molto comune (può interessare più di 1 adulto su 10)
- Ascesso (infezione) del dente
- Mal di testa
- Capogiro
- Sindrome delle gambe senza riposo (desiderio irresistibile di muovere le gambe per far cessare dolore, fastidio o sensazioni strane alle gambe soprattutto prima di dormire o durante la notte)
- Stitichezza
- Dolore alla schiena
- Spasmo muscolare
- Reazioni nel punto in cui è stata eseguita l’iniezione, che possono comprendere dolore o gonfiore
- Bassi livelli di vitamina D nel sangue
Comune (può interessare fino a 1 adulto su 10)
- Eruzione cutanea
- Aumento del fosfato nel sangue
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o all’infermiere. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema
nazionale di segnalazione riportato nell’ allegato V . Segnalando gli effetti indesiderati può contribuire
a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare CRYSVITA
Conservi CRYSVITA fuori dalla vista e dalla portata dei bambini.
Non usi CRYSVITA dopo la data di scadenza che è riportata sulla scatola e sull’etichetta dopo
“Scad.”. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2 ° C – 8 ° C). Non congelare.
Tenere la siringa preriempita nell’imballaggio esterno per proteggere il medicinale dalla luce.
Non usi CRYSVITA se contiene particelle visibili.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Questo aiuterà a proteggere
l’ambiente.
per le istruzioni sullo smaltimento dei medicinali inutilizzati e dei materiali forniti.
Per qualsiasi domanda su come eliminare i medicinali che non utilizza più, si rivolga all’operatore
sanitario o al farmacista.
6. Contenuto della confezione e altre informazioni
Cosa contiene CRYSVITA
Il principio attivo è burosumab.
Siringa preriempita da 10 mg:
Ogni siringa preriempita contiene 10 mg di burosumab in 0,33 mL di soluzione.
Siringa preriempita da 20 mg:
Ogni siringa preriempita contiene 20 mg di burosumab in 0,67 mL di soluzione.
Siringa preriempita da 30 mg:
Ogni siringa preriempita contiene 30 mg di burosumab in 1 mL di soluzione.
Gli altri componenti sono L-istidina, D-sorbitolo (E 420), polisorbato 80, L-metionina, acido
cloridrico 10%, e acqua per preparazioni iniettabili. (Vedere “CRYSVITA contiene sorbitolo” al
paragrafo 2 per ulteriori informazioni).
Descrizione dell’aspetto di CRYSVITA e contenuto della confezione
CRYSVITA è fornito in soluzione iniettabile da limpida a leggermente opalescente, da incolore a
marroncino-giallastro, in una siringa preriempita. Ogni confezione contiene 1 siringa preriempita.
I diversi dosaggi del medicinale possono essere identificati dai diversi colori del corpo dello stantuffo:
10 mg (blu), 20 mg (rosso) e 30 mg (verde).
Titolare dell’autorizzazione all’immissione in commercio
Kyowa Kirin Holdings B.V.
Bloemlaan 2
2132NP Hoofddorp
Paesi Bassi
[email protected]
Produttore
allphamed PHARBIL Arzneimittel GmbH
Hildebrandstr. 10-12
37081 Göttingen
Germania
Kyowa Kirin Holdings B.V.
Bloemlaan 2
2132NP Hoofddorp
Paesi Bassi
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, http://www.ema.europa.eu/ . Inoltre, sono riportati link ad altri siti web su malattie
rare e relativi trattamenti terapeutici.
ISTRUZIONI PER L’USO
Le seguenti Istruzioni per l’Uso sono destinate:
- all’autosomministrazione
- alla somministrazione da parte di una persona che assiste il paziente o di un operatore sanitario
Legga attentamente queste Istruzioni per l’Uso prima di utilizzare CRYSVITA:
- Somministri questo medicinale a sé stesso o ad altri solo se il suo medico le ha detto di farlo.
- Deve somministrare questo medicinale a sé stesso o ad altri solo dopo che avrà ricevuto adeguate istruzioni sulla tecnica di iniezione. La prima auto-iniezione dopo l’inizio del trattamento o dopo una modifica della dose deve essere eseguita in presenza di un medico, farmacista o infermiere (operatore sanitario).
- Usi questo medicinale seguendo sempre esattamente le istruzioni dell’operatore sanitario. Se ha dubbi si rivolga all’operatore sanitario.
- Il medico le prescriverà la dose corretta, misurata in milligrammi (mg).
- L’operatore sanitario le dirà la quantità di CRYSVITA da somministrare per sé o per altri. È possibile che per ottenere la dose corretta sia necessaria più di una siringa preriempita.
- Se l’operatore sanitario le dice che è necessaria più di un’iniezione per somministrare la dose richiesta, per ogni iniezione deve ripetere le Fasi da 2 a 4 illustrate qui di seguito.
- Usi materiali nuovi per ogni iniezione.
- Ogni siringa preriempita è solo monouso. Usi sempre una siringa preriempita di CRYSVITA nuova per ogni iniezione; vedere la fase 4 per le modalità di smaltimento delle siringe usate e degli altri materiali.
- Se possibile, scelga una zona diversa del corpo per ogni iniezione
- Quando CRYSVITA viene somministrato a un bambino piccolo, può essere utile la presenza di un’altra persona per fornire assistenza.
- Non usi CRYSVITA in caso di allergia a uno qualsiasi dei componenti di questo medicinale. Interrompa l’uso di CRYSVITA se ha una reazione allergica durante o dopo l’iniezione e contatti immediatamente l’operatore sanitario. Per maggiori informazioni, consulti il
CRYSVITA è disponibile in siringa preriempita di tre diversi dosaggi: 10 mg (blu), 20 mg (rosso) e
30 mg (verde). La quantità di liquido nelle siringhe preriempite varia a seconda del dosaggio. Le
siringhe che le saranno fornite dipendono dalla dose prescritta.
Queste istruzioni valgono per tutti i tre dosaggi.
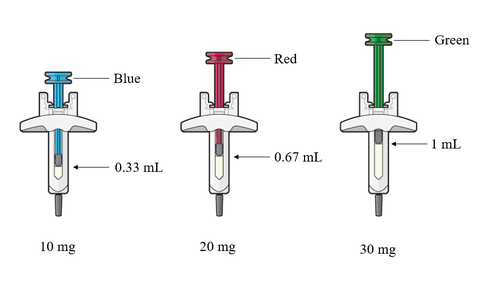
Verde
Rosso
Blu
1 mL
0,67 mL
0,33 mL
10 mg 20 mg 30 mg
Le parti della siringa preriempita di CRYSVITA sono raffigurate di seguito:

Prima dell’uso Dopo l’uso
Dispositivo di protezione
Corpo dello stantuffoattivato
Impugnatura per le dita
Finestra di visualizzazione
Ago ritratto
Medicinale
Corpo della siringaMolla del dispositivo di
protezione
Fase 1. Raccogliere e ispezionare i materiali forniti
CRYSVITA deve essere conservato in frigorifero prima dell’uso. Se deve somministrare CRYSVITA
a sé stesso o ad altri, estragga CRYSVITA dal frigorifero ma lo tenga nella confezione. Appoggi la
confezione su una superficie piana e pulita.
Osservi le confezioni di CRYSVITA per controllare il dosaggio di ogni siringa preriempita che le è
stata fornita.
Verifichi di avere il numero corretto di siringhe e i corretti dosaggi di ciascuna siringa preriempita
corrispondenti alla dose in milligrammi (mg), come consigliato dall’operatore sanitario.
Se ha dubbi consulti l’operatore sanitario.
Lasci che la confezione della siringa preriempita si riscaldi a temperatura ambiente per 45 minuti.
Nonriscaldi la siringa preriempita in altro modo, ad esempio con acqua calda o in un forno a
microonde. Nonesponga la siringa preriempita alla luce diretta del sole.
Dopo 45 minuti, apra la confezione di cartone ed estragga il vassoio di plastica. Prenda delicatamente
la siringa preriempita tenendola per il corpo e la estragga dal vassoio.
Nonsollevi la siringa tenendola dal corpo dello stantuffo o dal cappuccio dell’ago.
Nontocchi il corpo dello stantuffo e non rimuova il cappuccio dell’ago fino a quando non è pronto a
utilizzarli.

Posizioni tutti i materiali necessari su una
superficie piana e pulita. Per ogni iniezione
saranno necessari:
- Siringa preriempita di CRYSVITA
- Fazzolettini imbevuti di alcol
- Contenitore per oggetti taglienti
- Garza o batuffolo di cotone
Se non ha questi materiali, contatti l’operatore
sanitario.
Nonusi la siringa preriempita se il cappuccio dell’ago è mancante o non è saldamente applicato.
Nonusi la siringa preriempita se è incrinata o rotta in qualche modo.
Controlli il dosaggio sull’etichetta di ogni siringa preriempita.
Controlli la data di scadenza (indicata dopo Scad.) sull’etichetta di ogni siringa preriempita.
Nonusi la siringa preriempita se è stata superata la data di scadenza
Ispezioni il liquido contenuto nella siringa preriempita, senza agitare.
Il liquido di CRYSVITA deve essere da limpido a leggermente opalescente, da incolore a
marroncino-giallastro.
Nota: è normale che il medicinale presenti delle bolle d’aria. Le bolle d’aria non sono pericolose per
lei né influiscono sulla dose.
Nonusi la siringa preriempita se il liquido presenta alterazioni del colore, è torbido o contiene
particelle.
Si lavi le mani accuratamente con acqua e sapone prima di passare alla Fase 2.
Fase 2. Preparare il sito di iniezione
L’iniezione deve essere praticata nello strato di
grasso appena sotto la pelle. Dovrà scegliere un
sito di iniezione. Se esegue l’auto-iniezione le
zone adatte sono:
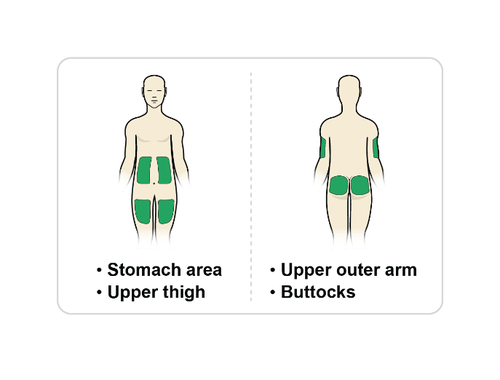
- addome, parte superiore delle cosce
Se effettua l’iniezione a qualcun altro le zone
adatte sono:
- addome, parte superiore delle cosce, zona esterna della parte superiore delle braccia, glutei
Noniniettare:
- in una zona che presenta infiammazione, rossore o lividi o dove la pelle presenta lesioni
- in una zona in cui vi sono smagliature o cicatrici (incluse ustioni)
- direttamente in un neo, o nella zona intorno a un neo
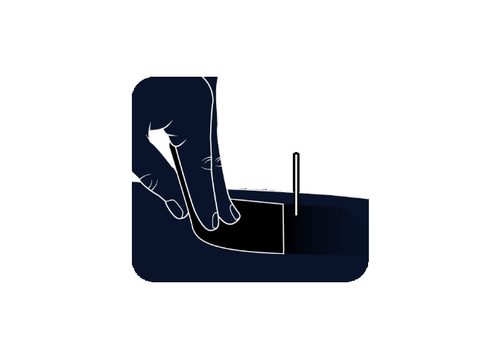
Sito di iniezionePulisca il sito di iniezione con un fazzolettino
imbevuto di alcol e lo lasci asciugare all’aria.
Nontocchi e non soffi sul sito di iniezione pulito.
Se effettua più di un’iniezione, scelga un sito diversoper ogni iniezione. Disinfetti ogni sito di
iniezione con un nuovo batuffolo imbevuto di alcol e lasci asciugare la pelle all’aria.
CRYSVITA deve essere iniettato nella pelle asciutta e pulita.
Fase 3. Iniettare CRYSVITA
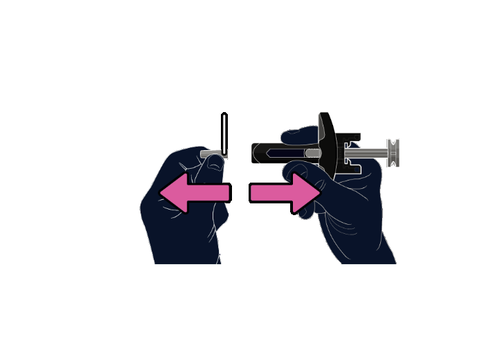
Tenga il corpo della siringacon una mano e con
il cappuccio dell’ago rivolto lontano da lei.
Rimuova il cappuccio dell’ago tirandolocon
l’altra mano.
Nonruoti il cappuccio dell’ago.
Getti il cappuccio dell’ago in un contenitore per
oggetti taglienti approvato.
Cappuccio dell’ago
- Nontocchi l’ago o il corpo dello stantuffo.
- Nonlasci che l’ago tocchi alcuna superficie una volta tolto il cappuccio.
- Nonusi la siringa se la fa cadere dopo avere tolto il cappuccio o se l’ago appare danneggiato.
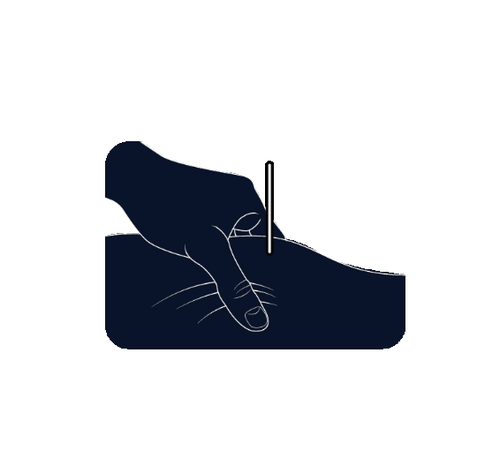
Sito di iniezione
Senza toccare il sito di iniezione pulito, stringa
saldamente la pelle circostante tra il pollice e le
dita, creando una zona di circa 5 cm di
grandezza.
OPPURE
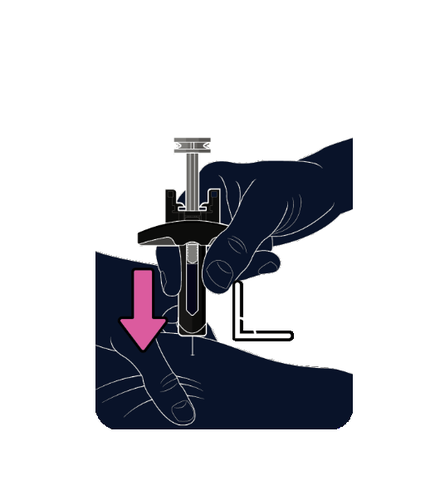
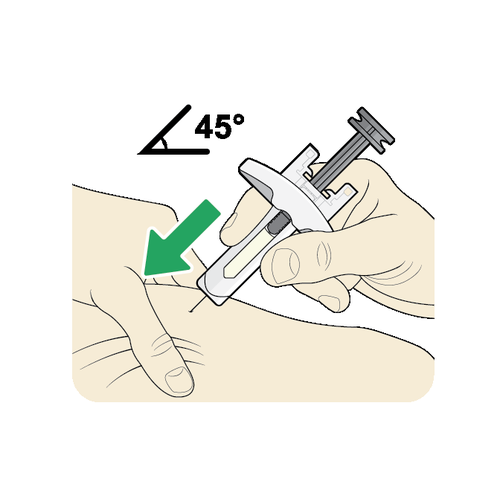
Tenga la siringa tra il pollice e l’indice della mano dominante.
L’ago deve essere inserito nella pelle a un angolo di 45° o di 90°.
L’operatore sanitario le indicherà quale angolo utilizzare.
Usi un movimento rapido, come per lanciare una freccetta, per inserire l’ago nella pelle che tiene
tra le dita.
Nonspinga lo stantuffo quando inserisce l’ago.
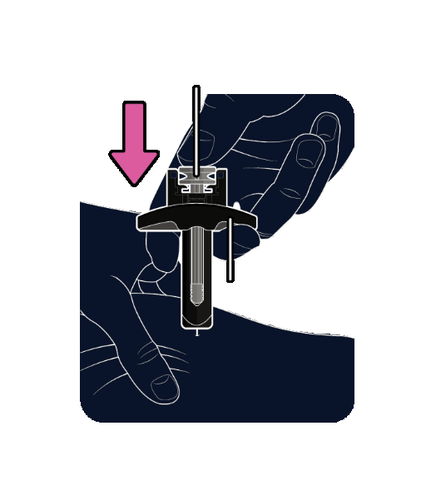
Corpo dello stantuffo
Quando l’ago è inserito non lo muova.
Continui a tenere la pelle tra le dita.
Afferri l’ impugnatura per le ditacon una
mano e prema lentamente e continuamenteil
corpo dello stantuffofino a quando la siringa è
vuota.
Nonrimuova ancora l’ago.
Impugnatura per le dita
Dopo avere somministrato la dose completa, tenga la siringa allo stesso angolo dell’iniezioneed
estragga delicatamente la siringa.
Noninclini la siringa quando la estrae.
Nonmassaggi il sito di iniezione.
Lasci andare la pelle che teneva tra le dita.
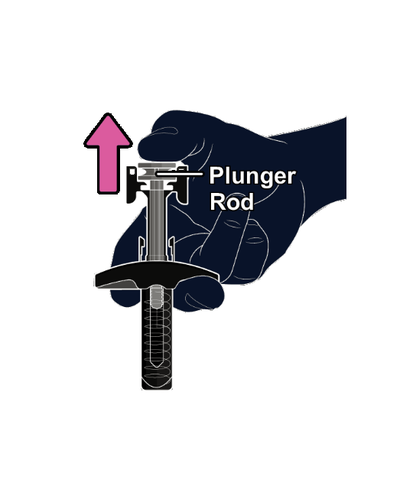
Rilasci il corpo dello stantuffo. Il dispositivo di
protezione si attiva e copre l’ago.
Per evitare lesioni, nonrimetta il cappuccio
sull’ago.
Nontocchi l’ago eventualmente esposto.
Corpo dello
stantuffo
In caso di sanguinamento, prema un batuffolo di cotone o una garza sul sito di iniezione per alcuni
secondi.
Fase 4. Dopo ogni iniezione
Getti i cappucci e le siringhe usati nel contenitore per lo smaltimento di oggetti taglienti.
Nongetti le siringhe nei rifiuti domestici.
Quando il contenitore per oggetti taglienti è quasi pieno, segua le linee guida locali per richiedere un
altro contenitore e per smaltirlo correttamente.
Promemoria:se effettua più di un’iniezione, ripeta le Fasi da 2 a 4 per ogni iniezione.
Usi nuovi materiali per ogni iniezione.
Annoti la data dell’iniezione e tutte le zone in cui ha praticato l’iniezione, in modo da usare, se
possibile, un sito diverso per l’iniezione successiva.
-

- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile, 10 MG
- Codice ATCM05BX05
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a CRYSVITAForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 105 MGPrincipio attivo: romosozumabProduttore: UCB PHARMA S.A.Prescrizione richiestaForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 60 mg/mLPrincipio attivo: denosumabProduttore: MABXIENCE RESEARCH SLPrescrizione richiestaForma farmaceutica: Soluzione iniettabile in siringa pre-riempita, 60 mg/mLPrincipio attivo: denosumabProduttore: SANDOZ GMBHPrescrizione richiesta
Medici online per CRYSVITA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di CRYSVITA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per CRYSVITA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.









