
Come usare BEOVU
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
Beovu 120 mg/ml soluzione iniettabile in siringa preriempita
brolucizumab
Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Beovu e a cosa serve
- 2. Cosa deve sapere prima che le venga somministrato Beovu
- 3. Come le verrà somministrato Beovu
- 4. Possibili effetti indesiderati
- 5. Come conservare Beovu
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Beovu e a cosa serve
Cos’è Beovu
Beovu contiene il principio attivo brolucizumab, che appartiene a un gruppo di medicinali chiamati
agenti antineovascolarizzazione. Beovu viene iniettato nell’occhio dal medico per curare disturbi
dell’occhio che possono influire sulla vista.
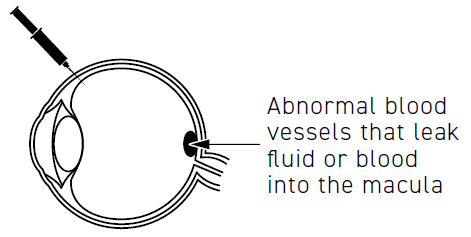
Vasi sanguigni anormali
che lasciano fuoriuscire
liquido o sangue nella
macula
A cosa serve Beovu
Beovu è usato negli adulti per trattare disturbi dell’occhio che si verificano quando vasi sanguigni
anormali si formano e crescono sotto la macula. La macula, che si trova nella parte posteriore
dell’occhio, è responsabile di una visione chiara. I vasi sanguigni anormali possono perdere liquidi o
sangue nell’occhio e interferire con la funzione della macula, con conseguenti malattie che possono
causare riduzione della vista quali:
- degenerazione maculare neovascolare (umida) correlata all’età (AMD)
- edema maculare diabetico (DME).
Come funziona Beovu
Beovu può rallentare la progressione della malattia e quindi mantenere, o anche migliorare, la visione.
2. Cosa deve sapere prima che le venga somministrato Beovu
Non deve ricevere Beovu:
- se è allergico a brolucizumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6);
- se ha un’infezione attiva o sospetta nell’occhio o nella zona circostante;
- se ha dolore o rossore nell’occhio (infiammazione dell’occhio). Se una di queste condizioni si applica al suo caso, informi il medico. Non deve ricevere Beovu.
Avvertenze e precauzioni
Si rivolga al medico prima che le venga somministrato Beovu se si verifica una delle seguenti
condizioni:
- se ha il glaucoma (una condizione dell’occhio generalmente causata da pressione alta nell’occhio);
- se in passato ha percepito lampi di luce o mosche volanti (punti neri volanti) e se ha un improvviso aumento delle dimensioni e del numero di mosche volanti;
- se ha subito un intervento chirurgico agli occhi nelle ultime 4 settimane o se è previsto un intervento chirurgico agli occhi nelle prossime quattro settimane;
- se ha mai avuto malattie degli occhi o trattamenti per gli occhi;
- se nell’ultimo anno ha avuto un’improvvisa perdita della vista dovuta al blocco dei vasi sanguigni nella parte posteriore dell'occhio (occlusione vascolare retinica) o infiammazione dei vasi sanguigni nella parte posteriore dell'occhio (vasculite retinica).
Informi immediatamente il medicose:
- manifesta arrossamento degli occhi, dolore agli occhi, aumento del fastidio, peggioramento del rossore agli occhi, visione offuscata o ridotta, aumento del numero di piccole particelle nella visione, aumento della sensibilità alla luce;
- sviluppa un’improvvisa perdita della vista, che può essere un segno di occlusione vascolare retinica. Uno qualsiasi dei suddetti sintomi può portare il medico a interrompere il trattamento con Beovu.
Inoltre è importante sapere che:
- la sicurezza e l’efficacia di Beovu quando somministrato in entrambi gli occhi contemporaneamente non sono state studiate e l’utilizzo in questo modo può portare ad un maggiore rischio di manifestare effetti indesiderati;
- le iniezioni di Beovu possono causare un aumento della pressione oculare (pressione intraoculare) in alcuni pazienti entro 30 minuti dall’iniezione. Il medico la monitorerà dopo ogni iniezione;
- il medico verificherà se sono presenti altri fattori di rischio che possono aumentare la possibilità di lacrimazione o distacco di uno degli strati nella parte posteriore dell’occhio (distacco o lacerazione della retina, e distacco o lacerazione dell’epitelio pigmentato retinico), nel qual caso Beovu deve essere somministrato con cautela.
L’uso sistemico di inibitori del VEGF, sostanze simili a quelle contenute in Beovu, è potenzialmente
correlato al rischio di coaguli di sangue che bloccano i vasi sanguigni (eventi tromboembolici
arteriosi) che possono causare infarto o ictus. Esiste un rischio teorico che tali eventi si verifichino
dopo l’iniezione di Beovu nell’occhio.
Bambini e adolescenti
Beovu non è usato nei bambini e negli adolescenti sotto i 18 anni di età.
Altri medicinali e Beovu
Informi il medico se sta assumendo, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico prima che le venga somministrato questo medicinale.
L’allattamento non è raccomandato durante il trattamento con Beovu e per almeno un mese dopo
l’interruzione del trattamento con il medicinale poiché non è noto se Beovu sia escreto nel latte
umano.
Le donne in età fertile devono usare un metodo contraccettivo efficace durante il trattamento e per
almeno un mese dopo l’interruzione del trattamento con Beovu. Se è in corso una gravidanza o
sospetta una gravidanza durante il trattamento, ne parli immediatamente con il medico. Beovu non
deve essere usato in gravidanza a meno che il potenziale beneficio non superi il potenziale rischio per
il feto.
Guida di veicoli e utilizzo di macchinari
Dopo il trattamento con Beovu, può riscontrare alcuni problemi di visione temporanei (per esempio
visione offuscata). Non guidi e non usi macchinari fino a quando questa condizione non si sarà risolta.
Beovu contiene sodio
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per dose, per cui è essenzialmente
“senza sodio”.
Beovu contiene polisorbati
Questo medicinale contiene 0,01 mg di polisorbato 80 per ogni dose (0,05 ml). I polisorbati possono
provocare reazioni allergiche. Informi il medico se ha allergie note.
3. Come le verrà somministrato Beovu
Quanto Beovu viene somministrato e per quanto tempo
La dose raccomandata è 6 mg di brolucizumab.
AMD umida
Trattamento iniziale (chiamato anche trattamento loading)
- Le verrà somministrata un’iniezione ogni mese per i primi 3 mesi.
- In alternativa, può essere trattato con un'iniezione ogni 6 settimane per le prime due dosi. Il medico deciderà se è necessaria una terza iniezione 12 settimane dopo l'inizio del trattamento in base alle condizioni del/i suo/i occhio/i. Trattamento di mantenimento
- Successivamente, può ricevere un’iniezione ogni 3 mesi. Il medico determinerà l’intervallo di trattamento in base alle condizioni dell’occhio; alcuni pazienti possono aver bisogno del trattamento ogni 2 mesi. Sulla base delle condizioni dell’occhio, il medico potrebbe prolungare o abbreviare l’intervallo di trattamento di non più di 1 mese alla volta. I dati sugli intervalli di trattamento superiori a 5 mesi sono limitati. L’intervallo di trattamento tra due dosi di Beovu non deve essere inferiore a 2 mesi.
TRATTAMENTO INIZIALE
(CHIAMATO ANCHE TRATTAMENTO
TRATTAMENTO DI
MANTENIMENTO
LOADING)
3 DOSI,
2 DOSI,
UNA OGNIUNA OGNIUNA OGNI
OPPURE
6
SETTIMANESETTIMANESETTIMANE
DME
- Le verrà somministrata un’iniezione ogni sei settimane per le prime cinque iniezioni.
- Successivamente, può ricevere un’iniezione ogni 3 mesi. Il medico determinerà l’intervallo di trattamento in base alla condizioni dell’occhio. Alcuni pazienti possono aver bisogno del trattamento ogni 2 mesi. Alcuni pazienti possono ricevere il trattamento ogni 4 mesi. Prime 5 dosi,
Successivamente,
una ogni
una ogni

settimanesettimane
Per le prime 5 dosi,Successivamente, 1 iniezione ogni
1 iniezione ogni12 settimane (3 mesi) o come
6 settimaneraccomandato dal medico
Modo di somministrazione
Beovu è somministrato da un oculista mediante iniezione nell’occhio (uso intravitreale).
Prima dell’iniezione, il medico pulirà accuratamente l’occhio, per prevenire un’infezione. Il medico le
darà anche un collirio (anestetico locale) per intorpidire l’occhio e ridurre o prevenire il dolore da
iniezione.
Quanto dura il trattamento con Beovu
Beovu è usato per trattare malattie croniche dell’occhio che richiedono un trattamento a lungo termine,
che può protrarsi per mesi o anni. Il medico verificherà che il trattamento stia funzionando durante le
regolari visite programmate. Il medico può anche controllare gli occhi nel tempo che intercorre tra le
iniezioni. Se ha domande su quanto durerà il trattamento con Beovu, si rivolga al medico.
Prima di interrompere il trattamento con Beovu
Parli con il medico prima di interrompere il trattamento. L’interruzione del trattamento può aumentare
il rischio di perdita della vista e la vista può peggiorare.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino. Gli effetti indesiderati a seguito di iniezione di Beovu sono dovuti sia al medicinale
stesso sia alla procedura d’iniezione e per la maggior parte interessano l’occhio.
Alcuni effetti indesiderati possono essere gravi
Consulti immediatamente un medico se si verifica una delle seguenti condizioni, che sono segni di
reazioni allergiche, infiammazioni o infezioni:
- una diminuzione improvvisa o una variazione della visione
- dolore, aumento del fastidio, peggioramento dell’arrossamento dell’occhio
Se si manifesta un qualsiasi effetto indesiderato, si rivolga immediatamente al medico.
Altri possibili effetti indesiderati
Altri effetti indesiderati che possono verificarsi dopo il trattamento con Beovu includono quelli
elencati di seguito.
La maggior parte degli effetti indesiderati sono lievi o moderati e generalmente scompaiono entro una
settimana dopo ogni iniezione.
Se questi effetti indesiderati diventano gravi, informi il medico.
Comune:può manifestarsi fino a 1 persona su 10
- infiammazione dello strato intermedio della parete dell’occhio (uveite)
- distacco della sostanza gelatinosa all’interno dell’occhio (distacco del vitreo)
- lacerazione della retina (la parte dietro l’occhio che rileva la luce) o di uno dei suoi strati (lacerazione epiteliale del pigmento retinico)
- riduzione della nitidezza visiva (riduzione dell’acuità visiva)
- sanguinamento nella retina (emorragia retinica)
- infiammazione dell’iride, la parte colorata dell’occhio (irite)
- infiammazione dell’iride e del tessuto adiacente dell’occhio (iridociclite)
- improvvisa perdita della vista a causa del blocco dei vasi sanguigni nella parte posteriore dell’occhio (occlusione vascolare della retina)
- sanguinamento nell’occhio (emorragia vitreale)
- opacizzazione del cristallino dell’occhio (cataratta)
- sanguinamento da piccoli vasi sanguigni nello strato esterno dell’occhio (emorragia della congiuntiva)
- corpi mobili nella visione (corpi mobili nel vitreo)
- dolore all’occhio
- pressione nell’occhio aumentata (pressione endoculare aumentata)
- arrossamento nella parte bianca dell’occhio (congiuntivite)
- visione offuscata o poco chiara
- cornea graffiata, danno allo strato trasparente del bulbo oculare che ricopre l’iride (abrasione corneale)
- danno allo strato trasparente del bulbo oculare che ricopre l’iride (cheratite puntata)
- reazioni allergiche (ipersensibilità)
Non comune:può manifestarsi fino a 1 persona su 100
- grave infiammazione all’interno dell’occhio (endoftalmite)
- cecità
- improvvisa perdita della vista dovuta al blocco di un’arteria nell’occhio (occlusione dell’arteria retinica)
- distacco della retina (distacco retinico)
- arrossamento dell’occhio (iperemia congiuntivale)
- aumento della produzione di lacrime (lacrimazione aumentata)
- sensazione anormale nell’occhio
- distacco di uno degli strati della retina (distacco dell’epitelio pigmentato retinico)
- infiammazione della sostanza gelatinosa all’interno dell’occhio (vitreite)
- infiammazione della parte anteriore dell’occhio (infiammazione della camera anteriore o flare)
- gonfiore della cornea, lo strato trasparente del bulbo oculare (edema corneale)
- infiammazione dei vasi sanguigni nella parte posteriore dell’occhio (vasculite retinica)
- infiammazione del rivestimento esterno bianco dell’occhio (sclerite)
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema nazionale di
segnalazione riportato nell’ allegato V . Segnalando gli effetti indesiderati può contribuire a fornire
maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Beovu
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola e sull’etichetta dopo
Scad./EXP. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2°C - 8°C).
Non congelare.
Tenere la siringa preriempita nel suo blister sigillato e nell’imballaggio esterno per proteggere il
medicinale dalla luce.
Prima dell’uso, il blister non aperto con la siringa preriempita può essere mantenuto a temperatura
ambiente (inferiore a 25°C) per un massimo di 24 ore.
6. Contenuto della confezione e altre informazioni
Cosa contiene Beovu
- Il principio attivo è brolucizumab. Un ml di soluzione iniettabile contiene 120 mg di brolucizumab. Ogni siringa preriempita contiene 19,8 mg di brolucizumab in 0,165 ml di soluzione. Questo fornisce una quantità utile alla somministrazione di una dose singola di 0,05 ml di soluzione contenente 6 mg di brolucizumab.
- Gli altri componenti sono: sodio citrato, saccarosio, polisorbato 80, acqua per preparazioni iniettabili (vedere paragrafo 2).
Descrizione dell’aspetto di Beovu e contenuto della confezione
Beovu 120 mg/ml soluzione iniettabile in siringa preriempita (preparazione iniettabile) è una soluzione
acquosa da limpida a leggermente opalescente, da incolore a leggermente gialla-brunastra.
Confezione con 1 siringa preriempita esclusivamente monouso.
Titolare dell’autorizzazione all’immissione in commercio
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlanda
Produttore
S.A. ALCON-COUVREUR N.V.
Rijksweg 14
2870 Puurs
Belgio
Novartis Pharma GmbH
Roonstraße 25
90429 Norimberga
Germania
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Lietuva
SIA Novartis Baltics Lietuvos filialas
Tel: +370 5 269 16 50
България
Novartis Bulgaria EOOD
Тел.: +359 2 489 98 28
Luxembourg/Luxemburg
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Česká republika
Novartis s.r.o.
Tel: +420 225 775 111
Magyarország
Novartis Hungária Kft.
Tel.: +36 1 457 65 00
Danmark
Novartis Healthcare A/S
Tlf.: +45 39 16 84 00
Malta
Novartis Pharma Services Inc.
Tel: +356 2122 2872
Deutschland
Novartis Pharma GmbH
Tel: +49 911 273 0
Nederland
Novartis Pharma B.V.
Tel: +31 88 04 52 111
Eesti
SIA Novartis Baltics Eesti filiaal
Tel: +372 66 30 810
Norge
Novartis Norge AS
Tlf: +47 23 05 20 00
Ελλάδα
Novartis (Hellas) A.E.B.E.
Τηλ: +30 210 281 17 12
Österreich
Novartis Pharma GmbH
Tel: +43 1 86 6570
España
Novartis Farmacéutica, S.A.
Tel: +34 93 306 42 00
Polska
Novartis Poland Sp. z o.o.
Tel.: +48 22 375 4888
France
Novartis Pharma S.A.S.
Tél: +33 1 55 47 66 00
Portugal
Novartis Farma - Produtos Farmacêuticos, S.A.
Tel: +351 21 000 8600
Hrvatska
Novartis Hrvatska d.o.o.
Tel. +385 1 6274 220
România
Novartis Pharma Services Romania SRL
Tel: +40 21 31299 01
Ireland
Novartis Ireland Limited
Tel: +353 1 260 12 55
Slovenija
Novartis Pharma Services Inc.
Tel: +386 1 300 75 50
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
Novartis Slovakia s.r.o.
Tel: +421 2 5542 5439
Italia
Novartis Farma S.p.A.
Tel: +39 02 96 54 1
Suomi/Finland
Novartis Finland Oy
Puh/Tel: +358 (0)10 6133 200
Κύπρος
Novartis Pharma Services Inc.
Τηλ: +357 22 690 690
Sverige
Novartis Sverige AB
Tel: +46 8 732 32 00
Latvija
SIA Novartis Baltics
Tel: +371 67 887 070
United Kingdom (Northern Ireland)
Novartis Ireland Limited
Tel: +44 1276 698370
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, https://www.ema.europa.eu.
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Istruzioni per l’uso della siringa preriempita
Conservazione e ispezione visiva
Conservare Beovu in frigorifero (2°C - 8°C). Non congelare. Tenere
la siringa preriempita nel suo blister sigillato e nell’imballaggio
esterno per proteggere il medicinale dalla luce.
Prima dell’uso, il blister non aperto con la siringa preriempita di
Beovu deve essere tenuto a temperatura ambiente (inferiore a 25°C)
per un massimo di 24 ore. Accertarsi che il confezionamento
contenga una siringa preriempita nel suo blister sigillato. Dopo
l’apertura del blister, procedere in condizioni di asepsi.


Beovu è una soluzione acquosa da limpida a leggermente
opalescente, da incolore a leggermente gialla-brunastra.
La soluzione deve essere ispezionata visivamente dopo essere stata
tolta dal frigorifero e prima della somministrazione. Se sono visibili
particelle o torbidità, la siringa preriempita non deve essere usata e
seguirà un’appropriata procedura di sostituzione.
La siringa preriempita è sterile e monouso. Non usare se il
confezionamento o la siringa preriempita sono danneggiati o scaduti.
Come preparare e somministrare Beovu
La siringa preriempita contiene più della dose raccomandata di 6 mg. Il volume estraibile della siringa
preriempita (0,165 ml) non deve essere utilizzato completamente. Il volume in eccesso deve essere
eliminato prima di procedere all’iniezione. L’i niezione dell'intero volume della siringa preriempita può
provocare sovradosaggio.
La procedura per l’iniezione intravitreale deve essere effettuata in condizioni asettiche, che includono la
disinfezione chirurgica delle mani l’uso di guanti sterili, di un telino sterile e di un blefarostato sterile (o
equivalente), oltre ad avere a disposizione l’attrezzatura per paracentesi sterile (se necessaria).
Prima dell’iniezione devono essere somministrati un’anestesia adeguata ed un antimicrobico topico ad
ampio spettro per disinfettare la superficie perioculare, oculare e palpebrale.
Per l’iniezione intravitreale, deve essere usato un ago sterile per iniezione da 30G x ½″. L’ago per
iniezione non è incluso nella confezione di Beovu.
Assicurarsi che l’iniezione venga somministrata subito dopo la preparazione della dose (passaggio 5).
Nota: La dose deve essere impostata a 0,05 ml.
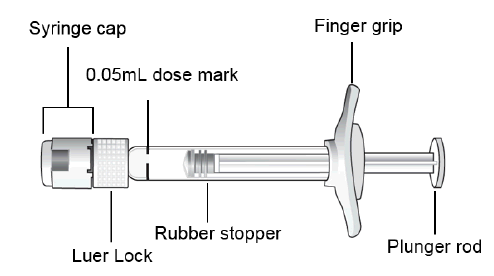
Procedura per l’iniezione
| e Sollevare il coperchio del blister della siringa e, in asepsi, rimuovere la siringa. |
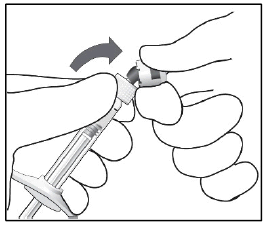 | d Staccare (non girare o ruotare) il cappuccio della siringa. a n a i l |
| a In asepsi e con forza inserire l’ago per iniezione da 30G x ½″ sulla siringa. |
t
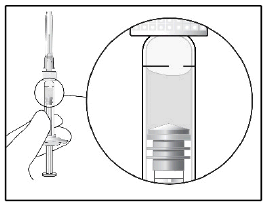 | Controllare le bolle d’aria, tenendo la siringa con l’ago verso l’alto. Se ci sono alcune bolle d’aria, picchiettare delicatamente la siringa con il dito fino a farle salire in superficie. Rimuovere attentamente il cappuccio dell’ago tirandolo. |
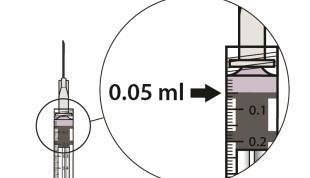
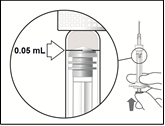 | Tenere la siringa a livello degli occhi e spingere delicatamente lo stantuffo finché il bordo inferiore della o cupola del tappo di gomma non sarà allineato alla linea di misurazione di 0,05 ml. Questo espellerà l'aria e la soluzione c in eccesso ed aggiusterà la dose a 0,05 ml. La siringa è pronta per l’iniezione. a |
| m Iniettare lentamente fino a che il tappo di gomma non arriverà sul fondo della siringa per raggiungere il volume iniettato di 0,05 ml. Accertarsi di iniettare l’intera dose controllando che r il tappo di gomma abbia raggiunto la fine del corpo della siringa. |
Nota: il materiale inutilizzato o quello di scarto deve essere smaltito in conformità alla normativa
locale vigente .
Domande e risposte comuni
D: Cosa fare se non riesco a rimuovere le bolle d’aria dal liquido?
R: È importante che il liquido sia privo di aria. Tuttavia, minuscole bolle d’aria che sono attaccate al
tappo normalmente non si staccano dal tappo durante l’iniezione e perciò non influenzano il volume
della dose.
Beovu 120 mg/ml soluzione iniettabile
brolucizumab
Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico. Vedere paragrafo 4.
Contenuto di questo foglio
- 1. Cos’è Beovu e a cosa serve
- 2. Cosa deve sapere prima che le venga somministrato Beovu
- 3. Come le verrà somministrato Beovu
- 4. Possibili effetti indesiderati
- 5. Come conservare Beovu
- 6. Contenuto della confezione e altre informazioni
1. Cos’è Beovu e a cosa serve
Cos’è Beovu
Beovu contiene il principio attivo brolucizumab, che appartiene a un gruppo di medicinali chiamati
agenti antineovascolarizzazione. Beovu viene iniettato nell’occhio dal medico per curare disturbi
dell’occhio che possono influire sulla vista.
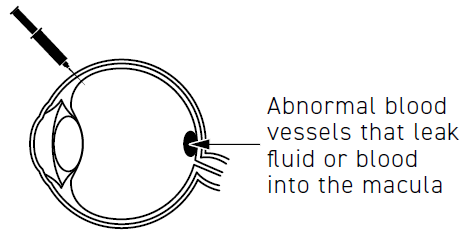
Vasi sanguigni anormali
che lasciano fuoriuscire
liquido o sangue nella
macula
A cosa serve Beovu
Beovu è usato negli adulti per trattare disturbi dell’occhio che si verificano quando vasi sanguigni
anormali si formano e crescono sotto la macula. La macula, che si trova nella parte posteriore
dell’occhio, è responsabile di una visione chiara. I vasi sanguigni anormali possono perdere liquidi o
sangue nell’occhio e interferire con la funzione della macula, con conseguenti malattie che possono
causare riduzione della vista quali:
- degenerazione maculare neovascolare (umida) correlata all’età (AMD)
- edema maculare diabetico (DME).
Come funziona Beovu
Beovu può rallentare la progressione della malattia e quindi mantenere, o anche migliorare, la visione.
2. Cosa deve sapere prima che le venga somministrato Beovu
Non deve ricevere Beovu:
- se è allergico a brolucizumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati al paragrafo 6).
- se ha un’infezione attiva o sospetta nell’occhio o nella zona circostante.
- se ha dolore o rossore nell’occhio (infiammazione dell’occhio). Se una di queste condizioni si applica al suo caso, informi il medico. Non deve ricevere Beovu.
Avvertenze e precauzioni
Si rivolga al medico prima che le venga somministrato Beovu se si verifica una delle seguenti
condizioni:
- se ha il glaucoma (una condizione dell’occhio generalmente causata da pressione alta nell’occhio);
- se in passato ha percepito lampi di luce o mosche volanti (punti neri volanti) e se ha un improvviso aumento delle dimensioni e del numero di mosche volanti;
- se ha subito un intervento chirurgico agli occhi nelle ultime 4 settimane o se è previsto un intervento chirurgico agli occhi nelle prossime quattro settimane;
- se ha mai avuto malattie degli occhi o trattamenti per gli occhi;
- se nell’ultimo anno ha avuto un’improvvisa perdita della vista dovuta al blocco dei vasi sanguigni nella parte posteriore dell'occhio (occlusione vascolare retinica) o infiammazione dei vasi sanguigni nella parte posteriore dell'occhio (vasculite retinica).
Informi immediatamente il medicose:
- manifesta arrossamento degli occhi, dolore agli occhi, aumento del fastidio, peggioramento del rossore agli occhi, visione offuscata o ridotta, aumento del numero di piccole particelle nella visione, aumento della sensibilità alla luce;
- sviluppa un’improvvisa perdita della vista, che può essere un segno di occlusione vascolare retinica. Uno qualsiasi dei suddetti sintomi può portare il medico a interrompere il trattamento con Beovu.
Inoltre è importante sapere che:
- la sicurezza ed efficacia di Beovu quando somministrato in entrambi gli occhi contemporaneamente non sono state studiate e l’utilizzo in questo modo può portare ad un maggiore rischio di manifestare effetti indesiderati;
- le iniezioni di Beovu possono causare un aumento della pressione oculare (pressione intraoculare) in alcuni pazienti entro 30 minuti dall’iniezione. Il medico la monitorerà dopo ogni iniezione;
- il medico verificherà se sono presenti altri fattori di rischio che possono aumentare la possibilità di lacrimazione o distacco di uno degli strati nella parte posteriore dell’occhio (distacco o lacerazione della retina, e distacco o lacerazione dell’epitelio pigmentato retinico), nel qual caso Beovu deve essere somministrato con cautela.
L’uso sistemico di inibitori del VEGF, sostanze simili a quelle contenute in Beovu, è potenzialmente
correlato al rischio di coaguli di sangue che bloccano i vasi sanguigni (eventi tromboembolici
arteriosi) che possono causare infarto o ictus. Esiste un rischio teorico che tali eventi si verifichino
dopo l’iniezione di Beovu nell’occhio.
Bambini e adolescenti
Beovu non è usato nei bambini e negli adolescenti sotto i 18 anni di età.
Altri medicinali e Beovu
Informi il medico se sta assumendo, ha recentemente assunto o potrebbe assumere qualsiasi altro
medicinale.
Gravidanza e allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza o se sta allattando con latte
materno chieda consiglio al medico prima che le venga somministrato questo medicinale.
L’allattamento non è raccomandato durante il trattamento con Beovu e per almeno un mese dopo
l’interruzione del trattamento con il medicinale poiché non è noto se Beovu sia escreto nel latte
umano.
Le donne in età fertile devono usare un metodo contraccettivo efficace durante il trattamento e per
almeno un mese dopo l’interruzione del trattamento con Beovu. Se è in corso una gravidanza o
sospetta una gravidanza durante il trattamento, ne parli immediatamente con il medico. Beovu non
deve essere usato in gravidanza a meno che il potenziale beneficio non superi il potenziale rischio per
il feto.
Guida di veicoli e utilizzo di macchinari
Dopo il trattamento con Beovu, può riscontrare alcuni problemi di visione temporanei (per esempio
visione offuscata). Non guidi e non usi macchinari fino a quando questa condizione non si sarà risolta.
Beovu contiene sodio
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per dose, per cui è essenzialmente
“senza sodio”.
Beovu contiene polisorbati
Questo medicinale contiene 0,01 mg di polisorbato 80 per ogni dose (0,05 ml). I polisorbati possono
provocare reazioni allergiche. Informi il medico se ha allergie note.
3. Come le verrà somministrato Beovu
Quanto Beovu viene somministrato e per quanto tempo
La dose raccomandata è 6 mg di brolucizumab.
AMD umida
Trattamento iniziale (chiamato anche trattamento loading)
- Le verrà somministrata un’iniezione ogni mese per i primi 3 mesi.
- In alternativa, può essere trattato con un'iniezione ogni 6 settimane per le prime due dosi. Il medico deciderà se è necessaria una terza iniezione 12 settimane dopo l'inizio del trattamento in base alle condizioni del/i suo/i occhio/i. Trattamento di mantenimento
- Successivamente, può ricevere un’iniezione ogni 3 mesi. Il medico determinerà l’intervallo di trattamento in base alle condizioni dell’occhio; alcuni pazienti possono aver bisogno del trattamento ogni 2 mesi. Sulla base delle condizioni dell’occhio, il medico potrebbe prolungare o abbreviare l’intervallo di trattamento di non più di 1 mese alla volta. I dati sugli intervalli di trattamento superiori a 5 mesi sono limitati. L’intervallo di trattamento tra due dosi di Beovu non deve essere inferiore a 2 mesi.
TRATTAMENTO INIZIALE
(CHIAMATO ANCHE TRATTAMENTO
TRATTAMENTO DI
MANTENIMENTO
LOADING)
3 DOSI,
2 DOSI,
UNA OGNIUNA OGNIUNA OGNI
OPPURE
6
SETTIMANESETTIMANESETTIMANE
DME
- Le verrà somministrata un’iniezione ogni sei settimane per le prime cinque iniezioni.
- Successivamente, può ricevere un’iniezione ogni 3 mesi. Il medico determinerà l’intervallo di trattamento in base alle condizioni dell’occhio Alcuni pazienti possono aver bisogno del trattamento ogni 2 mesi. Alcuni pazienti possono ricevere il trattamento ogni 4 mesi. Prime 5 dosi,
Successivamente,
una ogni
una ogni

settimanesettimane
Per le prime 5 dosi,Successivamente, 1 iniezione ogni
1 iniezione ogni12 settimane (3 mesi) o come
6 settimaneraccomandato dal medico
Modo di somministrazione
Beovu è somministrato da un oculista mediante iniezione nell’occhio (uso intravitreale).
Prima dell’iniezione, il medico pulirà accuratamente l’occhio, per prevenire un’infezione. Il medico le
darà anche un collirio (anestetico locale) per intorpidire l’occhio e ridurre o prevenire il dolore da
iniezione.
Quanto dura il trattamento con Beovu
Beovu è usato per trattare malattie croniche dell’occhio che richiedono un trattamento a lungo termine,
che può protrarsi per mesi o anni. Il medico verificherà che il trattamento stia funzionando durante le
regolari visite programmate. Il medico può anche controllare gli occhi nel tempo che intercorre tra le
iniezioni. Se ha domande su quanto durerà il trattamento con Beovu, si rivolga al medico.
Prima di interrompere il trattamento con Beovu
Parli con il medico prima di interrompere il trattamento. L’interruzione del trattamento può aumentare
il rischio di perdita della vista e la vista può peggiorare.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le persone
li manifestino. Gli effetti indesiderati a seguito di iniezione di Beovu sono dovuti sia al medicinale
stesso sia alla procedura d’iniezione e per la maggior parte interessano l’occhio.
Alcuni effetti indesiderati possono essere gravi
Consulti immediatamente un medico se si verifica una delle seguenti condizioni, che sono segni di
reazioni allergiche, infiammazioni o infezioni:
- una diminuzione improvvisa o una variazione della visione
- dolore, aumento del fastidio, peggioramento dell’arrossamento dell’occhio
Se si manifesta un qualsiasi effetto indesiderato, si rivolga immediatamente al medico.
Altri possibili effetti indesiderati
Altri effetti indesiderati che possono verificarsi dopo il trattamento con Beovu includono quelli
elencati di seguito.
La maggior parte degli effetti indesiderati sono lievi o moderati e generalmente scompaiono entro una
settimana dopo ogni iniezione.
Se questi effetti indesiderati diventano gravi, informi il medico.
Comune:può manifestarsi fino a 1 persona su 10
- infiammazione dello strato intermedio della parete dell’occhio (uveite)
- distacco della sostanza gelatinosa all’interno dell’occhio (distacco del vitreo)
- lacerazione della retina (la parte dietro l’occhio che rileva la luce) o di uno dei suoi strati (lacerazione epiteliale del pigmento retinico)
- riduzione della nitidezza della visiva (riduzione dell’acuità visiva)
- sanguinamento nella retina (emorragia retinica)
- infiammazione dell’iride, la parte colorata dell’occhio (irite)
- infiammazione dell’iride e del tessuto adiacente dell’occhio (iridociclite)
- improvvisa perdita della vista a causa del blocco dei vasi sanguigni nella parte posteriore dell'occhio (occlusione vascolare della retina)
- sanguinamento nell’occhio (emorragia vitreale)
- opacizzazione del cristallino dell’occhio (cataratta)
- sanguinamento da piccoli vasi sanguigni nello strato esterno dell’occhio (emorragia della congiuntiva)
- corpi mobili nella visione (corpi mobili nel vitreo)
- dolore all’occhio
- pressione dell’occhio aumentata (pressione endoculare aumentata)
- arrossamento nella parte bianca dell’occhio (congiuntivite)
- visione offuscata o poco chiara
- cornea graffiata, danno allo strato trasparente del bulbo oculare che ricopre l’iride (abrasione corneale)
- danno allo strato trasparente del bulbo oculare che ricopre l’iride (cheratite puntata)
- reazioni allergiche (ipersensibilità)
Non comune:può manifestarsi fino a 1 persona su 100
- grave infiammazione all’interno dell’occhio (endoftalmite)
- cecità
- improvvisa perdita della vista dovuta al blocco di un’arteria nell’occhio (occlusione dell’arteria retinica)
- distacco della retina (distacco retinico)
- arrossamento dell’occhio (iperemia congiuntivale)
- aumento della produzione di lacrime (lacrimazione aumentata)
- sensazione anormale nell’occhio
- distacco di uno degli strati della retina (distacco dell’epitelio pigmentato retinico)
- infiammazione della sostanza gelatinosa all’interno dell’occhio (vitreite)
- infiammazione della parte anteriore dell’occhio (infiammazione della camera anteriore o flare)
- gonfiore della cornea, lo strato trasparente del bulbo oculare (edema corneale)
- infiammazione dei vasi sanguigni nella parte posteriore dell’occhio (vasculite retinica)
- infiammazione del rivestimento esterno bianco dell’occhio (sclerite)
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico. Può inoltre segnalare gli effetti indesiderati direttamente tramite il sistema nazionale di
segnalazione riportato nell’ allegato V. Segnalando gli effetti indesiderati può contribuire a fornire
maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Beovu
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola e sull’etichetta dopo
Scad./EXP. La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2°C - 8°C).
Non congelare.
Tenere il flaconcino nell’imballaggio esterno per proteggere il medicinale dalla luce.
Prima dell’uso, il flaconcino non aperto può essere mantenuto a temperatura ambiente (inferiore a
25°C) per un massimo di 24 ore.
6. Contenuto della confezione e altre informazioni
Cosa contiene Beovu
- Il principio attivo è brolucizumab. Un ml di soluzione iniettabile contiene 120 mg di brolucizumab. Ogni flaconcino contiene 27,6 mg di brolucizumab in 0,23 ml di soluzione. Ciò fornisce una quantità utile alla somministrazione di una dose singola di 0,05 ml di soluzione contenente 6 mg di brolucizumab.
- Gli altri componenti sono: sodio citrato, saccarosio, polisorbato 80, acqua per preparazioni iniettabili (vedere paragrafo 2).
Descrizione dell’aspetto di Beovu e contenuto della confezione
Beovu 120 mg/ml soluzione iniettabile (preparazione iniettabile) è una soluzione acquosa da limpida a
leggermente opalescente, da incolore a leggermente gialla-brunastra.
Confezione con 1 flaconcino e 1 ago filtro smussato (18G x 1½″, 1,2 mm x 40 mm, 5 μm)
esclusivamente monouso.
Titolare dell’autorizzazione all’immissione in commercio
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlanda
Produttore
S.A. ALCON-COUVREUR N.V.
Rijksweg 14
2870 Puurs
Belgio
Novartis Pharma GmbH
Roonstraße 25
90429 Norimberga
Germania
Novartis Farmacéutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcelona
Spagna
Lek Pharmaceuticals d.d.
Verovškova ulica 57
Ljubljana, 1526
Slovenia
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
België/Belgique/Belgien
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Lietuva
SIA Novartis Baltics Lietuvos filialas
Tel: +370 5 269 16 50
България
Novartis Bulgaria EOOD
Тел.: +359 2 489 98 28
Luxembourg/Luxemburg
Novartis Pharma N.V.
Tél/Tel: +32 2 246 16 11
Česká republika
Novartis s.r.o.
Tel: +420 225 775 111
Magyarország
Novartis Hungária Kft.
Tel.: +36 1 457 65 00
Danmark
Novartis Healthcare A/S
Tlf,: +45 39 16 84 00
Malta
Novartis Pharma Services Inc.
Tel: +356 2122 2872
Deutschland
Novartis Pharma GmbH
Tel: +49 911 273 0
Nederland
Novartis Pharma B.V.
Tel: +31 88 04 52 111
Eesti
SIA Novartis Baltics Eesti filiaal
Tel: +372 66 30 810
Norge
Novartis Norge AS
Tlf: +47 23 05 20 00
Ελλάδα
Novartis (Hellas) A.E.B.E.
Τηλ: +30 210 281 17 12
Österreich
Novartis Pharma GmbH
Tel: +43 1 86 6570
España
Novartis Farmacéutica, S.A.
Tel: +34 93 306 42 00
Polska
Novartis Poland Sp. z o.o.
Tel.: +48 22 375 4888
France
Novartis Pharma S.A.S.
Tél: +33 1 55 47 66 00
Portugal
Novartis Farma - Produtos Farmacêuticos, S.A.
Tel: +351 21 000 8600
Hrvatska
Novartis Hrvatska d.o.o.
Tel. +385 1 6274 220
România
Novartis Pharma Services Romania SRL
Tel: +40 21 31299 01
Ireland
Novartis Ireland Limited
Tel: +353 1 260 12 55
Slovenija
Novartis Pharma Services Inc.
Tel: +386 1 300 75 50
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
Novartis Slovakia s.r.o.
Tel: +421 2 5542 5439
Italia
Novartis Farma S.p.A.
Tel: +39 02 96 54 1
Suomi/Finland
Novartis Finland Oy
Puh/Tel: +358 (0)10 6133 200
Κύπρος
Novartis Pharma Services Inc.
Τηλ: +357 22 690 690
Sverige
Novartis Sverige AB
Tel: +46 8 732 32 00
Latvija
SIA Novartis Baltics
Tel: +371 67 887 070
United Kingdom (Northern Ireland)
Novartis Ireland Limited
Tel: +44 1276 698370
Altre fonti d’informazioni
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia europea
per i medicinali, https://www.ema.europa.eu.
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Istruzioni per l’uso del flaconcino
Conservazione e ispezione visiva
Conservare Beovu in frigorifero (2°C - 8°C). Non congelare. Conservare
il flaconcino nell’imballaggio esterno per proteggere il medicinale dalla
luce.

Prima dell’uso, il flaconcino chiuso di Beovu deve essere tenuto a
temperatura ambiente (inferiore a 25°C) per un massimo di 24 ore. Dopo
l’apertura del flaconcino, procedere in condizioni di asepsi.

Beovu è una soluzione acquosa da limpida a leggermente opalescente, da
incolore a leggermente gialla-brunastra.
La soluzione deve essere ispezionata visivamente dopo essere stata tolta
dal frigorifero e prima della somministrazione. Se sono visibili particelle
o torbidità, il flaconcino non deve essere usato e dovrà essere seguita
un’appropriata procedura di sostituzione.
I contenuti del flaconcino e dell’ago filtro sono sterili e monouso. Non
usare se il confezionamento, il flaconcino e/o l’ago filtro sono
danneggiati o scaduti.
Come preparare e somministrare Beovu
Il flaconcino contiene un volume maggiore della dose raccomandata di 6 mg. Il volume estraibile del
flaconcino (0,23 ml) non deve essere usato completamente. Il volume in eccesso deve essere eliminato
prima di procedere all'iniezione. L'iniezione dell'intero volume del flaconcino può provocare
sovradosaggio.
La procedura per l’iniezione intravitreale deve essere effettuata in condizioni asettiche, che includono
la disinfezione chirurgica delle mani, l’uso di guanti sterili, di un telino sterile e di un blefarostato
sterile (o equivalente), oltre ad avere a disposizione l’attrezzatura per effettuare una paracentesi sterile
(se necessaria).
Prima dell’iniezione devono essere somministrati un’anestesia adeguata ed un antimicrobico topico ad
ampio spettro per disinfettare la superficie perioculare, oculare e palpebrale.
Per la preparazione e l’iniezione intravitreale sono necessari i seguenti dispositivi medici monouso:
- un ago sterile per iniezione 30G x ½”.
- una siringa sterile da 1 ml con una linea di misurazione dose da 0,05 ml.
- un ago filtro smussato sterile da 5 μm (18G x 1½”, 1,2 mm x 40 mm).
L’ago per iniezione e la siringa non sono inclusi nella confezione di Beovu.
Assicurarsi che l’iniezione venga somministrata subito dopo la preparazione della dose (passaggio 8).
Nota: La dose deve essere impostata a 0,05 ml.
Procedura per l’iniezione
| c Rimuovere il tappo del flaconcino e pulire il setto del a flaconcino (ad esempio con un tampone di alcol al 70%). m r a |
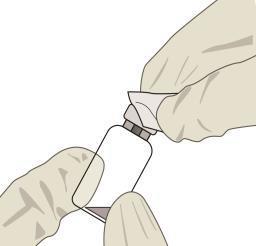 | F Assemblare l’ago filtro sulla siringa da 1 ml in condizioni di asepsi. |
| l Spingere l’ago filtro nel centro del setto del flaconcino fino e a che non toccherà il fondo del flaconcino. |
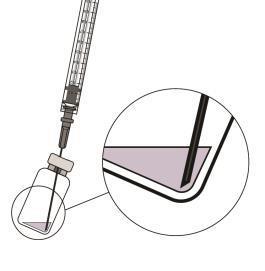 | d Per prelevare il liquido, tenere il flaconcino leggermente inclinato e prelevare lentamente tutto il liquido dal flaconcino e dall’ago filtro. a Assicurarsi che lo stantuffo della siringa sia tirato sufficientemente indietro quando si svuota il flaconcino in n modo da svuotare completamente l’ago filtro. a i l |
t
| a Staccare l’ago filtro dalla siringa in asepsi e smaltirlo. L’ago filtro non deve essere usato per l’iniezione intravitreale. |
I
| In asepsi e con forza inserire l’ago per iniezione da 30G x ½″ sulla siringa. |
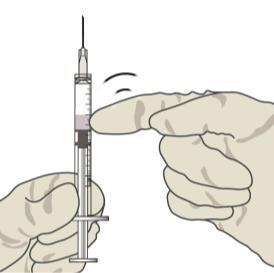 | Controllare le bolle d’aria, tenendo la siringa con l’ago verso l’alto. Se ci sono alcune bolle d’aria, picchiettare o delicatamente la siringa con il dito fino a farle salire in superficie. c a m |
| r a Tenere la siringa all'altezza degli occhi e spingere accuratamente lo stantuffo per espellere l'aria insieme alla F soluzione in eccesso dalla siringa e aggiustare la dose a 0,05 ml contrassegnati sulla siringa. La siringa è pronta per l’iniezione. l |
 | e Iniettare lentamente fino a che il tappo di gomma non d arriverà sul fondo della siringa per raggiungere il volume iniettato di 0,05 ml. Accertarsi di iniettare l’intera dose controllando che il tappo di gomma abbia raggiunto la fine del corpo della siringa. |
Nota: il materiale inutilizzato o quello di scarto deve essere smaltito in conformità alla normativa
locale vigente.
Domande e risposte comuni
D: Cosa fare se ho difficoltà a prelevare sufficiente liquido dal flaconcino?
R: Non scuotere il flaconcino prima del prelievo ma lasciare che il liquido si disponga sul fondo del
flaconcino. Assicurarsi che il flaconcino sia in verticale, in posizione leggermente inclinata. Tirare
indietro lentamentelo stantuffo e attendere che il liquido appaia nel corpo della siringa. Continuare a
prelevare lentamente fino a svuotare completamente il flaconcino e l’ago filtro.
D: Cosa fare se non riesco a rimuovere le bolle d’aria dal liquido?
R: È importante che il liquido sia privo di aria. Tuttavia, minuscole bolle d’aria che sono attaccate al
tappo normalmente non si staccano dal tappo durante l’iniezione e perciò non influenzano il volume
della dose.
-

- Paese di registrazione
- Forma farmaceuticaSoluzione iniettabile in siringa pre-riempita, 120 MG/ML
- Codice ATCS01LA06
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a BEOVUForma farmaceutica: Soluzione iniettabile, 40 mg/mLPrincipio attivo: afliberceptProduttore: SANDOZ GMBHPrescrizione richiestaForma farmaceutica: Soluzione iniettabile, 10 mg/mlPrincipio attivo: ranibizumabProduttore: SAMSUNG BIOEPIS NL B.V.Prescrizione richiestaForma farmaceutica: Soluzione iniettabile, 40MG/MLPrincipio attivo: afliberceptProduttore: BAYER AGPrescrizione richiesta
Medici online per BEOVU
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di BEOVU — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per BEOVU online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.













