
Come usare OLIMEL
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra originaleContenuto del foglietto illustrativo
- OLIMEL
- OLIMEL PERIFERICO N4E non deve essere somministrato contemporaneamente con il sangue
- OLIMEL PERIFERICO N4E si può integrare con elettroliti, sulla base della tabella seguente:
- OLIMEL
- Che cos’è OLIMEL N5E, emulsione per infusione e a che cosa serve
- Cosa deve sapere prima che le sia somministrato OLIMEL N5E emulsione per infusione
- Come usare OLIMEL N5E, emulsione per infusione
- Possibili effetti indesiderati
- Come conservare OLIMEL N5E, emulsione per infusione
- Contenuto della confezione e altre informazioni
- 500 mL 2.000 mL 2.500 mL
- OLIMEL
- OLIMEL N7. Ad esempio, i pazienti pediatrici possono avere un fabbisogno superiore a
- OLIMEL
- Che cos’è OLIMEL N7E, emulsione per infusione e a che cosa serve
- Cosa deve sapere prima che le sia somministrato OLIMEL N7E, emulsione per infusione
- Come usare OLIMEL N7E, emulsione per infusione
- POSSIBILI EFFETTI INDESIDERATI
- Come conservare OLIMEL N7E emulsione per infusione
- Contenuto della confezione e altre informazioni
- 000 mL 1.500 mL 2.000 mL
- OLIMEL
- Che cos’è OLIMEL N9 emulsione per infusione e a che cosa serve
- Cosa deve sapere prima che le sia somministrato OLIMEL N9 emulsione per infusione
- Come usare OLIMEL N9 emulsione per infusione
- Possibili effetti indesiderati
- Come conservare OLIMEL N9, emulsione per infusione
- Contenuto della confezione e altre informazioni
- 000 mL 1.500 mL 2.000 mL
- OLIMEL
- Che cos’è OLIMEL N9E emulsione per infusione e a che cosa serve
- Cosa deve sapere prima che le sia somministrato OLIMEL N9E emulsione per infusione
- Come usare OLIMEL N9E emulsione per infusione
- Possibili effetti indesiderati
- Come conservare OLIMEL N9E emulsione per infusione
- Contenuto della confezione e altre informazioni
- 000 mL 1.500 mL 2.000 mL
- OLIMEL
- Cos’è OLIMEL N12 emulsione per infusione e a cosa serve
- Cosa deve sapere prima che le sia somministrato OLIMEL N12 emulsione per infusione
- Come usare OLIMEL N12 emulsione per infusione
- Possibili effetti indesiderati
- Come conservare OLIMEL N12 emulsione per infusione
- Contenuto della confezione e altre informazioni
- Cos’è OLIMEL N12E emulsione per infusione e a cosa serve
- Cosa deve sapere prima che le sia somministrato OLIMEL N12E emulsione per infusione
- Come usare OLIMEL N12E emulsione per infusione
- Possibili effetti indesiderati
- Come conservare OLIMEL N12E emulsione per infusione
- Contenuto della confezione e altre informazioni
OLIMEL
PERIFERICO N4E, Emulsione per Infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale
poiché contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere. Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 1. Che cos'è OLIMEL PERIFERICO N4E emulsione per infusione e a che cosa serve
- 2. Cosa deve sapere prima che le sia somministrato OLIMEL PERIFERICO N4E emulsione per infusione
- 3. Come usare OLIMEL PERIFERICO N4E , emulsione per infusione
- 4. Possibili effetti indesiderati
- 5. Come conservare OLIMEL PERIFERICO N4E emulsione per infusione
- 6. Contenuto della confezione e altre informazioni
1. Che cos’è OLIMEL PERIFERICO N4E emulsione per infusione e a che cosa serve
OLIMEL PERIFERICO N4E è una emulsione per infusione. Si presenta sotto forma di sacca a 3
compartimenti.
Un compartimento contiene una soluzione di glucosio con calcio, il secondo un'emulsione di
lipidi e il terzo una soluzione di amminoacidi con altri elettroliti
OLIMEL PERIFERICO N4E si usa per fornire nutrimento ad adulti e bambini di età superiore a
due anni mediante un tubo in una vena, quando non sia idonea la normale alimentazione
per bocca.
OLIMEL PERIFERICO N4E deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL PERIFERICO N4E
emulsione per infusione
OLIMEL PERIFERICO N4E,emulsione per infusione non deve essere usata
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni Se è ipersensibile (allergico) alle proteine delle uova, dei semi di soia, dell’arachide, o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito) oppure a uno degli eccipienti.
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se ha iperglicemia (troppo zucchero nel sangue).
- Se ha una concentrazione abnormemente alta di uno qualsiasi degli elettroliti (sodio, potassio, magnesio, calcio e/o fosforo) nel sangue
In tutti i casi, il medico deciderà se Lei dovrà ricevere questo medicinale sulla base di fattori
quali età, peso e condizione medica, insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL PERIFERICO N4E .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale
totale, ciò può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali
di reazione allergica (come sudorazione, febbre, brividi, mal di testa, rush cutanei o
respirazione difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi
dell’uovo. I semi di soia e le proteine dell’uovo possono causare reazioni di ipersensibilità.
Sono state osservate reazioni allergiche crociate tra le proteine della soia e dell’arachide.
Olimel Periferico N4E contiene glucosio derivato dal mais che può causare reazioni di
ipersensibilità se Lei è allergico al mais o prodotti derivanti dal mais (vedere paragrafo
“OLIMEL PERIFERICO N4E, emulsione per infusione non deve essere usata” sopra)
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle,
che bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora
avvertisse difficoltà respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali
azioni intraprendere.
L'antibiotico denominato ceftriaxone non deve essere miscelato o somministrato
simultaneamente con qualsiasi soluzione contenente calcio (compreso OLIMEL PERIFERICO
N4E) che le viene somministrata mediante una flebo in vena.
Questi medicinali non le devono essere somministrati insieme neanche mediante linee di
infusione diverse o sedi di infusione diverse.
Tuttavia, lei potrà assumere OLIMEL PERIFERICO N4E e ceftriaxone in sequenza, uno dopo
l'altro, se si utilizzano linee di infusione in diverse sedi o se le linee di infusione vengono
sostituite o sono state accuratamente lavate con soluzione fisiologica tra un'infusione e
l'altra per evitare la formazione di precipitati (particelle di sale di calcio-ceftriaxone).
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri
nel sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere
endovenoso) viene inserito in vena. Il medico la monitorerà attentamente per eventuali
segni di infezione. I pazienti che richiedono la nutrizione parenterale (nutrizione attraverso
un tubo posto in vena) possono avere un maggior rischio di sviluppare infezioni dalle loro
condizioni mediche. L’utilizzo di tecniche asettiche (senza germi) durante il posizionamento e
la manutenzione del catetere e durante la preparazione della formula nutrizionale
(nutrizione parenterale totale)può ridurre tale rischio
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il
medico deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla
attentamente per prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine,
elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti
prima di iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo
medicinale e potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti ed
elementi in tracce, se ritiene che sia il caso.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o ictus secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà
esami clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato
questo medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può
provocare una “sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti
indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita
della soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà
interrotta immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di
erogazione di OLIMEL PERIFERICO N4E o le darà un medicinale per controllare il livello dello
zucchero nel sangue (insulina).
OLIMEL PERIFERICO N4E le può essere somministrato tramite un tubo (catetere) in una vena
del braccio o in una grande vena del torace (vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il
dosaggio corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità
dei bambini al rischio di infezione. L’integrazione di vitamine ed elementi in tracce è sempre
richiesta. Si devono utilizzare formulazioni pediatriche.
Altri medicinali eOLIMEL PERIFERICO N4E
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una
controindicazione. Se Lei assume altri medicinali, con o senza ricetta medica, informi
preventivamente il medico per verificarne la compatibilità.
OLIMEL PERIFERICO N4E non deve essere somministrato contemporaneamente con il sangue
attraverso lo stesso set di infusione.
OLIMEL PERIFERICO N4E contiene calcio. Non deve essere somministrato insieme
all’antibiotico ceftriaxone o attraverso lo stesso tubo, perché si possono formare delle
particelle. Se si utilizza lo stesso dispositivo per somministrarle questi medicinali in
successione, il dispositivo deve essere accuratamente lavato.
A causa del rischio di precipitazione, OLIMEL Periferico N4E non deve essere somministrato
attraverso la stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico
fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL PERIFERICO N4E contengono la vitamina K. Questa
vitamina generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti),
come la cumarina. Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di
laboratorio se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo
sangue (che di solito vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
OLIMEL PERIFERICO N4E contiene potassio. Porre particolare attenzione con i pazienti che
assumono diuretici, inibitori dell’ACE, antagonisti del recettore dell’angiotensina II (farmaci
per la cura dell’ipertensione) o immunosoppressivi. Questi tipi di farmaci possono
aumentare i livelli di potassio nel sangue.
Gravidanza, allattamento e fertilità
Se Lei ha in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta
allattando con latte materno chieda consiglio al medico prima di prendere questo
medicinale.
OLIMEL PERIFERICO N4E può essere preso in considerazione durante la gravidanza e
l’allattamento se necessario.
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL PERIFERICO N4E, emulsione per infusione
Dosaggio
OLIMEL PERIFERICO N4E deve essere somministrato solo in adulti e bambini di età superiore
a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere)
in una vena del braccio o in una grande vena del suo torace.
OLIMEL PERIFERICO N4E deve essere a temperatura ambiente prima dell'uso.
OLIMEL PERIFERICO N4E è esclusivamente per uso singolo.
L’ infusione di una sacca di solito dura tra le 12 e le 24 ore.
Dosaggio - Adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni
cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni
cliniche.
Dosaggio - Bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò
dipenderà dall'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo
di scindere e usare i componenti di OLIMEL PERIFERICO N4E.
Se le è stato somministrato più OLIMEL PERIFERICO N4E, emulsione per infusione, di
quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può
rendere il suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del
volume del sangue circolante). I livelli di glucosio nel sangue e nelle urine possono
aumentare e si può sviluppare una sindrome iperosmolare (eccessiva viscosità del sangue) e
il contenuto di lipidi può aumentare il livello di trigliceridi presenti nel Suo sangue. Ricevere
un’infusione troppo veloce o un volume di OLIMEL PERIFERICO N4E troppo grande può
causare nausea, vomito, brividi, mal di testa, vampate di calore, sudorazione eccessiva (iperidrosi)
e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere interrotta
immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare
i suoi reni a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico controllerà regolarmente la sua condizione
e testerà i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non
tutte le persone li manifestino.
Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il trattamento, lo
comunichi prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione verrà interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, come sudorazione, febbre, brividi, mal di testa, rash cutanei o difficoltà
nella respirazione.
Con OLIMEL PERIFERICO N4E sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore, irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 individuo su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- 1. Febbre
- 2. Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno (anemia).
- 3. Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- 4. Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- 5. Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- 6. Livelli elevati di grassi nel sangue (iperlipidemia)
- 7. Infiltrazione lipidica epatica (epatomegalia)
- 8. Deterioramento della funzionalità del fegato
- 9. Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia).
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia).
- Aumento dei livelli di azoto nel sangue (azotemia).
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio,
si rivolga al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati
direttamente tramite il sistema nazionale di segnalazione all’indirizzo :
http://www.agenziafarmaco.gov.it/content/come-segnalare-una-sospetta-reazione-avversa .
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla
sicurezza di questo medicinale .
5. Come conservare OLIMEL PERIFERICO N4E emulsione per infusione
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista
come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL PERIFERICO N4E, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-
amminoacidi al 6,3%(corrispondente a 6.3 g/100 mL) (alanina, arginina, glicina, istidina,
isoleucina, leucina, lisina (come lisina acetato), metionina, fenilalanina, prolina, serina,
treonina, triptofano, tirosina, valina, acido aspartico, acido glutammico) con elettroliti
(sodio, potassio, magnesio, fosfato, acetato, cloruro), una emulsione di lipidi al15%
(corrispondente a 15 g/100 mL) (olio di oliva purificato e olio di soia purificato) e una
soluzione di glucosio al 18,75%(corrispondente a 18,75 g/100 mL) (come glucosio
monoidrato) con calcio.
Gli eccipienti sono:
CompartimentoCompartimentoCompartimento
Emulsione di lipidiSoluzione di amminoacidiSoluzione di glucosio
Fosfatide purificato di uovo,
glicerolo, sodio oleato, sodio
idrossido (per l’aggiustamento del
pH), acqua per preparazioni
iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL PERIFERICO N4E, emulsione per infusione e contenuto delle confezioni
OLIMEL PERIFERICO N4E è un’emulsione per infusione confezionata in una sacca a tre
compartimenti. Un compartimento contiene un’emulsione di lipidi, un altro compartimento
una soluzione di amminoacidi con elettroliti ed il terzo compartimento una soluzione di
glucosio con calcio. Questi compartimenti sono separati da membrane non permanenti.
Prima della somministrazione il contenuto dei compartimenti deve essere miscelato
arrotolando la sacca su se stessa partendo dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
- Le soluzioni di amminoacidi e di glucosio sono limpide, chiare incolori o leggermente gialle.
- L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato
interno (di contatto) della sacca è studiato per essere compatibile con i costituenti e gli
additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro
esterno con barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 1.000 mL: 1 scatola con 6 sacche
sacca da 1.500 mL: 1 scatola con 4 sacche
sacca da 2.000 mL: 1 scatola con 4 sacche
sacca da 2.500 mL: 1 scatola con 2 sacche
1 sacca da 1.000 mL, 1.500 mL, 2.000 mL e 2.500 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80,
7860 Lessines –
Belgium
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i
seguenti nomi:
Francia, Portogallo, Bulgaria, Romania, Repubblica Ceca, Belgio, Spagna, Repubblica
Slovacca, Lussemburgo, Slovenia: PERIOLIMEL N4E
Estonia, Polonia, Lituania, Lettonia, Grecia, Cipro: OLIMEL PERI N4E
Paesi Bassi: Olimel Perifeer N4E
Austria: PeriOLIMEL 2,5 % mit Elektrolyten
Germania: Olimel Peri 2,5% E
Danimarca, Islanda, Svezia, Norvegia, Finlandia: Olimel Perifer N4E
Regno Unito, Irlanda, Malta: Triomel Peripheral 4g/L nitrogen 700 kcal/L with electrolytes
Ungheria: PeriOlimel 4 g/L nitrogén elektrolitokkal emulziós infúzió
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Categoria farmacoterapeutica: Soluzioni per nutrizione parenterale/combinazioni
Codice ATC: B05 BA10
- A.COMPOSIZIONE QUALITATIVA E QUANTITATIVA
OLIMEL PERIFERICO N4E si presenta sotto forma di sacca a 3 compartimenti.
Ogni sacca contiene una soluzione di glucosio con calcio, una emulsione di lipidi e una
soluzione di amminoacidi con altri elettroliti:
Contenuto per sacca
1.000 mL 1.500 mL 2.000 mL 2.500 mL
Soluzione di glucosio 18,75 %
(corrispondente a 18,75 g/100
mL)
400 mL 600 mL 800 mL 1.000 mL
Soluzione di amminoacidi 6,3 %
(corrispondente a 6,3 g/100 mL)
400 mL 600 mL 800 mL 1.000 mL
Emulsione di lipidi 15 %
(corrispondente a 15 g/100 mL)
200 mL 300 mL 400 mL 500 mL
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre
compartimenti:
Principi attivi1.000 mL1.500 mL2.000 mL2.500 mL
Olio di oliva purificato + olio di soia
purificato 30,00 g 45,00 g 60,00 g 75,00 g
Alanina 3,66 g 5,50 g 7,33 g 9,16 g
Arginina 2,48 g 3,72 g 4,96 g 6,20 g
Acido aspartico 0,73 g 1,10 g 1,46 g 1,83 g
Acido glutammico 1,26 g 1,90 g 2,53 g 3,16 g
Glicina 1,76 g 2,63 g 3,51 g 4,39 g
Istidina 1,51 g 2,26 g 3,02 g 3,77 g
Isoleucina 1,26 g 1,90 g 2,53 g 3,16 g
Leucina 1,76 g 2,63 g 3,51 g 4,39 g
Lisina
(equivalente a lisina acetato)
1,99 g
(2,81g)
- 2.99 g (4,21 g) 3,98 g (5,62 g) 4,98 g (7,02 g)
Metionina 1,26 g 1,90 g 2,53 g 3,16 g
Fenilalanina 1,76 g 2,63 g 3,51 g 4,39 g
Prolina 1,51 g 2,26 g 3,02 g 3,77 g
Serina 1,00 g 1,50 g 2,00 g 2,50 g
Treonina 1,26 g 1,90 g 2,53 g 3,16 g
Triptofano 0,42 g 0,64 g 0,85 g 1,06 g
Tirosina 0,06 g 0,10 g 0,13 g 0,16 g
Valina 1,62 g 2,43 g 3,24 g 4,05 g
Sodio acetato, triidrato 1,16 g 1,73 g 2,31 g 2,89 g
Sodio glicerofosfato, idrato 1,91 g 2,87 g 3,82 g 4,78 g
Potassio cloruro 1,19 g 1,79 g 2,38 g 2,98 g
Magnesio cloruro, esaidrato 0,45 g 0,67 g 0,90 g 1,12 g
Calcio cloruro, biidrato 0,30 g 0,44 g 0,59 g 0,74 g
Glucosio anidro
(equivalente a glucosio monoidrato)
187,50 g
(206,50 g)
75,00 g
(82,50 g)
112,50 g
(123,75 g)
150,00 g
(165,00 g)
Una miscela di olio di oliva purificato (circa 80%) e olio di soia purificato (circa 20%)
corrispondente a un rapporto acidi grassi essenziali / acidi grassi totali del 20%.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Fosfatide purificato di uovo,
glicerolo, sodio oleato, sodio
idrossido (per l’aggiustamento del
pH), acqua per preparazioni
iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
| I |
|
|
|
|
| Lipidi | 30 g | 45 g | 60 g | 75 g |
| a Amminoacidi | 25,3 g | 38,0 g | 50,6 g | 63,3 g |
| Azoto | 4,0 g | 6,0 g | 8,0 g | 10,0 g |
| i Glucosio | 75,0 g | 112,5 g | 150,0 g | 187,5 g |
| z Energia: n Calorie totali circa. e Calorie non proteiche. Calorie glucosio g Calorie lipidiche..(a) A Rapporto calorie non proteiche/azoto Rapporto calorie glucosio/lipidiche Calorie lipidiche/totali | 700 kcal 600 kcal 300 kcal 300 kcal 150 kcal/g 50/50 43% | 1050 kcal 900 kcal 450 kcal 450 kcal 150 kcal/g 50/50 43% | 1400 kcal 1200 kcal 600 kcal 600 kcal 150 kcal/g 50/50 43% | 1750 kcal 1500 kcal 750 kcal 750 kcal 150 kcal/g 50/50 43% |
| Elettroliti: |
Include calorie da fosfatidi purificati di uovo
Include fosfato fornito dall'emulsione di lipidi
- B. POSOLOGIA E MODO DI SOMMINISTRAZIONE
Posologia
OLIMEL PERIFERICO N4E non è raccomandato nei bambini al di sotto di 2 anni a causa della
composizione e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione
statica della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare
simultaneamente tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni
cliniche in cui i pazienti richiedano quantità di elementi nutritivi variabili rispetto alla
composizione della sacca statica. In tale situazione, qualunque aggiustamento del volume
(dose) deve prendere in considerazione l'effetto risultante che ciò avrà sul dosaggio di tutti
gli altri elementi nutritivi di OLIMEL PERIFERICO N4E. Ad esempio, i pazienti pediatrici
possono avere un fabbisogno superiore a 0,2 mmol/kg/giorno di fosfato. In queste
circostanze, gli operatori sanitari possono prendere in considerazione l'aggiustamento del
volume (dose) di OLIMEL PERIFERICO N4E al fine di soddisfare tale fabbisogno aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla
capacità di metabolizzare i costituenti di OLIMEL PERIFERICO N4E del paziente, oltre che
dall’energia o dalle proteine ulteriori fornite oralmente/enteralmente, pertanto i formati
della sacca devono essere scelti di conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico,
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per OLIMEL PERIFERICO N4E, la dose quotidiana massima è definita dall'apporto di liquidi, 40
mL/kg, corrispondenti a 1 g/kg amminoacidi, 3 g/kg glucosio, 1,2 g/kg lipidi, 0,8 mmol/kg
sodio e 0,6 mmol/kg di potassio. Per un paziente di 70 kg, questo sarebbe equivalente a
2800 mL OLIMEL PERIFERICO N4E al giorno, che si traduce in un apporto di 71 g
amminoacidi, 210 g glucosio e 84 g lipidi, ovvero 1680 kcal non proteiche e 1960 kcal totali.
| Sodio Potassio Magnesio Calcio Fosfato (b) Acetato Cloruro | 21 mmol 16,0 mmol 2,2 mmol 2,0 mmol 8,5 mmol 27 mmol 24 mmol | 31,5 mmol 24,0 mmol 3,3 mmol 3,0 mmol 12,7 mmol 41 mmol 37 mmol | 42,0 mmol 32,0 mmol 4,4 mmol 4,0 mmol 17,0 mmol 55 mmol 49 mmol | 52,5 mmol 40,0 mmol o 5,5 mmol 5,0 mmol c 21,2 mmol a 69 mmol 61 mmol |
| pH. | 6,4 | 6,4 | 6,4 | 6,4 |
| Osmolarità. | 760 mosm/L | 760 mosm/L | m 760 mosm/L | 760 mosm/L |
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima
ora quindi deve essere regolata per tener conto della dose da somministrare, i volumi da
assumere quotidianamente e la durata dell'infusione.
Per OLIMEL PERIFERICO N4E, la velocità d'infusione massima è 3,2 mL/kg/ora, corrispondenti
a 0,08 g/kg/ora per amminoacidi, 0,24 g/kg/ora per glucosio e 0,10 g/kg/ora per lipidi.
Nei bambini di età superiore a 2 anni
Non esistono studi eseguiti sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla
capacità di metabolizzare i costituenti di OLIMEL PERIFERICO N4E del paziente, oltre che da
energia o proteine ulteriori fornite oralmente/enteralmente, pertanto, i formati della sacca
devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di fluidi, azoto ed energia si riducono continuamente con
l'età.
Sono stati presi in considerazione 2 gruppi, età tra 2 e 11 anni, ed età tra 12 e 18 anni.
Per Olimel PERIFERICO N4E i fattori limitanti per i sopra citati gruppi pediatrici sono la
concentrazione dei fosfati per la dose giornaliera (0,2 mmol/kg/die) e la concentrazione dei
lipidi per la velocità oraria, risultanti nei seguenti apporti:
| Costituenti | n Da 2 a 11 anni | Da 12 a 18 anni | |||
| i Raccomandatoa l | a OLIMEL PERIFERICO N4E Vol Massimo | Raccomandatoa | OLIMEL PERIFERICO N4E Vol Massimo | ||
| Dose massima giornaliera | |||||
| Fluidi (mL/kg/d) | a
| 24 |
| 24 | |
| Amino acidi (g/kg/d) | t
| 0,6 |
| 0,6 | |
| Glucosio (g/kg/d) | I
| 1,8 |
| 1,8 | |
| Lipidi (g/kg/d) | a 0,5 - 3 | 0,7 | 0,5 - 2 (fino a 3) | 0,7 | |
| Energia totale (kcal/kg/d) | i
| 16 |
| 16 | |
| z Massima velocità all’ora | |||||
| n OLIMEL PERIFERICO N4E (mL/kg/h) | 4,3 | 4,3 | |||
| Amino acidi(g/kg/h) | 0,20 | 0,11 | 0,12 | 0,11 | |
| e Glucosio (g/kg/h) | 1,2 | 0,32 | 1,2 | 0,33 | |
| g Lipidi (g/kg/h) | 0,13 | 0,13 | 0,13 | 0,13 | |
a: Valori raccomandati dalla Linee Guida 2005 ESPGHAN/ ESPEN
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima
ora e poi deve essere regolata prendendo in considerazione la dose da somministrare,
l’apporto di volume giornaliero e la durata dell’infusione.
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera
bassa, e di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare immediatamente il contenuto della sacca dopo la sua apertura e non
conservarlo per un’infusione successiva.
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il
paragrafo 6.6.
Per la sua bassa osmolarità, OLIMEL PERIFERICO N4E può essere somministrato tramite vena
periferica o centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra
12 e 24 ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle
condizioni cliniche del paziente.
- C.INCOMPATIBILITÀ
Non aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o
all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della
preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da
contenuto non idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare
l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in
particolar modo sotto forma di sali minerali, può causare la formazione di precipitati di
fosfato di calcio.
OLIMEL Periferico N4E contiene ioni calcio che rappresentano un rischio ulteriore di
coagulazione nel sangue o in emocomponenti anticoagulati o conservati con citrato.
Il ceftriaxone non deve essere miscelato o somministrato in concomitanza con soluzioni
endovenose contenenti calcio, compreso OLIMEL Periferico N4E, attraverso la stessa linea di
infusione (per es., tramite un connettore a Y) a causa del rischio di precipitazione del sale di
ceftriaxone-calcio (vedere paragrafi 4.4 e 4.5 dell’RCP). Il ceftriaxone e le soluzioni
contenenti calcio possono essere somministrati in sequenza uno dopo l'altro se si utilizzano
linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state
accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la
formazione di precipitati.
A causa del rischio di precipitazione, OLIMEL Periferico N4E non deve essere somministrato
attraverso la stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico
fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo
stesso set di somministrazione, catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la
stessa linea, a causa del rischio di pseudoagglutinazione.
- D.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONE
Una visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL
Periferico N4E viene illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare
solo se la sacca non è danneggiata, se le membrane di separazione non permanenti sono
intatte (cioè non è presente miscelazione del contenuto dei 3 compartimenti), se la
soluzione di amminoacidi e la soluzione di glucosio sono limpide, incolori o lievemente gialle,
ed in pratica prive di particelle visibili, e se l'emulsione di lipidi è un liquido omogeneo con
aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
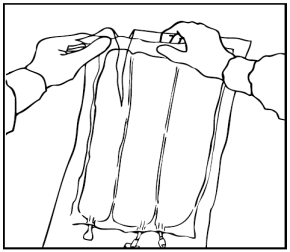
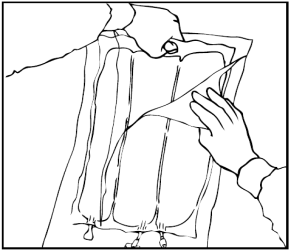
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con
cappio). Le membrane di separazione non permanenti scompariranno dal lato accanto alle
aperture. Continuare ad arrotolare la sacca finché le membrane di separazione non siano
aperte per circa metà della loro lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti
ed elementi in tracce.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura
delle membrane di separazione non permanenti e dopo la miscelazione del contenuto dei
tre compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela
sia ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima
della miscelazione dei tre compartimenti).
Quando si eseguono le aggiunte alle formulazioni contenenti elettroliti, si deve considerare
la quantità di elettroliti già presente nella sacca
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
OLIMEL PERIFERICO N4E si può integrare con elettroliti, sulla base della tabella seguente:
Valore corrispondente all'aggiunta del fosfato inorganico
Incluso il fosfato fornito dall'emulsione di lipidi
Elementi in tracce e vitamine:
La stabilità è stata dimostrata con preparazioni di vitamine e oligoelementi in commercio
(contenenti al massimo 1 mg di ferro).
La compatibilità di altri additivi è disponibile su richiesta.
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare
l'osmolarità finale della miscela.
Per eseguire un'aggiunta:
- l'operazione deve avvenire in condizione asettica.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
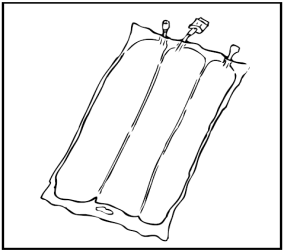
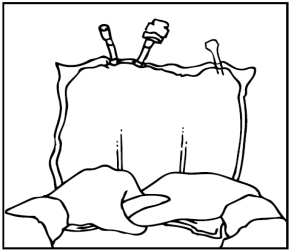
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
| Per 1.000 mL | |||
| Livello incluso | Aggiunta ulteriore massima | m Livello totale massimo | |
| Sodio | 21 mmol | 129 mmol | r 150 mmol |
| Potassio | 16 mmol | 134 mmol | a 150 mmol |
| Magnesio | 2,2 mmol | 3,4 mmol | 5,6 mmol |
| Calcio | 2,0 mmol | F 3,0 (1,5(a)) mmol | 5,0 (3,5(a)) mmol |
| Fosfato inorganico | 0 mmol | 8,0 mmol | 8,0 mmol |
| Fosfato organico | 8,5 mmol
| l e 15,0 mmol | 23,5 mmol (b) |
1 2 3

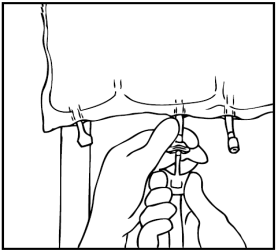
4 5 6
Somministrazione
Solo per uso singolo.
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non
permanenti tra i 3 compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle
fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai
la sacca aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas
contenuto nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi
necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di
stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente
mantenendo il catetere o la cannula inserito per il trattamento immediato del paziente. Se
possibile, eseguire un'aspirazione attraverso il catetere o la cannula inserito per ridurre la
quantità di liquido presente nei tessuti prima di rimuovere il catetere o la cannula. Se lo
stravaso interessa un arto, questo dovrebbe essere sollevato.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL
Periferico N4E, se applicabile) e dell'estensione o del grado di una possibile lesione, occorre
intraprendere misure specifiche appropriate. Le opzioni di trattamento possono includere un
intervento non farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande
entità, chiedere la consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24
ore, poi una volta al giorno.
L'infusione non dovrebbe essere riavviata nella stessa vena periferica o centrale.
OLIMEL
N5E, Emulsione per Infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 7. Che cos'è OLIMEL N5E emulsione per infusione e a che cosa serve
- 8. Cosa deve sapere prima che le sia somministrato OLIMEL N5E emulsione per infusione
- 9. Come usare OLIMEL N5E, emulsione per infusione
- 10. Possibili effetti indesiderati
- 11. Come conservare OLIMEL N5E emulsione per infusione
- 12. Contenuto della confezione e altre informazioni
1. Che cos’è OLIMEL N5E, emulsione per infusione e a che cosa serve
OLIMEL N5E è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio con calcio, il secondo un'emulsione di lipidi e il
terzo una soluzione di amminoacidi con altri elettroliti.
OLIMEL N5E si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante
un tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL N5E deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N5E emulsione per infusione
OLIMEL N5E, emulsione per infusione non deve essere usata :
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è ipersensibile (allergico) alle proteine delle uova, dei semi di soia, dell’arachide o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito), oppure a uno degli eccipienti.
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se soffre di iperglicemia (troppo zucchero nel sangue)
- Se ha una concentrazione abnormemente alta di uno qualsiasi degli elettroliti (sodio, potassio, magnesio, calcio e/o fosforo) nel sangue.
In tutti i casi, il suo medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali
età, peso e condizione medica , insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N5E .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come sudorazione, febbre, brividi, mal di testa, rash cutanei o respirazione
difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N5E contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivanti dal mais (vedere paragrafo “OLIMEL N5E, emulsione per
infusione non deve essere usata” sopra)
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
L'antibiotico denominato ceftriaxone non deve essere miscelato o somministrato simultaneamente
con qualsiasi soluzione contenente calcio (compreso OLIMEL N5E) che le viene somministrata
mediante una flebo in vena.
Questi farmaci non le devono essere somministrati neanche mediante linee di infusione diverse o
sedi di infusione diverse.
Tuttavia, lei potrà assumere OLIMEL N5E e ceftriaxone in sequenza, uno dopo l'altro, se si utilizzano
linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state
accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di
precipitati (particelle di sale di calcio-ceftriaxone).
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento e la manutenzione del catetere e durante
la preparazione della formula nutrizionale (nutrizione parenterale totale) può ridurre tale rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine, elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima di
iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti e elementi in tracce, se
ritiene che sia il caso.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o ictus secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il Suo medico effettuerà
esami clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà fornito questo
medicinale per diverse settimane, il Suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare una
“sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N5E o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N5E le può essere somministrato tramite un tubo (catetere) solo in una grande vena del
torace (vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed elementi in tracce è sempre richiesta. Si devono
Altri medicinali eOLIMEL N5E
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
OLIMEL N5E non deve essere somministrato contemporaneamente con il sangue attraverso lo stesso
set di infusione.
OLIMEL N5E contiene calcio. Non deve essere somministrato insieme all’antibiotico ceftriaxone o
attraverso lo stesso tubo, perché si possono formare delle particelle. Se si utilizza lo stesso
dispositivo per somministrarle questi medicinali in successione, il dispositivo deve essere
accuratamente lavato.
A causa del rischio di precipitazione, OLIMEL N5E non deve essere somministrato attraverso la
stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL N5E contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
OLIMEL N5E contiene potassio. Porre particolare attenzione con i pazienti che assumono diuretici,
inibitori dell’ACE, antagonisti del recettore dell’angiotensina II (farmaci per la cura dell’ipertensione)
o immunosoppressivi. Questi tipi di farmaci possono aumentare i livelli di potassio nel sangue.
Gravidanza, allattamento e fertilità
Se Lei ha in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando
con latte materno chieda consiglio al medico prima di prendere questo medicinale.
OLIMEL N5E può essere preso in considerazione durante la gravidanza e l’allattamento se necessario
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N5E, emulsione per infusione
Dosaggio
OLIMEL N5E deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena del
suo torace.
OLIMEL N5E deve essere a temperatura ambiente prima dell'uso.
OLIMEL N5E è esclusivamente per uso singolo.
L'infusione di 1 sacca di solito dura tra le 12 e le 24 ore
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N5E.
Se le è stato somministrato più OLIMEL N5E, emulsione per infusione, di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume del
sangue circolante). I livelli di glucosio nel sangue e nelle urine possono aumentare e si può sviluppare
una sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può aumentare il
livello di trigliceridi presenti nel Suo sangue. Ricevere un’ infusione troppo veloce o un volume di
OLIMEL N5E troppo grande può causare nausea, vomito, brividi, mal di testa, vampate di calore,
sudorazione eccessiva (iperidrosi) e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere
interrotta immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico controllerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di OLIMEL N5E, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati sebbene non tutte le
persone li manifestino.
Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il trattamento, lo comunichi
prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione verrà interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, come sudorazione, febbre, brividi, mal di testa, rash cutanei o difficoltà nella
respirazione.
Con OLIMEL N5E sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle .
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 individuo su 10000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- Febbre
- Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno (anemia).
- Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- Livelli elevati di grassi nel sangue (iperlipidemia)
- Infiltrazione lipidica epatica (epatomegalia)
- Deterioramento della funzionalità del fegato
- Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia).
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia).
- Aumento dei livelli di azoto nel sangue (azotemia).
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo: http://www.agenziafarmaco.gov.it/content/come-
segnalare-una-sospetta-reazione-avversa. Segnalando gli effetti indesiderati lei può contribuire a
fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare OLIMEL N5E, emulsione per infusione
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N5E, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
8,2%(corrispondente a 8,2 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico) con elettroliti (sodio, potassio, magnesio, fosfato, acetato,
cloruro), una emulsione di lipidi al20%(corrispondente a 20,0 g/100 mL) (olio di oliva purificato e
olio di soia purificato) e una soluzione di glucosio al 28,75%(corrispondente a 28,75 g/100 mL)
(come glucosio monoidrato) con calcio.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N5E, emulsione per infusione e contenuto delle confezioni
OLIMEL N5E è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro compartimento una soluzione di
amminoacidi con elettroliti ed il terzo compartimento una soluzione di glucosio con calcio. Questi
compartimenti sono separati da membrane non permanenti. Prima della somministrazione il
contenuto dei compartimenti deve essere miscelato arrotolando la sacca su se stessa partendo
dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
Le soluzioni di amminoacidi e di glucosio sono limpide, chiare incolori o leggermente gialle.
L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 1.500 mL: 1 scatola con 4 sacche
sacca da 2.000 mL: 1 scatola con 4 sacche
sacca da 2.500 mL: 1 scatola con 2 sacche
1 sacca da 1.500 mL, 2.000 mL e 2.500 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80,
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Francia, Portogallo, Estonia, Polonia, Lituania, Bulgaria, Romania, Lettonia, Repubblica Ceca, Belgio,
Spagna, Repubblica Slovacca, Paesi Bassi, Lussemburgo, Slovenia, Italia, Danimarca, Islanda, Svezia,
Norvegia, Finlandia, Grecia, Cipro: OLIMEL N5E
Austria: ZentroOLIMEL 3,3 % mit Elektrolyten >
Germania: Olimel 3,3% E
Regno Unito, Irlanda, Malta: Triomel 5g/L nitrogen 990 kcal/L with electrolytes
Ungheria: Olimel 5 g/L nitrogén elektrolitokkal emulziós infúzió
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Categoria farmacoterapeutica: Soluzioni per nutrizione parenterale/combinazioni
Codice ATC: B05 BA10
- C.COMPOSIZIONE QUALITATIVA E QUANTITATIVA
OLIMEL N5E si presenta sotto forma di sacca a 3 compartimenti.
Ogni sacca contiene una soluzione di glucosio con calcio, una emulsione di lipidi e una soluzione di
amminoacidi con altri elettroliti:
Contenuto per sacca
1.500 mL 2.000 mL 2.500 mL
Soluzione di glucosio 28,75%
(corrispondente a 28,75 g/100 mL)
600 mL 800 mL 1.000 mL
Soluzione di amminoacidi 8,2%
(corrispondente a 8,2 g/100 mL)
600 mL 800 mL 1.000 mL
Emulsione di lipidi 20%
(corrispondente a 20 g/100 mL)
300 mL 400 mL 500 mL
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
Principi attivi1.500 mL2.000 mL2.500 mL
Olio di oliva purificato + olio di soia purificato 60,00 g 80,00 g 100,00 g
Alanina 7,14 g 9,52 g 11,90 g
Arginina 4,84 g 6,45 g 8,06 g
Acido aspartico 1,43 g 1,90 g 2,38 g
Acido glutammico 2,47 g 3,29 g 4,11 g
Glicina 3,42 g 4,56 g 5,70 g
Istidina 2,95 g 3,93 g 4,91 g
Isoleucina 2,47 g 3,29 g 4,11 g
Leucina 3,42 g 4,56 g 5,70 g
Lisina
(equivalente a lisina acetato)
6,47 g
(9,13g)
Metionina 2,47 g 3,29 g 4,11 g
Fenilalanina 3,42 g 4,56 g 5,70 g
Prolina 2,95 g 3,93 g 4,91 g
Serina 1,95 g 2,60 g 3,25 g
Treonina 2,47 g 3,29 g 4,11 g
Triptofano 0,82 g 1,10 g 1,37 g
Tirosina 0,13 g 0,17 g 0,21 g
Valina 3,16 g 4,21 g 5,26 g
Sodio acetato, triidrato 2,24 g 2,99 g 3,74 g
Sodio glicerofosfato idrato 5,51 g 7,34 g 9,18 g
Potassio cloruro 3,35 g 4,47 g 5,59 g
Magnesio cloruro, esaidrato 1,22 g 1,62 g 2,03 g
Calcio cloruro, biidrato 0,77 g 1,03 g 1,29 g
Glucosio anidro
(equivalente a glucosio monoidrato)
3,88 g
(5,48g)
5,18 g
(7,30g)
172,50 g
(189,75 g)
230,00 g
(253,00 g)
287,50 g
(316,25g)
Una miscela di olio di oliva purificato (circa 80%) e olio di soia purificato (circa 20%) corrispondente
a un rapporto acidi grassi essenziali / acidi grassi totali del 20%.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
| e |
|
|
|
| Lipidi | 60 g | 80 g | 100 g |
| g Amminoacidi | 49,4 g | 65,8 g | 82,3 g |
| Azoto | 7,8 g | 10,4 g | 13,0 g |
| A Glucosio | 172,5 g | 230,0 g | 287,5 g |
| Energia: Calorie totali appross. Calorie non proteiche. Calorie glucosio | 1490 kcal 1290 kcal 690 kcal | 1980 kcal 1720 kcal 920 kcal | 2480 kcal 2150 kcal 1150 kcal |
Include calorie da fosfatidi purificati di uovo
Include fosfato fornito dall'emulsione di lipidi
- D. POSOLOGIA E MODO DI SOMMINISTRAZIONE
Posologia
L’uso di OLIMEL N5E non è raccomandato nei bambini al di sotto di 2 anni a causa della composizione
e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare simultaneamente
tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i pazienti
richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca statica. In tale
situazione, qualunque aggiustamento del volume (dose) deve prendere in considerazione l'effetto
risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di OLIMEL N5E. Ad esempio, i
pazienti pediatrici possono avere un fabbisogno superiore a 0,2 mmol/kg/giorno di fosfato. In queste
circostanze, gli operatori sanitari possono prendere in considerazione l'aggiustamento del volume
(dose) di OLIMEL N5E al fine di soddisfare tale fabbisogno aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N5E del paziente, oltre che dall’energia o dalle proteine
ulteriori fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di
conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico,
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per OLIMEL N5E la dose quotidiana massima è definita dall'apporto di liquidi, 40 mL/kg,
corrispondenti a 1,3 g/kg amminoacidi, 4,6 g/kg glucosio, 1,6 g/kg lipidi, 1,4 mmol/kg sodio e 1,2
mmol/kg potassio. Per un paziente di 70 kg questo sarebbe equivalente a 2800 mL di OLIMEL N5E al
giorno, che si traduce in un apporto di 92g amminoacidi, 322 g glucosio e 112 g lipidi, (ovvero 2.408
kcal non proteiche e 2.772 kcal totali).
| Calorie lipidiche.(a) Rapporto calorie non proteiche/azoto Rapporto calorie glucosio/lipidi Calorie lipidi/totali | 600 kcal 165 kcal/g 53/47 40% | 800 kcal 165 kcal/g 53/47 40% | 1000 kcal o 165 kcal/g 53/47 40% |
| Elettroliti: sodio potassio magnesio calcio fosfato (b) acetato cloruro | 52,5 mmol 45,0 mmol 6,0 mmol 5,3 mmol 22,5 mmol 55 mmol 68 mmol | 70,0 mmol 60,0 mmol 8,0 mmol 7,0 mmol r 30,0 mmol 73 mmol 90 mmol | c a 87,5 mmol m 75,0 mmol 10,0 mmol 8,8 mmol 37,5 mmol 91 mmol 113 mmol |
| pH. | 6,4 | a 6,4 | 6,4 |
| Osmolarità. |
|
|
|
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
Per OLIMEL N5E la velocità d'infusione massima è 2,1 mL/kg/ora, corrispondenti a 0,07 g/kg/ora
amminoacidi, 0,24 g/kg/ora glucosio e 0,08 g/kg/ora lipidi.
Nei bambini di età superiore a due anni
Non esistono studi eseguiti sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N5E del paziente, oltre che da energia o proteine ulteriori
fornite oralmente/enteralmente, pertanto, i formati della sacca devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, età tra 2 e 11 anni, ed età tra 12 e 18 anni.
Per Olimel N5E i fattori limitanti per i sopra citati gruppi pediatrici sono la concentrazione dei fosfati
per la dose giornaliera (0,2 mmol/kg/die) e la concentrazione dei lipidi per la velocità, risultanti nei
seguenti apporti:
| Costituenti | Da 2 a 11 anni | Da 12 a 18 anni | |||
| Raccomandatoa | d OLIMEL N5E Vol Massimo | Raccomandatoa | OLIMEL N5E Vol Massimo | ||
| a Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| 13 |
| 13 | |
| Amminoacidi (g/kg/d) |
| n 0,4 |
| 0,4 | |
| Glucosio (g/kg/d) |
| a 1,5 |
| 1,5 | |
| Lipidi (g/kg/d) | 0,5 - 3 | 0,5 |
| 0,5 | |
| Energia totale (kcal/kg/d) | i l
| 13 |
| 13 | |
| a Massima velocità all’ora | |||||
| OLIMEL N5E (mL/kg/h) | 3,3 | 3,3 | |||
| Amino acidi(g/kg/h) | t 0,20 | 0,11 | 0,12 | 0,11 | |
| Glucosio (g/kg/h) | I 1,2 | 0,38 | 1,2 | 0,38 | |
| Lipidi (g/kg/h) | 0,13 | 0,13 | 0,13 | 0,13 | |
a: Valori raccomandati dalla Linee Guida 2005 ESPGHAN/ ESPEN-
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora e poi
deve essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume
giornaliero e la durata dell’infusione.
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e
di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva.
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6.
Per la sua alta osmolarità, OLIMEL N5E può essere somministrato solo attraverso una vena centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e 24 ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle condizioni
cliniche del paziente.
- D.INCOMPATIBILITÀNon aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
OLIMEL N5E contiene ioni calcio che rappresentano un rischio ulteriore di coagulazione nel sangue o
in emocomponenti anticoagulati o conservati con citrato.
Il ceftriaxone non deve essere miscelato o somministrato in concomitanza con soluzioni endovenose
contenenti calcio, compreso OLIMEL N5E, attraverso la stessa linea di infusione (per es., tramite un
connettore a Y) a causa del rischio di precipitazione del sale di ceftriaxone-calcio (vedere paragrafi
- 4.4 e 4.5 dell’RCP). Il ceftriaxone e le soluzioni contenenti calcio possono essere somministrati in sequenza uno dopo l'altro se si utilizzano linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di precipitati. A causa del rischio di precipitazione, OLIMEL Periferico N5E non deve essere somministrato attraverso la stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di somministrazione , catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- E.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONEUna visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N5E viene illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
elementi in tracce.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Quando si eseguono le aggiunte alle formulazioni contenenti elettroliti, si deve considerare la
quantità di elettroliti già presente nella sacca
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
OLIMEL N5E si può integrare con elettroliti, sulla base della tabella seguente:
Valore corrispondente all'aggiunta del fosfato inorganico
Incluso il fosfato fornito dall'emulsione di lipidi
Elementi in tracce e vitamine:
La stabilità è stata dimostrata con preparazioni di vitamine e oligoelementi in commercio (contenenti
al massimo 1 mg di ferro).
La compatibilità di altri additivi è disponibile su richiesta.
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- l'operazione deve avvenire in condizione asettica.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
| Per 1.000 mL | |||
| Livello incluso | Aggiunta ulteriore massima | o Livello totale massimo | |
| sodio | 35 mmol | 115 mmol | 150 mmol |
| potassio | 30 mmol | 120 mmol | c 150 mmol |
| magnesio | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| calcio | 3,5 mmol | 1,5 (0,0(a)) mmol | a 5,0 (3,5(a))mmol |
| Fosfato inorganico | 0 mmol | 3,0 mmol | 3,0 mmol |
| Fosfato organico | 15 mmol (b) | 10 mmol | m 25 mmol (b) |
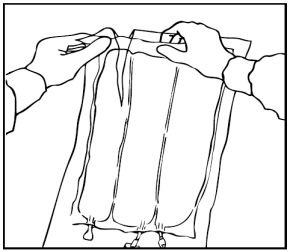
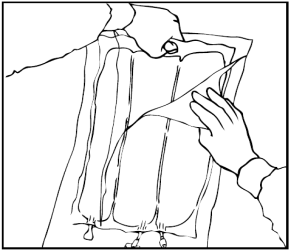
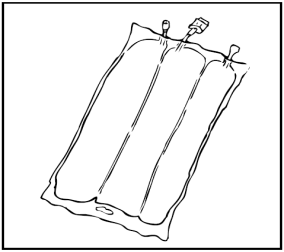
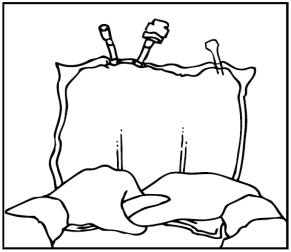

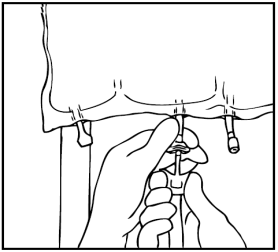
Somministrazione
Solo per uso singolo.
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas
contenuto nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N5E, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
OLIMEL
N7, Emulsione per infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere Vedere paragrafo 4
Contenuto di questo foglio:
- 13. Che cos'è OLIMEL N7 emulsione per infusione e a che cosa serve
- 14. Cosa deve sapere prima che le sia somministrato OLIMEL N7 emulsione per infusione
- 15. Come usare OLIMEL N7, emulsione per infusione
- 16. Possibili effetti indesiderati
- 17. Come conservare OLIMEL N7 emulsione per infusione
- 18. Contenuto della confezione e altre informazioni
1. CHE COS’È OLIMEL N7 E A CHE COSA SERVE
OLIMEL N7 è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio, il secondo un'emulsione di lipidi e il terzo una
soluzione di amminoacidi.
OLIMEL N7 si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante un
tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL N7 deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N7 emulsione per infusione
OLIMEL N7,emulsione per infusione non deve essere usatonei seguenti casi
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è ipersensibile (allergico) alle proteine delle uova, dei semi di soia, dell’ arachide o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito) oppure a uno degli eccipienti. Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- -Se ha livelli di grassi nel sangue particolarmente alti.
- -Se soffre di iperglicemia (troppo zucchero nel sangue) .
In tutti i casi, il medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali età,
peso e condizione medica , insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N7 .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come, sudorazione, febbre, brividi,mal di testa, eruzioni cutanee o difficoltà di
respiro). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N7 contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivanti dal mais (vedere paragrafo “OLIMEL N7, emulsione per infusione
non deve essere usata” sopra)
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento, e la manutenzione del catetere e
durante la preparazione della formula nutrizionale (nutrizione parenterale totale) può ridurre tale
rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine, elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima di
iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti e elementi in tracce, se
ritiene che sia il caso.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o ictus secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà esami
clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato questo
medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare
una “sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati.
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N7 o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N7 le può essere somministrato tramite un tubo (catetere) solo in una grande vena del
torace (vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed elementi in tracce è sempre richiesta. Si devono
utilizzare formulazioni pediatriche.
Altri medicinali e OLIMEL N7
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
OLIMEL N7 non deve essere somministrato contemporaneamente con il sangue attraverso lo stesso
set di infusione.
A causa del rischio di precipitazione, OLIMEL N7 non deve essere somministrato attraverso la stessa
linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina
Gli oli di oliva e di semi di soia in OLIMEL N7 contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
Gravidanza, allattamento e fertilità
Se Lei ha in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando
con latte materno chieda consiglio al medico prima di prendere questo medicinale.
OLIMEL N7 può essere preso in considerazione durante la gravidanza e l’allattamento se necessario
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N7, emulsione per infusione
Dosaggio
OLIMEL N7 deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena .
OLIMEL N7 deve essere a temperatura ambiente prima dell'uso.
OLIMEL N7 è esclusivamente per uso singolo.
L'infusione di una sacca di solito dura tra le 12 e le 24 ore.
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N7.
Se le è stato somministrato più OLIMEL N7, emulsione per infusione di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume del
sangue circolante). I livelli di glucosio nel sangue e nelle sue urine possono aumentare e si può
sviluppare una sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può
aumentare i trigliceridi presenti nel Suo sangue. Ricevere un’ infusione troppo veloce o un volume
eccessivamente alto può causare nausea, vomito, brividi mal di testa, vampate di calore, sudorazione
eccessiva (iperidrosi) e disturbi degli elettroliti. In tali situazioni l’infusione deve essere interrotta
immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di OLIMEL N7, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale , , può causare effetti indesiderati, sebbene non tutte le
persone li manifestino. Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il
trattamento, lo comunichi prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione verrà interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, ad esempio febbre, brividi, mal di testa, eruzioni cutanee o difficoltà respiratorie.
Con OLIMEL N7 sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusionedolore irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 individuo su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi: Febbre Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affannno(anemia). Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia) Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia) Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi Livelli elevati di grassi nel sangue (iperlipidemia) Infiltrazione lipidica epatica (epatomegalia) Deterioramento della funzionalità del fegato Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia).
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia).
- Aumento dei livelli di azoto nel sangue (azotemia)
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo http://www.agenziafarmaco.gov.it/content/come-
segnalare-una-sospetta-reazione-avversa Segnalando gli effetti indesiderati lei può contribuire a
fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare OLIMEL N7, emulsione per infusione
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N7, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
11,1%(corrispondente a 11,1 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico), una emulsione di lipidi al20%(corrispondente a 20,0 g/100 mL)
(olio di oliva purificato e olio di soia purificato) e una soluzione di glucosio al 35%(corrispondente a
35,0 g/100 mL) (come glucosio monoidrato).
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Fosfatide purificato di uovo,
glicerolo, sodio oleato, sodio
idrossido (per l’aggiustamento del
pH), acqua per preparazioni
iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N7, emulsione per infusione e contenuto delle confezioni
OLIMEL N7 è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro una soluzione di amminoacidi e il terzo una
soluzione di glucosio. Questi compartimenti sono separati da membrane non permanenti. Prima
della somministrazione il contenuto dei compartimenti deve essere miscelato arrotolando la sacca su
se stessa partendo dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
Le soluzioni di amminoacidi e di glucosio sono limpide, chiare incolori o leggermente gialle.
L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a tre compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 1.000 mL: 1 scatola con 6 sacche
sacca da 1.500 mL: 1 scatola con 4 sacche
sacca da 2.000 mL: 1 scatola con 4 sacche
1 sacca da 1.000 mL, 1.500 mL e 2.000 mL
È possibile che non tutte le confezioni siano commercializzate.
Per ulteriori informazioni su OLIMEL N7, contatti il rappresentate locale del titolare
dell'autorizzazione all’immissione in commercio:
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80,
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Francia, Portogallo, Estonia, Polonia, Lituania, Bulgaria, Romania, Lettonia, Repubblica Ceca, Belgio,
Spagna, Repubblica Slovacca, Paesi Bassi, Lussemburgo, Slovenia, Italia Danimarca, Islanda, Svezia,
Norvegia, Finlandia, Grecia, Cipro: OLIMEL N7
Austria: Zentro OLIMEL 4,4 % >
Germania: Olimel4,4%
Regno Unito, Irlanda, Malta: Triomel 7g/L nitrogen 1.140 kcal/L
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Categoria farmacoterapeutica: Soluzioni per nutrizione parenterale/combinazioni
Codice ATC: B05 BA10
- E.COMPOSIZIONE QUALITATIVA E QUANTITATIVA
OLIMEL N7 si presenta sotto forma di sacca a 3 compartimenti.
Ogni sacca contiene una soluzione di glucosio, una emulsione di lipidi e una soluzione di
amminoacidi:
Contenuto per sacca
mL
Soluzione di glucosio 35%
(corrispondente a 35 g/100 mL)
400 mL 600 mL 800 mL
mLmL
Soluzione di amminoacidi 11,1%
(corrispondente a 11,1 g/100 mL)
400 mL 600 mL 800 mL
Emulsione di lipidi 20 %
(corrispondente a 20 g/100 mL)
200 mL 300 mL 800 mL
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
Principi attivi1.000 mL1.500 mL2.000 mL
Olio di oliva purificato + olio di soia purificato 40,00 g 60,00 g 80,00 g
Alanina 6,41 g 9,61 g 12,82 g
Arginina 4,34 g 6,51 g 8,68 g
Acido aspartico 1,28 g 1,92 g 2,56 g
Acido glutammico 2,21 g 3,32 g 4,42 g
Glicina 3,07 g 4,60 g 6,14 g
Istidina 2,64 g 3,97 g 5,29 g
Isoleucina 2,21 g 3,32 g 4,42 g
Leucina 3,07 g 4,60 g 6,14 g
Lisina
(equivalente a lisina acetato)
6,97 g
(9,75 g)
Metionina 2,21 g 3,32 g 4,42 g
Fenilalanina 3,07 g 4,60 g 6,14 g
Prolina 2,64 g 3,97 g 5,29 g
Serina 1,75 g 2,62 g 3,50 g
Treonina 2,21 g 3,32 g 4,42 g
Triptofano 0,74 g 1,10 g 1,47 g
Tirosina 0,11 g 0,17 g 0,22 g
Valina 2,83 g 4,25 g 5,66 g
Glucosio anidro
(come Glucosio monoidrato)
3,48 g
(4,88 g)
5,23 g
(7,31 g)
140,00 g
(154,00) g
210,00 g
(231,00 g)
280,00 g
(308,00 g)
Una miscela di olio di oliva purificato (circa 80%) e olio di soia purificato (circa 20%) corrispondente
a un rapporto acidi grassi essenziali / acidi grassi totali del 20%.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
| a
|
| |
| Lipidi | 40 g | 60 g | 80 g |
| Amminoacidi | 44,3 g | F 66,4 g | 88,6 g |
| Azoto | 7,0 g | 10,5 g | 14,0 g |
| Glucosio | 140,0 g | l 210,0 g | 280,0 g |
| Energia: Calorie totali appross. Calorie non proteiche appross. Calorie glucosio Calorie lipidiche appross..(a) Rapporto calorie non proteiche/azoto Rapporto calorie glucosio/lipidi Calorie lipidi/totali | d 1140 kcal 960 kcal 560 kcal a 400 kcal n 137 kcal/g 58/42 35% | e 1710 kcal 1440 kcal 840 kcal 600 kcal 137 kcal/g 58/42 35% | 2270 kcal 1920 kcal 1120 kcal 800 kcal 137 kcal/g 58/42 35% |
| Elettroliti: i Fosfato( b) l acetato | a 3,0 mmol 31 mmol | 4,5 mmol 46 mmol | 6,0 mmol 62 mmol |
| pH appross. | 6,4 | 6,4 | 6,4 |
| a Osmolarità. | 1220 mosm/L | 1220 mosm/L | 1220 mosm/L |
Include calorie da fosfatidi purificati di uovo
Fosfato fornito dall'emulsione di lipidi
- B.POSOLOGIA E MODO DI SOMMINISTRAZIONE
Posologia
L’uso di OLIMEL N7 non è raccomandato nei bambini al di sotto di 2 anni a causa della composizione
e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare il
simultaneamente tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i
pazienti richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca
statica. In tale situazione, qualunque aggiustamento del volume (dose) deve prendere in
considerazione l'effetto risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di
OLIMEL N7. Ad esempio, i pazienti pediatrici possono avere un fabbisogno superiore a
0,2 mmol/kg/giorno di fosfato. In queste circostanze, gli operatori sanitari possono prendere in
considerazione l'aggiustamento del volume (dose) di OLIMEL N7 al fine di soddisfare tale fabbisogno
aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N9E del paziente, oltre che dall’energia o dalle proteine
ulteriori fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di
conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico,
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese. Per Olimel N7 la dose quotidiana massima è definita dall'apporto totale calorico, 40 kcal fornite in un volume di 35 mL/kg, corrispondenti a 1,5 g/kg di amminoacidi, 4,9 g/kg di glucosio, e 1,4 g/kg di lipidi. Per un paziente di 70 kg questo sarebbe equivalente a 2800 mL di OLIMEL N7 al giorno, che si traduce in un apporto di 108 g di amminoacidi, 343 g di glucosio e 98 g di lipidi,(cioè 2352 kcal non proteiche e 2793 kcal totali).
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora e
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
Per OLIMEL N7 la velocità d'infusione massima è 1,7 mL/kg/ora, corrispondenti a 0,08 g/kg/ora per
gli amminoacidi; 0,24 g/kg/ora per il glucosio e 0,07 g/kg/ora per i lipidi.
Nei bambini di età superiore a due anni
Non esistono studi eseguiti sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico del paziente e dalla capacità di
metabolizzare i costituenti di OLIMEL N7, oltre che dall'energia o delle proteine aggiuntive fornite per
via orale/enterale.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, età tra 2 e 11 anni, ed età tra 12 e 18 anni.
Per Olimel N7, nel gruppo di età tra 2 e 11 anni i fattori limitanti sono la concentrazione dei fosfati
per la dose giornaliera (0,2 mmol/kg/die) a e la concentrazione dei lipidi per la velocità oraria. Nel
gruppo di età tra 12 e 18 anni il fattore limitante è la concentrazione degli ammino acidi sia per la
dose giornaliera che per la velocità oraria. Gli apporti risultanti sono mostrati di seguito:
| g Costituenti | Da 2 a 11 anni | Da 12 a 18 anni | |||
| Raccomandatoa | OLIMEL N7 Vol Massimo | Raccomandatoa | OLIMEL N7 Vol Massimo | ||
| A Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| 67 |
| 45 | |
| Amminoacidi (g/kg/d) |
| 2,9 |
| 2,0 | |
| Glucosio (g/kg/d) |
| 9,3 |
| 6,4 | |
- a: Valori raccomandati dalla Linee Guida 2005 ESPGHAN/ ESPEN
- Normalmente, la velocità del flusso si deve aumentare gradualmente durante la prima ora e poi deve essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume giornaliero e la durata dell’infusione.
- In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
- Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva .
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6.
Per la sua alta osmolarità, OLIMEL N7 può essere somministrato solo attraverso una vena centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e 24
ore.Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle
condizioni cliniche del paziente.
- C.INCOMPATIBILITÀ
Non aggiungere altri medicinali o altre sostanze a uno dei tre costituenti della sacca o all'emulsione
ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante
(in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
A causa del rischio di precipitazione, OLIMEL N7 non deve essere somministrato attraverso la stessa
linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di infusione, catetere o cannula.
| 18) | |||||
| Lipidi (g/kg/d) | 0,5 - 3 | 2,7 | 0,5 - 2 (fino a 3) | 1,8 | |
| Energia totale (kcal/kg/d) |
| 76 |
| o 52 | |
| Massima velocità all’ora | |||||
| OLIMEL N7 (mL/kg/h) | 3,3 | c 2,7 | |||
| Amino acidi(g/kg/h) | 0,20 | 0,15 | 0,12 | 0,12 | |
| Glucosio (g/kg/h) | 1,2 | 0,46 | 1,2 | a 0,38 | |
| Lipidi (g/kg/h) | 0,13 | 0,13 | 0,13 | 0,11 | |
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- D.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONE
Una visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N7 viene
illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
elementi in tracce.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Quando si eseguono le aggiunte alle formulazioni contenenti elettroliti, si deve considerare la
quantità di elettroliti già presente nella sacca
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
Valore corrispondente all'aggiunta del fosfato inorganico
Incluso il fosfato fornito dall'emulsione di lipidi
Elementi in tracce e vitamine:
È stata dimostrata la stabilità fino alla dose giornaliera raccomandata.
La compatibilità di altri additivi è disponibile su richiesta.
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- L'operazione deve avvenire in condizione asettica.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
| Per 1.000 mL | |||
| Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | |
| sodio | 0 mmol | 150 mmol | 150 mmol |
| potassio | 0 mmol | 150 mmol | 150 mmol |
| magnesio | 0 mmol | 5,6 mmol | c 5,6 mmol |
| calcio | 0 mmol | 5,0 (3,5(a)) mmol | a 5,0 (3,5a)) mmol |
| Fosfato inorganico | 0 mmol | 8,0 mmol | 8,0 mmol |
| Fosfato organico | 3 mmol (b) | 22 mmol | 25 mmol (b) |
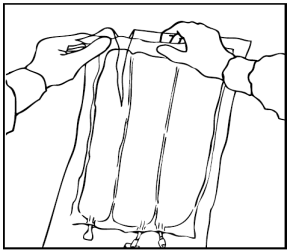
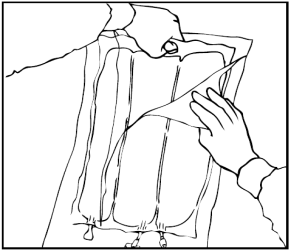
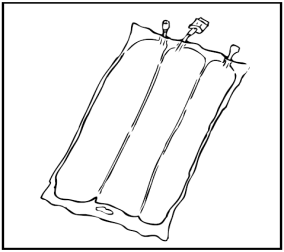
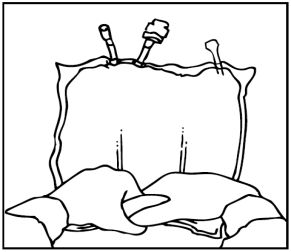

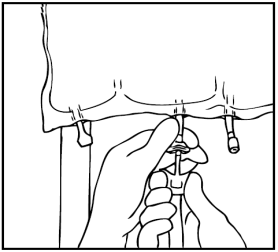
Somministrazione
Solo per uso singolo.
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas
contenuto nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N7, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
OLIMEL
N7E, emulsione per infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 19. Che cos'è OLIMEL N7E emulsione per infusione e a che cosa serve
- 20. Cosa deve sapere prima che le sia somministrato OLIMEL N7E emulsione per infusione
- 21. Come usare OLIMEL N7E, emulsione per infusione
- 22. Possibili effetti indesiderati
- 23. Come conservare OLIMEL N7E emulsione per infusione
- 24. Contenuto della confezione e altre informazioni
1. Che cos’è OLIMEL N7E, emulsione per infusione e a che cosa serve
OLIMEL è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio con calcio, il secondo un'emulsione di lipidi e il
terzo una soluzione di amminoacidi con altri elettroliti.
OLIMEL si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante un
tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N7E, emulsione per infusione
OLIMEL N7E, emulsione per infusionenon deve essere usato:
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è ipersensibile (allergico) alle proteine delle uova, dei semi di soia, dell’arachide o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito), oppure a uno degli eccipienti.
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se soffre di iperglicemia (troppo zucchero nel sangue).
- Se ha una concentrazione abnormemente alta di uno qualsiasi degli elettroliti (sodio, potassio, magnesio, calcio e/o fosforo) nel sangue.
In tutti i casi, il medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali età,
peso e condizione medica , insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N7E .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come sudorazione, febbre, brividi, mal di testa, rush cutanei o respirazione
difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N7E contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivanti dal mais (vedere paragrafo “OLIMEL N7E, emulsione per
infusione non deve essere usata” sopra)
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
L'antibiotico denominato ceftriaxone non deve essere miscelato o somministrato simultaneamente
con qualsiasi soluzione contenente calcio (compreso OLIMEL N7E) che le viene somministrata
mediante una flebo in vena.
Questi medicinali non le devono essere somministrati neanche mediante linee di infusione diverse o
sedi di infusione diverse.
Tuttavia, lei potrà assumere OLIMEL N7E e ceftriaxone in sequenza, uno dopo l'altro, se si utilizzano
linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state
accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di
precipitati (particelle di sale di calcio-ceftriaxone).
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento e la manutenzione del catetere e durante
la preparazione della formula nutrizionale (nutrizione parenterale totale può ridurre tale rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine, elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima di
iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti ed elementi in tracce, se
ritiene che sia il caso.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o ictus secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà esami
clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato questo
medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare una
“sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N7E o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N7E le può essere somministrato tramite un tubo (catetere) solo in una grande vena del
torace (vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed elementi in tracce è sempre richiesta. Si devono
utilizzare formulazioni pediatriche.
Altri medicinali e OLIMEL N7E
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
OLIMEL N7E non deve essere somministrato contemporaneamente con il sangue attraverso lo stesso
set di infusione.
OLIMEL N7E contiene calcio. Non deve essere somministrato insieme all’antibiotico cefriaxone o
attraverso lo stesso tubo, perché si possono formare delle particelle. Se si utilizza lo stesso
dispositivo per somministrarle questi medicinali in successione, il dispositivo deve essere
accuratamente lavato.
A causa del rischio di precipitazione, OLIMEL N7E non deve essere somministrato attraverso la
stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL N7E contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
OLIMEL N7E contiene potassio. Porre particolare attenzione con i pazienti che assumono diuretici,
inibitori dell’ACE, antagonisti del recettore dell’angiotensina II (farmaci per la cura dell’ipertensione)
o immunosoppressivi. Questi tipi di farmaci possono aumentare i livelli di potassio nel sangue.
Gravidanza, allattamento e fertilità
Se Lei ha in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando
con latte materno chieda consiglio al medico prima di prendere questo medicinale.
OLIMEL N7E può essere preso in considerazione durante la gravidanza e l’allattamento se necessario
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N7E, emulsione per infusione
Dosaggio
OLIMEL deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena del
suo torace.
OLIMEL deve essere a temperatura ambiente prima dell'uso.
OLIMEL N7E è esclusivamente per uso singolo.
l'infusione di 1 sacca dura di solito da 12 a 24 ore
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N7E.
Se le è stato somministrato più OLIMEL N7E, emulsione per infusione di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume de l
sangue circolante). I livelli di glucosio nel sangue e nelle urine possono aumentare e si può sviluppare
una sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può aumentare il
livello di trigliceridi presenti nel Suo sangue. Ricevere un’infusione troppo veloce o un volume di
OLIMEL N7E troppo grande può causare nausea, vomito, brividi mal di testa, vampate di calore,
sudorazione eccessiva (iperidrosi) e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere
interrotta immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di questo prodotto , si rivolga al medico.
4. POSSIBILI EFFETTI INDESIDERATI
Come tutti i medicinali, questo medicinale , può causare effetti indesiderati, sebbene non tutte le
persone li manifestino. Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il
trattamento, lo comunichi prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione verrà interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, come sudorazione, febbre, brividi, mal di testa, rash cutanei o difficoltà nella
respirazione.
Con OLIMEL N7E sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione). Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore, irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 individuo su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- Febbre
- Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno (anemia).
- Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- Livelli elevati di grassi nel sangue (iperlipidemia)
- Infiltrazione lipidica epatica (epatomegalia)
- Deterioramento della funzionalità del fegato
- Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenza- Non nota: frequenza non definibile sulla base dei dati disponibili:
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia).
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia).
- Aumento dei livelli di azoto nel sangue (azotemia)
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo : http://www.agenziafarmaco.gov.it/content/come-
segnalare-una-sospetta-reazione-avversa. Segnalando gli effetti indesiderati lei può contribuire a
fornire maggiori informazioni sulla sicurezza di questo medicina
5. Come conservare OLIMEL N7E emulsione per infusione
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini .
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del mese.
Non congelare.
Conservare nell'involucro esterno
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista
come eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente .
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N7E, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
11,1%(corrispondente a 11,1 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico) con elettroliti (sodio, potassio, magnesio, fosfato, acetato,
cloruro), una emulsione di lipidi al20%(corrispondente a 20 g/100 mL) (olio di oliva purificato e olio
di soia purificato) e una soluzione di glucosio al 35%(corrispondente a 35 g/100 mL) (come glucosio
monoidrato) con calcio.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Fosfatide purificato di uovo,
glicerolo, sodio oleato, sodio
idrossido (per l’aggiustamento del
pH), acqua per preparazioni
iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N7E, emulsione per infusione e contenuto delle confezioni
OLIMEL N7E è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro compartimento una soluzione di
amminoacidi con elettroliti ed il terzo compartimento una soluzione di glucosio con calcio. Questi
compartimenti sono separati da membrane non permanenti. Prima della somministrazione il
contenuto dei compartimenti deve essere miscelato arrotolando la sacca su se stessa partendo
dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
Le soluzioni di amminoacidi e di glucosio sono limpide, chiare incolori o leggermente gialle.
L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 1.000 mL: 1 scatola con 6 sacche
sacca da 1.500 mL: 1 scatola con 4 sacche
sacca da 2.000 mL: 1 scatola con 4 sacche
1 sacca da 1.000 mL, 1.500 mL e 2.000 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80,
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Francia, Portogallo, Estonia, Polonia, Lituania, Bulgaria, Romania, Lettonia, Repubblica Ceca, Belgio,
Spagna, Repubblica Slovacca, Paesi Bassi, Lussemburgo, Slovenia, Italia, Danimarca, Islanda, Svezia,
Norvegia, Finlandia, Grecia, Cipro : OLIMEL N7E
Austria: ZentroOLIMEL 4,4 % mit Elektrolyten >
Germania: Olimel 4,4% E
Regno Unito, Irlanda, Malta: Triomel 7g/L nitrogen 1140 kcal/L with electrolytes
Ungheria: Olimel 7 g/L nitrogén elektrolitokkal emulziós infúzió
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Categoria farmacoterapeutica: Soluzioni per nutrizione parenterale/combinazioni
Codice ATC: B05 BA10
- F.COMPOSIZIONE QUALITATIVA E QUANTITATIVA
OLIMEL N7E si presenta sotto forma di sacca a 3 compartimenti.
Ogni sacca contiene una soluzione di glucosio con calcio, una emulsione di lipidi e una soluzione di
amminoacidi con altri elettroliti:
Contenuto per sacca
1.000 mL 1.500 mL 2.000 mL
Soluzione di glucosio 35%
(corrispondente a 35 g/100 mL)
400 mL 600 mL 800 mL
Soluzione di amminoacidi 11,1%
(corrispondente a 11,1 g/100 mL)
400 mL 600 mL 800 mL
Emulsione di lipidi 20%
(corrispondente a 20 g/100 mL)
200 mL 300 mL 400 mL
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
Principi attivi1.000 mL1.500 mL2.000 mL
Olio di oliva purificato + olio di soia purificato 40,00 g 60,00 g 80,00 g
Alanina 6,41 g 9,61 g 12,82 g
Arginina 4,34 g 6,51 g 8,68 g
Acido aspartico 1,28 g 1,92 g 2,56 g
Acido glutammico 2,21 g 3,32 g 4,42 g
Glicina 3,07 g 4,60 g 6,14 g
Istidina 2,64 g 3,97 g 5,29 g
Isoleucina 2,21 g 3,32 g 4,42 g
Leucina 3,07 g 4,60 g 6,14 g
Lisina
(equivalente a lisina acetato)
6,97 g
(9,75g)
Metionina 2,21 g 3,32 g 4,42 g
Fenilalanina 3,07 g 4,60 g 6,14 g
Prolina 2,64 g 3,97 g 5,29 g
Serina 1,75 g 2,62 g 3,50 g
Treonina 2,21 g 3,32 g 4,42 g
Triptofano 0,74 g 1,10 g 1,47 g
Tirosina 0,11 g 0,17 g 0,22 g
Valina 2,83 g 4,25 g 5,66 g
Sodio acetato, triidrato 1,50 g 2,24 g 2,99 g
Sodio glicerofosfato idrato 3,67 g 5,51 g 7,34 g
Potassio cloruro 2,24 g 3,35 g 4,47 g
Magnesio cloruro, esaidrato 0,81 g 1,22 g 1,62 g
Calcio cloruro, biidrato 0,52 g 0,77 g 1,03 g
Glucosio anidro
(equivalente a Glucosio monoidrato)
3,48 g
(4,88 g)
5,23 g
(7,31 g)
140,00 g
(154,00 g)
210,00 g
(231,00 g)
280,00 g
(308,00 g)
Una miscela di olio di oliva purificato (circa 80%) e olio di soia purificato (circa 20%) corrispondente
a un rapporto acidi grassi essenziali / acidi grassi totali del 20%.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
| n |
|
|
|
| e Lipidi | 40 g | 60 g | 80 g |
| Amminoacidi | 44,3 g | 66,4 g | 88,6 g |
| g Azoto | 7,0 g | 10,5 g | 14,0 g |
| Glucosio | 140,0 g | 210,0 g | 280,0 g |
| A Energia: Calorie totali appross. Calorie non proteiche. Calorie glucosio Calorie lipidiche.(a) |
|
|
|
Include calorie da fosfatidi purificati di uovo
Include fosfato fornito dall'emulsione di lipidi
- G.POSOLOGIA E MODO DI SOMMINISTRAZIONEPosologia L’uso di OLIMEL N7E non è raccomandato nei bambini al di sotto di 2 anni a causa della composizione e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare simultaneamente
tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i pazienti
richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca statica. In tale
situazione, qualunque aggiustamento del volume (dose) deve prendere in considerazione l'effetto
risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di OLIMEL N7E. Ad esempio, i
pazienti pediatrici possono avere un fabbisogno superiore a 0,2 mmol/kg/giorno di fosfato. In queste
circostanze, gli operatori sanitari possono prendere in considerazione l'aggiustamento del volume
(dose) di OLIMEL N7E al fine di soddisfare tale fabbisogno aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N7E del paziente, oltre che dall’energia o dalle proteine
ulteriori fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di
conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico,
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per Olimel N7E la dose quotidiana massima è definita dall'apporto totale calorico, 40 kcal fornite in
un volume di 35 mL/kg, corrispondenti a 1,5g/kg amminoacidi, 4,9 g/kg glucosio, e 1,4 g/kg lipidi,1,2
mmol/kg sodio e 1,1 mmol/kg potassio. Per un paziente di 70 kg questo sarebbe equivalente a 2450
mL di OLIMEL N7E al giorno, che si traduce in un apporto di 108g amminoacidi, 343 g glucosio e 98 g
lipidi (cioè 2352 kcal non proteiche e 2793 kcal totali).
| Rapporto calorie non proteiche/azoto Rapporto calorie glucosio/lipidi Calorie lipidi/totali | 137 kcal/g 58/42 35% | 137 kcal/g 58/42 35% | 137 kcal/g o 58/42 35% |
| Elettroliti: sodio potassio magnesio calcio Fosfato (b) acetato cloruro | 35,0 mmol 30,0 mmol 4,0 mmol 3,5 mmol 15,0 mmol 45 mmol 45 mmol | 52,5 mmol 45,0 mmol m 6,0 mmol 5,3 mmol 22,5 mmol r 67 mmol 68 mmol | c 70,0 mmol a 60,0 mmol 8,0 mmol 7,0 mmol 30,0 mmol 89 mmol 90 mmol |
| pH. | 6,4 | 6,4 | 6,4 |
| Osmolarità. |
| a
|
|
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
Per OLIMEL N7E la velocità d'infusione massima è 1,7 mL/kg/ora, corrispondenti a 0,08 g/kg/ora
amminoacidi, 0,24 g/kg/ora glucosio e 0,07 g/kg/ora lipidi.
Nei bambini di età superiore a due anni
Non esistono studi eseguiti sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N7E del paziente, oltre che da energia o proteine ulteriori
fornite oralmente/enteralmente, pertanto, i formati della sacca devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, età tra 2 e 11 anni, ed età tra 12 e 18 anni.
Per Olimel N7E, nel gruppo di età tra 2 e 11 anni i fattori limitanti sono la concentrazione dei fosfati
per la dose giornaliera (0,2 mmol/kg/die)a e la concentrazione dei lipidi per la velocità oraria. Nel
gruppo di età tra 12 e 18 anni i fattori limitanti sono la concentrazione dei fosfati per la dose
giornaliera (0,2 mmol/kg/die)a e la concentrazione degli amminoacidi per la velocità oraria. Gli
apporti risultanti sono mostrati di seguito:
| Costituenti | Da 2 a 11 anni | Da 12 a 18 anni | |||
| Raccomandatoa | a n OLIMEL N7E Vol Massimo | Raccomandatoa | OLIMEL N7E Vol Massimo | ||
| Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| a 13 |
| 13 | |
| Amminoacidi (g/kg/d) |
| 0,6 |
| 0,6 | |
| Glucosio (g/kg/d) | i l
| 1,9 |
| 1,9 | |
| Lipidi (g/kg/d) | a 0,5 - 3 | 0,5 |
| 0,5 | |
| Energia totale (kcal/kg/d) | t
| 15 |
| 15 | |
| I Massima velocità all’ora | |||||
| OLIMEL N7E (mL/kg/h) | 3,3 | 2,7 | |||
| Amino acidi(g/kg/h) | a 0,20 | 0,15 | 0,12 | 0,12 | |
| Glucosio (g/kg/h) | i 1,2 | 0,46 | 1,2 | 0,38 | |
| z Lipidi (g/kg/h) | 0,13 | 0,13 | 0,13 | 0,11 | |
a: Valori raccomandati dalla Linee Guida 2005 ESPGHAN/ ESPEN
Normalmente, la velocità del flusso si deve aumentare gradualmente durante la prima ora e poi deve
essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume
giornaliero e la durata dell’infusione
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e
di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva. .
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6.
Per la sua alta osmolarità, OLIMEL N7E può essere somministrato solo attraverso una vena centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e
24 ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle condizioni
cliniche del paziente.
- E.INCOMPATIBILITÀNon aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
OLIMEL N7E contiene ioni calcio che rappresentano un rischio ulteriore di coagulazione nel sangue o
in emocomponenti anticoagulati o conservati con citrato.
Il ceftriaxone non deve essere miscelato o somministrato in concomitanza con soluzioni endovenose
contenenti calcio, compreso OLIMEL N7E, attraverso la stessa linea di infusione (per es., tramite un
connettore a Y) a causa del rischio di precipitazione del sale di ceftriaxone-calcio (vedere paragrafi
- 4.4 e 4.5 dell’RCP). Il ceftriaxone e le soluzioni contenenti calcio possono essere somministrati in sequenza uno dopo l'altro se si utilizzano linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di precipitati. A causa del rischio di precipitazione, OLIMEL N7E non deve essere somministrato attraverso la stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di somministrazione, catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- F.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONE
Una visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N7E viene
illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
elementi in tracce.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Quando si eseguono le aggiunte alle formulazioni contenenti elettroliti, si deve considerare la
quantità di elettroliti già presente nella sacca
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
OLIMEL N7E si può integrare con elettroliti, sulla base della tabella seguente:
| e Per 1.000 mL | |||
| g | Livello incluso | Aggiunta ulteriore massima | Livello totale massimo |
| sodio | 35 mmol | 115 mmol | 150 mmol |
| potassio | 30 mmol | 120 mmol | 150 mmol |
| A magnesio | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| calcio | 3,5 mmol | 1,5 (0,0(a)) mmol | 5,0 (3,5(a)) mmol |
| Fosfato inorganico | 0 mmol | 3,0 mmol | 3,0 mmol |
| Fosfato organico | 15 mmol (b) | 10 mmol | 25 mmol (b) |
Valore corrispondente all'aggiunta del fosfato inorganico
Incluso il fosfato fornito dall'emulsione di lipidi
Elementi in tracce e vitamine:
La stabilità è stata dimostrata con preparazioni di vitamine e oligoelementi in commercio (contenenti
al massimo 1 mg di ferro).
La compatibilità di altri additivi è disponibile su richiesta.
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- L'operazione deve avvenire in condizione asettica.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
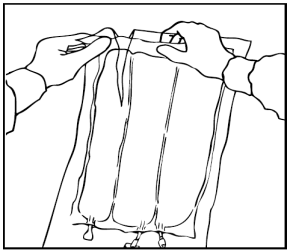
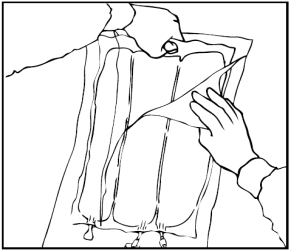
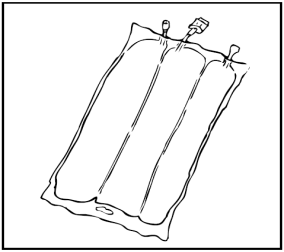
1 2 3
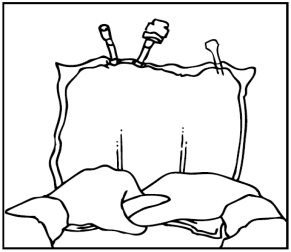

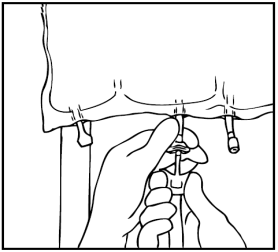
4 5 6
Somministrazione
Solo per uso singolo.
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas
contenuto nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N7E, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
OLIMEL
N9, emulsione per infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere Vedere paragrafo 4
Contenuto di questo foglio:
- 25. Che cos'è OLIMEL N9 emulsione per infusione e a che cosa serve
- 26. Cosa deve sapere prima che le sia somministrato OLIMEL N9 emulsione per infusione
- 27. Come usare OLIMEL N9, emulsione per infusione
- 28. Possibili effetti indesiderati
- 29. Come conservare OLIMEL N9 emulsione per infusione
- 30. Contenuto della confezione e altre informazioni
1. Che cos’è OLIMEL N9 emulsione per infusione e a che cosa serve
OLIMEL N9 è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio, il secondo un'emulsione di lipidi e il terzo una
soluzione di amminoacidi.
OLIMEL N9 si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante un
tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL N9 deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N9 emulsione per infusione
OLIMEL N9 emulsione per infusione non deve essere usato nei seguenti casi
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è ipersensibile (allergico) alle proteine delle uova, dei semi di soia, dell’arachide o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito), oppure a uno degli eccipienti.
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se soffre di iperglicemia (troppo zucchero nel sangue) .
In tutti i casi, il medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali età,
peso e condizione medica , insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N9 .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come sudorazione, febbre, brividi, mal di testa, rush cutanei o respirazione
difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N9 contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivati dal mais (vedere paragrafo “OLIMEL N9, emulsione per infusione
non deve essere usata” sopra)
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento, , e la manutenzione del catetere e
durante la preparazione della formula nutrizionale (nutrizione parenterale totale) può ridurre tale
rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine, elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima di
iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti ed elementi in tracce, se
ritiene che sia il caso.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o ictus secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà esami
clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato questo
medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare una
“sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N9 o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N9 le può essere somministrato tramite un tubo (catetere) in una grande vena del torace
(vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed elementi in tracce è sempre richiesta. Si devono
utilizzare formulazioni pediatriche.
Altri medicinali e OLIMEL N9
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
OLIMEL N9 non deve essere somministrato contemporaneamente con il sangue attraverso lo stesso
set di infusione.
A causa del rischio di precipitazione, OLIMEL N9 non deve essere somministrato attraverso la stessa
linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL N9 contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
Gravidanza, allattamento e fertilità
Se Lei è in gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con latte
materno chieda consiglio al medico prima di prendere questo medicinale.
OLIMEL N9 può essere preso in considerazione durante la gravidanza e l’allattamento se necessario
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N9 emulsione per infusione
Dosaggio
OLIMEL deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena del
suo torace.
OLIMEL deve essere a temperatura ambiente prima dell'uso.
OLIMEL N9è esclusivamente per uso singolo.
L'infusione di 1 sacca dura di solito da 12 a 24 ore.
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N9.
Se le è stato somministrato più OLIMEL N9, emulsione per infusione di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume del
sangue circolante). I livelli di glucosio nel sangue e nelle urine può aumentare e si può sviluppare una
sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può aumentare il livello
di trigliceridi presenti nel Suo sangue. Ricevere un’ infusione troppo veloce o un volume di OLIMEL
N9 troppo grande può causare nausea, vomito, brividi mal di testa, vampate di calore, sudorazione
eccessiva (iperidrosi) e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere interrotta
immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di OLIMEL N9, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale, può causare effetti indesiderati, sebbene non tutte le
persone li manifestino. Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il
trattamento, lo comunichi prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione verrà interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, ad esempio febbre, brividi, mal di testa, eruzioni cutanee o difficoltà respiratorie.
Con OLIMEL N9 sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10:
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione). Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore, irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 individuo su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti segni di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- Febbre
- Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno (anemia).
- Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- Livelli elevati di grassi nel sangue (iperlipidemia)
- Infiltrazione lipidica epatica (epatomegalia)
- Deterioramento della funzionalità del fegato
- Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenza Non nota: frequenza non definibile sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia).
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia).
- Aumento dei livelli di azoto nel sangue (azotemia).
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo: http://www.agenziafarmaco.gov.it/content/come-
segnalare-una-sospetta-reazione-avversa. Segnalando gli effetti indesiderati lei può contribuire a
fornire maggiori informazioni sulla sicurezza di questo medicinale
5. Come conservare OLIMEL N9, emulsione per infusione
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini .
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N9, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
14,2%(corrispondente a 14,2 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico), una emulsione di lipidi al20%(corrispondente a 20,0 g/100 mL)
(olio di oliva purificato e olio di soia purificato) e una soluzione di glucosio al 27,5%(corrispondente
a 27,5 g/100 mL) (come glucosio monoidrato).
Gli eccipienti sono:
CompartimentoCompartimentoCompartimento
Emulsione di lipidiSoluzione di amminoacidiSoluzione di glucosio
Fosfatide purificato di uovo,
glicerolo, sodio oleato, sodio
idrossido (per l’aggiustamento del
pH), acqua per preparazioni
iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N9, emulsione per infusione e contenuto delle confezioni
OLIMEL N9 è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro compartimento una soluzione di
amminoacidi con elettroliti ed il terzo compartimento una soluzione di glucosio con calcio. Questi
compartimenti sono separati da membrane non permanenti. Prima della somministrazione il
contenuto dei compartimenti deve essere miscelato arrotolando la sacca su se stessa partendo
dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
- Le soluzioni di amminoacidi e di glucosio sono limpide, chiare incolori o leggermente gialle.
- L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 1.000 mL: 1 scatola con 6 sacche
sacca da 1.500 mL: 1 scatola con 4 sacche
sacca da 2.000 mL: 1 scatola con 4 sacche
1 sacca da 1.000 mL, 1.500 mL e 2.000 mL.
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80,
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Francia, Portogallo, Estonia, Polonia, Lituania, Bulgaria, Romania, Lettonia, Repubblica Ceca, Belgio,
Spagna, Repubblica Slovacca, Paesi Bassi, Lussemburgo, Slovenia, Italia, Danimarca, Islanda, Svezia,
Norvegia, Finlandia, Grecia, Cipro : OLIMEL N9
Austria: ZentroOLIMEL 5,7 % >
Germania: Olimel 5,7%
Regno Unito, Irlanda, Malta: Triomel 9g/L nitrogen 1070 kcal/L
Ungheria: Olimel 9 g/L nitrogén emulziós infúzió
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Categoria farmacoterapeutica: Soluzioni per nutrizione parenterale/combinazioni
Codice ATC: B05 BA10
- H.COMPOSIZIONE QUALITATIVA E QUANTITATIVAOLIMEL N9 si presenta sotto forma di sacca a 3 compartimenti.
Ogni sacca contiene una soluzione di glucosio, una emulsione di lipidi e una soluzione di
amminoacidi:
Contenuto per sacca
1.000 mL 1.500 mL 2.000 mL
Soluzione di glucosio 27,5%
(corrispondente a 27,5 g/100 mL)
400 mL 600 mL 800 mL
Soluzione di amminoacidi 14,2% 400 mL 600 mL 800 mL
(corrispondente a 14,2 g/100 mL)
Emulsione di lipidi 20 %
(corrispondente a 20 g/100 mL)
200 mL 300 mL 400 mL
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
Principi attivi1.000 mL1.500 mL2.000 mL
Olio di oliva purificato + olio di soia purificato 40,00 g 60,00 g 80,00 g
Alanina 8,24 g 12,36 g 16,48 g
Arginina 5,58 g 8,37 g 11,16 g
Acido aspartico 1,65 g 2,47 g 3,30 g
Acido glutammico 2,84 g 4,27 g 5,69 g
Glicina 3,95 g 5,92 g 7,90 g
Istidina 3,40 g 5,09 g 6,79 g
Isoleucina 2,84 g 4,27 g 5,69 g
Leucina 3,95 g 5,92 g 7,90 g
Lisina
(equivalente a lisina acetato)
8,96 g
(12,64 g)
Metionina 2,84 g 4,27 g 5,69 g
Fenilalanina 3,95 g 5,92 g 7,90 g
Prolina 3,40 g 5,09 g 6,79 g
Serina 2,25 g 3,37 g 4,50 g
Treonina 2,84 g 4,27 g 5,69 g
Triptofano 0,95 g 1,42 g 1,90 g
Tirosina 0,15 g 0,22 g 0,30 g
Valina 3,64 g 5,47 g 7,29 g
Glucosio anidro
(come glucosio monoidrato)
4,48 g
(6,32 g)
6,72 g
(9,48 g)
110,00 g
(121,00 g)
165,00 g
(181,50 g)
220,00 g
(242,00 g)
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Fosfatide purificato di uovo,
glicerolo, sodio oleato, sodio
idrossido (per l’aggiustamento del
pH), acqua per preparazioni
iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
|
|
| |
| g Lipidi | 40 g | 60 g | 80 g |
| Amminoacidi | 56,9 g | 85,4 g | 113,9 g |
| A Azoto | 9,0 g | 13,5 g | 18,0 g |
| Glucosio | 110,0 g | 165,0 g | 220,0 g |
| Energia: Calorie totali appross. | 1070 kcal | 1600 kcal | 2140 kcal |
Include calorie da fosfatidi purificati di uovo
Include fosfato fornito dall'emulsione di lipidi
- C.POSOLOGIA E MODO DI SOMMINISTRAZIONEPosologia L’uso di OLIMEL N9 non è raccomandato nei bambini al di sotto di 2 anni a causa della composizione e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare simultaneamente
tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i pazienti
richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca statica. In tale
situazione, qualunque aggiustamento del volume (dose) deve prendere in considerazione l'effetto
risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di OLIMEL N9. Ad esempio, i
pazienti pediatrici possono avere un fabbisogno superiore a 0,2 mmol/kg/giorno di fosfato. In queste
circostanze, gli operatori sanitari possono prendere in considerazione l'aggiustamento del volume
(dose) di OLIMEL N9 al fine di soddisfare tale fabbisogno aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N9 del paziente, oltre che dall’energia o dalle proteine ulteriori
fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico,
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per OLIMEL N9 la dose quotidiana massima è definita dall'apporto fluidi degli amminoacidi, 35
mL/kg, corrispondenti a 2,0 g/kg amminoacidi, 3,9 g/kg glucosio e 1,4 g/kg lipidi. Per un paziente di
70 kg questo sarebbe equivalente a 2450 mL di OLIMEL N9 al giorno, che si traduce in un apporto di
140 g amminoacidi, 270 g glucosio e 98 g lipidi, (cioè 2058 kcal non proteiche e 2622 kcal totali).
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
| Calorie non proteiche. Calorie glucosio Calorie lipidiche..(a) Rapporto calorie non proteiche/azoto Rapporto calorie glucosio/lipidi Calorie lipidi/totali | 840 kcal 440 kcal 400 kcal 93 kcal/g 52/48 37% | 1260 kcal 660 kcal 600 kcal 93 kcal/g 52/48 37% | 1680 kcal 880 kcal 800 kcal c 93 kcal/g 52/48 37% |
| Elettroliti: Fosfato (b) acetato | 3,0 mmol 40 mmol | 4,5 mmol 60 mmol | a m 6,0 mmol 80 mmol |
| pH appross. | 6,4 | 6,4 | 6,4 |
| Osmolarità. | 1170 mosm/L | 1170 mosm/L | r 1170 mosm/L |
Per OLIMEL N9 la velocità d'infusione massima è 1,8 mL/kg/ora, corrispondenti a 0,10 g/kg/ora
amminoacidi; 0,19 g/kg/ora glucosio e 0,07 g/kg/ora lipidi.
Nei bambini di età superiore a due anni
Non esistono studi eseguiti sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N9 del paziente, oltre che da energia o proteine ulteriori fornite
oralmente/enteralmente, pertanto, i formati della sacca devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, età tra 2 e 11 anni, ed età tra 12 e 18 anni.
Per Olimel N9 nel gruppo da 2 a 11 anni di età, i fattori limitanti sono la concentrazione di
amminoacidi per la dose giornaliera e la concentrazione dei lipidi per la velocità oraria Nel gruppo da
12 a 18 anni di età, i fattori limitanti sono la concentrazione di amminoacidi sia per la dose
giornaliera che per la velocità oraria. Gli apporti risultanti sono mostrati di seguito:
| Costituenti | Da 2 a 11 anni | l Da 12 a 18 anni | |||
| Raccomandatoa | e OLIMEL N9 Vol Massimo | Raccomandatoa | OLIMEL N9 Vol Massimo | ||
| d Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| 53 |
| 45 | |
| Amminoacidi (g/kg/d) |
| 3 |
| 2 | |
| Glucosio (g/kg/d) |
| a 5,8 |
| 3,9 | |
| Lipidi (g/kg/d) | 0,5 - 3 | n 2,1 | 0,5 - 2 (fino a 3) | 1,4 | |
| Energia totale (kcal/kg/d) |
| a 56 |
| 37 | |
| Massima velocità all’ora | |||||
| OLIMEL N9 (mL/kg/h) | i | 3,3 | 2,1 | ||
| Amino acidi(g/kg/h) | l 0,20 | 0,19 | 0,12 | 0,12 | |
| Glucosio (g/kg/h) | a 1,2 | 0,36 | 1,2 | 0,23 | |
| Lipidi (g/kg/h) | 0,13 | 0,13 | 0,13 | 0,08 | |
a: Valori raccomandati dalla Linee Guida 2005 ESPGHAN/ ESPEN
Normalmente, la velocità del flusso si deve aumentare gradualmente durante la prima ora e poi deve
essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume
giornaliero e la durata dell’infusione.
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e
di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva.
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6.
Per la sua alta osmolarità, OLIMEL N9 può essere somministrato solo attraverso una vena centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e 24
ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle condizioni
cliniche del paziente.
- C.INCOMPATIBILITÀNon aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
A causa del rischio di precipitazione, OLIMEL N9 non deve essere somministrato attraverso la stessa
linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di somministrazione, catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- D.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONEUna visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N9 viene illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
elementi in tracce.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Quando si eseguono le aggiunte alle formulazioni contenenti elettroliti, si deve considerare la
quantità di elettroliti già presente nella sacca
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
OLIMEL N9 si può integrare con elettroliti, sulla base della tabella seguente:
| e Per 1.000 mL | |||
| Livello incluso | d Aggiunta ulteriore massima | Livello totale massimo | |
| sodio | 0 mmol | 150 mmol | 150 mmol |
| potassio | 0 mmol | 150 mmol | 150 mmol |
| magnesio | 0 mmol | a 5,6 mmol | 5,6 mmol |
| calcio | 0 mmol | 5,0 (3,5(a)) mmol | 5,0 (3,5a)) mmol |
| Fosfato inorganico | 0 mmol | n 8,0 mmol | 8,0 mmol |
| Fosfato organico | 3 mmol (b) | a 22 mmol | 25 mmol (b) |
Valore corrispondente all'aggiunta del fosfato inorganico
Incluso il fosfato fornito dall'emulsione di lipidi
Elementi in tracce e vitamine:
La stabilità è stata dimostrata con preparazioni di vitamine e oligoelementi in commercio (contenenti
al massimo 1 mg di ferro).
La compatibilità di altri additivi è disponibile su richiesta.
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- L'operazione deve avvenire in condizione asettica.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
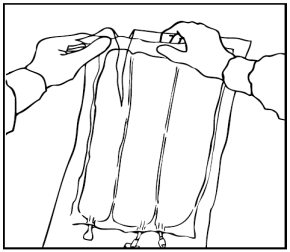
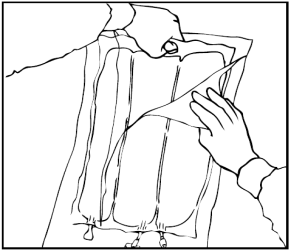
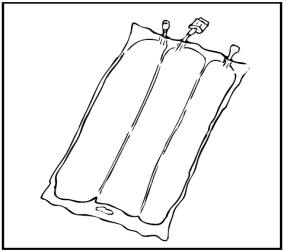
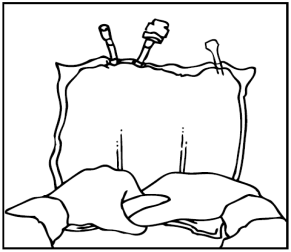

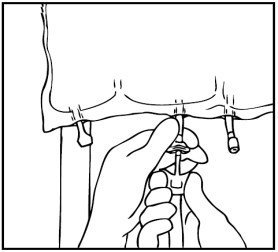
Somministrazione
Solo per uso singolo.
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas
contenuto nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N9, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno.
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
OLIMEL
N9E emulsione per infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 31. Che cos'è OLIMEL N9E emulsione per infusione e a che cosa serve
- 32. Cosa deve sapere prima che le sia somministrato OLIMEL N9E emulsione per infusione
- 33. Come usare OLIMEL N9E, emulsione per infusione
- 34. Possibili effetti indesiderati
- 35. Come conservare OLIMEL N9E emulsione per infusione
- 36. Contenuto della confezione e altre informazioni
1. Che cos’è OLIMEL N9E emulsione per infusione e a che cosa serve
OLIMEL N9E è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio con calcio, il secondo un'emulsione di lipidi e il
terzo una soluzione di amminoacidi con altri elettroliti.
OLIMEL N9E si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante
un tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL N9E deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N9E emulsione per infusione
OLIMEL N9E emulsione per infusione non deve essere usato nei seguenti casi
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è ipersensibile (allergico) alle proteine delle uova, dei semi di soia, dell’arachide o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito), oppure a uno degli eccipienti.
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se soffre di iperglicemia (troppo zucchero nel sangue) .
- Se ha una concentrazione abnormemente alta di uno qualsiasi degli elettroliti (sodio, potassio, magnesio, calcio e/o fosforo) nel sangue .
In tutti i casi, il suo medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali
età, peso e condizione medica , insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N9E .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come sudorazione, febbre, brividi, mal di testa, rush cutanei o respirazione
difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N9E contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivanti dal mais (vedere paragrafo “OLIMEL N9E, emulsione per
infusione non deve essere usata” sopra)
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
L'antibiotico denominato ceftriaxone non deve essere miscelato o somministrato simultaneamente
con qualsiasi soluzione contenente calcio (compreso OLIMEL N9E) che le viene somministrata
mediante una flebo in vena.
Questi medicinali non le devono essere somministrati insieme neanche mediante linee di infusione
diverse o sedi di infusione diverse.
Tuttavia, lei potrà assumere OLIMEL N9E e ceftriaxone in sequenza, uno dopo l'altro, se si utilizzano
linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state
accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di
precipitati (particelle di sale di calcio-ceftriaxone).
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento, e la manutenzione del catetere e
durante la preparazione della formula nutrizionale (nutrizione parenterale totale) può ridurre tale
rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima
di iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti ed elementi in tracce, se
ritiene che sia il caso.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o ictus secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà esami
clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato questo
medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare una
“sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N9E o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N9E le può essere somministrato tramite un tubo (catetere) in una grande vena del torace
(vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed elementi in tracce è sempre richiesta. Si devono
utilizzare formulazioni pediatriche.
Altri medicinali eOLIMEL N9E
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
OLIMEL N9E non deve essere somministrato contemporaneamente con il sangue attraverso lo stesso
set di infusione.
OLIMEL N9E contiene calcio. Non deve essere somministrato insieme all’antibiotico ceftriaxone o
attraverso lo stesso tubo, perché si possono formare delle particelle. Se si utilizza lo stesso
dispositivo per somministrarle questi medicinali in successione, il dispositivo deve essere
accuratamente lavato.
A causa del rischio di precipitazione, OLIMEL N9E non deve essere somministrato attraverso la
stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL N9E contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
OLIMEL N9E contiene potassio. Porre particolare attenzione con i pazienti che assumono diuretici,
inibitori dell’ACE, antagonisti del recettore dell’angiotensina II (farmaci per la cura dell’ipertensione)
o immunosoppressivi. Questi tipi di farmaci possono aumentare i livelli di potassio nel sangue.
Gravidanza, allattamento e fertilità
Se Lei ha in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando
con latte materno chieda consiglio al medico prima di prendere questo medicinale.
OLIMEL N9E può essere preso in considerazione durante la gravidanza e l’allattamento se necessario.
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N9E emulsione per infusione
Dosaggio
OLIMEL N9E deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena del
suo torace.
OLIMEL N9E deve essere a temperatura ambiente prima dell'uso.
OLIMEL N9E è esclusivamente per uso singolo.
L'infusione di una sacca di solito dura tra le 12 e le 24 ore.
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N9E.
Se le è stato somministrato più OLIMEL N9E emulsione per infusione di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume del
sangue circolante). I livelli di glucosio nel sangue e nelle urine possono aumentare e si può sviluppare
una sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può aumentare il
livello di trigliceridi presenti nel Suo sangue. Ricevere un’infusione troppo veloce o un volume di
OLIMEL N9E troppo grande può causare nausea, vomito, brividi mal di testa, vampate di calore,
sudorazione eccessiva (iperidrosi) e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere
interrotta immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di OLIMEL N9E, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati, sebbene non tutte le
persone li manifestino.
Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il trattamento, lo comunichi
prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione verrà interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, come sudorazione, febbre, brividi, mal di testa, rash cutanei o difficoltà nella
respirazione.
Con OLIMEL N9E sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione).
Frequenza - Non nota: frequenza non definibile sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore, irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 individuo su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- Febbre
- Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno(anemia).
- Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- Livelli elevati di grassi nel sangue (iperlipidemia)
- Infiltrazione lipidica epatica (epatomegalia)
- Deterioramento della funzionalità del fegato
- Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenzanon nota: frequenza non definibile sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia).
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia).
- Aumento dei livelli di azoto nel sangue (azotemia)
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo:http://www.agenziafarmaco.gov.it/content/come-
segnalare-una-sospetta-reazione-avversa . Segnalando gli effetti indesiderati lei può contribuire a
fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare OLIMEL N9E emulsione per infusione
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno del mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N9E, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
14,2%(corrispondente a 14,2 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico) con elettroliti (sodio, potassio, magnesio, fosfato, acetato,
cloruro), una emulsione di lipidi al20%(corrispondente a 20 g/100 mL) (olio di oliva purificato e olio
di soia purificato) e una soluzione di glucosio al 27,5%(corrispondente a 27,5 g/100 mL) (come
glucosio monoidrato) con calcio.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N9E, emulsione per infusione e contenuto delle confezioni
OLIMEL N9E è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro compartimento una soluzione di
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
amminoacidi con elettroliti ed il terzo compartimento una soluzione di glucosio con calcio. Questi
compartimenti sono separati da membrane non permanenti. Prima della somministrazione il
contenuto dei compartimenti deve essere miscelato arrotolando la sacca su se stessa partendo
dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
Le soluzioni di amminoacidi e di glucosio sono limpide, chiare incolori o leggermente gialle.
L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 1.000 mL: 1 scatola con 6 sacche
sacca da 1.500 mL: 1 scatola con 4 sacche
sacca da 2.000 mL: 1 scatola con 4 sacche
1 sacca da 1.000 mL, 1.500 mL e 2.000 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Francia, Portogallo, Estonia, Polonia, Lituania, Bulgaria, Romania, Lettonia, Repubblica Ceca, Belgio,
Spagna, Repubblica Slovacca, Paesi basssi, Lussemburgo, Slovenia, Italia, Danimarca, Islanda, Svezia,
Norvegia, Finlandia, Grecia, Cipro: OLIMEL N9E
Austria: ZentroOLIMEL 5,7 % mit Elektrolyten
Germania: Olimel 5,7% E
Regno Unito, Irlanda, Malta: Triomel 9g/L nitrogen 1070 kcal/L with electrolytes
Ungheria: Olimel 9 g/L nitrogén elektrolitokkal emulziós infúzió
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
Categoria farmacoterapeutica: Soluzioni per nutrizione parenterale/combinazioni
Codice ATC: B05 BA10
- I.COMPOSIZIONE QUALITATIVA E QUANTITATIVAOLIMEL N9E si presenta sotto forma di sacca a 3 compartimenti. Ogni sacca contiene una soluzione di glucosio con calcio, una emulsione di lipidi e una soluzione di amminoacidi con altri elettroliti:
Contenuto per sacca
1.000 mL 1.500 mL 2.000 mL
Soluzione di glucosio 27,5%
(corrispondente a 27,5 g/100 mL)
400 mL 600 mL 800 mL
soluzione di amminoacidi 14,2%
(corrispondente a 14,2 g/100 mL)
400 mL 600 mL 800 mL
Emulsione di lipidi 20%
(corrispondente a 20 g/100 mL)
200 mL 300 mL 400 mL
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
Principi attivi1.000 mL1.500 mL2.000 mL
Olio di oliva purificato + olio di soia purificato 40,00 g 60,00 g 80,00 g
Alanina 8,24 g 12,36 g 16,48 g
Arginina 5,58 g 8,37 g 11,16 g
Acido aspartico 1,65 g 2,47 g 3,30 g
Acido glutammico 2,84 g 4,27 g 5,69 g
Glicina 3,95 g 5,92 g 7,90 g
Istidina 3,40 g 5,09 g 6,79 g
Isoleucina 2,84 g 4,27 g 5,69 g
Leucina 3,95 g 5,92 g 7,90 g
Lisina
(come lisina acetato)
8,96 g
(12,64 g)
Metionina 2,84 g 4,27 g 5,69 g
Fenilalanina 3,95 g 5,92 g 7,90 g
Prolina 3,40 g 5,09 g 6,79 g
Serina 2,25 g 3,37 g 4,50 g
Treonina 2,84 g 4,27 g 5,69 g
Triptofano 0,95 g 1,42 g 1,90 g
Tirosina 0,15 g 0,22 g 0,30 g
Valina 3,64 g 5,47 g 7,29 g
Sodio acetato, triidrato 1,50 g 2,24 g 2,99 g
Sodio glicerofosfato idrato 3,67 g 5,51 g 7,34 g
Potassio cloruro 2,24 g 3,35 g 4,47 g
Magnesio cloruro, esaidrato 0,81 g 1,22 g 1,62 g
Calcio cloruro, biidrato 0,52 g 0,77 g 1,03 g
Glucosio anidro
(come glucosio monoidrato)
4,48 g
(6,32 g)
6,72 g
(9,48 g)
110,00 g
(121,00 g)
165,00 g
(181,50 g)
220,00 g
(242,00 g)
Una miscela di olio di oliva purificato (circa 80%) e olio di soia purificato (circa 20%) corrispondente
a un rapporto acidi grassi essenziali / acidi grassi totali del 20%.
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico(per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili,
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
Include calorie da fosfatidi purificati di uovo
Include fosfato fornito dall'emulsione di lipidi
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
|
|
| |
| Lipidi | 40 g | a 60 g | 80 g |
| Amminoacidi | 56,9 g | 85,4 g | 113,9 g |
| Azoto | 9,0 g | F 13,5 g | 18,0 g |
| Glucosio | 110,0 g | 165,0 g | 220,0 g |
| Energia: Calorie totali appross. Calorie non proteiche. Calorie glucosio Calorie lipidiche..(a) Rapporto calorie non proteiche/azoto Rapporto calorie glucosio/lipidi Calorie lipidiche/totali |
| l e
|
|
| Elettroliti: sodio potassio l magnesio a calcio Fosfato (b) t acetato cloruro | a 35,0 mmol i 30,0 mmol 4,0 mmol 3,5 mmol 15,0 mmol 54 mmol 45 mmol | 52,5 mmol 45,0 mmol 6,0 mmol 5,3 mmol 22,5 mmol 80 mmol 68 mmol | 70,0 mmol 60,0 mmol 8,0 mmol 7,0 mmol 30,0 mmol 107 mmol 90 mmol |
| I pH. | 6,4 | 6,4 | 6,4 |
| Osmolarità. | 1310 mosm/L | 1310 mosm/L | 1310 mosm/L |
- J.POSOLOGIA E MODO DI SOMMINISTRAZIONE
Posologia
L’uso di OLIMEL N9E non è raccomandato nei bambini al di sotto di 2 anni a causa della composizione
e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare il
simultaneamente tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i
pazienti richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca
statica. In tale situazione, qualunque aggiustamento del volume (dose) deve prendere in
considerazione l'effetto risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di
OLIMEL N9E. Ad esempio, i pazienti pediatrici possono avere un fabbisogno superiore a
0,2 mmol/kg/giorno di fosfato. In queste circostanze, gli operatori sanitari possono prendere in
considerazione l'aggiustamento del volume (dose) di OLIMEL N9E al fine di soddisfare tale fabbisogno
aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N9E del paziente, oltre che dall’energia o dalle proteine
ulteriori fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di
conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico,
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per OLIMEL N9E la dose quotidiana massima è definita dall'apporto di amminoacidi, 35 mL/kg,
corrispondenti a 2,0 g/kg amminoacidi, 3,9 g/kg glucosio, 1,4 g/kg lipidi, 1,2 mmol/kg sodio e 1,1
mmol/kg potassio. Per un paziente di 70 kg questo sarebbe equivalente a 2.450 mL di OLIMEL N9E al
giorno, che si traduce in un apporto di 140 g amminoacidi, 270 g glucosio e 98 g lipidi, (cioè 2.058
kcal non proteiche e 2.622 kcal totali).
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
Per OLIMEL N9E la velocità d'infusione massima è 1,8 mL/kg/ora, corrispondenti a 0,10 g/kg/ora
amminoacidi; 0,19 g/kg/ora glucosio e 0,07 g/kg/ora lipidi.
Nei bambini di età superiore ai 2 anni
Non esistono studi eseguiti sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N9E del paziente, oltre che da energia o proteine ulteriori
fornite oralmente/enteralmente, pertanto, i formati della sacca devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, età tra 2 e 11 anni, ed età tra 12 e 18 anni.
Per Olimel N9E nel gruppo da 2 a 11 anni di età, i fattori limitanti sono la concentrazione dei fosfati
per la dose giornaliera (0,2 mmol/kg/die) e la concentrazione dei lipidi per la velocità oraria Nel
gruppo da 12 a 18 anni di età i fattori limitanti sono la concentrazione dei fosfati per la dose
giornaliera (0,2 mmol/kg/die) e la concentrazione di amminoacidi per la velocità oraria. Gli apporti
risultanti sono mostrati di seguito:
| e Costituenti | Da 2 a 11 anni | Da 12 a 18 anni | |||
| Raccomandatoa | OLIMEL N9E Vol Massimo | Raccomandatoa | OLIMEL N9E Vol Massimo | ||
| g Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| 13 |
| 13 | |
| A Amminoacidi (g/kg/d) |
| 0,8 |
| 0,8 | |
| Glucosio (g/kg/d) |
| 1,5 |
| 1,5 | |
| Lipidi (g/kg/d) | 0,5 - 3 | 0,5 |
| 0,5 | |
a: Valori raccomandati dalla Linee Guida 2005 ESPGHAN/ ESPEN
Normalmente, la velocità del flusso si deve aumentare gradualmente durante la prima ora e poi deve
essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume
giornaliero e la durata dell’infusione.
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e
di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva.
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6.
Per la sua alta osmolarità, OLIMEL N9E può essere somministrato solo attraverso una vena centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e 24
ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle condizioni
cliniche del paziente.
- F.INCOMPATIBILITÀNon aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
OLIMEL N9E contiene ioni calcio che rappresentano un rischio ulteriore di coagulazione nel sangue o
in emocomponenti anticoagulati o conservati con citrato.
Il ceftriaxone non deve essere miscelato o somministrato in concomitanza con soluzioni endovenose
contenenti calcio, compreso OLIMEL N9E, attraverso la stessa linea di infusione (per es., tramite un
connettore a Y) a causa del rischio di precipitazione del sale di ceftriaxone-calcio (vedere paragrafi
- 4.4 e 4.5 dell’RCP). Il ceftriaxone e le soluzioni contenenti calcio possono essere somministrati in sequenza uno dopo l'altro se si utilizzano linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di precipitati.
| Energia totale (kcal/kg/d) |
| 14 |
| 14 | |
| Massima velocità all’ora | |||||
| OLIMEL N9E (mL/kg/h) | 3,3 | o 2,1 | |||
| Amino acidi(g/kg/h) | 0,20 | 0,19 | 0,12 | 0,12 | |
| Glucosio (g/kg/h) | 1,2 | 0,36 | 1,2 | c 0,23 | |
| Lipidi (g/kg/h) | 0,13 | 0,13 | 0,13 | 0,08 | |
A causa del rischio di precipitazione, OLIMEL N9E non deve essere somministrato attraverso la
stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di infusione, catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- G.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONE
Una visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N9E viene
illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
elementi in tracce.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Quando si eseguono le aggiunte alle formulazioni contenenti elettroliti, si deve considerare la
quantità di elettroliti già presente nella sacca.
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
OLIMEL N9E si può integrare con elettroliti, sulla base della tabella seguente:
Valore corrispondente all'aggiunta del fosfato inorganico
Incluso il fosfato fornito dall'emulsione di lipidi
Elementi in tracce e vitamine:
La stabilità è stata dimostrata con preparazioni di vitamine e oligoelementi in commercio (contenenti
al massimo 1 mg di ferro).
La compatibilità di altri additivi è disponibile su richiesta.
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- Operare in condizioni asettiche.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
| Per 1.000 mL | |||
| Livello incluso | Aggiunta ulteriore massima | o Livello totale massimo | |
| sodio | 35 mmol | 115 mmol | c 150 mmol |
| potassio | 30 mmol | 120 mmol | 150 mmol |
| magnesio | 4,0 mmol | 1,6 mmol | a 5,6 mmol |
| calcio | 3,5 mmol | 1,5 (0,0(a)) mmol | 5,0 (3,5(a)) mmol |
| Fosfato inorganico | 0 mmol | 3,0 mmol | m 3,0 mmol |
| Fosfato organico | 15 mmol ( b) | 10 mmol | 25 mmol ( b) |
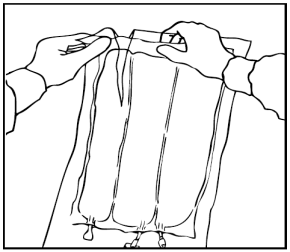
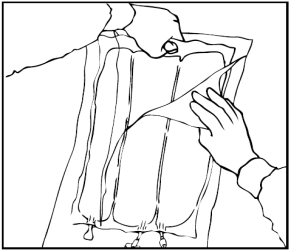
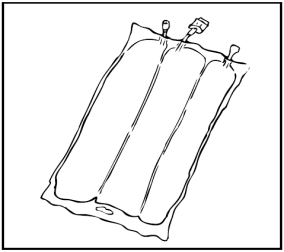
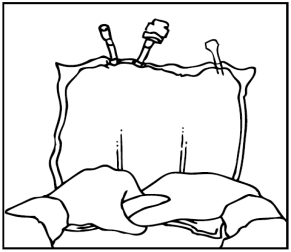

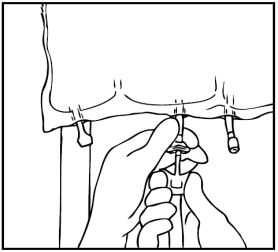
Somministrazione
Solo per uso singolo.
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas
contenuto nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N9E, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno.
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
OLIMEL
N12 emulsione per infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 37. Cos'è OLIMEL N12 e a cosa serve
- 38. Cosa deve sapere prima che le sia somministrato OLIMEL N12 emulsione per infusione
- 39. Come usare OLIMEL N12, emulsione per infusione
- 40. Possibili effetti indesiderati
- 41. Come conservare OLIMEL N12 emulsione per infusione
- 42. Contenuto della confezione e altre informazioni
1. Cos’è OLIMEL N12 emulsione per infusione e a cosa serve
OLIMEL N12 è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio, il secondo un'emulsione di lipidi e il terzo una
soluzione di amminoacidi.
OLIMEL N12 si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante
un tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL N12 deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N12 emulsione per infusione
OLIMEL N12 emulsione per infusione non deve essere usato
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è allergico alle proteine delle uova, dei semi di soia, dell’arachide o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito), o ad uno degli altri componenti di questo farmaco (elencati nel paragrafo 6).
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se soffre di iperglicemia (troppo zucchero nel sangue).
In tutti i casi, il suo medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali
età, peso e condizione medica, insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N12 .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come sudorazione, febbre, brividi, mal di testa, rush cutanei o respirazione
difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N12 contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivanti dal mais (vedere paragrafo “OLIMEL N12, emulsione per
infusione non deve essere usata” sopra).
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento, e la manutenzione del catetere e
durante la preparazione della formula nutrizionale (nutrizione parenterale totale) può ridurre tale
rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima
di iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti ed oligoelementi, se
ritiene che sia il caso.
Disturbi del fegato inclusi problemi con l'eliminazione della bile (colestasi), accumulo di grasso
(steatosi epatica), fibrosi, che potrebbe portare a insufficienza epatica, così come colecistite e
colelitiasi sono stati riportati in pazienti che assumono terapia nutrizionale per via endovenosa. Si
ritiene che la causa di questi disturbi sia dovuta a molteplici fattori e possa differire tra i pazienti. Se
si soffre di sintomi come nausea, vomito, dolore addominale, ingiallimento della pelle o degli occhi,
consultare il proprio medico per consentire l'identificazione di possibili fattori causali e contributivi e
possibili misure terapeutiche e preventive.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o shock cardiogeno secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà esami
clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato questo
medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare una
“sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N12 o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N12 le può essere somministrato tramite un tubo (catetere) in una grande vena del torace
(vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed oligoelementi è sempre richiesta. Si devono
utilizzare formulazioni pediatriche.
Altri medicinali e OLIMEL N12
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
Informi il medico se sta prendendo o sta ricevendo uno dei seguenti:
- insulina
- eparina
OLIMEL N12 non deve essere somministrato contemporaneamente con il sangue attraverso lo stesso
set di infusione.
A causa del rischio di precipitazione, OLIMEL N12 non deve essere somministrato attraverso la stessa
linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL N12 contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
Gravidanza, allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con
latte materno chieda consiglio al medico prima di prendere questo medicinale.
Non ci sono esperienze adeguate sull'uso di OLIMEL N12 in donne in gravidanza o che allattano.
OLIMEL N12 può essere preso in considerazione durante la gravidanza e l'allattamento, se
necessario. OLIMEL N12 deve essere somministrato a donne in gravidanza o che allattano solo dopo
un'attenta valutazione.
Fertilità
Non sono disponibili dati adeguati
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N12 emulsione per infusione
Dosaggio
OLIMEL N12 deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena del
suo torace.
OLIMEL N12 deve essere a temperatura ambiente prima dell'uso.
OLIMEL N12 è esclusivamente per uso singolo.
L'infusione di una sacca di solito dura tra le 12 e le 24 ore.
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N12.
Se le è stato somministrato più OLIMEL N12emulsione per infusione di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume del
sangue circolante). I livelli di glucosio nel sangue e nelle urine possono aumentare e si può sviluppare
una sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può aumentare il
livello di trigliceridi presenti nel Suo sangue. Ricevere un’infusione troppo veloce o un volume di
OLIMEL N12 troppo grande può causare nausea, vomito, brividi mal di testa, vampate di calore,
sudorazione eccessiva (iperidrosi) e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere
interrotta immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di OLIMEL N12, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati, sebbene non tutte le
persone li manifestino.
Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il trattamento, lo comunichi
prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione deve essere interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, come sudorazione, febbre, brividi, mal di testa, rash cutanei o difficoltà nella
respirazione.
Con OLIMEL sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione).
Frequenza - Non nota: la frequenza non può essere definita sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore, irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 persona su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- Febbre
- Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno(anemia).
- Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- Livelli elevati di grassi nel sangue (iperlipidemia)
- Infiltrazione lipidica epatica (epatomegalia)
- Deterioramento della funzionalità del fegato
- Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenzanon nota: la frequenza non può essere stabilita sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia)
- Malattia epatica associata all'alimentazione parenterale (vedere "Avvertenze e precauzioni" nella sezione 2)
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia)
- Aumento dei livelli di azoto nel sangue (azotemia)
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo: www.agenziafarmaco.gov.it/content/come-segnalare-
una-sospetta-reazione-avversa . Segnalando gli effetti indesiderati lei può contribuire a fornire
maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare OLIMEL N12 emulsione per infusione
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno di quel
mese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N12, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
14,2%(corrispondente a 14,2 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico) (, una emulsione di lipidi al17,5%(corrispondente a 17,5 g/100
mL) (olio di oliva purificato e olio di soia purificato) e una soluzione di glucosio al 27,5%
(corrispondente a 27,5 g/100 mL) (come glucosio monoidrato).
Gli altrieccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N12, emulsione per infusione e contenuto delle confezioni
OLIMEL N12 è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro compartimento una soluzione di
amminoacidi ed il terzo compartimento una soluzione di glucosio. Questi compartimenti sono
separati da membrane non permanenti. Prima della somministrazione il contenuto dei
compartimenti deve essere miscelato arrotolando la sacca su se stessa partendo dall’alto fino a che
le membrane si aprono.
Aspetto prima della ricostituzione:
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
Le soluzioni di amminoacidi e di glucosio sono limpide, incolori o leggermente gialle.
L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 650 mL: 1 scatola con 10 sacche
sacca da 1000 mL: 1 scatola con 6 sacche
sacca da 1500 mL: 1 scatola con 4 sacche
sacca da 2000 mL: 1 scatola con 4 sacche
1 sacca da 650 mL ,1000 mL, 1500 mL e 2000 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Belgium, Czech Republic, France, Greece, Italy, Luxembourg, The Netherlands, Slovenia, Spain:
Austria:
Germany:
Denmark, Iceland, Sweden, Norway, Finland, Portugal:
Ireland, Malta, The United Kingdom:
< TRIOMEL 12 g/l nitrogen 950 kcal
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
- K.COMPOSIZIONE QUALITATIVA E QUANTITATIVAOLIMEL N12 si presenta sotto forma di sacca a 3 compartimenti. Ogni sacca contiene una soluzione di glucosio, una emulsione di lipidi e una soluzione di amminoacidi:
| Contenuto per sacca | ||||
| 650 mL | 1000 mL | m 1500 mL | 2000 mL | |
| Soluzione di glucosio 27,5% (corrispondente a 27,5 g/100 mL) | 173 mL | 267 mL | r 400 mL | 533 mL |
| soluzione di amminoacidi 14,2% (corrispondente a 14,2 g/100 mL) | 347 mL | 533 mL | a 800 mL | 1067 mL |
| Emulsione di lipidi 17,5% (corrispondente a 17,5 g/100 mL) | 130 mL | F 200 mL | 300 mL | 400 mL |
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
| Principi attivi | 650 mL | 1000 mL | 1500 mL | 2000 mL |
| a Olio di oliva purificato + olio di soia purificato | 22,75 g | d 35,00 g | 52,50 g | 70,00 g |
| Alanina | 7,14 g | 10,99 g | 16,48 g | 21,97 g |
| Arginina | a 4,84 g | 7,44 g | 11,16 g | 14,88 g |
| Acido Aspartico | n 1,43 g | 2,20 g | 3,30 g | 4,39 g |
| Acido glutammico | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Glicina | a 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| i Istidina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| l Isoleucina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| a Leucina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| t I Lisina (come lisina acetato) | 3,88 g (5,48 g) | 5,97 g (8,43 g) | 8,96 g (12,64 g) | 11,95 g (16,85 g) |
| Metionina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| a Fenilalanina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| i Prolina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| z Serina | 1,95 g | 3,00 g | 4,50 g | 5,99 g |
| n Treonina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Triptofano | 0,82 g | 1,26 g | 1,90 g | 2,53 g |
| e Tirosina | 0,13 g | 0,20 g | 0,30 g | 0,39 g |
| g Valina | 3,16 g | 4,86 g | 7,29 g | 9,72 g |
| A Glucosio (come glucosio monoidrato) | 47,67 g (52,43 g) | 73,33 g (80,67 g) | 110,00 g (121,00 g) | 146,67 g (161,33 g) |
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi
Compartimento
Soluzione di glucosio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
| 650 mL | 1000 mL | a 1500 mL | 2000 mL | |
| Lipidi | 22,8 g | 35,0 g | F 52,5 g | 70,0 g |
| Amminoacidi | 49,4 g | 75,9 g | 113,9 g | 151,9 g |
| Azoto | 7,8 g | l 12,0 g | 18,0 g | 24,0 g |
| Glucosio | 47,7 g | e 73,3 g | 110,0 g | 146,7 g |
| Energia: | ||||
| Calorie totali circa | 620 kcal | d 950 kcal | 1420 kcal | 1900 kcal |
| Calorie non proteiche, | 420 kcal | 640 kcal | 960 kcal | 1280 kcal |
| Calorie glucosio | a 190 kcal | 290 kcal | 430 kcal | 580 kcal |
| Calorie lipidiche,(a) | n 230 kcal | 350 kcal | 520 kcal | 700 kcal |
| Rapporto calorie non proteiche/azoto | a 53 kcal/g | 53 kcal/g | 53 kcal/g | 53 kcal/g |
| Rapporto calorie glucosio/lipidi | i 45/55 | 45/55 | 45/55 | 45/55 |
| Calorie lipidiche/totali | l 37% | 37% | 37% | 37% |
| Elettroliti: | a | |||
| t Fosfatob | 1,7 mmoL | 2,6 mmoL | 3,9 mmoL | 5,2 mmoL |
| I Acetato | 35 mmoL | 54 mmoL | 80 mmoL | 107 mmoL |
| pH |
|
|
|
|
| a Osmolarità circa | 1130 mOsm/L | 1130 mOsm/L | 1130 mOsm/L | 1130 mOsm/L |
POSOLOGIA E MODO DI SOMMINISTRAZIONE
Posologia
L’uso di OLIMEL N12 non è raccomandato nei bambini al di sotto di 2 anni a causa della composizione
e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare simultaneamente
tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i pazienti
richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca statica. In tale
situazione, qualunque aggiustamento del volume (dose) deve prendere in considerazione l'effetto
risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di OLIMEL N12. In queste
circostanze, gli operatori sanitari possono prendere in considerazione l'aggiustamento del volume
(dose) di OLIMEL N12 al fine di soddisfare tale fabbisogno aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N12 del paziente, oltre che dall’energia o dalle proteine
ulteriori fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di
conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico. Popolazioni speciali possono richiedere fino a 0,4 g di azoto / kg di peso corporeo (2,5 g di aminoacidi / kg).
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per OLIMEL N12 la dose quotidiana massima è definita dall'apporto di amminoacidi, 26 mL/kg,
corrispondenti a 2,0 g/kg amminoacidi, 1,9 g/kg glucosio, 0,9 g/kg lipidi. Per un paziente di 70 kg
questo sarebbe equivalente a 1820 mL di OLIMEL N12 al giorno, che si traduce in un apporto di 138 g
amminoacidi, 133 g glucosio e 64 g lipidi, (cioè 1171 kcal non proteiche e 1723 kcal totali).
In terapia sostitutiva renale continua (Continuous Renal Replacement Therapy-CRRT):Per OLIMEL
N12, la dose massima giornaliera è definita dall'assunzione di amminoacidi, 33 ml/ kg corrispondenti
a 2,5 g / kg di aminoacidi, 2,4 g/ kg di glucosio, 1,2 g/ kg di lipidi. Per un paziente di 70 kg, questo
equivarrebbe a 2310 ml di OLIMEL N12
al giorno, risultando in un'assunzione di 175 g di aminoacidi, 169 g di glucosio e 81 g di lipidi (cioè
1486 kcal non proteiche e 2187 kcal totali).
Nei pazienti con obesità patologica: il dosaggio deve essere calcolato sulla base del peso corporeo
ideale (PCI). Per OLIMEL N12, la dose massima giornaliera è definita dall'assunzione di amminoacidi,
33 ml/kg di PCI corrispondenti a 2,5 g/kg di aminoacidi, 2,4 g/kg di glucosio, 1,2 g/kg di lipidi. Per un
paziente di 70 kg, questo equivarrebbe a 2310 ml di OLIMEL N12 al giorno, risultando in
un'assunzione di 175 g di aminoacidi, 169 g di glucosio e 81 g di lipidi (cioè 1486 kcal non proteiche e
2187 kcal totali).
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
Per OLIMEL N12 la velocità d'infusione massima è 1,3 mL/kg/ora, corrispondenti a 0,10 g/kg/ora di
amminoacidi; 0,10 g/kg/ora di glucosio e 0,05 g/kg/ora di lipidi.
Nei bambini di età superiore ai 2 anni e negli adolescenti
Non sono stati eseguiti studi sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N12 del paziente, oltre che da energia o proteine ulteriori
fornite oralmente/enteralmente, pertanto, i formati della sacca devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, tra 2 e 11 annidi età, ed età tra 12 e 18 anni di età.
Per Olimel N12 nel gruppo da 2 a 11 anni di età, la concentrazione di amminoacidi è il fattore
limitante per il dosaggio giornaliero e per la velocità oraria.
Nel gruppo da 12 a 18 anni di età, la concentrazione di amminoacidi è il fattore limitante per
il dosaggio giornaliero e per la velocità oraria.
Gli apporti risultanti sono mostrati di seguito:
| Costituenti | Da 2 a 11 anni | Da 12 a 18 anni | |||
| Raccomandatoa | OLIMEL N12 Vol Massimo | r a Raccomandatoa | OLIMEL N12 Vol Massimo | ||
| Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| 33 | F
| 26 | |
| Amminoacidi (g/kg/d) |
| 2,5 |
| 2 | |
| Glucosio (g/kg/d) | 1,4 – 8,6 | 2,4 | 0,7 – 5,8 | 1,9 | |
| Lipidi (g/kg/d) | 0,5 - 3 | 1,2 | l
| 0,9 | |
| Energia totale (kcal/kg/d) | 30-75 | e 31,4 | 20-55 | 24,7 | |
| d Massima velocità all’ora | |||||
| OLIMEL N12 (mL/kg/h) | 2,6 | 1,6 | |||
| Amino acidi (g/kg/h) | 0,20 | 0,20 | 0,12 | 0,12 | |
| Glucosio (g/kg/h) | 0,36 | a 0,19 | 0,24 | 0,12 | |
| Lipidi (g/kg/h) | 0,13 | 0,09 | 0,13 | 0,06 | |
Normalmente, la velocità del flusso si deve aumentare gradualmente durante la prima ora e poi deve
essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume
giornaliero e la durata dell’infusione.
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e
di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
La velocità massima di infusione è di 2,6 ml/kg/ora nei bambini di età compresa tra 2 e 11 anni e 1,6
ml/kg/ora nei bambini di età compresa tra 12 e 18 anni.
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva.
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6 del Riassunto delle Caratteristiche del Prodotto.
Per la sua alta osmolarità, OLIMEL N12 deve essere somministrato solo attraverso una vena centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e 24
ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle condizioni
cliniche del paziente.
- G.INCOMPATIBILITÀNon aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
A causa del rischio di precipitazione, OLIMEL N12 non deve essere somministrato attraverso la stessa
linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di infusione, catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- H.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONE
Una visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N12 viene
illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
oligoelementi.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
La formulazione OLIMEL N12 può essere supplementata con elettroliti, fosfato inorganico/organico e
con preparazioni disponibili in commercio di prodotti multi-vitaminici (come Cernevit) e multi-
oligoelementi (come Nutryelt). I livelli massimi totali di additivi elencati nella tabella seguente sono
stati dimostrati dai dati di stabilità e non devono essere considerate raccomandazioni sul dosaggio.
La supplementazione deve essere dettata dalle esigenze cliniche del paziente e non deve superare le
linee guida nutrizionali. Gli elettroliti già presenti nella sacca dovrebbero essere tenuti in
considerazione quando si raggiunge il livello totale massimo.
La compatibilità può variare tra prodotti provenienti da fonti diverse e gli operatori sanitari sono
invitati a effettuare controlli appropriati quando mescolano OLIMEL N12 con altre soluzioni
parenterali.
| Possibili aggiunte per 1000 mL di OLIMEL N12 (pediatria): | |||
| Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | |
| Sodio | 0 mmol | 150 mmol | 150 mmol |
| Potassio | 0 mmol | 150 mmol | 150 mmol |
| Magnesio | 0 mmol | 5,6 mmol | o 5,6 mmol |
| Calcio | 0 mmol | 5,0 mmol | 5,0 mmol |
| Fosfato inorganico | 0 mmol | 0/10 mmol b | c 0/10 mmol b |
| Fosfato organico | 3 mmol a | 22/12 mmol b | a 25/15 mmol a,b |
| Altre aggiunte (oligoelementi, vitamine, selenio e zinco) c | |||
| Oligoelementi – Junyelt d | m 1 fiala per sacca (10mL soluzione concentrata) | ||
| Vitamine e | r 1 fiala (liofilizzato) | ||
| Selenio | a 60 µg per sacca | ||
| Zinco | F 3 mg per sacca | ||
| l Possibili aggiunte per 1000 mL di OLIMEL N12 (per adulti): | |||||
| a t Livello incluso | Aggiunta ulteriore massima | Livello totale massimo | |||
| Sodio | I 0 mmol | 150 mmol | 150 mmol | ||
| Potassio | 0 mmol | 150 mmol | 150 mmol | ||
| Magnesio | a 0 mmol | 5,6 mmol | 5,6 mmol | ||
| Calcio | i 0 mmol | 5,0 mmol | 5,0 mmol | ||
| Fosfato inorganico | z 0 mmol | 0/10 mmol b | 0/10 mmol b | ||
| Fosfato organico | 3 mmol a | 22/12 mmol b | 25/15 mmol a,b | ||
| n Altre aggiunte (oligoelementi, vitamine, selenio e zinco) c | |||||
| e g Oligoelementi– Nutryelt d | 2 fiale per sacca (10mL soluzione concentrata) | ||||
| Vitamine– Cernevit e | 1 fiala (5 mLliofilizzato) | ||||
| A Selenio | 500 µg per sacca | ||||
| Zinco | 20 mg per sacca | ||||
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- Operare in condizioni asettiche.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Validità Dopo la ricostituzione:
La stabilità chimica e fisica durante l'uso è stata dimostrata per 7 giorni a 2°C - 8°C, seguita da 48 ore
a temperatura non superiore a 30°C.
Da un punto di vista microbiologico, il prodotto deve essere utilizzato immediatamente. Se non
utilizzato immediatamente, i tempi e le condizioni di conservazione in uso prima dell'uso sono
responsabilità dell'utente e normalmente non dovrebbero essere superiori a 24 ore a 2-8 °C, a meno
che la ricostituzione non sia avvenuta in condizioni asettiche controllate e validate.
Validità Dopo aggiunta di integrazioni:
Per specifiche miscelazioni, la stabilità in uso chimico fisica è stata dimostrata per 7 giorni a 2°C - 8°C,
seguita da 48 ore a una temperatura non superiore a 30°C.
Da un punto di vista microbiologico, qualunque miscela va utilizzata immediatamente. In caso
contrario, i tempi e le condizioni di conservazione in uso dopo la miscelazione e prima dell’uso sono
responsabilità dell'utente e non devono durare normalmente oltre 24 ore, a 2°C- 8°C, a meno che
l'aggiunta delle integrazioni non sia avvenuta in condizioni asettiche controllate e validate.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
Figura 1. Procedimento per la somministrazione di OLIMEL
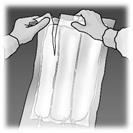
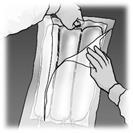

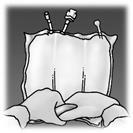
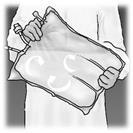
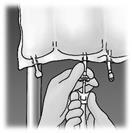
Somministrazione
Solo per uso singolo
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas contenuto
nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N12, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno.
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
OLIMEL
N12E emulsione per infusione
Legga attentamente questo foglio prima che le sia somministrato questo medicinale poiché
contiene importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all'infermiere.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico o all’infermiere. Vedere paragrafo 4.
Contenuto di questo foglio:
- 43. Cos'è OLIMEL N12E e a che cosa serve
- 44. Cosa deve sapere prima che le sia somministrato OLIMEL N12E emulsione per infusione
- 45. Come usare OLIMEL N12E, emulsione per infusione
- 46. Possibili effetti indesiderati
- 47. Come conservare OLIMEL N12E emulsione per infusione
- 48. Contenuto della confezione e altre informazioni
1. Cos’è OLIMEL N12E emulsione per infusione e a cosa serve
OLIMEL N12E è una emulsione per infusione. Si presenta sotto forma di sacca a 3 compartimenti.
Un compartimento contiene una soluzione di glucosio con calcio, il secondo un'emulsione di lipidi e il
terzo una soluzione di amminoacidi con altri elettroliti.
OLIMEL N12E si usa per fornire nutrimento ad adulti e bambini di età superiore a due anni mediante
un tubo in una vena, quando non sia idonea la normale alimentazione per bocca.
OLIMEL N12E deve essere usato esclusivamente sotto controllo medico.
2. Cosa deve sapere prima che le sia somministrato OLIMEL N12E emulsione per infusione
OLIMEL N12E emulsione per infusione non deve essere usato
- In neonati prematuri, infanti e bambini di età inferiore ai 2 anni
- Se è allergico alle proteine delle uova, dei semi di soia, d’arachidi o al mais/prodotti derivati dal mais (vedere anche il paragrafo “ Avvertenze e precauzioni”di seguito), o ad uno qualsiasi degli altri componenti di questo farmaco (elencati nel paragrafo 6).
- Se l'uso di determinati amminoacidi crea problemi al suo corpo.
- Se ha livelli di grassi nel sangue particolarmente alti.
- Se soffre di iperglicemia (troppo zucchero nel sangue).
- Se ha una concentrazione abnormemente alta di uno qualsiasi degli elettroliti (sodio, potassio, magnesio, calcio e/o fosforo) nel sangue.
In tutti i casi, il suo medico deciderà se Lei dovrà ricevere questa medicina sulla base di fattori quali
età, peso e condizione medica, insieme ai risultati degli esami eseguiti.
Avvertenze e precauzioni
Si rivolga al medico o all'infermiere prima che le sia somministrato OLIMEL N12E .
Se le vengono somministrate troppo rapidamente soluzioni per alimentazione parenterale totale, ciò
può provocare lesioni o morte.
L’infusione deve essere interrotta immediatamente se si sviluppano segni o sintomi anomali di
reazione allergica (come sudorazione, febbre, brividi, mal di testa, rush cutanei o respirazione
difficoltosa). Questo medicinale contiene olio di semi di soia e fosfatidi dell’uovo. I semi di soia e le
proteine dell’uovo possono causare reazioni di ipersensibilità. Sono state osservate reazioni
allergiche crociate tra le proteine della soia e dell’arachide.
Olimel N12E contiene glucosio derivato dal mais che può causare reazioni di ipersensibilità se Lei è
allergico al mais o prodotti derivanti dal mais (vedere paragrafo “OLIMEL N12E, emulsione per
infusione non deve essere usata” sopra).
La difficoltà respiratoria può anche essere un segno che si sono formate piccole particelle, che
bloccano i vasi sanguigni nei polmoni (precipitati vascolari polmonari). Qualora avvertisse difficoltà
respiratorie, lo riferisca al medico o all'infermiere, che decideranno quali azioni intraprendere.
L'antibiotico denominato ceftriaxone non deve essere miscelato o somministrato simultaneamente
con qualsiasi soluzione contenente calcio (compreso OLIMEL N12E) che le viene somministrata
mediante una flebo in vena.
Questi medicinali non le devono essere somministrati insieme neanche mediante linee di infusione
diverse o sedi di infusione diverse.
Tuttavia, lei potrà assumere OLIMEL N12E e ceftriaxone in sequenza, uno dopo l'altro, se si utilizzano
linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state
accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di
precipitati (particelle di sale di calcio-ceftriaxone).
Alcuni farmaci e malattie possono aumentare il rischio di sviluppare infezione o sepsi (batteri nel
sangue). Esiste un particolare rischio di infezione o sepsi, quando un tubo (catetere endovenoso)
viene inserito in vena. Il medico la monitorerà attentamente per eventuali segni di infezione. I
pazienti che richiedono la nutrizione parenterale (nutrizione attraverso un tubo posto in vena)
possono avere un maggior rischio di sviluppare infezioni dalle loro condizioni mediche. L’utilizzo di
tecniche asettiche (senza germi) durante il posizionamento, e la manutenzione del catetere e
durante la preparazione della formula nutrizionale (nutrizione parenterale totale) può ridurre tale
rischio.
Se Lei è gravemente malnutrito, in modo tale da ricevere nutrimento per via endovenosa, il medico
deve iniziare lentamente il trattamento. Inoltre il medico deve controllarla attentamente per
prevenire improvvisi cambiamenti nei suoi livelli di liquido, vitamine elettroliti e sali minerali.
Il bilanciamento di acqua e sale nel suo corpo e i disturbi del metabolismo verranno corretti prima
di iniziare l'infusione. Il medico monitorerà la sua condizione mentre Lei riceve questo medicinale e
potrà modificare la dose o darle ulteriori nutrienti, quali vitamine, elettroliti ed oligoelementi, se
ritiene che sia il caso.
Disturbi del fegato inclusi problemi con l'eliminazione della bile (colestasi), accumulo di grasso
(steatosi epatica), fibrosi, che potrebbe portare a insufficienza epatica, così come colecistite e
colelitiasi sono stati riportati in pazienti che assumono terapia nutrizionale per via endovenosa. Si
ritiene che la causa di questi disturbi sia dovuta a molteplici fattori e possa differire tra i pazienti. Se
si soffre di sintomi come nausea, vomito, dolore addominale, ingiallimento della pelle o degli occhi,
consultare il proprio medico per consentire l'identificazione di possibili fattori causali e contributivi e
possibili misure terapeutiche e preventive.
Il medico deve essere informato in caso di:
- grave problema renale. Lei deve informare il medico se è in dialisi (rene artificiale) o se è in terapia con un altro trattamento di depurazione del sangue;
- grave problema epatico;
- problema di coagulazione del sangue;
- funzionamento inadeguato delle ghiandole surrenali (insufficienza surrenale), che sono ghiandole a forma triangolare, poste sopra i reni;
- insufficienza cardiaca;
- malattia polmonare;
- accumulo di acqua nell’organismo (iperidratazione);
- acqua insufficiente nell’organismo (disidratazione);
- livelli elevati di zuccheri nel sangue (diabete mellito) non trattati;
- attacco cardiaco o shock cardiogeno secondario a un’improvvisa insufficienza cardiaca;
- acidosi metabolica grave (quando il sangue è troppo acido);
- infezione generalizzata (setticemia);
- coma.
Per verificare l'efficacia e la sicurezza generale della somministrazione, il medico effettuerà esami
clinici e di laboratorio mentre Lei riceve questo medicinale. Se Le verrà somministrato questo
medicinale per diverse settimane, il suo sangue verrà monitorato su base regolare.
La ridotta capacità dell’organismo di rimuovere i grassi contenuti in questo medicinale può provocare una
“sindrome da sovraccarico di grasso” (vedere paragrafo 4 - Possibili effetti indesiderati).
Se durante l'infusione presenta dolore, bruciore o gonfiore nel sito di infusione o fuoriuscita della
soluzione di infusione, informi il medico o l'infermiere. La somministrazione verrà interrotta
immediatamente e riavviata in un'altra vena.
Se il livello di zucchero nel sangue diventa troppo alto, il medico regolerà la velocità di erogazione di
OLIMEL N12E o le darà un medicinale per controllare il livello dello zucchero nel sangue (insulina).
OLIMEL N12E le può essere somministrato tramite un tubo (catetere) in una grande vena del torace
(vena centrale).
Bambini e adolescenti
Se il paziente è di età inferiore a 18 anni, verrà prestata particolare attenzione a fornire il dosaggio
corretto. Verranno adottate maggiori precauzioni anche per la maggiore sensibilità dei bambini al
rischio di infezione. L’integrazione di vitamine ed oligoelementi è sempre richiesta. Si devono
utilizzare formulazioni pediatriche.
Altri medicinali e OLIMEL N12E
Informi il medico se sta assumendo o usando, ha recentemente assunto o usato o potrebbe
assumere o usare qualsiasi altro medicinale.
L’assimilazione contemporanea di altri medicinali non è generalmente una controindicazione. Se Lei
assume altri medicinali, con o senza ricetta medica, informi preventivamente il medico per
verificarne la compatibilità.
Informi il medico se sta prendendo o sta ricevendo uno dei seguenti:
- insulina
- eparina
OLIMEL N12E non deve essere somministrato contemporaneamente con il sangue attraverso lo
stesso set di infusione.
OLIMEL N12E contiene calcio. Non deve essere somministrato insieme all’antibiotico ceftriaxone o
attraverso lo stesso tubo, perché si possono formare delle particelle. Se si utilizza lo stesso
dispositivo per somministrarle questi medicinali in successione, il dispositivo deve essere
accuratamente lavato.
A causa del rischio di precipitazione, OLIMEL N12E non deve essere somministrato attraverso la
stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Gli oli di oliva e di semi di soia in OLIMEL N12E contengono la vitamina K. Questa vitamina
generalmente non influisce sui farmaci che fluidificano il sangue (anticoagulanti), come la cumarina.
Tuttavia informi il medico se assume farmaci anticoagulanti.
I lipidi contenuti in questa emulsione possono interferire con i risultati di alcune analisi di laboratorio
se il campione di sangue è prelevato prima dell’eliminazione dei lipidi dal suo sangue (che di solito
vengono eliminati dopo un periodo di 5 o 6 ore senza riceverne).
OLIMEL N12E contiene potassio. Porre particolare attenzione con i pazienti che assumono diuretici,
inibitori dell’ACE, antagonisti del recettore dell’angiotensina II (farmaci per la cura dell’ipertensione)
o immunosoppressivi. Questi tipi di farmaci possono aumentare i livelli di potassio nel sangue.
Gravidanza, allattamento
Se è in corso una gravidanza, se sospetta o sta pianificando una gravidanza, o se sta allattando con
latte materno chieda consiglio al medico prima di prendere questo medicinale.
Non ci sono esperienze adeguate sull'uso di OLIMEL N12E in donne in gravidanza o che allattano.
OLIMEL N12E può essere preso in considerazione durante la gravidanza e l'allattamento, se
necessario. OLIMEL N12E deve essere somministrato a donne in gravidanza o che allattano solo dopo
un'attenta valutazione.
Fertilità
Non sono disponibili dati adeguati
Guida e utilizzo di macchinari
Non rilevante
3. Come usare OLIMEL N12E emulsione per infusione
Dosaggio
OLIMEL N12E deve essere somministrato solo in adulti e bambini di età superiore a due anni.
Si tratta di una emulsione per infusione, da somministrare tramite un tubo (catetere) in una vena del
suo torace.
OLIMEL N12E deve essere a temperatura ambiente prima dell'uso.
OLIMEL N12E è esclusivamente per uso singolo.
L'infusione di una sacca di solito dura tra le 12 e le 24 ore.
Dosaggio - adulti
Il medico specificherà una velocità di flusso corrispondente alle Sue necessità e condizioni cliniche.
La prescrizione può proseguire per tutto il tempo richiesto, secondo le Sue condizioni cliniche.
Dosaggio - bambini di età superiore ai due anni e adolescenti
Il medico deciderà la dose e per quanto tempo il medicinale sarà somministrato. Ciò dipenderà
dal'età, dal peso, dall'altezza, dalle condizioni mediche e dalla capacità del corpo di scindere e usare i
componenti di OLIMEL N12E.
Se le è stato somministrato più OLIMEL N12Eemulsione per infusione di quanto deve
Se la dose data è troppo alta o l'infusione è troppo veloce, il contenuto di amminoacidi può rendere il
suo sangue troppo acido e possono verificarsi sintomi di ipervolemia (aumento del volume del
sangue circolante). I livelli di glucosio nel sangue e nelle urine possono aumentare e si può sviluppare
una sindrome iperosmolare (eccessiva viscosità del sangue) e il contenuto di lipidi può aumentare il
livello di trigliceridi presenti nel Suo sangue. Ricevere un’infusione troppo veloce o un volume di
OLIMEL N12E troppo grande può causare nausea, vomito, brividi, mal di testa, vampate di calore,
sudorazione eccessiva (iperidrosi) e alterazioni elettrolitiche. In tali situazioni l’infusione deve essere
interrotta immediatamente.
In alcuni casi gravi, il medico può sottoporla temporaneamente a dialisi renale per aiutare i suoi reni
a eliminare il prodotto in eccesso.
Per impedire che accadano tali eventi, il medico monitorerà regolarmente la sua condizione e testerà
i suoi parametri ematici.
Se ha qualsiasi dubbio sull’uso di OLIMEL N12E, si rivolga al medico.
4. Possibili effetti indesiderati
Come tutti i medicinali, questo medicinale può causare effetti indesiderati, sebbene non tutte le
persone li manifestino.
Se percepisce cambiamenti nel modo in cui si sente, durante o dopo il trattamento, lo comunichi
prontamente al medico o all’infermiere.
Gli esami che effettuerà il medico mentre Lei assume il medicinale riducono i rischi di effetti
indesiderati.
L'infusione deve essere interrotta immediatamente in caso di sviluppo di segni o sintomi anomali di
reazione allergica, come sudorazione, febbre, brividi, mal di testa, rash cutanei o difficoltà nella
respirazione.
Con OLIMEL sono stati riportati i seguenti effetti indesiderati:
Frequenza-Comune: può interessare fino a 1 persona su 10
- Frequenza cardiaca veloce (tachicardia).
- Diminuzione di appetito.
- Aumento del livello dei grassi nel sangue (ipertrigliceridemia).
- Dolore addominale.
- Diarrea.
- Nausea.
- Pressione arteriosa aumentata (ipertensione).
Frequenza - Non nota: la frequenza non può essere definita sulla base dei dati disponibili
- Fuoriuscita dell'infusione nel tessuto circostante (stravaso) che può provocare in sede di infusione dolore, irritazione, tumefazione/edema, arrossamento (eritema)/calore, morte delle cellule tessutali (necrosi della cute) o vesciche / vescicole, infiammazione, ispessimento o costrizione della pelle
Con prodotti simili di nutrizione parenterale sono stati riportati i seguenti effetti indesiderati:
Frequenza- Molto rara: può interessare fino a 1 persona su 10.000
- Ridotta capacità di rimuovere i lipidi (sindrome da sovraccarico di grassi) associata a un improvviso e brusco deterioramento delle condizioni mediche del paziente. I seguenti sintomi di sindrome da sovraccarico di grassi sono solitamente reversibili dopo l'interruzione dell'infusione dell'emulsione di lipidi:
- Febbre
- Riduzione dei globuli rossi che può rendere pallida la pelle e causare debolezza o affanno(anemia).
- Bassa conta dei globuli bianchi, che può accrescere il rischio di infezione (leucopenia)
- Bassa conta delle piastrine, che può accrescere il rischio di contusioni e/o sanguinamento (trombocitopenia)
- Disturbi della coagulazione che compromettono la capacità del sangue di coagularsi
- Livelli elevati di grassi nel sangue (iperlipidemia)
- Infiltrazione lipidica epatica (epatomegalia)
- Deterioramento della funzionalità del fegato
- Manifestazioni a carico del sistema nervoso centrale (per es., coma).
Frequenzanon nota: frequenza non definibile sulla base dei dati disponibili
- Reazioni allergiche.
- Risultati degli esami del sangue anomali per la funzione epatica.
- Problemi nell'eliminazione della bile (colestasi)
- Aumento delle dimensioni del fegato (epatomegalia)
- Malattia epatica associata all'alimentazione parenterale (vedere "Avvertenze e precauzioni" nella sezione 2)
- Ittero (itterizia).
- Riduzione del numero di piastrine (trombocitopenia)
- Aumento dei livelli di azoto nel sangue (azotemia)
- Enzimi epatici elevati
- Formazione di piccole particelle che possono provocare il blocco dei vasi sanguigni nei polmoni (precipitati vascolari polmonari) e determinare un'embolia vascolare polmonare e difficoltà respiratorie (sofferenza respiratoria).
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico o al farmacista. Lei può inoltre segnalare gli effetti indesiderati direttamente tramite il
sistema nazionale di segnalazione all’indirizzo: www.agenziafarmaco.gov.it/content/come-segnalare-
una-sospetta-reazione-avversa . Segnalando gli effetti indesiderati lei può contribuire a fornire
maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare OLIMEL N12E emulsione per infusione
Conservi questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sul contenitore e sulla
confezione esterna (MM/AAAA). La data di scadenza si riferisce all’ultimo giorno di
quelmese.
Non congelare.
Conservare nell'involucro esterno.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione e altre informazioni
Cosa contiene OLIMEL N12E, emulsione per infusione
Le sostanze attivedi ogni sacca dell'emulsione ricostituita sono una soluzione di L-amminoacidi al
14,2%(corrispondente a 14,2 g/100 mL) (alanina, arginina, glicina, istidina, isoleucina, leucina, lisina
(come lisina acetato), metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina,
acido aspartico, acido glutammico) con elettroliti (sodio, potassio, magnesio, fosfato, acetato,
cloruro), una emulsione di lipidi al17,5%(corrispondente a 17,5 g/100 mL) (olio di oliva purificato e
olio di soia purificato) e una soluzione di glucosio al 27,5%(corrispondente a 27,5 g/100 mL) (come
glucosio monoidrato) con calcio.
Gli altri eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi ed
Compartimento
Soluzione di glucosio e
elettroliticalcio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Aspetto di OLIMEL N12E, emulsione per infusione e contenuto delle confezioni
OLIMEL N12E è un’emulsione per infusione confezionata in una sacca a tre compartimenti. Un
compartimento contiene un’emulsione di lipidi, un altro compartimento una soluzione di
amminoacidi con elettroliti ed il terzo compartimento una soluzione di glucosio con calcio. Questi
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
compartimenti sono separati da membrane non permanenti. Prima della somministrazione il
contenuto dei compartimenti deve essere miscelato arrotolando la sacca su se stessa partendo
dall’alto fino a che le membrane si aprono.
Aspetto prima della ricostituzione:
Le soluzioni di amminoacidi e di glucosio sono limpide, incolori o leggermente gialle.
L'emulsione di lipidi è omogenea con aspetto lattiginoso.
Aspetto dopo ricostituzione: emulsione omogenea di aspetto lattiginoso
La sacca a 3 compartimenti è una sacca in plastica multistrato. Il materiale dello strato interno (di
contatto) della sacca è studiato per essere compatibile con i costituenti e gli additivi autorizzati.
Per prevenire il contatto con l’ossigeno dell’aria, la sacca è confezionata in un involucro esterno con
barriera per l’ossigeno, che contiene un sacchetto assorbitore di ossigeno.
Confezioni:
sacca da 650 mL: 1 scatola con 10 sacche
sacca da 1000 mL: 1 scatola con 6 sacche
sacca da 1500 mL: 1 scatola con 4 sacche
sacca da 2000 mL: 1 scatola con 4 sacche
1 sacca da 650 mL ,1000 mL, 1500 mL e 2000 mL
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Baxter S.p.A.
Piazzale dell’Industria 20
00144 Roma
Italia
Produttore:
Baxter S.A.,
Boulevard René Branquart, 80
7860 Lessines
Belgio
Questo farmaco è autorizzato negli stati membri della comunità economica europea con i seguenti
nomi:
Belgium, Bulgaria, Croatia, Cyprus, Czech Republic, Estonia, France, Greece, Italy, Latvia, Lithuania,
Luxemburg, The Netherlands, Romania, Slovenia, Slovakia, Spain:
Austria:
Germany:
Denmark, Iceland, Sweden, Norway, Finland, Poland, Portugal:
Ireland, Malta, The United Kingdom:
Hungary:
< Olimel 12 g/l nitrogén elektrolitokkal emulziós infúzió
--------------------------------------------------------------------------------------------------------------
Le informazioni seguenti sono destinate esclusivamente ai medici o agli operatori sanitari:
- L.COMPOSIZIONE QUALITATIVA E QUANTITATIVAOLIMEL N12E si presenta sotto forma di sacca a 3 compartimenti. Ogni sacca contiene una soluzione di glucosio con calcio, una emulsione di lipidi e una soluzione di amminoacidi con altri elettroliti:
| Contenuto per sacca | ||||
| 650 mL | 1000 mL | m 1500 mL | 2000 mL | |
| Soluzione di glucosio 27,5% (corrispondente a 27,5 g/100 mL) | 173 mL | 267 mL | r 400 mL | 533 mL |
| soluzione di amminoacidi 14,2% (corrispondente a 14,2 g/100 mL) | 347 mL | 533 mL | a 800 mL | 1067 mL |
| Emulsione di lipidi 17,5% (corrispondente a 17,5 g/100 mL) | 130 mL | F 200 mL | 300 mL | 400 mL |
Composizione dell'emulsione ricostituita dopo la miscelazione del contenuto dei tre compartimenti:
| Principi attivi | 650 mL | 1000 mL | 1500 mL | 2000 mL |
| a Olio di oliva purificato + olio di soia purificato | 22,75 g | d 35,00 g | 52,50 g | 70,00 g |
| Alanina | 7,14 g | 10,99 g | 16,48 g | 21,97 g |
| Arginina | a 4,84 g | 7,44 g | 11,16 g | 14,88 g |
| Acido Aspartico | n 1,43 g | 2,20 g | 3,30 g | 4,39 g |
| Acido glutammico | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Glicina | a 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| i Istidina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| l Isoleucina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| a Leucina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| t I Lisina (come lisina acetato) | 3,88 g (5,48 g) | 5,97 g (8,43 g) | 8,96 g (12,64 g) | 11,95 g (16,85 g) |
| Metionina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| a Fenilalanina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| i Prolina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| z Serina | 1,95 g | 3,00 g | 4,50 g | 5,99 g |
| n Treonina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Triptofano | 0,82 g | 1,26 g | 1,90 g | 2,53 g |
| e Tirosina | 0,13 g | 0,20 g | 0,30 g | 0,39 g |
| g Valina | 3,16 g | 4,86 g | 7,29 g | 9,72 g |
| Sodio acetato, triidrato | 0,97 g | 1,5 g | 2,24 g | 2,99 g |
| A Sodio glicerofosfato idrato | 2,39 g | 3,67 g | 5,51 g | 7,34 g |
| Potassio cloruro | 1,45 g | 2,24 g | 3,35 g | 4,47 g |
| Magnesio cloruro, esaidrato | 0,53 g | 0,81 g | 1,22 g | 1,62 g |
| Principi attivi | 650 mL | 1000 mL | 1500 mL | 2000 mL |
| Calcio cloruro, biidrato | 0,34 g | 0,52 g | 0,77 g | 1,03 g |
| Glucosio (come glucosio monoidrato) | 47,67 g (52,43 g) | 73,33 g (80,67 g) | 110,00 g (121,00 g) | o 146,67 g (161,33 g) |
Gli eccipienti sono:
Compartimento
Emulsione di lipidi
Compartimento
Soluzione di amminoacidi ed
Compartimento
Soluzione di glucosio e
elettroliticalcio
Acido cloridrico (per
l’aggiustamento del pH),
acqua per preparazioni
iniettabili
Apporto nutritivo della emulsione ricostituita per ciascun formato della sacca:
Fosfatide purificato di uovo, glicerolo,
sodio oleato, sodio idrossido (per
l’aggiustamento del pH), acqua per
preparazioni iniettabili
Acido acetico glaciale (per
l’aggiustamento del pH), acqua
per preparazioni iniettabili
| 650 mL | d 1000 mL | 1500 mL | 2000 mL | |
| Lipidi | 22,8 g | 35,0 g | 52,5 g | 70,0 g |
| Amminoacidi | a 49,4 g | 75,9 g | 113,9 g | 151,9 g |
| Azoto | n 7,8 g | 12,0 g | 18,0 g | 24,0 g |
| Glucosio | 47,7 g | 73,3 g | 110,0 g | 146,7 g |
| Energia: | a | |||
| Calorie totalicirca | i l 620 kcal | 950 kcal | 1420 kcal | 1900 kcal |
| Calorie non proteiche, | a 420 kcal | 640 kcal | 960 kcal | 1280 kcal |
| t Calorie glucosio | 190 kcal | 290 kcal | 430 kcal | 580 kcal |
| I Calorie lipidiche,(b) | 230 kcal | 350 kcal | 520 kcal | 700 kcal |
| Rapporto calorie non proteiche/azoto | 53 kcal/g | 53 kcal/g | 53 kcal/g | 53 kcal/g |
| a Rapporto calorie glucosio/lipidi | 45/55 | 45/55 | 45/55 | 45/55 |
| i Calorie lipidiche/totali | 37% | 37% | 37% | 37% |
| z Elettroliti: | ||||
| Sodio | 22,8 mmol | 35,0 mmol | 52,5 mmol | 70,0 mmol |
| n Potassio | 19,5 mmol | 30,0 mmol | 45,0 mmol | 60,0 mmol |
| e Magnesio | 2,6 mmol | 4,0 mmol | 6,0 mmol | 8,0 mmol |
| g Calcio | 2,3 mmol | 3,5 mmol | 5,3 mmol | 7,0 mmol |
| Fosfatoc. | 9,5 mmol | 15,0 mmol | 21,9 mmol | 29,2 mmol |
| A Acetato | 46 mmol | 70 mmol | 105 mmol | 140 mmol |
| Cloruri | 30 mmol | 45 mmol | 68 mmol | 90 mmol |
| pH | 6,4 | 6,4 | 6,4 | 6,4 |
POSOLOGIA E MODO DI SOMMINISTRAZIONE
Posologia
L’uso di OLIMEL N12E non è raccomandato nei bambini al di sotto di 2 anni a causa della
composizione e del volume non adeguati (vedere paragrafi 4.4, 5.1 e 5.2 dell’RCP).
Non superare la dose massima giornaliera riportata di seguito. A causa della composizione statica
della sacca a compartimenti multipli, può non essere possibile riuscire a soddisfare simultaneamente
tutti i fabbisogni nutritivi del paziente. Possono verificarsi situazioni cliniche in cui i pazienti
richiedano quantità di elementi nutritivi variabili rispetto alla composizione della sacca statica. In tale
situazione, qualunque aggiustamento del volume (dose) deve prendere in considerazione l'effetto
risultante che ciò avrà sul dosaggio di tutti gli altri elementi nutritivi di OLIMEL N12E. In queste
circostanze, gli operatori sanitari possono prendere in considerazione l'aggiustamento del volume
(dose) di OLIMEL N12E al fine di soddisfare tale fabbisogno aumentato.
Negli adulti:
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N12E del paziente, oltre che dall’energia o dalle proteine
ulteriori fornite oralmente/enteralmente, pertanto i formati della sacca devono essere scelti di
conseguenza.
I requisiti medi giornalieri sono:
- 0,16-0,35 g azoto/kg peso corporeo (1-2 g di amminoacidi/kg), secondo lo stato nutrizionale del paziente e il grado di stress catabolico. Popolazioni speciali possono richiedere fino a 0,4 g di azoto / kg di peso corporeo (2,5 g di aminoacidi / kg).
- 20-40 kcal/kg,
- 20-40 mL fluidi /kg o 1-1,5 mL per kcal spese.
Per OLIMEL N12E la dose quotidiana massima è definita dall'apporto di amminoacidi, 26 mL/kg,
corrispondenti a 2,0 g/kg amminoacidi, 1,9 g/kg glucosio, 0,9 g/kg lipidi. Per un paziente di 70 kg
questo sarebbe equivalente a 1820 mL di OLIMEL N12E al giorno, che si traduce in un apporto di
138 g amminoacidi, 133 g glucosio e 64 g lipidi, (cioè 1171 kcal non proteiche e 1723 kcal totali).
In terapia sostitutiva renale continua (Continuous Renal Replacement Therapy-CRRT):Per OLIMEL
N12E, la dose massima giornaliera è definita dall'assunzione di amminoacidi, 33 ml/ kg
corrispondenti a 2,5 g / kg di aminoacidi, 2,4 g/ kg di glucosio, 1,2 g/ kg di lipidi. Per un paziente di 70
kg, questo equivarrebbe a 2310 ml di OLIMEL N12E al giorno, risultando in un'assunzione di 175 g di
aminoacidi, 169 g di glucosio e 81 g di lipidi (cioè 1486 kcal non proteiche e 2187 kcal totali).
Nei pazienti con obesità patologica: il dosaggio deve essere calcolato sulla base del peso corporeo
ideale (PCI). Per OLIMEL N12E, la dose massima giornaliera è definita dall'assunzione di amminoacidi,
33 ml/kg di PCI corrispondenti a 2,5 g/kg di aminoacidi, 2,4 g/kg di glucosio, 1,2 g/kg di lipidi. Per un
paziente di 70 kg, questo equivarrebbe a 2310 ml di OLIMEL N12E al giorno, risultando in
un'assunzione di 175 g di aminoacidi, 169 g di glucosio e 81 g di lipidi (cioè 1486 kcal non proteiche e
2187 kcal totali).
| 650 mL | 1000 mL | 1500 mL | 2000 mL | |
| Osmolarità circa | 1270 mOsm/L | 1270 mOsm/L | 1270 mOsm/L | 1270 mOsm/L |
Normalmente, la velocità del flusso deve essere aumentata gradualmente durante la prima ora
quindi deve essere regolata per tener conto della dose da somministrare, i volumi da assumere
quotidianamente e la durata dell'infusione.
Per OLIMEL N12E la velocità d'infusione massima è 1,3 mL/kg/ora, corrispondenti a 0,10 g/kg/ora di
amminoacidi; 0,10 g/kg/ora di glucosio e 0,05 g/kg/ora di lipidi.
Nei bambini di età superiore ai 2 anni e negli adolescenti
Non sono stati eseguiti studi sulla popolazione pediatrica.
Il dosaggio dipende dal dispendio di energie, dallo stato clinico, dal peso corporeo e dalla capacità di
metabolizzare i costituenti di OLIMEL N12E del paziente, oltre che da energia o proteine ulteriori
fornite oralmente/enteralmente, pertanto, i formati della sacca devono essere scelti di conseguenza.
Inoltre, le esigenze quotidiane di liquidi, azoto ed energia si riducono continuamente con l'età.
Sono stati presi in considerazione 2 gruppi, tra 2 e 11 annidi età, e tra 12 e 18 anni di età.
Per Olimel N12E nel gruppo da 2 a 11 anni di età, le concentrazioni di amminoacidi e
magnesio sono i fattori limitanti per il dosaggio giornaliero. In questo gruppo di età, la
concentrazione di amminoacidi è il fattore limitante per la velocità oraria.
Nel gruppo da 12 a 18 anni di età, le concentrazioni di amminoacidi e magnesio sono i
fattori limitanti per il dosaggio giornaliero. In questo gruppo di età, la concentrazione di
amminoacidi è il fattore limitante per la velocità oraria. Gli apporti risultanti sono mostrati di
seguito:
Normalmente, la velocità del flusso si deve aumentare gradualmente durante la prima ora e poi deve
essere regolata prendendo in considerazione la dose da somministrare, l’apporto di volume
giornaliero e la durata dell’infusione.
In generale, nei bambini piccoli si raccomanda di iniziare l'infusione con una dose giornaliera bassa, e
di aumentarla gradualmente fino al dosaggio massimo (vedere sopra).
La velocità massima di infusione è di 2,6 ml/kg/ora nei bambini di età compresa tra 2 e 11 anni e 1,6
ml/kg/ora nei bambini di età compresa tra 12 e 18 anni.
Modo e durata di somministrazione
Solo per uso singolo.
Si raccomanda di usare il contenuto immediatamente dopo l’apertura della sacca e di non
conservarlo per un’infusione successiva.
Dopo la ricostituzione, la miscela è omogenea e ha un aspetto lattiginoso.
Per istruzioni sulla preparazione e la manipolazione dell'emulsione per infusione, vedere il paragrafo
- 6.6 del Riassunto delle Caratteristiche del Prodotto.
Per la sua alta osmolarità, OLIMEL N12E deve essere somministrato solo attraverso una vena
centrale.
La durata d'infusione raccomandata per una sacca per nutrizione parenterale è compresa tra 12 e 24
ore.
Il trattamento con nutrizione parenterale può proseguire per tutto il tempo richiesto dalle condizioni
cliniche del paziente.
- H.INCOMPATIBILITÀNon aggiungere altro medicinale o altre sostanze a uno qualsiasi dei costituenti della sacca o all'emulsione ricostituita senza averne prima verificato la compatibilità e la stabilità della preparazione risultante (in particolare la stabilità dell'emulsione lipidica).
| Costituenti | Da 2 a 11 anni | Da 12 a 18 anni | |||
| Raccomandatoa | OLIMEL N12E Vol Massimo | Raccomandatoa | o OLIMEL N12E Vol Massimo | ||
| Dose massima giornaliera | |||||
| Liquidi (mL/kg/d) |
| 33 |
| c 26 | |
| Amminoacidi (g/kg/d) |
| 2,5 |
| 2 | |
| Glucosio (g/kg/d) | 1,4 – 8,6 | 2,4 | 0,7 – 5,8 | a 1,9 | |
| Lipidi (g/kg/d) | 0,5 - 3 | 1,2 | 0,5 – 2 (fino a 3) | 0,9 | |
| Energia totale (kcal/kg/d) | 30-75 | 31,4 | m 20-55 | 24,7 | |
| r Massima velocità all’ora | |||||
| OLIMEL N12E (mL/kg/h) | 2,6 | a | 1,6 | ||
| Amino acidi (g/kg/h) | 0,20 | 0,20 | 0,12 | 0,12 | |
| Glucosio (g/kg/h) | 0,36 | 0,19 | F 0,24 | 0,12 | |
| Lipidi (g/kg/h) | 0,13 | 0,09 | 0,13 | 0,06 | |
Le incompatibilità possono derivare, ad esempio, da eccessiva acidità (pH basso) o da contenuto non
idoneo di cationi bivalenti (Ca e Mg ) che possono destabilizzare l'emulsione di lipidi.
Come con qualsiasi altra miscela per la nutrizione parenterale, è necessario prendere in
considerazione il rapporto calcio/fosfato. Un’eccessiva aggiunta di calcio e fosfato, in particolar modo
sotto forma di sali minerali, può causare la formazione di precipitati di fosfato di calcio.
OLIMEL N12E contiene ioni calcio che rappresentano un rischio ulteriore di coagulazione nel sangue
o in emocomponenti anticoagulati o conservati con citrato.
Il ceftriaxone non deve essere miscelato o somministrato in concomitanza con soluzioni endovenose
contenenti calcio, compreso OLIMEL N12E, attraverso la stessa linea di infusione (per es., tramite un
connettore a Y) a causa del rischio di precipitazione del sale di ceftriaxone-calcio (vedere paragrafi
- 4.4 e 4.5 dell’RCP). Il ceftriaxone e le soluzioni contenenti calcio possono essere somministrati in sequenza uno dopo l'altro se si utilizzano linee di infusione in diverse sedi o se le linee di infusione vengono sostituite o sono state accuratamente lavate con soluzione fisiologica tra un'infusione e l'altra per evitare la formazione di precipitati. A causa del rischio di precipitazione, OLIMEL N12E non deve essere somministrato attraverso la stessa linea di infusione o mescolato con l’antibiotico ampicillina o l’antiepilettico fosfenitoina.
Verificare la compatibilità con le soluzioni somministrate contemporaneamente attraverso lo stesso
set di infusione, catetere o cannula.
Non somministrare prima, contemporaneamente o dopo una emotrasfusione tramite la stessa linea,
a causa del rischio di pseudoagglutinazione.
- I.PRECAUZIONI PARTICOLARI PER LO SMALTIMENTO E LA MANIPOLAZIONE
Una visione di insieme degli vari stadi di preparazione per la somministrazione di OLIMEL N12E viene
illustrata nella Figura 1 .
Apertura
Rimuovere l'involucro esterno di protezione.
Gettare il sacchetto dell'assorbitore di ossigeno.
Verificare l'integrità della sacca e delle membrane di separazione non permanenti. Usare solo se la
sacca non è danneggiata, se le membrane di separazione non permanenti sono intatte (cioè non è
presente miscelazione del contenuto dei 3 compartimenti), se la soluzione di amminoacidi e la
soluzione di glucosio sono limpide, incolori o lievemente gialle, ed in pratica prive di particelle visibili,
e se l'emulsione di lipidi è un liquido omogeneo con aspetto lattiginoso.
Miscelazione delle soluzioni e dell'emulsione
Accertarsi che il prodotto sia a temperatura ambiente quando si rompono le membrane di
separazione non permanenti.
Arrotolare manualmente la sacca su se stessa, partendo dalla parte alta (estremità con cappio). Le
membrane di separazione non permanenti scompariranno dal lato accanto alle aperture. Continuare
ad arrotolare la sacca finché le membrane di separazione non siano aperte per circa metà della loro
lunghezza.
Mescolare la sacca capovolgendola almeno 3 volte.
Dopo la ricostituzione la miscela è una emulsione omogenea di aspetto lattiginoso.
Aggiunte:
La sacca è dotata di una capacità sufficiente a consentire aggiunte, quali vitamine, elettroliti ed
oligoelementi.
Un'eventuale aggiunta (incluse le vitamine) va fatta nella miscela ricostituita (dopo l'apertura delle
membrane di separazione non permanenti e dopo la miscelazione del contenuto dei tre
compartimenti).
È possibile aggiungere vitamine anche nel compartimento del glucosio prima che la miscela sia
ricostituita (prima dell'apertura delle membrane di separazione non permanenti e prima della
miscelazione dei tre compartimenti).
Le aggiunte devono essere effettuate da personale qualificato in condizioni asettiche.
La formulazione OLIMEL N12E può essere supplementata con elettroliti, fosfato inorganico/organico
e con preparazioni disponibili in commercio di prodotti multi-vitaminici (come Cernevit) e multi-
oligoelementi (come Nutryelt). I livelli massimi totali di additivi per elencati nella tabella seguente
sono stati dimostrati dai dati di stabilità e non devono essere considerate raccomandazioni sul
dosaggio. La supplementazione deve essere dettata dalle esigenze cliniche del paziente e non deve
superare le linee guida nutrizionali. Gli elettroliti già presenti nella sacca dovrebbero essere tenuti in
considerazione quando si raggiunge il livello totale massimo.
La compatibilità può variare tra prodotti provenienti da fonti diverse e gli operatori sanitari sono
invitati a effettuare controlli appropriati quando mescolano OLIMEL N12E con altre soluzioni
parenterali.
| a Possibili aggiunte per 1000 mL di OLIMEL N12E (pediatria): | |||
| Livello incluso | n Aggiunta ulteriore massima | Livello totale massimo | |
| Sodio | 35 mmol | 115 mmol | 150 mmol |
| Potassio | 30 mmol | a 120 mmol | 150 mmol |
| Magnesio | i l 4,0 mmol | 1,6 mmol | 5,6 mmol |
| Calcio | a 3,5 mmol | 1,5 mmol | 5,0 mmol |
| Fosfato inorganico | 0 mmol | 0/10 mmol b | 0/10 mmol b |
| Fosfato organico | t I 15 mmol a | 10/0 mmol b | 25/15 mmol a,b |
| Altre aggiunte (oligoelementi, vitamine, selenio e zinco) c | |||
| Oligoelementi – Junyelt d | a 1 fiala per sacca (10mL soluzione concentrata) | ||
| Vitamine e | i 1 fiala (liofilizzato) | ||
| Selenio | z 60 µg per sacca | ||
| n Zinco | 3 mg per sacca | ||
Nell'effettuare aggiunte, prima della somministrazione in vena periferica, misurare l'osmolarità finale
della miscela.
Per eseguire un'aggiunta:
- Operare in condizioni asettiche.
- Preparare il punto d'iniezione della sacca.
- Forare il punto di iniezione e iniettare gli additivi mediante un ago per iniezione o un dispositivo di ricostituzione.
- Miscelare il contenuto della sacca e le aggiunte.
Validità Dopo la ricostituzione:
La stabilità chimica e fisica durante l'uso è stata dimostrata per 7 giorni a 2°C - 8°C, seguita da 48 ore
a temperatura non superiore a 30°C.
Da un punto di vista microbiologico, il prodotto deve essere utilizzato immediatamente. Se non
utilizzato immediatamente, i tempi e le condizioni di conservazione in uso e prima dell'uso sono
| c Possibili aggiunte per 1000 mL di OLIMEL N12E (per adulti): | |||||
| Livello incluso | Aggiunta ulteriore massima | a Livello totale massimo | |||
| Sodio | 35 mmol | 115 mmol | m 150 mmol | ||
| Potassio | 30 mmol | 120 mmol | 150 mmol | ||
| Magnesio | 4,0 mmol | 1,6 mmol | r 5,6 mmol | ||
| Calcio | 3,5 mmol | 1,5 mmol | a 5,0 mmol | ||
| Fosfato inorganico | 0 mmol | 0/10 mmol b | F 0/10 mmol b | ||
| Fosfato organico | 15 mmol a | 10/0 mmol b | 25/15 mmol a,b | ||
| l Altre aggiunte (oligoelementi, vitamine, selenio e zinco) c | |||||
| Oligoelementi– Nutryelt d | e 2 fiale per sacca (10mL soluzione concentrata) | ||||
| Vitamine– Cernevit e | d 1 fiala (5 mLliofilizzato) | ||||
| Selenio | 500 µg per sacca | ||||
| Zinco | a 20 mg per sacca | ||||
responsabilità dell'utente e normalmente non dovrebbero essere superiori a 24 ore a 2-8 °C, a meno
che la ricostituzione non sia avvenuta in condizioni asettiche controllate e validate.
Validità Dopo aggiunta di integrazioni:
Per specifiche miscelazioni, la stabilità in uso chimico fisica è stata dimostrata per 7 giorni a 2°C - 8°C,
seguita da 48 ore a una temperatura non superiore a 30°C.
Da un punto di vista microbiologico, qualunque miscela va utilizzata immediatamente. In caso
contrario, i tempi e le condizioni di conservazione in uso dopo la miscelazione e prima dell’uso sono
responsabilità dell'utente e non devono durare normalmente oltre 24 ore, a 2°C- 8°C, a meno che
l'aggiunta delle integrazioni non sia avvenuta in condizioni asettiche controllate e validate.
Preparazione dell'infusione
L'operazione deve avvenire in condizione asettica.
Sospendere la sacca.
Rimuovere la protezione in plastica dal punto di somministrazione.
Inserire saldamente lo spike del set di infusione nel punto di somministrazione.
Figura 1. Procedimento per la somministrazione di OLIMEL
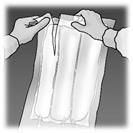
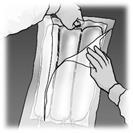

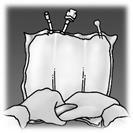
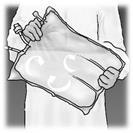
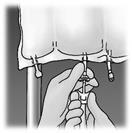
Somministrazione
Solo per uso singolo
Somministrare il prodotto solo dopo la rottura delle membrane di separazione non permanenti tra i 3
compartimenti e la miscelazione del contenuto dei 3 compartimenti.
Accertarsi che l'emulsione finale per l'infusione non mostri evidenza di separazione delle fasi.
Dopo l'apertura della sacca, il contenuto si deve usare immediatamente. Non conservare mai la sacca
aperta per un'infusione successiva.
Non ricollegare eventuali sacche parzialmente utilizzate.
Non collegare le sacche in serie onde evitare la possibilità di embolia gassosa dovuta al gas contenuto
nella sacca principale.
Eliminare eventuale prodotto non utilizzato, eventuali rifiuti derivati e tutti i dispositivi necessari.
Stravaso
La sede del catetere deve essere controllata regolarmente per individuare possibili segni di stravaso.
In caso di stravaso, la somministrazione deve essere interrotta immediatamente mantenendo il
catetere o la cannula inserito per il trattamento immediato del paziente. Se possibile, eseguire
un'aspirazione attraverso il catetere o la cannula inserito per ridurre la quantità di liquido presente
nei tessuti prima di rimuovere il catetere o la cannula.
A seconda del prodotto stravasato (inclusi uno o più prodotti mescolati con OLIMEL N12E, se
applicabile) e dell'estensione o del grado di una possibile lesione, occorre intraprendere misure
specifiche appropriate. Le opzioni di trattamento possono includere un intervento non
farmacologico, farmacologico e/o chirurgico. In caso di stravaso di grande entità, chiedere la
consulenza del chirurgo plastico entro le prime 72 ore.
La sede dello stravaso dovrebbe essere monitorata almeno ogni 4 ore durante le prime 24 ore, poi
una volta al giorno.
L'infusione non dovrebbe essere riavviata nella stessa vena centrale.
-


- Paese di registrazione
- Forma farmaceuticaEmulsione per infusione endovenosa, 1000 ML
- Codice ATCB05BA10
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a OLIMELForma farmaceutica: Soluzione per infusione, 10%Principio attivo: combinationsProduttore: B. BRAUN MELSUNGEN AGPrescrizione richiestaForma farmaceutica: Soluzione per infusione, 1000 MLPrincipio attivo: combinationsProduttore: B. BRAUN MELSUNGEN AGPrescrizione richiestaForma farmaceutica: Soluzione per infusione, 1000 MLPrincipio attivo: combinationsProduttore: BAXTER S.P.A.Prescrizione richiesta
Medici online per OLIMEL
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di OLIMEL — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per OLIMEL online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.














