
Come usare AVTOZMA
Tradotto con IA
Questa pagina fornisce informazioni generali e non sostituisce la consultazione di un medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Rivolgiti ai servizi di emergenza se i sintomi sono gravi.
Mostra traduzioneContenuto del foglietto illustrativo
- Avtozma 20 mg/mL concentrato per soluzione per infusione
- Avtozma 162 mg soluzione iniettabile in siringa preriempita
- Cos’è Avtozma e a cosa serve
- Cosa deve sapere prima di usare Avtozma
- Come usare Avtozma
- Possibili effetti indesiderati
- Come conservare Avtozma
- Contenuto della confezione e altre informazioni
- Istruzioni per l’uso
- Procurarsi tutto il necessario per l’iniezione.
- Ispezionare l’astuccio
- Ispezionare la siringa preriempita.
- Attendere 30 minuti.
- Ispezionare il medicinale.
- Lavarsi le mani.
- Scegliere un sito di iniezione appropriato (vedere
- Pulire il sito di iniezione.
- Rimuovere il cappuccio.
- Inserire la siringa preriempita nel sito di
- Eseguire l’iniezione.
- Rimuovere la siringa preriempita dal sito di
- Cura del sito di iniezione.
- Smaltimento della siringa preriempita.
- Registrazione dell’iniezione.
- Avtozma 162 mg soluzione iniettabile in penna preriempita
- Cos’è Avtozma e a cosa serve
- Cosa deve sapere prima di usare Avtozma
- Come usare Avtozma
- Possibili effetti indesiderati
- Come conservare Avtozma
- Contenuto della confezione e altre informazioni
- Istruzioni per l’uso
- Procurarsi tutto il necessario per l’iniezione.
- Ispezionare l’astuccio
- Ispezionare la penna preriempita.
- Attendere 45 minuti.
- Ispezionare il medicinale.
- Lavarsi le mani.
- Scegliere un sito di iniezione appropriato (vedere
- Pulire il sito di iniezione.
- Rimuovere il cappuccio.
- Inserire la penna preriempita nel sito di iniezione.
- Eseguire l’iniezione.
- Rimuovere la penna preriempita dal sito di
- Cura del sito di iniezione.
- Smaltimento di Avtozma.
- Registrazione dell’iniezione.
Avtozma 20 mg/mL concentrato per soluzione per infusione
tocilizumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima che le venga dato questo medicinale perché contiene
importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei.
- Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, informi il medico o l’infermiere. Vedere paragrafo 4.
contiene importanti informazioni di sicurezza che lei deve conoscere prima che le venga
somministrato Avtozma e durante il trattamento con Avtozma.
Contenuto di questo foglio:
- 1. Cos’è Avtozma e a cosa serve
- 2. Cosa deve sapere prima che le venga somministrato Avtozma
- 3. Come viene somministrato Avtozma
- 4. Possibili effetti indesiderati
- 5. Come conservare Avtozma
- 6. Contenuto della confezione ed altre informazioni
1. Cos’è Avtozma e a cosa serve
Avtozma contiene la sostanza attiva tocilizumab, una proteina prodotta da cellule immunitarie
specifiche (anticorpo monoclonale), che blocca l’azione di una specifica proteina (citochina) chiamata
interleuchina-6. Questa proteina è coinvolta nei processi infiammatori dell’organismo e il suo blocco
può ridurre l’infiammazione nel suo organismo. Avtozma aiuta a ridurre i sintomi come il dolore e la
tumefazione delle articolazioni e può inoltre il suo rendimento nelle attività quotidiane. Avtozma ha
dimostrato di rallentare il danno alla cartilagine e all’osso delle articolazioni causato dalla malattia e di
migliorare la sua capacità di svolgere le normali attività quotidiane.
- Avtozma è utilizzato per trattare adulticon artrite reumatoide (AR) attiva da moderata a grave, una malattia autoimmune, se le precedenti terapie non hanno funzionato abbastanza bene. Avtozma è solitamente usato in associazione con metotressato. Avtozma può anche essere utilizzato da solo se il medico ritiene che metotressato sia inappropriato.
- Avtozma può anche essere utilizzato per trattare pazienti adulti precedentemente non trattati con metotressato se affetti da artrite reumatoide grave, attiva e progressiva.
- Avtozma è utilizzato per trattare bambini con AIGs. Avtozma è usato per bambini di età pari o superiore ai 2 anni che hanno l’ artrite idiopatica giovanile sistemica (AIGs) attiva, una malattia infiammatoria che causa dolore e tumefazione di una o più articolazioni, accompagnata da febbre e rash. Avtozma è usato per migliorare i sintomi dell’AIGs e può essere somministrato in associazione con metotressato o da solo.
- Avtozma è utilizzato nei bambini con AIGp.Avtozma è usato per bambini di età pari o superiore ai 2 anni con artrite idiopatica giovanile poliarticolare (AIGp) attiva, una malattia infiammatoria che causa dolore e tumefazione di una o più articolazioni. Avtozma è usato per migliorare i sintomi dell’AIGp e può essere somministrato in associazione con metotressato o da solo.
- Avtozma è utilizzato per trattare adulti e bambinidi età pari o superiore ai 2 anni con sindrome da rilascio di citochine (CRS)grave o potenzialmente letale, un effetto indesiderato che colpisce i pazienti sottoposti a terapie a base di linfociti CAR-T ( chimeric antigen receptorT-cell) usate per trattare alcune forme tumorali maligne.
- Avtozma è utilizzato per trattare adulticon malattia da coronavirus 2019 (COVID-19) in terapia con corticosteroidi sistemici e che necessitano di ossigenoterapia supplementare o ventilazione meccanica.
2. Cosa deve sapere prima che le venga somministrato Avtozma
Non le verrà somministrato Avtozma
- se è allergicoa tocilizumab o ad uno qualsiasi degli eccipienti di questo medicinale (elencati al paragrafo 6) (vedere le avvertenze speciali alla fine di questo paragrafo con il sottotitolo “Avtozma contiene polisorbato”)
- se ha un’infezione grave attiva. Se una di queste condizioni la riguarda, informi il medico o il personale infermieristico che le esegue l’infusione.
Avvertenze e precauzioni
Informi il medico o l’infermiere prima che le venga somministrato Avtozma.
- Se manifesta reazioni allergiche, quali oppressione al torace, respiro sibilante, forti capogiri una sensazione di stordimento, tumefazione delle labbra o eruzione cutanea durante l’infusione o subito dopo, informi immediatamente il medico.
- Se ha un’ infezionedi qualche tipo di breve o lunga durata, oppure se ha frequenti infezioni. Informi immediatamente il medicose si sente poco bene. Avtozma può ridurre la capacità del corpo di rispondere alle infezioni e potrebbe peggiorare un’infezione esistente o aumentare le possibilità di incorrere in una nuova infezione.
- Se ha avuto la tubercolosi,informi il medico. Il medico ricercherà segni e sintomi della tubercolosi prima di iniziare la terapia con Avtozma. Se i sintomi della tubercolosi (tosse persistente, perdita di peso, svogliatezza, febbre lieve), o qualsiasi altra infezione appaiono durante o dopo la terapia, informi immediatamente il medico.
- Se ha una storia di ulcere intestinalio diverticolite, informi il medico. Tra i sintomi vi potrebbero essere dolore addominale e variazioni inspiegabili degli abituali movimenti intestinali associate a febbre.
- Se ha una malattia del fegato, informi il medico. Prima di usare Avtozma il medico potrebbe voler fare un esame del sangue per esaminare la funzionalità del suo fegato.
- Se un paziente è stato recentemente vaccinato(sia che si tratti di un adulto o di un bambino), o prevede di sottoporsi ad una vaccinazione, informi il medico. Tutti i pazienti, soprattutto i bambini, devono essere in regola con tutte le vaccinazioni prima di iniziare il trattamento con Avtozma, a meno che non sia necessario avviarlo urgentemente. Alcuni tipi di vaccini non devono essere utilizzati durante il trattamento con Avtozma.
- Se ha un tumore, informi il medico. Il medico dovrà decidere se potrà ancora ricevere Avtozma.
- Se ha fattori di rischio cardiovascolariquali aumento della pressione arteriosa o aumento dei livelli di colesterolo, informi il medico. Questi fattori devono essere monitorati mentre assume Avtozma.
- Se ha problemi di funzionalità renaledi grado da moderato a grave, il medico la terrà sotto controllo.
- Se ha mal di testa persistente.
Il medico la sottoporrà ad esami del sangue prima di somministrarle Avtozma e durante il trattamento,
per stabilire se presenta un basso numero dei globuli bianchi o delle piastrine, oppure un elevato
livello degli enzimi del fegato.
Bambini e adolescenti
L’uso di Avtozma non è raccomandato in bambini di età inferiore ai 2 anni.
Se un bambino ha una storia di sindrome da attivazione macrofagica(attivazione e proliferazione
incontrollata di cellule del sangue specifiche), informi il medico. Questi dovrà decidere se il paziente
possa ancora ricevere Avtozma.
Altri medicinali e Avtozma
Informi il medico se lei sta assumendo qualsiasi altro medicinale (o il suo bambino, nel caso questi sia
il paziente) o se ne ha recentemente assunto uno, inclusi medicinali ottenibili senza prescrizione
medica. Avtozma può influire sulle modalità di azione di alcuni medicinali e la dose di questi può
necessitare di aggiustamenti. Informi il medicose sta usando medicinali che contengono i seguenti
principi attivi:
- metilprednisolone, desametasone utilizzati per ridurre l’infiammazione
- simvastatina o atorvastatina, usate per ridurre i livelli di colesterolo
- bloccanti dei canali del calcio (ad es. amlodipina), usati per trattare l’ aumento della pressionesanguigna
- teofillina, usata per trattare l’ asma
- warfarin o fenprocumone, anticoagulanti usati per rendere più fluido il sangue
- fenitoina, usata per trattare le convulsioni
- ciclosporina, usata per sopprimere il sistema immunitariodurante il trapianto di organi
- benzodiazepine (ad es. temazepam), usate per trattare l’ansia.
A causa della mancanza di esperienza clinica, tocilizumab non è indicato per l’uso con altri farmaci
biologici per il trattamento dell’AR, dell’AIGs o dell’AIGp.
Gravidanza, allattamento e fertilità
Avtozma non deve essere usato in gravidanzase non strettamente necessario.
Informi il medico se è in stato di gravidanza, se potrebbe esserlo o se pianifica una gravidanza.
Le donne in età fertiledevono fare uso di un contraccettivo efficace durante e fino a 3 mesi dopo il
trattamento.
Interrompa l’allattamento se sta per esserle dato Avtozmaed informi il medico.
Prima di iniziare l’allattamento, devono passare almeno 3 mesi dall’ultima assunzione di Avtozma.
Non è noto se Avtozma passi nel latte materno
I dati disponibili finora non indicano un effetto sulla fertilità da questo trattamento.
Guida di veicoli e utilizzo di macchinari
Questo medicinale può causare capogiri. Se avverte giramenti di testa, non guidi o usi macchinari.
Avtozma contiene polisorbato
Questo medicinale contiene 0,5 mg di polisorbato 80 per ogni mL. I polisorbati possono provocare
reazioni allergiche. Informi il medico se ha allergie note.
3. Come viene somministrato Avtozma
Questo medicinale è soggetto a prescrizione medica limitata dal medico.
Avtozma sarà somministrato goccia a goccia in vena da un medico o un infermiere.Essi diluiranno
una soluzione, allestiranno l’infusione endovenosa e la terranno sotto osservazione durante e dopo la
somministrazione.
Pazienti adulti affetti da AR
La dose usuale di Avtozma è 8 mg per kg di peso corporeo. A seconda della sua risposta, il medico
potrà diminuire la dose a 4 mg/kg e riportarla a 8 mg/kg quando appropriato.
Ai pazienti adulti Avtozma sarà somministrato ogni 4 settimane attraverso un’iniezione goccia a
goccia in vena (infusione endovenosa) per un’ora.
Bambini affetti da AIGs (di età pari o superiore a 2 anni)
La dose usuale di Avtozma dipende dal peso corporeo.
- Se il peso corporeo è inferiore a 30 kg: la dose è 12 mg per ogni chilogrammo di pesocorporeo.
- Se il peso corporeo è 30 kg o più: la dose è 8 mg per ogni chilogrammo di peso corporeo. La dose viene calcolata in base al peso corporeo ad ogni somministrazione.
Ai bambini affetti da AIGs Avtozma sarà somministrato ogni 2 settimane attraverso un’iniezione
goccia a goccia in vena (infusione endovenosa) per un’ora.
Bambini affetti da AIGp (di età pari o superiore a 2 anni)
La dose usuale di Avtozma dipende dal peso corporeo.
- Se il peso corporeo è inferiore a 30 kg: la dose è 10 mg per ogni chilogrammo di pesocorporeo.
- Se il peso corporeo è 30 kg o più: la dose è 8 mg per ogni chilogrammo di peso corporeoLa dose è calcolata in base al peso corporeo ad ogni somministrazione
Ai bambini con AIGp sarà somministrato Avtozma ogni 4 settimane attraverso un’iniezione goccia a
goccia in vena (infusione endovenosa) per un’ora.
Pazienti con CRS
Nei pazienti di peso uguale o superiore a 30 kg, la dose abituale di Avtozma è pari a 8 mg per ogni
chilogrammo di peso corporeo.
Nei pazienti di peso inferiore a 30 kg, la dose è pari a 12 mg per ogni chilogrammo di peso
corporeo.
Avtozma può essere somministrato da solo o in associazione con corticosteroidi.
Pazienti affetti da COVID-19
La dose indicata di Avtozma è pari a 8 mg per ogni chilogrammo di peso corporeo. Potrebbe
rendersi necessaria una seconda dose.
Se le viene dato più Avtozma di quanto dovuto
Dal momento che Avtozma le verrà somministrato da un medico o da un infermiere, è improbabile che
gliene venga dato troppo. Tuttavia, se ha delle preoccupazioni in merito, si rivolga al medico.
Se non riceve una dose di Avtozma
Dal momento che Avtozma le verrà somministrato da un medico o da un infermiere, è improbabile che
salti una dose. Tuttavia, se ha delle preoccupazioni in merito, si rivolga al medico o all’infermiere.
Se interrompe il trattamento con Avtozma
Non deve sospendere il trattamento con Avtozma senza averne prima parlato con il medico.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico o all’infermiere.
4. Possibili effetti indesiderati
Come tutti i medicinali, Avtozma può causare effetti indesiderati sebbene non tutte le persone li
manifestino. Gli effetti indesiderati possono verificarsi fino a 3 mesi dopo l’ultima assunzione di
Avtozma.
Possibili comuni effetti indesiderati gravi:riferisca immediatamente al medico.
Questi sono comuni: possono colpire fino a 1 utilizzatore su 10
Reazioni allergichedurante o dopo l’infusione:
- difficoltà a respirare, oppressione al torace o stordimento
- eruzione cutanea, prurito, orticaria, tumefazione delle labbra, della lingua o del viso Se nota la comparsa di uno qualsiasi di questi sintomi, informi immediatamenteil medico.
Segni di infezioni gravi
- febbre e brividi
- vesciche nella bocca o sulla pelle
- mal di stomaco
Segni e sintomi di tossicità epatica
Questi possono colpire fino a 1 utilizzatore su 1000
- stanchezza
- dolore addominale
- ittero (ingiallimento della pelle e della parte bianca degli occhi)
Se notasse qualcuno di questi sintomi informi il medico il prima possibile.
Effetti indesiderati molto comuni
Questi possono colpire più di 1 utilizzatore su 10
- infezioni delle vie aeree superiori con tipici sintomi quali tosse, naso chiuso, naso che cola, mal di gola e mal di testa
- livelli elevati di grassi nel sangue (colesterolo).
Effetti indesiderati comuni
Questi possono colpire fino a 1 utilizzatore su 10
- infezione polmonare (polmonite)
- fuoco di Sant’Antonio (herpes zoster)
- febbre delle labbra (herpes simplex orale), formazione di vesciche
- infezioni della pelle (cellulite) talvolta associate a febbre e brividi
- eruzione cutanea e prurito, orticaria
- reazioni allergiche (ipersensibilità)
- infezione agli occhi (congiuntivite)
- mal di testa, capogiri, pressione sanguigna elevata
- ulcere della bocca, mal di stomaco
- ritenzione idrica (edema) nella parte inferiore delle gambe, aumento del peso
- tosse, respiro corto
- basso numero dei globuli bianchi (neutropenia, leucopenia) rilevato tramite gli esami del sangue
- anomalie nei test di funzionalità del fegato (aumento delle transaminasi)
- aumento della bilirubina come evidenziato negli esami del sangue
- bassi livelli di fibrinogeno nel sangue (una proteina coinvolta nella coagulazione del sangue).
Effetti indesiderati non comuni
Questi possono colpire fino a 1 utilizzatore su 100
- diverticolite (febbre, nausea, diarrea, stipsi, mal di stomaco)
- aree arrossate e gonfie nella bocca
- elevati livelli di grassi nel sangue (trigliceridi)
- ulcera gastrica
- calcoli renali
- ipotiroidismo
Effetti indesiderati rari
Questi possono colpire fino a 1 utilizzatore su 1000
- sindrome di Stevens-Johnson (eruzione cutanea, che può comportare formazione di vesciche gravi e desquamazione della pelle)
- reazioni allergiche fatali (anafilassi [fatale])
- infiammazione del fegato (epatite), ittero
Effetti indesiderati molto rari
Questi possono colpire fino a 1 utilizzatore su 10.000
- basso numero dei globuli bianchi, dei globuli rossi e delle piastrine negli esami del sangue
- insufficienza epatica
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Lei può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ allegato V .
Segnalando gli effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza
di questo medicinale.
Bambini affetti da AIGs
In generale, nei pazienti affetti da AIGs sono stati osservati effetti indesiderati di tipo simile a quelli
nei pazienti adulti affetti da AR. Alcuni effetti indesiderati sono stati osservati più frequentemente:
infiammazione di naso e gola, diarrea, bassi globuli bianchi e aumento delle transaminasi del fegato.
Bambini affetti da AIGp
In generale, gli effetti indesiderati nei pazienti AIGp erano di tipo simile a quelli osservati nei pazienti
adulti con AR. Alcuni effetti indesiderati sono stati osservati più frequentemente: infiammazione di
naso e gola, mal di testa, sensazione di malessere (nausea) e bassi globuli bianchi.
5. Come conservare Avtozma
Tenere Avtozma fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sulla scatola. La data di scadenza si
riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2 °C – 8 °C). Non congelare.
Tenere il flaconcino nell’imballaggio esterno per proteggere il medicinale dalla luce.
Se necessario, la soluzione per infusione diluita con soluzione iniettabile di cloruro di sodio 0,9% o
con soluzione iniettabile di cloruro di sodio 0,45% può essere conservata in frigorifero per un massimo
di 1 mese o a una temperatura ambiente non superiore a 30 °C per un massimo di 48 ore.
Non getti alcun medicinale nell’acqua di scarico e nei rifiuti domestici. Chieda al farmacista come
eliminare i medicinali che non utilizza più. Questo aiuterà a proteggere l’ambiente.
6. Contenuto della confezione ed altre informazioni
Cosa contiene Avtozma
- Il principio attivo è tocilizumab. Ciascun flaconcino da 4 mL contiene 80 mg di tocilizumab (20 mg/mL). Ciascun flaconcino da 10 mL contiene 200 mg di tocilizumab (20 mg/mL). Ciascun flaconcino da 20 mL contiene 400 mg di tocilizumab (20 mg/mL).
- Gli eccipienti sono L-istidina, L-treonina, L-metionina, polisorbato 80 e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Avtozma e contenuto della confezione
Avtozma è un concentrato per soluzione per infusione. Il concentrato è un liquido di aspetto da
limpido a leggermente opalescente, da incolore a giallo chiaro.
Avtozma è fornito in flaconcini contenenti 4 mL, 10 mL e 20 mL di concentrato per soluzione per
infusione. Confezioni da 1 e 4 flaconcini. È possibile che non tutte le confezioni siano
commercializzate.
Titolare dell'autorizzazione all'immissione in commercio
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungheria
Produttore
Nuvisan France SARL
2400, Route des Colles,
06410, Biot,
Francia
Midas Pharma GmbH
Rheinstr. 49,
55218 Ingelheim,
Germania
KYMOS S.L.
Ronda Can Fatjó, 7B.
08290 Cerdanyola del Vallès,
Barcelona,
Spagna
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all'immissione in commercio:
België/Belgique/Belgien
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 2 643 71 81
[email protected]
Lietuva
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
Luxembourg/Luxemburg
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 2 643 71 81
[email protected]
Česká republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
България
Celltrion Healthcare Hungary Kft.
Teл.: +36 1 231 0493
Magyarország
Celltrion Healthcare Hungary Kft.
Tel:. +36 1 231 0493
Danmark
Celltrion Healthcare Hungary Kft.
Tlf: +36 1 231 0493
Malta
Mint Health Ltd.
Tel: +356 2093 9800
Deutschland
Celltrion Healthcare Deutschland GmbH
Tel: +49(0)30 346494150
[email protected]
Nederland
Celltrion Healthcare Netherlands B.V.
Tel: + 31 20 888 7300
[email protected]
Eesti
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Norge
Celltrion Healthcare Hungary Kft.
Tlf: +36 1 231 0493
España
CELLTRION FARMACEUTICA (ESPAÑA)
S.L.
Tel: +34 919 94 23 90
Österreich
Astro-Pharma GmbH
Tel: +43 1 97 99 860
Ελλάδα
ΒΙΑΝΕΞ Α.Ε.
Τηλ: +30 210 8009111
Polska
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
France
Celltrion Healthcare France SAS
Tél.: +33 (0)1 71 25 27 00
Portugal
CELLTRION PORTUGAL, UNIPESSOAL
LDA.
Tel: +351 21 936 8542
Hrvatska
Oktal Pharma d.o.o.
Tel: +385 1 6595 777
România
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Ireland
Celltrion Healthcare Ireland Limited
Tel: +353 1 223 4026
Slovenija
OPH Oktal Pharma d.o.o.
Tel.: +386 1 519 29 22
Ísland
Celltrion Healthcare Hungary Kft.
Sími: +36 1 231 0493
Slovenská republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Italia
Celltrion Healthcare Italy S.r.l.
Tel: +39 02 47927040
Suomi/Finland
Celltrion Healthcare Finland Oy.
Puh/Tel: +358 29 170 7755
Κύπρος
C.A. Papaellinas Ltd
Τηλ: +357 22741741
Sverige
Celltrion Sweden AB
[email protected]
Latvija
Celltrion Healthcare Hungary Kft.
Tālr.: +36 1 231 0493
Altre fonti di informazione
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web dell’Agenzia Europea
dei Medicinali: https://www.ema.europa.eu.
Le informazioni seguenti sono destinate esclusivamente agli operatori sanitari:
Istruzioni per la diluizione prima della somministrazione
I medicinali da somministrare per via parenterale devono essere sottoposti a un esame visivo prima
della somministrazione, onde escludere la presenza di sostanza particellata o segni di alterazione del
colore. Si devono diluire solo le soluzioni di aspetto da limpido a leggermente opalescente, da incolore
a giallo chiaro, prive di particelle visibili. Usare un ago e una siringa sterili per preparare Avtozma.
Per le sacche per infusione in cloruro di polivinile (PVC), devono essere utilizzate sacche per
infusione prive di di-2-etilesilftalato (DEHP-free).
Pazienti adulti affetti da AR, COVID-19 e CRS (≥ 30 kg)
In condizioni asettiche, prelevare un volume di soluzione iniettabile sterile, non pirogenica, di cloruro
di sodio 9 mg/mL (0,9%) o 4,5 mg/mL (0,45%) da una sacca per infusione da 100 mL pari al volume
di Avtozma concentrato necessario alla dose del paziente. La quantità necessaria di Avtozma
concentrato (0,4 mL/kg) deve essere prelevata dal flaconcino e immessa nella sacca per infusione da
100 mL. Il volume finale deve essere di 100 mL. Per miscelare la soluzione, capovolgere
delicatamente la sacca per infusione per evitare la formazione di schiuma.
Utilizzo nella popolazione pediatrica
Pazienti affetti da AIGs, AIGp e CRS di peso ≥ 30 kg
In condizioni asettiche, prelevare un volume di soluzione iniettabile sterile, non pirogenica, di cloruro
di sodio 9 mg/mL (0,9%) o 4,5 mg/mL (0,45%) da una sacca per infusione da 100 mL pari al volume
di Avtozma concentrato necessario alla dose del paziente. La quantità necessaria di Avtozma
concentrato ( 0,4 mL/kg) deve essere prelevata dal flaconcino e immessa nella sacca per infusione da
100 mL. Il volume finale deve essere di 100 mL. Per miscelare la soluzione, capovolgere
delicatamente la sacca per infusione per evitare la formazione di schiuma.
Pazienti affetti da AIGs e CRS di peso < 30 kg
In condizioni asettiche, prelevare un volume di soluzione iniettabile sterile, non pirogenica, di cloruro
di sodio 9 mg/mL (0,9%) o 4,5 mg/mL (0,45%) da una sacca per infusione da 50 mL pari al volume di
Avtozma concentrato necessario alla dose del paziente. La quantità necessaria di Avtozma concentrato
( 0,6 mL/kg) deve essere prelevata dal flaconcino e immessa nella sacca per infusione da 50 mL. Il
volume finale deve essere di 50 mL. Per miscelare la soluzione, capovolgere delicatamente la sacca
per infusione per evitare la formazione di schiuma.
Pazienti affetti da AIGp di peso < 30 kg
In condizioni asettiche, prelevare un volume di soluzione iniettabile sterile, non pirogenica, di cloruro
di sodio 9 mg/mL (0,9%) o 4,5 mg/mL (0,45%) da una sacca per infusione da 50 mL pari al volume di
Avtozma concentrato necessario al dosaggio del paziente. La quantità necessaria di Avtozma
concentrato (0,5 mL/kg) deve essere prelevata dal flaconcino e immessa nella sacca per infusione da
50 mL. Il volume finale deve essere di 50 mL. Per miscelare la soluzione, capovolgere delicatamente
la sacca da infusione per evitare la formazione di schiuma.
Avtozma è monouso.
Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità
alla normativa locale vigente.
Avtozma 162 mg soluzione iniettabile in siringa preriempita
tocilizumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di prendere questo medicinale, perché contiene
informazioni importanti per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4
contiene importanti informazioni di sicurezza che lei deve conoscere prima che le venga
somministrato Avtozma e durante il trattamento con Avtozma.
Contenuto di questo foglio:
- 1. Cos’è Avtozma e a cosa serve
- 2. Cosa deve sapere prima di usare Avtozma
- 3. Come usare Avtozma
- 4. Possibili effetti indesiderati
- 5. Come conservare Avtozma
- 6. Contenuto della confezione ed altre informazioni
- 7. Istruzioni per l’uso
1. Cos’è Avtozma e a cosa serve
Avtozma contiene la sostanza attiva tocilizumab, una proteina prodotta da cellule immunitarie
specifiche (anticorpo monoclonale) che blocca l’azione di una specifica proteina (citochina) chiamata
interleuchina-6. Questa proteina è coinvolta nei processi infiammatori dell’organismo e il suo blocco
può ridurre l’infiammazione nel suo organismo. Avtozma è utilizzato per trattare:
- adulti con artrite reumatoide (AR) attiva da moderata a grave, una malattia autoimmune, se le precedenti terapie non hanno funzionato abbastanza.
- adulti con artrite reumatoide (AR) grave, attiva e in progressione,precedentemente non trattati con metotressato.
Avtozma aiuta a ridurre i sintomi della AR, come il dolore e la tumefazione delle articolazioni, e
può inoltre migliorare le sue capacità di effettuare le attività quotidiane. Avtozma ha dimostrato
di rallentare il danno alla cartilagine e all’osso delle articolazioni causato dalla malattia e di
migliorare la sua capacità di svolgere le normali attività quotidiane.
Avtozma è solitamente usato in associazione con un altro medicinale per la AR chiamato
metotressato. Avtozma può comunque essere usato da solo se il medico decide che il
trattamento con metotressato è inappropriato.
- adulti con una malattia delle arterie chiamata arterite a cellule giganti( ACG), provocata dall’infiammazione delle arterie più grosse del corpo, specialmente quelle che portano il sangue alla testa e al collo. I sintomi includono mal di testa, affaticamento e dolore alla mandibola/mascella. Gli effetti possono includere ictus e cecità.
Avtozma può ridurre il dolore e il rigonfiamento di arterie e vene nella testa, nel collo e nelle
braccia.
La ACG è spesso trattata con medicinali chiamati steroidi, che generalmente sono efficaci, ma
possono provocare effetti indesiderati se usati a dosi elevate per periodi prolungati. Inoltre, la
riduzione della dose di steroidi può provocare una riacutizzazione della ACG. Aggiungere
Avtozma al trattamento significa poter utilizzare gli steroidi per un periodo più breve, tendendo
comunque sotto controllo la ACG.
- bambini e adolescenti, di età uguale o superiore a 1 anno, con artrite idiopatica giovanilesistemica (AIGs) attiva, una malattia infiammatoria che causa dolore e tumefazione a carico di una o più articolazioni, nonché febbre ed eruzione cutanea.
Avtozma è usato per determinare un miglioramento dei sintomi dell’AIGs. Può essere
somministrato in combinazione con metotressato o da solo.
- bambini e adolescenti, di età uguale o superiore a 2 anni, con artrite idiopatica giovanilepoliarticolare (AIGp) attiva, una malattia infiammatoria che causa dolore e tumefazione a carico di una o più articolazioni.
Avtozma è usato per determinare un miglioramento dei sintomi dell’AIGp. Può essere
somministrato in combinazione con metotressato o da solo.
2. Cosa deve sapere prima di usare Avtozma
Non usi Avtozma
- se lei o un paziente pediatrico di cui si prende cura è allergico a tocilizumab o ad uno qualsiasi degli eccipienti di questo medicinale (elencati nel paragrafo 6) (vedere le avvertenze speciali alla fine di questo paragrafo con il sottotitolo “Avtozma contiene polisorbato”).
- se lei o un paziente pediatrico di cui si prende cura ha un’infezione grave attiva.
Se una di queste condizioni la riguarda, informi il medico. Non usi Avtozma.
Avvertenze e precauzioni
Parli con il medico, il farmacista o l’infermiere prima di usare Avtozma.
- Se manifesta reazioni allergiche, quali oppressione al torace, respiro sibilante, forti capogiri o una sensazione di stordimento, tumefazione delle labbra, della lingua, prurito alla pelle o al viso, orticaria o eruzione cutanea durante l’iniezione o subito dopo, informi immediatamente ilmedico.
- Se dopo la somministrazione di Avtozma manifesta qualsiasi sintomo indicativo di una reazione allergica, non assuma la dose successiva finché non avrà informato il medico E questi non le avrà detto di prenderla.
- Se ha un’ infezionedi qualsiasi tipo di breve o lunga durata, oppure se ha frequenti infezioni. Informi immediatamente il medicose si sente poco bene. Avtozma può ridurre la capacità del corpo di rispondere alle infezioni e potrebbe peggiorare un’infezione esistente o aumentare le possibilità di incorrere in una nuova infezione.
- Se ha avuto la tubercolosi, informi il medico. Il medico ricercherà segni e sintomi della tubercolosi prima di iniziare la terapia con Avtozma. Se i sintomi della tubercolosi (tosse persistente, perdita di peso, svogliatezza, febbre lieve) o qualsiasi altra infezione appaiono durante o dopo la terapia, informi immediatamente il medico.
- Se ha avuto ulcere intestinalio diverticolite, informi il medico. Tra i sintomi vi potrebbero essere dolore addominale e variazioni inspiegabili delle abitudini intestinali associate a febbre.
- Se ha una malattia del fegato, informi il medico. Prima di usare Avtozma il medico potrebbe voler fare un esame del sangue per esaminare la funzionalità del suo fegato.
- Se un paziente è stato vaccinato di recente o prevede di sottoporsi ad una vaccinazione, informi il medico. Tutti i pazienti devono essere in regola con tutte le vaccinazioni prima di iniziare il trattamento con Avtozma. Alcuni tipi di vaccini non devono essere somministrati durante la terapia con Avtozma.
- Se ha un tumore, informi il medico. Il medico dovrà decidere se potrà ancora ricevere Avtozma.
- Se ha fattori di rischio cardiovascolariquali aumento della pressione arteriosa o aumento dei livelli di colesterolo, informi il medico. Questi fattori devono essere monitorati mentre assume Avtozma.
- Se ha problemi di funzionalità renaledi grado da moderato a grave, il medico la terrà sotto controllo.
- Se ha mal di testa persistente.
Il medico la sottoporrà ad un esame del sangue prima di somministrarle Avtozma, per stabilire se
presenta un basso numero di globuli bianchi o di piastrine, oppure un elevato livello degli enzimi del
fegato.
Bambini e adolescenti
L’uso di Avtozma nella soluzione iniettabile sottocutanea non è raccomandato in bambini di età
inferiore a 1 anno. Avtozma non deve essere somministrato a bambini affetti da AIGs che pesano
meno di 10 kg.
Se un bambino presenta una storia di sindrome da attivazione macrofagica(attivazione e
proliferazione incontrollata di specifiche cellule del sangue), informi il medico. Questi dovrà decidere
se il paziente possa essere comunque trattato con Avtozma.
Altri medicinali e Avtozma
Informi il medico se sta assumendo qualsiasi altro medicinale o se recentemente ne ha assunto uno.
Avtozma può influire sulle modalità di azione di alcuni medicinali e la dose di questi può necessitare
di aggiustamenti. Informi il medicose sta usando medicinali che contengono i seguenti principi attivi:
- metilprednisolone, desametasone utilizzati per ridurre l’infiammazione
- simvastatina o atorvastatina, usate per ridurre i livelli di colesterolo
- bloccanti dei canali del calcio (ad es. amlodipina), usati per trattare l’aumento della pressione sanguigna
- teofillina, usata per trattare l’asma
- warfarin o fenprocumone, anticoagulanti usati per rendere più fluido il sangue
- fenitoina, usata per trattare le convulsioni
- ciclosporina, usata per sopprimere il sistema immunitario durante il trapianto di organi
- benzodiazepine (ad es. temazepam), usate per trattare l’ansia
A causa della mancanza di esperienza clinica, tocilizumab non è indicato per l’uso con altri farmaci
biologici per il trattamento dell’AR, dell’AIGs, dell’AIGp o dell’ACG.
Gravidanza, allattamento e fertilità
Avtozma non deve essere usato in gravidanzase non strettamente necessario. Informi il medico se è
in stato di gravidanza, se potrebbe esserlo o se pianifica una gravidanza.
Le donne in età fertile devonofare uso di un contraccettivo efficace durante e fino a 3 mesi dopo il
trattamento.
Interrompa l’allattamento se sta per esserle dato Avtozmaed informi il medico. Prima di iniziare
l’allattamento, devono passare almeno 3 mesi dall’ultima assunzione di Avtozma. Non è noto se
Avtozma passi nel latte materno
Guida di veicoli e utilizzo di macchinari
Questo medicinale può causare capogiri. Se avverte giramenti di testa, non guidi o usi macchinari.
Avtozma contiene polisorbato
Questo medicinale contiene 0,2 mg di polisorbato 80 per ogni siringa preriempita. I polisorbati
possono provocare reazioni allergiche. Informi il medico se ha allergie note.
3. Come usare Avtozma
Usi sempre questo medicinale seguendo sempre esattamente le istruzioni del medico, del farmacista o
dell'infermiere. Se non è sicuro deve consultare il medico, il farmacista o l’infermiere.
Il trattamento sarà prescritto e iniziato da operatori sanitari esperti nella diagnosi e nel trattamento
della AR, dell’AIGs, dell’AIGp o della ACG.
Dose raccomandata
La dose per gli adulti affetti da AR e ACG è di 162 mg (il contenuto di 1 siringa preriempita)
somministrata una volta a settimana.
Bambini e adolescenti con AIGs (di età uguale o superiore a 1 anno)
La dose abituale di Avtozma dipende dal peso del paziente.
- Se il paziente pesa meno di 30 kg: la dose è pari a 162 mg (il contenuto di 1 siringa preriempita) una volta ogni 2 settimane.
- Se il paziente pesa 30 kg o più: la dose è pari a 162 mg (il contenuto di 1 siringa preriempita) una volta a settimana.
Bambini e adolescenti con AIGp (di età uguale o superiore a 2 anni)
La dose abituale di Avtozma dipende dal peso del paziente.
- Se il paziente pesa meno di 30 kg: la dose è pari a 162 mg (il contenuto di 1 siringa preriempita) una volta ogni 3 settimane.
- Se il paziente pesa 30 kg o più: la dose è pari a 162 mg (il contenuto di 1 siringa preriempita) una volta ogni 2 settimane.
Avtozma è somministrato mediante iniezione sotto la pelle ( sottocutanea). All’inizio, Avtozma potrà
esserle somministrato dal medico o dall’infermiere. Tuttavia, il medico potrebbe decidere che lei è in
grado di iniettarsi Avtozma da solo. In questo caso, lei verrà istruito su come autoiniettarsi Avtozma. I
genitori e coloro che si prendono cura dei pazienti verranno istruiti su come iniettare Avtozma nei
pazienti che non sono in grado di autoiniettarsi il medicinale, quali i bambini.
Parli con il medico se ha eventuali domande sull’autosomministrazione di un’iniezione o sul bambino
somministrazione”.
Se usa più Avtozma di quanto deve
Dal momento che Avtozma le verrà somministrato mediante una siringa preriempita, è improbabile
che gliene venga dato troppo. Tuttavia, se ha delle preoccupazioni in merito, si rivolga al medico, al
farmacista o all’infermiere.
Se un adulto con AR o ACG oppure un bambino o un adolescente con AIGs salta o dimentica
una dose
È molto importante usare Avtozma esattamente come prescritto dal medico. Tenga traccia della sua
prossima dose.
- Se ha dimenticato la dose settimanale e sono trascorsi meno di 7 giorni dalla dose dimenticata, si somministri la dose il successivo giorno programmato.
- Se ha dimenticato la dose a settimane alterne e sono trascorsi meno di 7 giorni dalla dose dimenticata, si inietti la dose non appena se ne ricorda e si somministri quella successiva regolarmente nel giorno e all’ora previsti.
- Se ha dimenticato la dose e sono trascorsi più di 7 giorni dalla dose dimenticata, oppure non è sicuro di quando iniettare Avtozma, si rivolga al medico o al farmacista.
Se un bambino o un adolescente con AIGp salta o dimentica una dose
È molto importante usare Avtozma esattamente come prescritto dal medico. Tenga traccia della
prossima dose.
- Se è stata dimenticata una dose e sono trascorsi meno di 7 giorni dalla dose dimenticata, inietti la dose non appena se ne ricorda e somministri quella successiva regolarmente nel giorno e all’ora previsti.
- Se è stata dimenticata una dose e sono trascorsi più di 7 giorni dalla dose dimenticata, oppure non è sicuro di quando iniettare Avtozma, si rivolga al medico o al farmacista.
Se interrompe il trattamento con Avtozma
Non deve sospendere il trattamento con Avtozma senza averne prima parlato con il medico.
Se ha qualsiasi dubbio sull’uso di questo medicinale, si rivolga al medico, al farmacista o
all’infermiere
4. Possibili effetti indesiderati
Come tutti i medicinali, Avtozma può causare effetti indesiderati sebbene non tutte le persone li
manifestino.
Gli effetti indesiderati potrebbero verificarsi fino a 3 mesi o più dopo l’ultima assunzione di Avtozma.
Possibili effetti indesiderati gravi comuni: riferisca immediatamente al medico.
Questi sono comuni: possono colpire fino a 1 utilizzatore su 10
Reazioni allergichedurante o dopo l’iniezione:
- difficoltà a respirare, oppressione al torace o stordimento;
- eruzione cutanea, prurito, orticaria, tumefazione delle labbra, della lingua o del viso.
Se nota la comparsa di uno qualsiasi di questi sintomi, informi immediatamenteil medico.
Segni di infezioni gravi:
- febbre e brividi
- vesciche nella bocca o sulla pelle
- mal di stomaco
Segni e sintomi di tossicità epatica
Questi possono colpire fino a 1 utilizzatore su 1000
- stanchezza
- dolore addominale
- ittero (ingiallimento della pelle e della parte bianca degli occhi)
Se nota la comparsa di uno qualsiasi di questi sintomi, informi il medico il prima possibile.
Effetti indesiderati molto comuni:
Possono interessare 1 paziente su 10 o più
- infezioni delle vie aeree superiori con sintomi tipici quali tosse, naso chiuso, naso che cola, mal di gola e mal di testa
- livelli elevati di grassi nel sangue (colesterolo)
- reazioni in sede di iniezione.
Effetti indesiderati comuni:
Possono interessare fino a 1 paziente su 10
- infezione polmonare (polmonite)
- fuoco di Sant’Antonio (herpes zoster)
- febbre delle labbra (herpes simplex orale), formazione di vesciche
- infezioni della pelle (cellulite) talvolta associate a febbre e brividi
- eruzione cutanea e prurito, orticaria
- reazioni allergiche (ipersensibilità)
- infezione agli occhi (congiuntivite)
- mal di testa, capogiri, pressione sanguigna elevata
- ulcerazione della bocca, mal di stomaco
- ritenzione idrica (edema) nella parte inferiore delle gambe, aumento del peso
- tosse, respiro corto
- basso numero dei globuli bianchi come evidenziato dagli esami del sangue (neutropenia, leucopenia)
- anomalie nei test di funzionalità del fegato (aumento delle transaminasi)
- aumento della bilirubina come evidenziato dagli esami del sangue.
- bassi livelli di fibrinogeno nel sangue (una proteina coinvolta nella coagulazione del sangue).
Effetti indesiderati non comuni:
Possono interessare fino a 1 paziente su 100
- diverticolite (febbre, nausea, diarrea, stipsi, mal di stomaco)
- aree arrossate e gonfie nella bocca
- elevati livelli di grassi nel sangue (trigliceridi)
- ulcera gastrica
- calcoli renali
- ipotiroidismo.
Effetti indesiderati rari:
Questi possono colpire fino a 1 utilizzatore su 1000
- sindrome di Stevens-Johnson (eruzione cutanea, che può comportare formazione di vesciche gravi e desquamazione della pelle)
- reazioni allergiche fatali (anafilassi [fatale])
- infiammazione del fegato (epatite), ittero.
Effetti indesiderati molto rari:
Possono interessare fino a 1 paziente su 10.000
- basso numero dei globuli bianchi, dei globuli rossi e delle piastrine negli esami del sangue
- insufficienza epatica.
Effetti indesiderati nei bambini e negli adolescenti con AIGs o AIGp
Gli effetti indesiderati osservati nei bambini e negli adolescenti con AIGs o AIGp sono generalmente
simili a quelli registrati negli adulti. Alcuni effetti indesiderati vengono riscontrati più spesso nei
bambini e negli adolescenti: infiammazione del naso e della gola, mal di testa, sensazione di malessere
(nausea) e basse conte dei globuli bianchi.
Se manifesta uno di questi effetti indesiderati, informi il medico, il farmacista o l’infermiere. Questo
Segnalazione degli effetti indesiderati
Se si manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si
rivolga al medico, al farmacista o all’infermiere. Lei può inoltre segnalare gli effetti indesiderati
direttamente tramite il sistema nazionale di segnalazione riportato nell’ allegato V . Segnalando gli
effetti indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza di questo
medicinale.
5. Come conservare Avtozma
Tenere questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sull’astuccio e sull'etichetta della
siringa preriempita (Scad.). La data di scadenza si riferisce all’ultimo giorno del mese.
Conservare in frigorifero (2°C – 8°C). Non congelare. Una volta tolta dal frigorifero, la siringa
preriempita può essere conservata per un massimo di 3 settimane a temperatura pari o inferiore a
30°C.
Tenere le siringhe preriempite nell’imballaggio esterno per proteggerle dalla luce e dall’umidità.
Il medicinale non deve essere usato se la soluzione è torbida o contiene particelle, se non è trasparente
o presenta un colore diverso dal giallo, o se qualsiasi parte della siringa preriempita appare
danneggiata.
La siringa non deve essere agitata. Dopo aver rimosso il cappuccio, l'iniezione deve essere avviata
entro 5 minuti per evitare che il medicinale si secchi e blocchi l'ago. Se la siringa preriempita non
viene utilizzata entro 5 minuti dalla rimozione del cappuccio, è necessario smaltirla in un contenitore
resistente alla perforazione e utilizzare una nuova siringa preriempita.
Se dopo l'inserimento dell'ago non è possibile spingere lo stantuffo, è necessario gettare la siringa
preriempita in un contenitore resistente alla perforazione e utilizzare una nuova siringa preriempita.
6. Contenuto della confezione e altre informazioni
Cosa contiene Avtozma
- Il principio attivo è tocilizumab. Ciascuna siringa preriempita da 0,9 mL contiene 162 mg di tocilizumab.
- Gli altri eccipienti sono L-istidina, L-treonina, L-metionina, polisorbato 80 e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Avtozma e contenuto della confezione
Avtozma è una soluzione iniettabile. La soluzione è da trasparente a giallo.
Avtozma è fornito in siringa preriempita da 0,9 mL contenente 162 mg di tocilizumab soluzione
iniettabile.
La siringa preriempita di Avtozma per l’uso da parte dei pazienti è disponibile in confezioni
contenenti:
- 1 siringa preriempita
- 4 siringhe preriempite
- 12 (3 confezioni da 4) siringhe preriempite (confezioni multiple)
È probabile che non tutte le confezioni siano commercializzate.
Titolare dell'autorizzazione all'immissione in commercio
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungheria
Produttore
Nuvisan France SARL
2400, Route des Colles,
06410, Biot,
Francia
Midas Pharma GmbH
Rheinstr. 49,
55218 Ingelheim,
Germania
KYMOS S.L.
Ronda Can Fatjó, 7B.
08290 Cerdanyola del Vallès,
Barcelona,
Spagna
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all'immissione in commercio:
België/Belgique/Belgien
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 2 643 71 81
[email protected]
Lietuva
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
България
Celltrion Healthcare Hungary Kft.
Teл.: +36 1 231 0493
Luxembourg/Luxemburg
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 2 643 71 81
[email protected]
Česká republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Magyarország
Celltrion Healthcare Hungary Kft.
Tel:. +36 1 231 0493
Danmark
Celltrion Healthcare Hungary Kft.
Tlf: +36 1 231 0493
Malta
Mint Health Ltd.
Tel: +356 2093 9800
Deutschland
Celltrion Healthcare Deutschland GmbH
Tel: +49 (0)30 346494150
[email protected]
Nederland
Celltrion Healthcare Netherlands B.V.
Tel: + 31 20 888 7300
[email protected]
Eesti
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Norge
Celltrion Healthcare Hungary Kft.
Tlf: +36 1 231 0493
España
CELLTRION FARMACEUTICA (ESPAÑA)
S.L.
Tel: +34 919 94 23 90
Österreich
Astro-Pharma GmbH
Tel: +43 1 97 99 860
Ελλάδα
ΒΙΑΝΕΞ Α.Ε.
Τηλ: +30 210 8009111
Polska
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
France
Celltrion Healthcare France SAS
Tél.: +33 (0)1 71 25 27 00
Portugal
CELLTRION PORTUGAL, UNIPESSOAL
LDA.
Tel: +351 21 936 8542
Hrvatska
Oktal Pharma d.o.o.
Tel: +385 1 6595 777
România
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Ireland
Celltrion Healthcare Ireland Limited
Tel: +353 1 223 4026
Slovenija
OPH Oktal Pharma d.o.o.
Tel.: +386 1 519 29 22
Ísland
Celltrion Healthcare Hungary Kft.
Sími: +36 1 231 0493
Slovenská republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Italia
Celltrion Healthcare Italy S.r.l.
Tel: +39 02 47927040
Suomi/Finland
Celltrion Healthcare Finland Oy.
Puh/Tel: +358 29 170 7755
Κύπρος
C.A. Papaellinas Ltd
Τηλ: +357 22741741
Sverige
Celltrion Sweden AB
[email protected]
Latvija
Celltrion Healthcare Hungary Kft.
Tālr.: +36 1 231 0493
Altre fonti di informazione
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia Europea
dei Medicinali: https://www.ema.europa.eu .
7. Istruzioni per l’uso
Legga e segua le istruzioni per l’uso allegate alla sua siringa preriempita di Avtozma prima di iniziare
a usarla ogni volta che ottiene una ricarica. Potrebbero esserci nuove informazioni. Prima di usare
Avtozma per la prima volta, un operatore sanitario le mostrerà come farlo in modo corretto.
Informazioni importanti
- Nonrimuovere il cappuccio della siringa preriempita fino a quando non si è pronti a iniettarsi Avtozma.
- Non cercare mai di smontare la siringa preriempita.
- Nonriutilizzare mai la stessa siringa.
- Nonagitare la siringa preriempita.
- Nonusare la siringa preriempita se è caduta o appare danneggiata.
- Indicazioni per il paziente sulle reazioni di ipersensibilità (o anafilassi):nel caso in cui, durante o a seguito di un’iniezione, sviluppi in qualsiasi momento, mentre non si trova in ambulatorio, sintomi quali, ma non limitati a, eruzione cutanea, prurito, brividi, gonfiore del volto, delle labbra, della lingua o della gola, dolore al torace, respiro sibilante, difficoltà a respirare o a deglutire, capogiri o svenimento, deve immediatamente recarsi al pronto soccorso.
Conservazione di Avtozma
- Conservare la siringa preriempita non utilizzata nell’astuccio originale e in frigorifero a una temperatura compresa tra 2 °C e 8 ºC. Noncongelare.
- Una volta tolto dal frigorifero, Avtozma può essere conservato per un massimo di 3 settimane a temperatura pari o inferiore a 30 °C. Se non utilizzato entro 3 settimane, Avtozma deve essere smaltito.
- Tenere la siringa preriempita lontano dalla luce solare diretta.
- Nonrimuovere la siringa preriempita dall’astuccio originale durante la conservazione.
- Nonlasciare la siringa preriempita incustodita.
- Tenere la siringa preriempita fuori dalla portata dei bambini. Contiene parti piccole.
Parti della siringa preriempita (vedere Figura A).
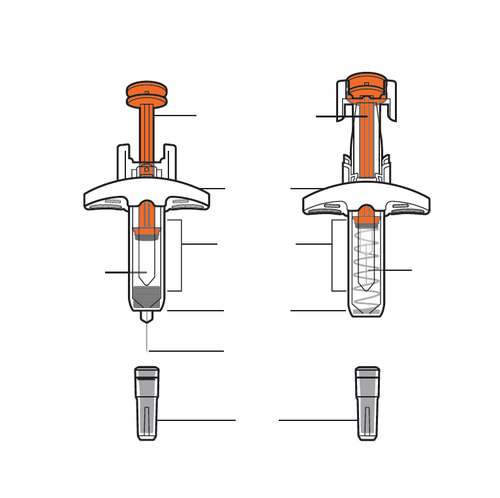
Prima dell’usoDopo l’uso
Stantuffo
arancione
Impugnatura
bianca
Finestra di
osservazione
MedicinaleAgo
Protezione
dell’ago
Ago
Cappuccio
Figura A
Preparazione dell’iniezione
1. Procurarsi tutto il necessario per l’iniezione.
- a.Prepari una superficie pulita e piatta, come ad esempio un tavolo o un bancone, in una zona ben illuminata.
- b.Tolga l’astuccio contenente la siringa preriempita dal frigorifero.
- c.Si assicuri di avere a disposizione l’occorrente di seguito specificato (vedere Figura B):
- Astuccio contenente la siringa preriempita di Avtozma
Non in dotazione nell’astuccio:
- Batuffolo di cotone o garza
- Cerotto
- Contenitore per materiali taglienti
- Tampone imbevuto d’alcol
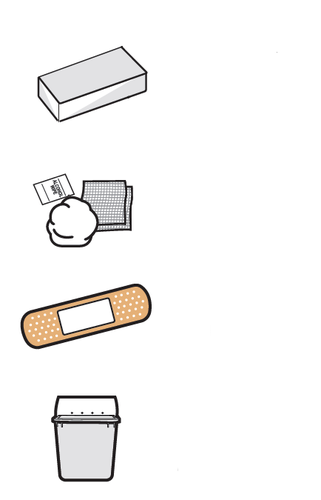
Astuccio
contenente la
siringa
preriempita
Batuffolo di
cotone o garza
e tampone
imbevuto di
alcol
Cerotto
Contenitore
per materiali
taglienti
Figura B
2. Ispezionare l’astuccio
- a.Esamini l’astuccio e si assicuri di avere il medicinale (Avtozma) e il dosaggio corretti.
- b.Controlli la data di scadenza riportata sull’astuccio per assicurarsi che non sia passata.
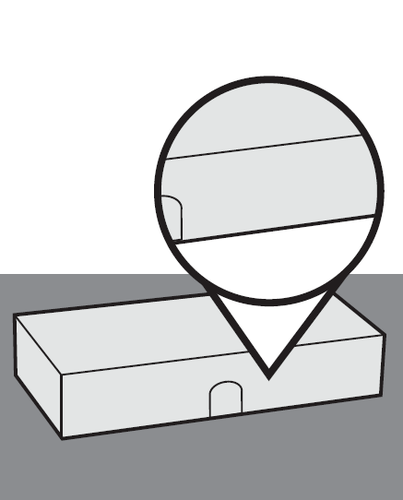
- Nonusi la siringa preriempita se la data di scadenza è già passata.
- Nonusi la siringa preriempita se sta aprendo l’astuccio per la prima volta e le sembra che sia già stato aperto o che sia danneggiato e controlli che sia correttamente sigillato.
Figura C
3. Ispezionare la siringa preriempita.
- a.Apra l’astuccio ed estragga 1 siringa preriempita monodose. Rimetta in frigorifero le eventuali siringhe preriempite di Avtozma presenti nell’astuccio.
- b.Controlli la data di scadenza riportata sulla siringa preriempita di Avtozma ( vedere Figura D).
- Nonusi la siringa preriempita se la data di scadenza è passata. Se la data di scadenza è passata, getti la siringa preriempita nel contenitore per materiali taglienti e ne prenda una nuova.
- c.Controlli la siringa preriempita per verificare che non sia danneggiata e non vi siano segni di fuoriuscite di liquido.
- Nonusi la siringa preriempita se è caduta, è danneggiata o presenta fuoriuscite di liquido.
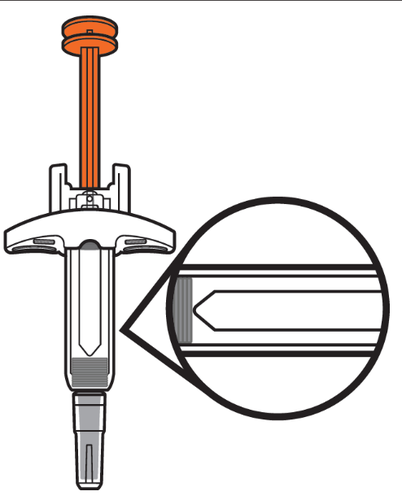
Figura D
4. Attendere 30 minuti.
- a.Lasci la siringa preriempita fuori dall’astuccio a temperatura ambiente (tra 20 °C e 25 °C) per 30 minuti affinché si riscaldi (vedere Figura E).
- Nonriscaldi la siringa preriempita utilizzando fonti di calore come ad esempio acqua calda o microonde.
- Nonlasci la siringa preriempita alla luce solare diretta.
- Nonrimuova il cappuccio mentre la siringa preriempita raggiunge la temperatura ambiente.
- Se la siringa preriempita non raggiunge la temperatura ambiente, potrebbe provare fastidio e avere difficoltà a premere lo stantuffo.
30
minuti
Figura E
5. Ispezionare il medicinale.
- a.Tenga Avtozma con il cappuccio indirizzato verso il basso.
- b.Osservi il medicinale e si assicuri che il liquido sia trasparente e da incolore a giallo chiaro e che non contenga particelle o scaglie (vedere Figura F).
- Nonusi la siringa preriempita se il liquido è torbido, di colore alterato o se contiene particelle o scaglie. Getti la siringa preriempita in un contenitore per materiali taglienti e ne usi una nuova.
- La presenza di bolle d’aria è normale.
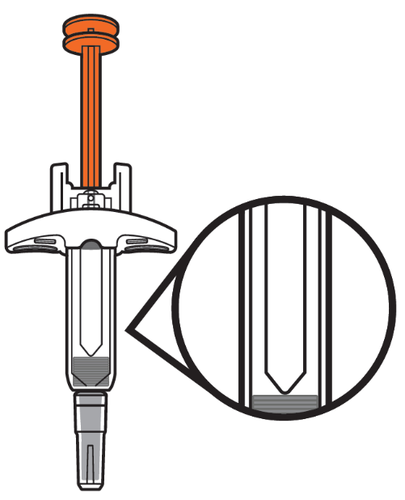
Figura F
6. Lavarsi le mani.
- a.Si lavi bene le mani con acqua e sapone e le asciughi (vedere Figura G).
Figura G
7. Scegliere un sito di iniezione appropriato (vedere
Figura H).
- a.I siti in cui è possibile effettuare l’iniezione sono:
- la parte anteriore delle cosce;
- l’addome, ad eccezione dell’area di 5 cm attorno all’ombelico;
- la zona esterna della parte superiore delle braccia (solo se a eseguire l’iniezione è la persona che le presta assistenza o l’operatore sanitario).
- Nonsi autosomministri l’iniezione nella zona esterna della parte superiore delle braccia.
- Ogni volta che si somministra un’iniezione deve essere utilizzata una sede diversa ad almeno 2,5 cm di distanza dall’area utilizzata per l’iniezione precedente.
- Nonesegua l’iniezione su nei, cicatrici, lividi o nelle aree in cui la pelle si presenta dolente, arrossata o indurita.
- Nonpratichi l’iniezione attraverso i vestiti.
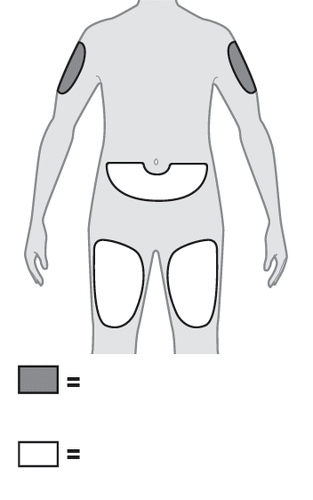
Figura H
8. Pulire il sito di iniezione.
- a.Disinfetti il sito di iniezione utilizzando un tampone imbevuto di alcol e lo lasci asciugare per circa 10 secondi (vedere Figura I). Questo ridurrà il rischio di infezione.
- Si assicuri di nontoccare quest’area prima di eseguire l’iniezione.
- Nonsoffi, né sventoli l’area disinfettata.
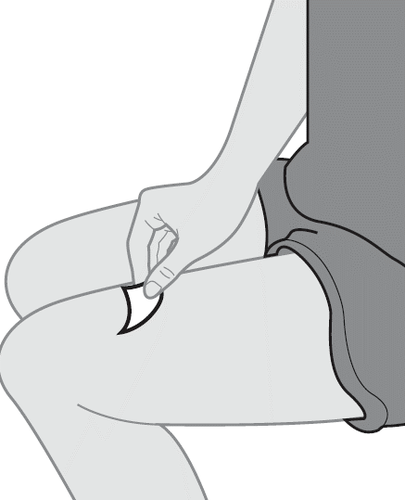
Figura I
Somministrazione dell’iniezione
9. Rimuovere il cappuccio.
- a.Tenga con una mano la siringa preriempita afferrandola per il corpo. Con l’altra mano sfili delicatamente il cappuccio tirandolo in orizzontale (vedere Figura J). Nota: se non riesce a rimuovere il cappuccio, chieda aiuto alla persona che le presta ssistenza o si rivolga all’operatore sanitario.
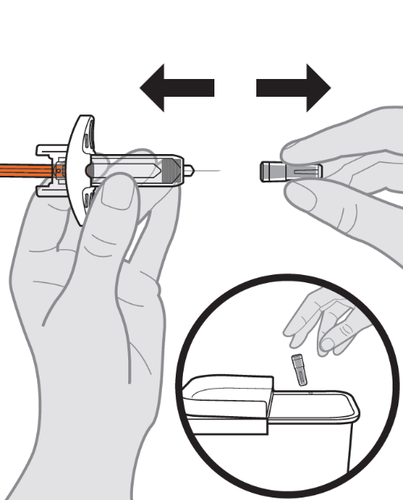
- Nontenga lo stantuffo mentre rimuove il cappuccio.
- È possibile che noti una goccia di liquido sulla punta dell’ago. Si tratta di una condizione normale.
- Nel caso in cui non venga utilizzata entro 5 minuti dalla rimozione del cappuccio dell’ago, la siringa preriempita deve essere smaltita in un contenitore resistente alla perforazione o in un contenitore per materiali taglienti e deve essere impiegata una nuova siringa preriempita.
- b.Smaltisca immediatamente il cappuccio nel contenitore per materiali taglienti (vedere fase 14“ Smaltimento della siringa preriempita”e Figura N) Figura J
- Nonreinserisca il cappuccio sulla siringa preriempita.
- Nontocchi il manicotto di sicurezza per l’ago collocato sulla punta della siringa preriempita al fine di evitare una lesione da puntura accidentale.
10. Inserire la siringa preriempita nel sito di
iniezione.
- a.Con una mano pizzichi delicatamente una plica di cute in corrispondenza del sito di iniezione.
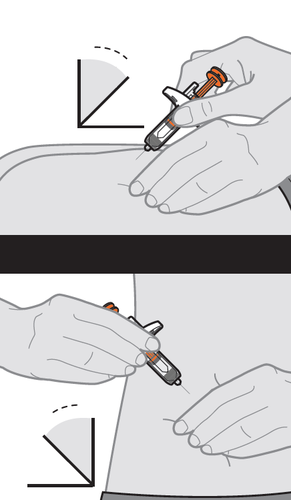
90°
45°
OK
Nota: questa operazione è importante per garantire
che l’iniezione avvenga sotto la pelle (nel tessuto
adiposo) e non a una profondità maggiore (nel
muscolo).
O
- Nontiri indietro lo stantuffo.
- b.Inserisca l’ago in tutta la sua lunghezza nella plica cutanea con un angolo di inclinazione compreso tra 45° e 90°, effettuando un movimento rapido e deciso (vedere Figura K). 90°45°OKNota: la scelta dell’angolo di inclinazione corretto è importante poiché assicura che il medicinale venga rilasciato sotto la pelle (nel tessuto adiposo); in caso contrario l’iniezione potrebbe risultare dolorosa e il medicinale non efficace. Figura K
- Nontocchi lo stantuffo mentre inserisce l’ago nella pelle.
11. Eseguire l’iniezione.
- a.Dopo aver inserito l’ago, rilasci la plica cutanea.
- b.Prema lentamente lo stantuffo fino a fine corsa, fino a quando non è stata somministrata l’intera dose di medicinale e la siringa è vuota (vedere Figura L).
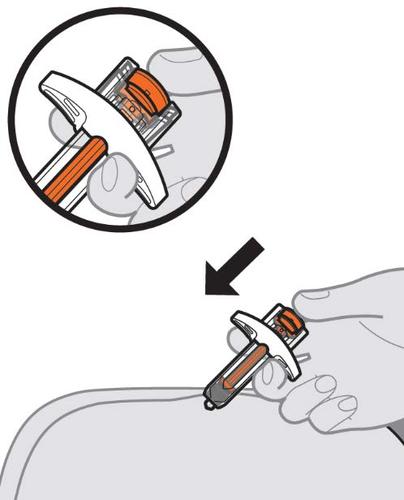
- Se non è possibile premere verso il basso lo stantuffo, è necessario smaltire la siringa preriempita e usare una nuova siringa preriempita.
- Nonmodifichi la posizione della siringa preriempita dopo aver iniziato a iniettare il medicinale.
- Se lo stantuffo non viene premuto completamente, la protezione dell’ago non si estenderà per coprire l’ago quando quest’ultimo viene estratto.
- Se l’ago non viene coperto, proceda con cautela e smaltisca la siringa (vedere fase 14“Smaltimento della siringa preriempita”). Figura L
12. Rimuovere la siringa preriempita dal sito di
iniezione.
- a.Quando la siringa preriempita è vuota, rimuova l’ago dal sito di iniezione e rilasci lo stantuffo fino a quando l’ago non viene completamente coperto dalla protezione (vedere Figura M).
- Potrebbero verificarsi eventi di sanguinamento (vedere fase 13 “Cura del sito di iniezione”).
- In caso di contatto del medicinale con la cute, lavare l’area con acqua.
- Nonriutilizzare la siringa preriempita.
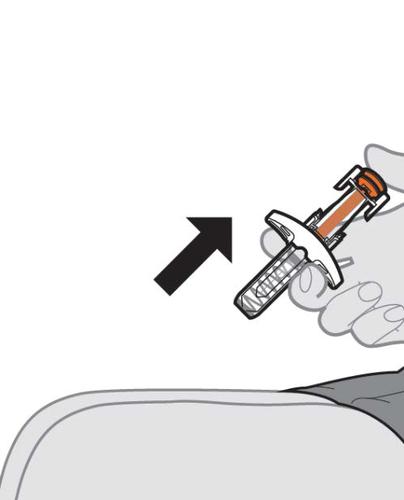
Figura M
Dopo l’iniezione
13. Cura del sito di iniezione.
- a.Se nota la presenza di qualche goccia di sangue, può trattare il sito di iniezione premendo delicatamente, senza strofinare, un batuffolo di cotone o una garza sul sito e applicare un cerotto, se necessario.
- Nonstrofini il sito di iniezione.
14. Smaltimento della siringa preriempita.
- a.Riponga la siringa preriempita nel contenitore per materiali taglienti subito dopo l’uso (vedere Figura N).
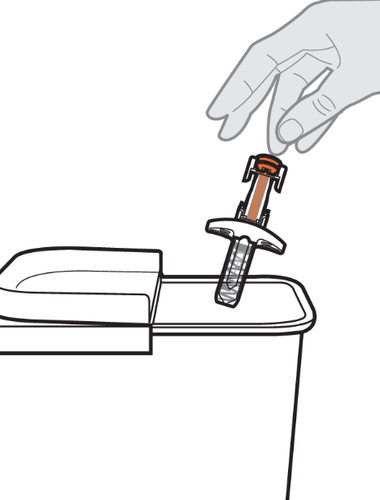
Nota: se l’iniezione le viene somministrata da
un’altra persona, questa persona deve fare attenzione
durante la rimozione della siringa preriempita e il suo
smaltimento al fine di evitare una lesione da puntura
accidentale e la trasmissione di un’infezione .
- Nonriutilizzi la siringa preriempita.
- Nonreinserisca il cappuccio sulla siringa preriempita.
- Nongetti (smaltisca) il contenitore per materiali taglienti nei rifiuti domestici.
- Nonricicli il contenitore per materiali taglienti.
- Tenga la siringa preriempita di Avtozma e il contenitore per materiali taglienti fuori dalla portata dei bambini.
Smaltisca il contenitore pieno attenendosi alle istruzioni
ricevute dall’operatore sanitario o dal farmacista. Se non
dispone di un contenitore per materiali taglienti, può
utilizzare un contenitore per i rifiuti domestici richiudibile e
resistente alla perforazione. Il medicinale non utilizzato e i
rifiuti derivati da tale medicinale devono essere smaltiti in
conformità alla normativa locale vigente.
15. Registrazione dell’iniezione.
- a.Annoti la data, l’ora e la parte del corpo specifica in cui ha praticato l’iniezione. Figura N
Avtozma 162 mg soluzione iniettabile in penna preriempita
tocilizumab
Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di
nuove informazioni sulla sicurezza. Lei può contribuire segnalando qualsiasi effetto indesiderato
riscontrato durante l’assunzione di questo medicinale. Vedere la fine del paragrafo 4 per le
informazioni su come segnalare gli effetti indesiderati.
Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
importanti informazioni per lei.
- Conservi questo foglio. Potrebbe aver bisogno di leggerlo di nuovo.
- Se ha qualsiasi dubbio, si rivolga al medico, al farmacista o all’infermiere.
- Questo medicinale è stato prescritto soltanto per lei. Non lo dia ad altre persone, anche se i sintomi della malattia sono uguali ai suoi, perché potrebbe essere pericoloso.
- Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga al medico, al farmacista o all’infermiere. Vedere paragrafo 4.
contiene importanti informazioni di sicurezza che lei deve conoscere prima che le venga
somministrato Avtozma e durante il trattamento con Avtozma.
Contenuto di questo foglio:
- 1. Cos’è Avtozma e a cosa serve
- 2. Cosa deve sapere prima di usare Avtozma
- 3. Come usare Avtozma
- 4. Possibili effetti indesiderati
- 5. Come conservare Avtozma
- 6. Contenuto della confezione e altre informazioni
- 7. Istruzioni per l’uso
1. Cos’è Avtozma e a cosa serve
Avtozma contiene il principio attivo tocilizumab, una proteina prodotta da cellule immunitarie
specifiche (anticorpo monoclonale) che blocca l’azione di una specifica proteina (citochina) chiamata
interleuchina-6. Questa proteina è coinvolta nei processi infiammatori dell’organismo e il suo blocco
può ridurre l’infiammazione nel suo organismo. Avtozma è utilizzato per trattare:
- adulti con artrite reumatoide (AR) attiva da moderata a grave, una malattia autoimmune, se le precedenti terapie non hanno funzionato abbastanza.
- adulti con artrite reumatoide (AR) grave, attiva e in progressione,precedentemente non trattati con metotressato.
Avtozma aiuta a ridurre i sintomi della AR, come il dolore e la tumefazione delle articolazioni, e
può inoltre migliorare le sue capacità di effettuare le attività quotidiane. Avtozma ha dimostrato
di rallentare il danno alla cartilagine e all’osso delle articolazioni causato dalla malattia e di
migliorare la sua capacità di svolgere le normali attività quotidiane.
Avtozma è solitamente usato in associazione con un altro medicinale per la AR chiamato
metotressato. Avtozma può comunque essere usato da solo se il medico decide che il
trattamento con metotressato è inappropriato.
- adulti con una malattia delle arterie chiamata arterite a cellule giganti( ACG), provocata dall’infiammazione delle arterie più grosse del corpo, specialmente quelle che portano il sangue alla testa e al collo. I sintomi includono mal di testa, affaticamento e dolore alla mandibola/mascella. Gli effetti possono includere ictus e cecità.
Avtozma può ridurre il dolore e il rigonfiamento di arterie e vene nella testa, nel collo e nelle
braccia.
La ACG è spesso trattata con medicinali chiamati steroidi, che generalmente sono efficaci, ma
possono provocare effetti indesiderati se usati a dosi elevate per periodi protratti. Inoltre, la
riduzione della dose di steroidi può provocare una riacutizzazione della ACG. Aggiungere
Avtozma al trattamento significa poter utilizzare gli steroidi per un periodo più breve, tenendo
comunque sotto controllo la ACG.
- bambini e adolescenti, di età uguale o superiore a 12 anni, conartrite idiopatica giovanilesistemica(AIGs) attiva, una malattia infiammatoria che causa dolore e tumefazione a carico di una o più articolazioni, nonché febbre ed eruzione cutanea.
Avtozma è usato per determinare un miglioramento dei sintomi dell’AIGs. Può essere
somministrato in combinazione con metotressato o da solo.
- bambini e adolescenti, di età uguale o superiore a 12 anni, conartrite idiopatica giovanilepoliarticolare(AIGp) attiva, una malattia infiammatoria che causa dolore e tumefazione a carico di una o più articolazioni.
Avtozma è usato per determinare un miglioramento dei sintomi dell’AIGp. Può essere
somministrato in combinazione con metotressato o da solo.
2. Cosa deve sapere prima di usare Avtozma
Non usi Avtozma
- se lei o un paziente pediatrico di cui si prende cura è allergico a tocilizumab o ad uno qualsiasi degli altri componenti di questo medicinale (elencati nel paragrafo 6) (vedere le avvertenze speciali alla fine di questo paragrafo con il sottotitolo “Avtozma contiene polisorbato”).
- se lei o un paziente pediatrico di cui si prende cura ha un’infezione grave attiva.
Se una di queste condizioni la riguarda, informi il medico. Non usi Avtozma.
Avvertenze e precauzioni
Parli con il medico, il farmacista o l’infermiere prima di usare Avtozma.
- Se manifesta reazioni allergiche, quali oppressione al torace, respiro sibilante, forti capogiri o una sensazione di stordimento, tumefazione delle labbra, della lingua, prurito alla pelle o al viso, orticaria o eruzione cutanea durante l’iniezione o subito dopo, informi immediatamente ilmedico.
- Se dopo la somministrazione di Avtozma manifesta qualsiasi sintomo indicativo di una reazione allergica, non assuma la dose successiva finché non avrà informato il medico E questi non le avrà detto di prenderla.
- Se ha un’ infezionedi qualsiasi tipo di breve o lunga durata, oppure se ha frequenti infezioni. Informi immediatamente il medicose si sente poco bene. Avtozma può ridurre la capacità del corpo di rispondere alle infezioni e potrebbe peggiorare un’infezione esistente o aumentare le possibilità di incorrere in una nuova infezione.
- Se ha avuto la tubercolosi, informi il medico. Il medico ricercherà segni e sintomi della tubercolosi prima di iniziare la terapia con Avtozma. Se i sintomi della tubercolosi (tosse persistente, perdita di peso, svogliatezza, febbre lieve) o qualsiasi altra infezione appaiono durante o dopo la terapia, informi immediatamente il medico.
- Se ha avuto ulcere intestinalio diverticolite, informi il medico. Tra i sintomi vi potrebbero essere dolore addominale e variazioni inspiegabili delle abitudini intestinali associate a febbre.
- Se ha una malattia del fegato, informi il medico. Prima di usare Avtozma il medico potrebbe voler fare un esame del sangue per esaminare la funzionalità del suo fegato.
- Se un paziente è stato vaccinato di recenteo prevede di sottoporsi ad una vaccinazione, deve informare il medico. Tutti i pazienti devono essere in regola con tutte le vaccinazioni prima di iniziare il trattamento con Avtozma. Alcuni tipi di vaccini non devono essere somministrati durante la terapia con Avtozma.
- Se ha un tumore, informi il medico. Il medico dovrà decidere se potrà ancora ricevere Avtozma.
- Se ha fattori di rischio cardiovascolariquali aumento della pressione arteriosa o aumento dei livelli di colesterolo, informi il medico. Questi fattori devono essere monitorati mentre assume Avtozma.
- Se ha problemi di funzionalità renaledi grado da moderato a grave, il medico la terrà sotto controllo.
- Se ha mal di testa persistente.
Il medico la sottoporrà ad esami del sangue prima di somministrarle Avtozma, per stabilire se presenta
un basso numero dei globuli bianchi o delle piastrine, oppure un elevato livello degli enzimi del
fegato.
Bambini e adolescenti
L’uso di Avtozma in penna preriempita non è raccomandato in bambini di età inferiore a 12 anni.
Avtozma non deve essere somministrato a bambini affetti da AIGs che pesano meno di 10 kg.
Se un bambino presenta una storia di sindrome da attivazione macrofagica(attivazione e
proliferazione incontrollata di specifiche cellule del sangue), informi il medico. Il medico dovrà
decidere se il paziente possa essere comunque trattato con Avtozma.
Altri medicinali e Avtozma
Informi il medico se sta assumendo o ha recentemente assunto qualsiasi altro medicinale. Avtozma
può influire sulle modalità di azione di alcuni medicinali e la dose di questi può necessitare di
aggiustamenti. Informi il medicose sta usando medicinali che contengono i seguenti principi attivi:
- metilprednisolone, desametasone utilizzati per ridurre l’infiammazione
- simvastatina o atorvastatina, usate per ridurre i livelli di colesterolo
- bloccanti dei canali del calcio (ad es. amlodipina), usati per trattare l’aumento della pressione sanguigna
- teofillina, usata per trattare l’asma
- warfarin o fenprocumone, anticoagulanti usati per rendere più fluido il sangue
- fenitoina, usata per trattare le convulsioni
- ciclosporina, usata per sopprimere il sistema immunitario durante il trapianto di organi
- benzodiazepine (ad es. temazepam), usate per trattare l’ansia.
A causa della mancanza di esperienza clinica, tocilizumab non è indicato per l’uso con altri farmaci
biologici per il trattamento della AR, della AIGs, della AIGp o della ACG.
Gravidanza, allattamento e fertilità
Avtozma non deve essere usato in gravidanzase non strettamente necessario. Informi il medico se è
in stato di gravidanza, se potrebbe esserlo o se pianifica una gravidanza.
Le donne in età fertile devonofare uso di un contraccettivo efficace durante e fino a 3 mesi dopo il
trattamento.
Interrompa l’allattamento se sta per esserle dato Avtozmae informi il medico. Prima di iniziare
l’allattamento, devono passare almeno 3 mesi dall’ultima assunzione di Avtozma. Non è noto se
Avtozma passi nel latte materno.
Guida di veicoli e utilizzo di macchinari
Questo medicinale può causare capogiri. Se avverte giramenti di testa, non guidi o usi macchinari.
Avtozma contiene polisorbato
Questo medicinale contiene 0,2 mg di polisorbato 80 per ogni siringa preriempita. I polisorbati
possono provocare reazioni allergiche. Informi il medico se ha allergie note.
3. Come usare Avtozma
Usi questo medicinale seguendo sempre esattamente le istruzioni del medico, del farmacista o
dell’infermiere. Se ha dubbi consulti il medico, il farmacista o l’infermiere.
Il trattamento sarà prescritto e iniziato da operatori sanitari esperti nella diagnosi e nel trattamento
della AR, della AIGs, della AIGp o della ACG.
Dose raccomandata
La dose per tutti gli adulti affetti da AR o ACG è di 162 mg (il contenuto di 1 penna preriempita)
somministrati una volta a settimana.
Adolescenti con AIGs (di età uguale o superiore a 12 anni)
La dose abituale di Avtozma dipende dal peso del paziente.
- Se il paziente pesa meno di 30 kg: la dose è pari a 162 mg (il contenuto di 1 penna preriempita) una volta ogni 2 settimane.
- Se il paziente pesa 30 kg o più: la dose è pari a 162 mg (il contenuto di 1 penna preriempita) una volta a settimana.
La penna preriempita non deve essere usata per trattare bambini di età inferiore a 12 anni.
Adolescenti con AIGp (di età uguale o superiore a 12 anni) La dose abituale di Avtozma dipende
dal peso del paziente.
- Se il paziente pesa meno di 30 kg: la dose è pari a 162 mg (il contenuto di 1 penna preriempita)
- una volta ogni 3 settimane.
- Se il paziente pesa 30 kg o più: la dose è pari a 162 mg (il contenuto di 1 penna preriempita) una volta ogni 2 settimane.
La penna preriempita non deve essere usata per trattare bambini di età inferiore a 12 anni.
Avtozma è somministrato mediante iniezione sotto la pelle (sottocutanea). All’inizio, Avtozma potrà
esserle somministrato dal medico o dall’infermiere. Tuttavia, il medico potrebbe decidere che lei è in
grado di iniettarsi Avtozma da solo. In questo caso, lei verrà istruito su come autoiniettarsi Avtozma. I
genitori e coloro che si prendono cura dei pazienti verranno istruiti su come iniettare Avtozma nei
pazienti che non sono in grado di autoiniettarsi il medicinale.
Parli con il medico se ha eventuali domande sull’autosomministrazione di un’iniezione o sulla
somministrazione di un’iniezione in un paziente adolescente di cui si prende cura. Alla fine di questo
Se usa più Avtozma di quanto deve
Dal momento che Avtozma le verrà somministrato mediante una penna preriempita, è improbabile che
gliene venga dato troppo. Tuttavia, se ha delle preoccupazioni in merito, si rivolga al medico, al
farmacista o all’infermiere.
Se un adulto con AR o ACG oppure un adolescente con AIGs salta o dimentica una dose
È molto importante che usi Avtozma esattamente come prescritto dal medico. Tenga traccia della sua
prossima dose.
- Se salta la sua iniezione settimanale entro 7 giorni, assuma la dose programmata successiva.
- Se salta la sua iniezione a settimane alterne entro 7 giorni, assuma la dose dimenticata non appena se ne ricorda e quelle successive come programmato.
- Se salta la sua iniezione settimanale o la sua iniezione a settimane alterne per oltre i 7 giorni o non è sicuro su quando iniettare Avtozma, chiami il medico o il farmacista.
Se un adolescente con AIGp salta o dimentica una dose
È molto importante usare Avtozma esattamente come prescritto dal medico. Tenga traccia della
prossima dose.
- Se è stata saltata una dose e sono trascorsi meno di 7 giorni dalla dose saltata, inietti una dose non appena se ne ricorda e somministri quella successiva regolarmente nel giorno e all’ora previsti.
- Se è stata saltata una dose e sono trascorsi più di 7 giorni dalla dose saltata, oppure non è sicuro su quando iniettare Avtozma, si rivolga al medico o al farmacista.
Se interrompe il trattamento con Avtozma
Non deve sospendere il trattamento con Avtozma senza averne prima parlato con il medico.
Se ha qualsiasi dubbio sull’uso di questo medicinale si rivolga al medico, al farmacista o
all’infermiere.
4. Possibili effetti indesiderati
Come tutti i medicinali, Avtozma può causare effetti indesiderati, sebbene non tutte le persone li
manifestino.
Gli effetti indesiderati possono verificarsi fino a 3 mesi o più dopo l’ultima assunzione di Avtozma.
Possibili effetti indesiderati gravi: riferisca immediatamente al medico.
Questi sono comuni: possono interessare fino a 1 paziente su 10
Reazioni allergichedurante o dopo l’iniezione:
- difficoltà a respirare, oppressione al torace o stordimento;
- eruzione cutanea, prurito, orticaria, tumefazione delle labbra, della lingua o del viso. Se nota la comparsa di uno qualsiasi di questi sintomi, informi immediatamenteil medico.
Segni di infezioni gravi:
- febbre e brividi
- vesciche nella bocca o sulla pelle
- mal di stomaco
Segni e sintomi di tossicità epatica
Questi possono colpire fino a 1 utilizzatore su 1000
- stanchezza
- dolore addominale
- ittero (ingiallimento della pelle e della parte bianca degli occhi)
Se nota la comparsa di uno qualsiasi di questi sintomi, informi il medico il prima possibile.
Effetti indesiderati molto comuni:
Possono interessare 1 paziente su 10 o più
- infezioni delle vie aeree superiori con sintomi tipici quali tosse, naso chiuso, naso che cola, mal di gola e mal di testa
- livelli elevati di grassi nel sangue (colesterolo)
- reazioni correlate al sito di iniezione.
Effetti indesiderati comuni:
Possono interessare fino a 1 paziente su 10
- infezione polmonare (polmonite)
- fuoco di Sant’Antonio (herpes zoster)
- febbre delle labbra (herpes simplex orale), formazione di vesciche
- infezioni della pelle (cellulite) talvolta associate a febbre e brividi
- eruzione cutanea e prurito, orticaria
- reazioni allergiche (ipersensibilità)
- infezione agli occhi (congiuntivite)
- mal di testa, capogiri, pressione sanguigna elevata
- ulcerazione della bocca, mal di stomaco
- ritenzione idrica (edema) nella parte inferiore delle gambe, aumento del peso
- tosse, respiro corto
- basso numero dei globuli bianchi come evidenziato dagli esami del sangue (neutropenia, leucopenia)
- anomalie nei test di funzionalità del fegato (aumento delle transaminasi)
- aumento della bilirubina come evidenziato dagli esami del sangue
- bassi livelli di fibrinogeno nel sangue (una proteina coinvolta nella coagulazione del sangue).
Effetti indesiderati non comuni:
Possono interessare fino a 1 paziente su 100
- diverticolite (febbre, nausea, diarrea, stipsi, mal di stomaco)
- aree arrossate e gonfie nella bocca
- elevati livelli di grassi nel sangue (trigliceridi)
- ulcera gastrica
- calcoli renali
- ipotiroidismo.
Effetti indesiderati rari:
Questi possono colpire fino a 1 utilizzatore su 1000
- sindrome di Stevens-Johnson (eruzione cutanea, che può comportare formazione di vesciche gravi e desquamazione della pelle)
- reazioni allergiche fatali (anafilassi [fatale])
- infiammazione del fegato (epatite), ittero.
Effetti indesiderati molto rari:
Possono interessare fino a 1 paziente su 10.000
- basso numero dei globuli bianchi, dei globuli rossi e delle piastrine negli esami del sangue
- insufficienza epatica.
Effetti indesiderati nei bambini e negli adolescenti con AIGs o AIGp
Gli effetti indesiderati osservati nei bambini e negli adolescenti con AIGs o AIGp sono generalmente
simili a quelli registrati negli adulti. Alcuni effetti indesiderati vengono riscontrati più spesso nei
bambini e negli adolescenti: infiammazione del naso e della gola, mal di testa, sensazione di malessere
(nausea) e conte più basse dei globuli bianchi.
Segnalazione degli effetti indesiderati
Se manifesta un qualsiasi effetto indesiderato, compresi quelli non elencati in questo foglio, si rivolga
al medico, al farmacista o all’infermiere. Lei può inoltre segnalare gli effetti indesiderati direttamente
tramite il sistema nazionale di segnalazione riportato nell’ Allegato V . Segnalando gli effetti
indesiderati lei può contribuire a fornire maggiori informazioni sulla sicurezza di questo medicinale.
5. Come conservare Avtozma
Tenga questo medicinale fuori dalla vista e dalla portata dei bambini.
Non usi questo medicinale dopo la data di scadenza che è riportata sull’astuccio e sull’etichetta della
penna preriempita (Scad). La data di scadenza si riferisce all’ultimo giorno di quel mese.
Conservare in frigorifero (2 °C-8 °C). Non congelare. Una volta tolta dal frigorifero, la penna
preriempita può essere conservata per un massimo di 3 settimane a temperatura pari o inferiore a
30°C.
Tenere le penne preriempite nell’imballaggio esterno per proteggerle dalla luce e dall’umidità.
Il medicinale non deve essere usato se la soluzione è torbida o contiene particelle, se non è trasparente
o presenta un colore diverso dal giallo, o se qualsiasi parte della siringa preriempita appare
danneggiata.
La penna non deve essere agitata. Dopo aver rimosso il cappuccio, l’iniezione deve essere avviata
entro 3 minuti per evitare che il medicinale si secchi e blocchi l’ago. Se la penna preriempita non
viene utilizzata entro 3 minuti dalla rimozione del cappuccio, è necessario smaltirla in un contenitore
resistente alla perforazione e utilizzare una nuova penna preriempita.
Se dopo aver premuto la copertura dell’ago l’indicatore arancione non si muove, è necessario gettare
la penna preriempita in un contenitore resistente alla perforazione. Noncercare di riutilizzare la penna
preriempita. Quando si tenta di riutilizzarla, la penna preriempita è bloccata e l’ago è coperto
all’interno della copertura dell’ago. Non ripetere l’iniezione con un’altra penna preriempita. Contattare
l’operatore sanitario per ricevere assistenza.
6. Contenuto della confezione e altre informazioni
Cosa contiene Avtozma
- Il principio attivo è tocilizumab. Ciascuna penna preriempita contiene 162 mg di tocilizumab in 0,9 mL.
- Gli altri componenti sono L-istidina, L-treonina, L-metionina, polisorbato 80 e acqua per preparazioni iniettabili.
Descrizione dell’aspetto di Avtozma e contenuto della confezione
Avtozma è una soluzione iniettabile. La soluzione è da trasparente a gialla.
Avtozma è fornito in penna preriempita da 0,9 mL contenente 162 mg di tocilizumab soluzione
iniettabile.
La penna preriempita di Avtozma per l’uso da parte dei pazienti è disponibile in confezioni contenenti:
- 1 penna preriempita
- 4 penne preriempite
- 12 (3 confezioni da 4) penne preriempite (confezioni multiple)
È possibile che non tutte le confezioni siano commercializzate.
Titolare dell’autorizzazione all’immissione in commercio
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungheria
Produttore
Nuvisan France SARL
2400, Route des Colles,
06410, Biot,
Francia
Midas Pharma GmbH
Rheinstr. 49,
55218 Ingelheim,
Germania
KYMOS S.L.
Ronda Can Fatjó, 7B.
08290 Cerdanyola del Vallès,
Barcelona,
Spagna
Per ulteriori informazioni su questo medicinale, contatti il rappresentante locale del titolare
dell’autorizzazione all’immissione in commercio:
Lietuva
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
България
Celltrion Healthcare Hungary Kft.
Teл.: +36 1 231 0493
België/Belgique/Belgien
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 2 643 71 81
[email protected]
Luxembourg/Luxemburg
Celltrion Healthcare Belgium BVBA
Tél/Tel: +32 2 643 71 81
[email protected]
Česká republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Magyarország
Celltrion Healthcare Hungary Kft.
Tel:. +36 1 231 0493
Danmark
Celltrion Healthcare Hungary Kft.
Tlf: +36 1 231 0493
Malta
Mint Health Ltd.
Tel: +356 2093 9800
Deutschland
Celltrion Healthcare Deutschland GmbH
Tel: +49 (0)30 346494150
[email protected]
Nederland
Celltrion Healthcare Netherlands B.V.
Tel: + 31 20 888 7300
[email protected]
Eesti
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Norge
Celltrion Healthcare Hungary Kft.
Tlf: +36 1 231 0493
España
CELLTRION FARMACEUTICA (ESPAÑA)
S.L.
Tel: +34 919 94 23 90
Österreich
Astro-Pharma GmbH
Tel: +43 1 97 99 860
Ελλάδα
ΒΙΑΝΕΞ Α.Ε.
Τηλ: +30 210 8009111
Polska
Celltrion Healthcare Hungary Kft.
Tel.: +36 1 231 0493
France
Celltrion Healthcare France SAS
Tél.: +33 (0)1 71 25 27 00
Portugal
CELLTRION PORTUGAL, UNIPESSOAL
LDA.
Tel: +351 21 936 8542
Hrvatska
Oktal Pharma d.o.o.
Tel: +385 1 6595 777
România
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Ireland
Celltrion Healthcare Ireland Limited
Tel: +353 1 223 4026
Slovenija
OPH Oktal Pharma d.o.o.
Tel.: +386 1 519 29 22
Ísland
Celltrion Healthcare Hungary Kft.
Sími: +36 1 231 0493
Slovenská republika
Celltrion Healthcare Hungary Kft.
Tel: +36 1 231 0493
Italia
Celltrion Healthcare Italy S.r.l.
Tel: +39 02 47927040
Suomi/Finland
Celltrion Healthcare Finland Oy.
Puh/Tel: +358 29 170 7755
Κύπρος
C.A. Papaellinas Ltd
Τηλ: +357 22741741
Sverige
Celltrion Sweden AB
[email protected]
Latvija
Celltrion Healthcare Hungary Kft.
Tālr.: +36 1 231 0493
Altre fonti di informazione
Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea
dei medicinali, https://www.ema.europa.eu/.
7. Istruzioni per l’uso
Legga e segua le istruzioni per l’uso allegate alla sua penna preriempita di Avtozma prima di iniziare a
usarla ogni volta che ottiene una ricarica. Potrebbero esserci nuove informazioni. Prima di usare
Avtozma per la prima volta, un operatore sanitario le mostrerà come farlo in modo corretto.
Informazioni importanti
- Nonrimuovere il cappuccio della penna preriempita fino a quando non si è pronti a iniettarsi Avtozma.
- Noncercare mai di smontare la penna preriempita.
- Nonriutilizzare la stessa penna.
- Nonagitare la penna preriempita.
- Nonusare la penna preriempita se è caduta o appare danneggiata.
- Indicazioni per il paziente sulle reazioni di ipersensibilità (o anafilassi):nel caso in cui, durante o a seguito di un’iniezione, sviluppi in qualsiasi momento, mentre non si trova in ambulatorio, sintomi quali, ma non limitati a, eruzione cutanea, prurito, brividi, gonfiore del volto, delle labbra, della lingua o della gola, dolore al torace, respiro sibilante, difficoltà a respirare o a deglutire, capogiri o svenimento, deve immediatamente recarsi al pronto soccorso.
Conservazione di Avtozma
- Conservare la penna preriempita non utilizzata nell’astuccio originale e in frigorifero a una temperatura compresa tra 2 °C e 8 ºC. Noncongelare.
- Una volta tolto dal frigorifero, Avtozma può essere conservato per un massimo di 3 settimane a temperatura pari o inferiore a 30 °C. Se non utilizzato entro 3 settimane, Avtozma deve essere smaltito.
- Tenere la penna preriempita lontano dalla luce solare diretta.
- Nonrimuovere la penna preriempita dall’astuccio originale durante la conservazione.
- Nonlasciare la penna preriempita incustodita.
- Tenere la penna preriempita fuori dalla portata dei bambini. Contiene parti piccole.
Parti della penna preriempita di Avtozma (vedere Figura A).
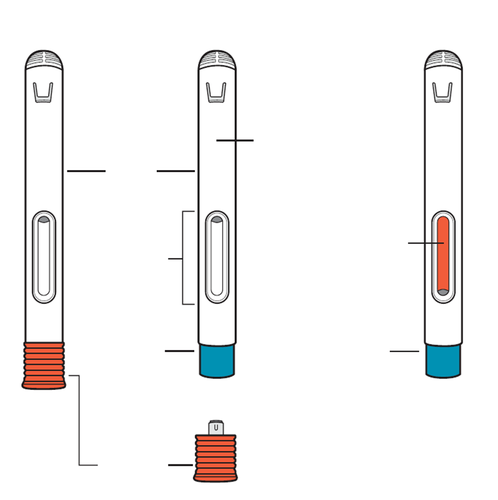
Prima dell’uso
Dopo l’uso
Data di
scadenza
Corpo
Indicatore
arancione
“iniezione
completa”
Finestra
Copertura
Copertura
dell’ago blu
(bloccata e ago
dell’ago
blu (ago
all’interno)
all’interno)
Cappuccio
arancione
Figura A
Preparazione dell’iniezione
1. Procurarsi tutto il necessario per l’iniezione.
- a.Prepari una superficie pulita e piatta, come ad esempio un tavolo o un bancone, in una zona ben illuminata.
- b.Tolga l’astuccio contenente la penna preriempita dal frigorifero.
- c.Si assicuri di avere a disposizione l’occorrente di seguito specificato (vedere Figura B):
- Astuccio contenente la penna preriempita di Avtozma
Non in dotazione nell’astuccio:
- Batuffolo di cotone o garza
- Cerotto
- Contenitore per materiali taglienti
- Tampone imbevuto d’alcol
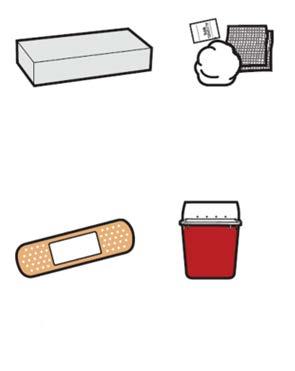
Figura B
2. Ispezionare l’astuccio
- a.Esamini l’astuccio e si assicuri di avere il (Avtozma) medicinale e il dosaggio corretti.
- b.Controlli la data di scadenza riportata sull’astuccio per assicurarsi che non sia passata.
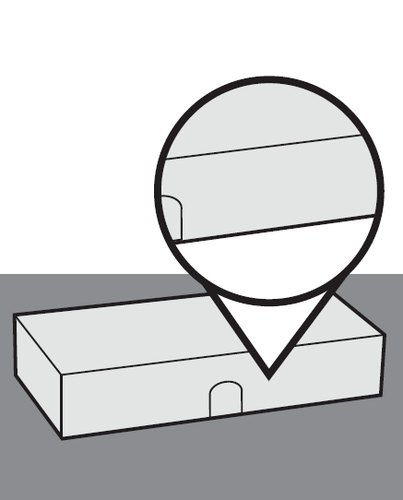
- Nonusi la penna preriempita se la data di scadenza è già passata.
- Se sta aprendo l’astuccio per la prima volta, si assicuri che sia correttamente sigillato.
- Nonusi la penna preriempita se le sembra che l’astuccio sia stato aperto o che sia danneggiato.
Figura C
3. Ispezionare la penna preriempita.
- a.Apra l’astuccio ed estragga 1 penna preriempita monodose. Rimetta in frigorifero le eventuali penne preriempite di Avtozma presenti nell’astuccio.
- b.Controlli la data di scadenza riportata sulla penna preriempita di Avtozma ( vedere Figura D).
- Nonusi la penna preriempita se la data di scadenza è passata. Se la data di scadenza è passata, getti la penna preriempita nel contenitore per materiali taglienti e ne prenda una nuova.
- c.Controlli la penna preriempita per verificare che non sia danneggiata e non vi siano segni di fuoriuscite di liquido.
- Nonusi la penna preriempita se è caduta, è danneggiata o se presenta fuoriuscite di liquido. Nota: un piccolo spazio tra il cappuccio arancione e il corpo dell’iniettore è normale.
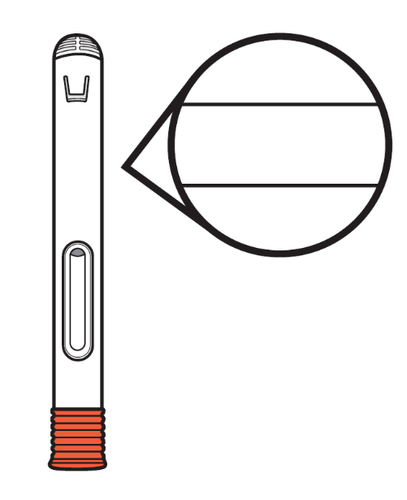
Figura D
4. Attendere 45 minuti.
- a.Lasci la penna preriempita fuori dall’astuccio a temperatura ambiente (tra 20 °C e 25 °C) per 45 minuti affinché si riscaldi (vedere Figura E).
- Nonriscaldi la penna preriempita utilizzando fonti di calore come ad esempio acqua calda o microonde.
- Nonlasci la penna preriempita alla luce solare diretta.
- Nonrimuova il cappuccio mentre la penna preriempita raggiunge la temperatura ambiente .
- Se la penna preriempita non raggiunge la temperatura ambiente, potrebbe provare fastidio.
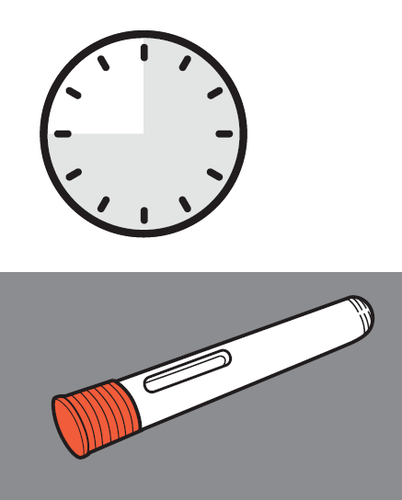
45
minuti
Figura E
5. Ispezionare il medicinale.
- a.Tenga Avtozma con il cappuccio indirizzato verso il basso.
- b.Osservi il medicinale e si assicuri che il liquido sia da trasparente a leggermente opalescente e da incolore a giallo e che non contenga particelle o scaglie (vedere Figura F).
- Nonusi la penna preriempita se il liquido è torbido, di colore alterato o se contiene particelle o scaglie. Getti la penna preriempita in un contenitore per materiali taglienti e ne usi una nuova.
- La presenza di bolle d’aria è normale.
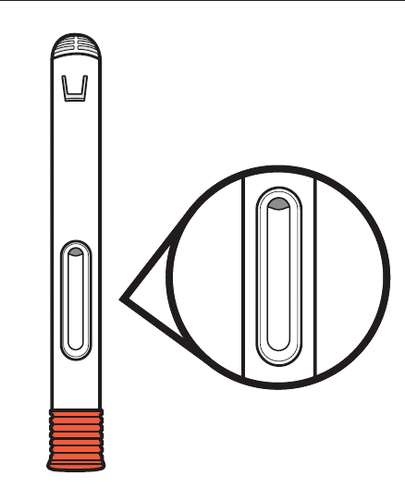
Figura F
6. Lavarsi le mani.
- a.Si lavi bene le mani con acqua e sapone e le asciughi (vedere Figura G).
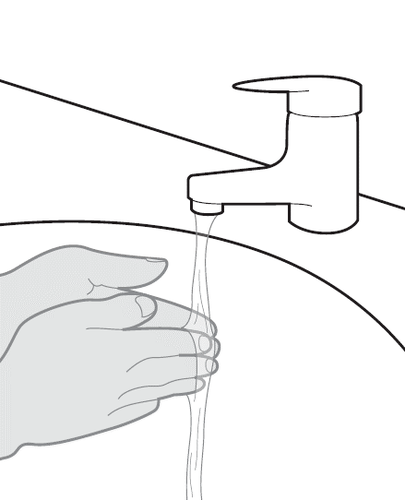
Figura G
7. Scegliere un sito di iniezione appropriato (vedere
Figura H).
- a.I siti in cui è possibile effettuare l’iniezione sono:
- la parte anteriore delle cosce ;
- l’addome, ad eccezione dell’area di 5 cm attorno all’ombelico;
- la zona esterna della parte superiore delle braccia (solo se a eseguire l’iniezione è la persona che le presta assistenza o l’operatore sanitario ).
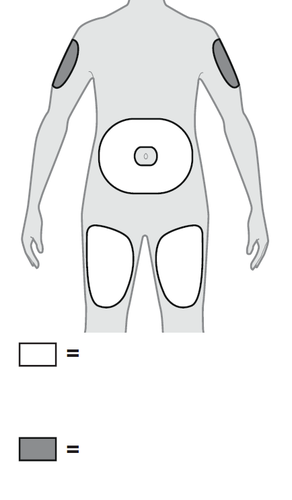
- Nonsi autosomministri l’iniezione nella zona esterna della parte superiore delle braccia.
- Ogni volta che si somministra un’iniezione deve essere utilizzata una sede diversa ad almeno 2,5 cm di distanza dall’area utilizzata per l’iniezione precedente.
- Nonesegua l’iniezione su nei, cicatrici, lividi o nelle aree in cui la pelle si presenta dolente, arrossata o indurita .
Figura H
8. Pulire il sito di iniezione.
- a.Disinfetti il sito di iniezione utilizzando un tampone imbevuto di alcol e lo lasci asciugare (vedere Figura I). Questo ridurrà il rischio di infezione.
- Si assicuri di nontoccare quest’area prima di eseguire l’iniezione.
- Nonsoffi, né sventoli l’area disinfettata.
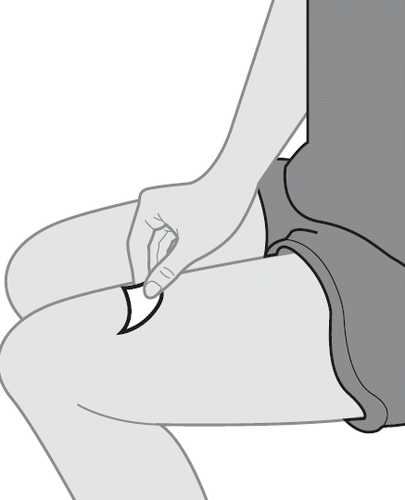
Figura I
Somministrazione dell’iniezione
9. Rimuovere il cappuccio.
- a.Tenga con una mano la penna preriempita afferrandola per il corpo dell’iniettore con il cappuccio inserito. Con l’altra mano sfili delicatamente il cappuccio tirandolo in orizzontale (vedere Figura J). Nota: se non riesce a rimuovere il cappuccio, chieda aiuto alla persona che le presta ssistenza o si rivolga all’operatore sanitario.
- b.Smaltisca immediatamente il cappuccio nel contenitore per materiali taglienti (vedere fase 14e Figura O)
- Nonreinserisca il cappuccio sulla penna preriempita.
- Nontocchi il manicotto di sicurezza per l’ago collocato sulla punta della penna preriempita al fine di evitare una lesione da puntura accidentale.
- Una volta rimosso il cappuccio, la penna preriempita è pronta per l’uso. Nel caso in cui non venga utilizzata entro 3 minuti dalla rimozione del cappuccio, la penna preriempita deve essere smaltita in un contenitore per materiali taglienti e deve essere impiegata una nuova penna preriempita .
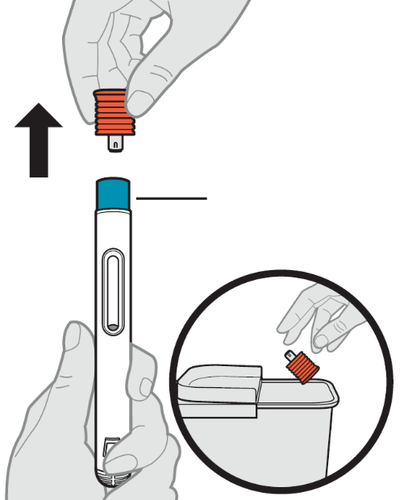
Copertura
dell’ago
Figura J
10. Inserire la penna preriempita nel sito di iniezione.
- a.Con una mano, tenga comodamente la penna preriempita in modo tale da poter vedere la finestra (vedere Figura K).
- b.Senza pizzicare o tirare la pelle, inserisca la penna preriempita nella cute con un angolo di 90° (vedere Figura L).
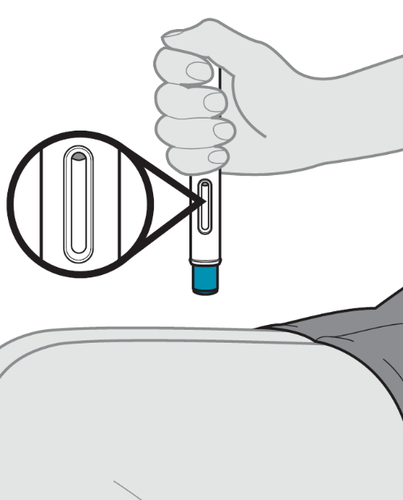
Nota: la scelta dell’angolo di inclinazione corretto è
importante poiché assicura che il medicinale venga
rilasciato sotto la pelle (nel tessuto adiposo); in caso
contrario l’iniezione potrebbe risultare dolorosa e il
medicinale non efficace.
- Noninietti il medicinale nel muscolo o in un Figura Kvaso sanguigno .
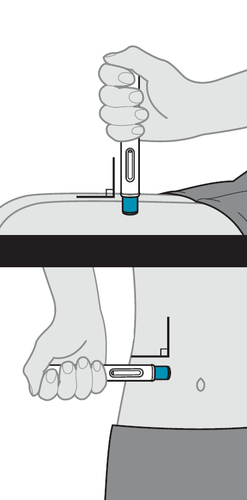
90°
O
90°
Figura L
11. Eseguire l’iniezione.
- a.Prema con decisione la penna preriempita nella cute per iniziare l’iniezione.
- b.Quando l’iniezione inizia, sentirà il primo “clic” e l’indicatore arancione inizierà a riempire la finestra (vedere Figura M).
- c.Tenga la penna preriempita premuta saldamente contro la cute fino a udire il secondo “clic”.
- d.Dopo aver udito il secondo “clic”, continui a tenere la penna preriempita saldamente premuta contro la cute e conti lentamente fino a 5affinché venga somministrata l’intera dose (vedere Figura M).
- e.Segua l’indicatore arancione finché non smette di avanzare e raggiunge la fine della finestra per accertarsi di aver iniettato la dose completa del medicinale . Nota: se l’indicatore arancione non si muove, gettare la penna preriempita e usarne una nuova.
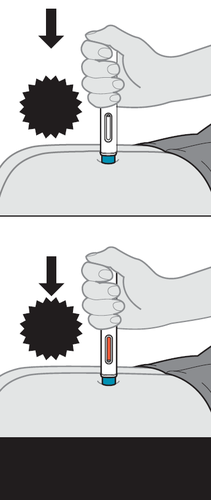
1°
clic
2°
clic
Poi contare
lentamente fino a 5
Figure M
12. Rimuovere la penna preriempita dal sito di
iniezione.
- a.Quando l’indicatore arancione si arresta, sollevi la penna preriempita dal sito di iniezione con un angolo di inclinazione di 90° per estrarre l’ago dalla cute.
- La copertura dell’ago uscirà automaticamente e si bloccherà coprendo l’ago (vedere Figura N). Nota: se la finestra non è diventata completamente arancione o se sta ancora iniettando il medicinale, significa che non ha ricevuto l’intera dose. Riponga con attenzione la penna preriempita nel contenitore per materiali taglienti e contatti immediatamente l’operatore sanitario .
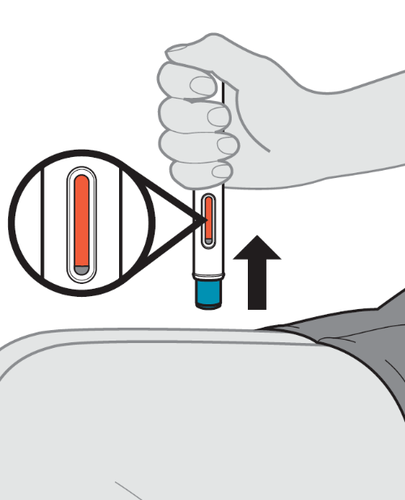
Figura N• Nontocchi la copertura dell’ago della penna
preriempita.
- Noncerchi di riutilizzare la penna preriempita.
- Nonripeta l’iniezione con un’altra penna preriempita.
Dopo l’iniezione
13. Cura del sito di iniezione.
- a.Se nota la presenza di qualche goccia di sangue, può trattare il sito di iniezione premendo delicatamente, senza strofinare, un batuffolo di cotone o una garza sul sito e applicare un cerotto, se necessario.
- Nonstrofini il sito di iniezione.
14. Smaltimento di Avtozma.
- a.Riponga la penna preriempita nel contenitore per materiali taglienti subito dopo l’uso (vedere Figura O).
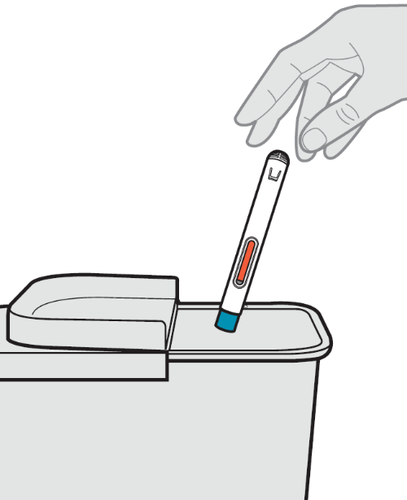
Note: se l’iniezione le viene somministrata da
un’altra persona, questa persona deve fare attenzione
durante la rimozione della siringa preriempita e il suo
smaltimento al fine di evitare una lesione da puntura
accidentale e la trasmissione di un’infezione .
- Nonriutilizzi la penna preriempita.
- Nonreinserisca il cappuccio sulla penna preriempita.
- Nonsmaltisca il contenitore per materiali taglienti usato nei rifiuti domestici.
- Nonricicli il contenitore per materiali taglienti usato.
- Tenga la penna preriempita di Avtozma e il contenitore per materiali taglienti fuori dalla portata dei bambini.
- Smaltisca il contenitore pieno attenendosi alle istruzioni ricevute dall’operatore sanitario o dal farmacista. Se non dispone di un contenitore per materiali taglienti, può utilizzare un contenitore per i rifiuti domestici richiudibile e resistente alla perforazione. Il medicinale non utilizzato e i rifiuti derivati da tale medicinale devono essere smaltiti in conformità alla normativa locale vigente
15. Registrazione dell’iniezione.
- a.Annoti la data, l’ora e la parte del corpo specifica in cui ha praticato l’iniezione. Figura O
- Paese di registrazione
- Forma farmaceuticaConcentrato per soluzione per infusione, 20 mg/mL
- Codice ATCL04AC07
- Principio attivo
- Prescrizione richiestaSì
- Produttore
- Queste informazioni sono solo a scopo informativo e non costituiscono un parere medico. Consulta sempre un medico prima di assumere qualsiasi medicinale. Oladoctor non è responsabile delle decisioni mediche basate su questo contenuto.
- Alternative a AVTOZMAForma farmaceutica: Concentrato per soluzione per infusione, 20 MG/MLPrincipio attivo: tocilizumabProduttore: ROCHE REGISTRATION GMBHPrescrizione richiestaForma farmaceutica: Concentrato per soluzione per infusione, 20 mg/mLPrincipio attivo: tocilizumabProduttore: BIOGEN NETHERLANDS BVPrescrizione richiestaForma farmaceutica: Concentrato per soluzione per infusione, 20 mg/mlPrincipio attivo: tocilizumabProduttore: FRESENIUS KABI DEUTSCHLAND GMBHPrescrizione richiesta
Medici online per AVTOZMA
Valutazione del dosaggio, effetti indesiderati, interazioni, controindicazioni e rinnovo della prescrizione di AVTOZMA — soggetto a valutazione medica e alle normative locali.
Ottieni una ricetta per AVTOZMA online
Compila un modulo di 2 minuti
Raccontaci i tuoi sintomi, la tua storia clinica e il medicinale che stai richiedendo.
Scegli un medico o lascia che lo assegniamo noi
Scegli uno specialista o ti abbineremo al primo medico disponibile.
Il medico esamina il tuo caso
Di solito entro 30 minuti. Potrebbe farti domande aggiuntive via chat.
Ritira la ricetta in qualsiasi farmacia
Ricetta elettronica inviata alla tua email — valida in tutta la Spagna.
Domande frequenti

Rimani aggiornato su Oladoctor
Novità su nuovi servizi, aggiornamenti del prodotto e contenuti utili per i pazienti.






